天蚕片、天蚕胶囊中僵蛹成分鉴定
2020-12-13杨鹏飞杨成宇林玲胡建慧周莹孙小祥夏国华杨
杨鹏飞 杨成宇林 玲胡建慧周 莹孙小祥夏国华杨 欢*
(1.常州市金坛区人民医院,江苏常州 214000;2.江苏大学药学院,江苏镇江 212013;3.镇江市中医院,江苏镇江 212003)
僵蛹为蚕蛾科昆虫家蚕Bombyx moriL.的蛹接种白僵菌Beauveria bassiana发酵后的制品,常作为僵蚕的代用品,可用于治疗高热惊厥、癫痫、上呼吸道感染、流行性腮腺炎等,还具有抗凝、抗癌和其他药理作用[1]。
僵蚕(蛹)的应用广泛,需求量大,市面上出现了一些伪品,如感染绿僵菌Metarhizium anisopliae致死的家蚕和黑死蚕等[2],对临床用药的安全性和有效性造成了负面影响。目前以僵蛹入药的临床常用中成药有天蚕胶囊和天蚕片,传统的性状与显微鉴别方法无法实现其中僵蛹成分的准确鉴定。DNA分子鉴定技术对不同物种具有高度特异性,比传统鉴定方法更为可靠[3],近年来在中药鉴定领域备受关注。如DNA条形码技术,是利用DNA片段自身在物种种内的特异性和种间的多样性对物种进行鉴定[4-7],结果准确度高,但是产物需要测序,操作步骤繁琐,尤其是不适用于混合物;而特异性引物扩增是根据基因序列存在的差异所设计的引物进行PCR,在样品检验过程中无需测序,可同时测定多个物种,且适用于混合物,弥补了DNA条形码技术的不足[8-9]。
本研究根据僵蛹中家蚕和白僵菌及其常见伪品绿僵菌的线粒体全基因(mtDNA)序列的差异设计引物,进而基于特异性引物扩增建立了具有较强专属性且能够简便快速地检测天蚕片和天蚕胶囊中僵蛹成分的技术,以期为市面中成药产品的质量控制提供参考。
1 材料
1.1 仪器 恒温混匀仪(拓普森科学仪器有限公司);TGL-16C型高速台式离心机(上海安亭科学仪器厂);SHZ型恒温振荡器(国华电器有限公司);NanoDrop 1000型核酸蛋白分析仪 (美国Thermo公司);T100型PCR仪、Basic型电泳仪(美国Bio-Rad公司);JY-SPFT型水平电泳槽(北京君意东方电泳设备有限公司);GenoSens 1860型凝胶成像系统(上海勤翔科学仪器有限公司)。
1.2 试剂与药物 白僵菌购自中国工业微生物菌种保藏管理中心,保藏编号为CICC41021;绿僵菌购自北京北纳创联生物技术研究院,保藏编号为BNCC 114445;家蚕对照药材(B/N 121457-200501)购自中国食品药品检定研究院;中成药天蚕片、天蚕胶囊购自药房,具体信息见表1;蚕蛹由中国农业科学院蚕业研究所提供。Tris平衡酚(北京索莱宝科技有限公司);dNTP Mix、DreamTaq Green DNA Polymerase (美国Thermo公司);Agarose-Low EEO (上海碧云天生物技术有限公司);Ethidium Bromide (美国Sigma公司);Low ladder SN127 (南京生兴生物技术有限公司)为生物级;其他试剂均为分析纯,购自国药集团化学试剂有限公司和上海阿拉丁生化科技股份有限公司;引物由上海生工生物工程有限公司合成。
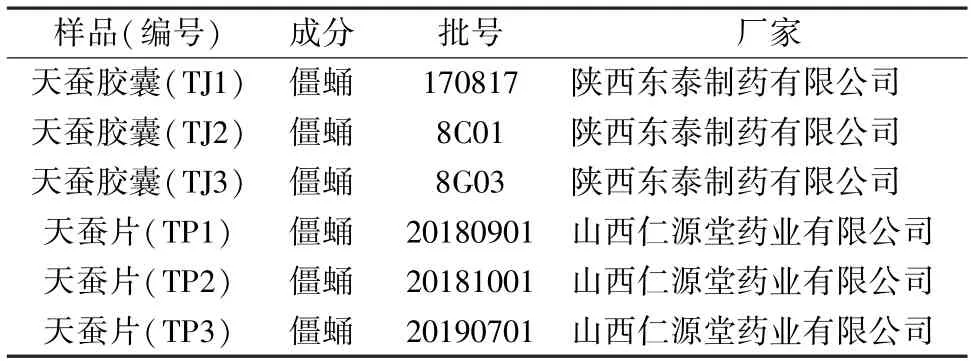
表1 样品信息
2 方法与结果
2.1 自制僵蛹 参考文献[10],称取蚕蛹粉10.0 g,加10 mL水混匀,121 ℃灭菌30 min,冷却至室温,作为发酵基质。无菌环境下进行白僵菌液接种,(27±1)℃培养,15 d后,待基质内外长满菌丝体时取出,60 ℃干燥24 h,制得10批白僵蛹(BJ1~BJ10)。同法自制10批绿僵蛹(LJ1~LJ10)和10批不接菌种的空白蚕蛹(NJ1~NJ10)。
2.2 供试品溶液制备 称取家蚕对照品、白僵菌、绿僵菌、自制僵蛹各20.0 mg,加入CTAB提取液1 000 μL,65 ℃孵育2 h后离心,上清液加入等体积70%甲醇,充分混匀,置于-20 ℃下冷冻1 h,离心,待甲醇挥干后,加入CTAB提取液500 μL,65 ℃孵育1 h,离心,上清液加入等体积的三氯甲烷/Tris-饱和酚(1 ∶1),混匀,离心,加入等体积的三氯甲烷/异戊醇(24 ∶1),混匀,离心,加入3 mol/L醋酸钾溶液100 μL,再加入与上清液等体积的预冷异丙醇,混匀后置于-20 ℃下冷冻1 h,离心,沉淀中加入预冷的70%乙醇500 μL洗涤后,室温晾干,以TE缓冲液25 μL溶解,得到DNA供试品溶液,4 ℃保存。
2.3 特异性引物设计 从GenBank数据库中搜索下载家蚕、白僵菌及其常见伪品绿僵菌的线粒体全基因组序列,并采用DNAMAN软件比对3个物种的基因差异,利用Oligo 7软件设计特异性引物,并通过NCBI Primer-BLAST评估,特异性引物的序列等信息如表2所示。
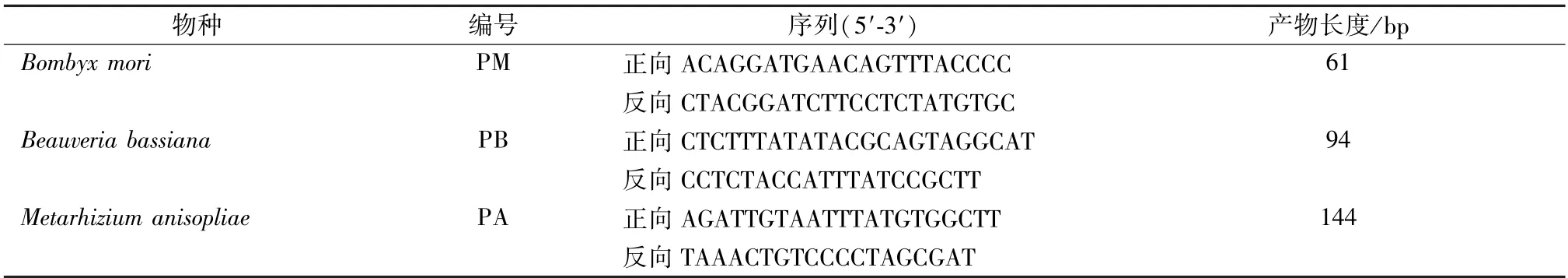
表2 特异性引物
2.4 PCR扩增 PCR反应体系由以下成分组成[11]:1×扩增缓冲液,200 μmol/L dNTPs,引物对1.0 μL (正向与反向各半),1 μL模板DNA (10 ng),Taq DNA聚合酶0.625 U,200 μmol/L MgCl2,再加入无菌双蒸水至25 μL。反应结束后将扩增产物载入2%TBE琼脂糖凝胶进行分离,紫外下观察目的片段条带。研究中还优化了退火温度、引物浓度以及循环数等,最终建立了PCR扩增条件,见表3。
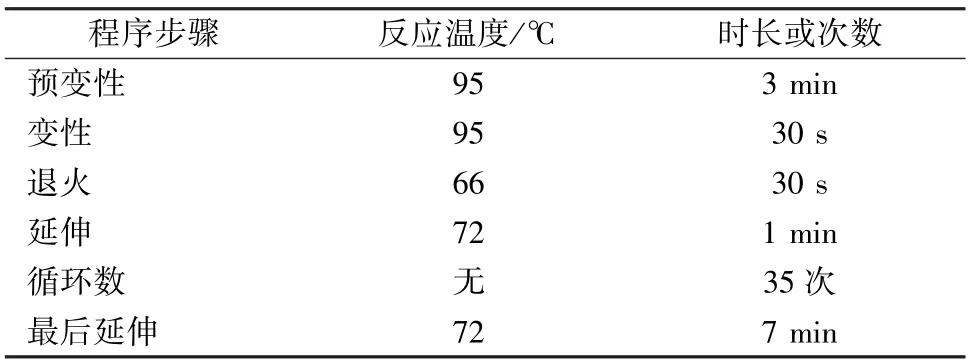
表3 PCR扩增条件
2.5 特异性及灵敏度 将不同批3种自制样品在“2.4”项条件下与3种特异性引物(PM、PB、PA)进行扩增以验证特异性。图1显示,家蚕、白僵菌的DNA经扩增后分别在61、94 bp处产生条带,而绿僵菌的DNA经扩增后,在144 bp处产生条带;各引物之间无交叉反应,体现出了很强的专属性。
保持引物PM、PB、PA的浓度均为0.2 μmol/L,分别加入0.01、0.1、1、10 ng/μL DNA模板各1 μL,进行PCR以考察灵敏度。从图2中可以看出,在以特异性引物PM或PA扩增时,如DNA模板质量浓度分别为1、10 ng/μL,可检出目的片段条带;引物PB在模板质量浓度分别为10、1、0.1 ng/μL时均能检出条带,故对家蚕和绿僵菌的检出限为1 ng,而对白僵菌的检出限为0.1 ng。
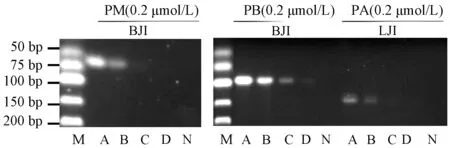
图2 灵敏度检测电泳图
2.6 自制僵蛹检测 以特异性引物PM、PB和PA对20批自制僵蛹和10批空白蚕蛹进行PCR扩增,以考察该技术的准确性。从图3可以看出,10批白僵蛹及其常见伪品绿僵蛹的DNA经扩增后,产生的条带位置与预期目的片段的长度一致。
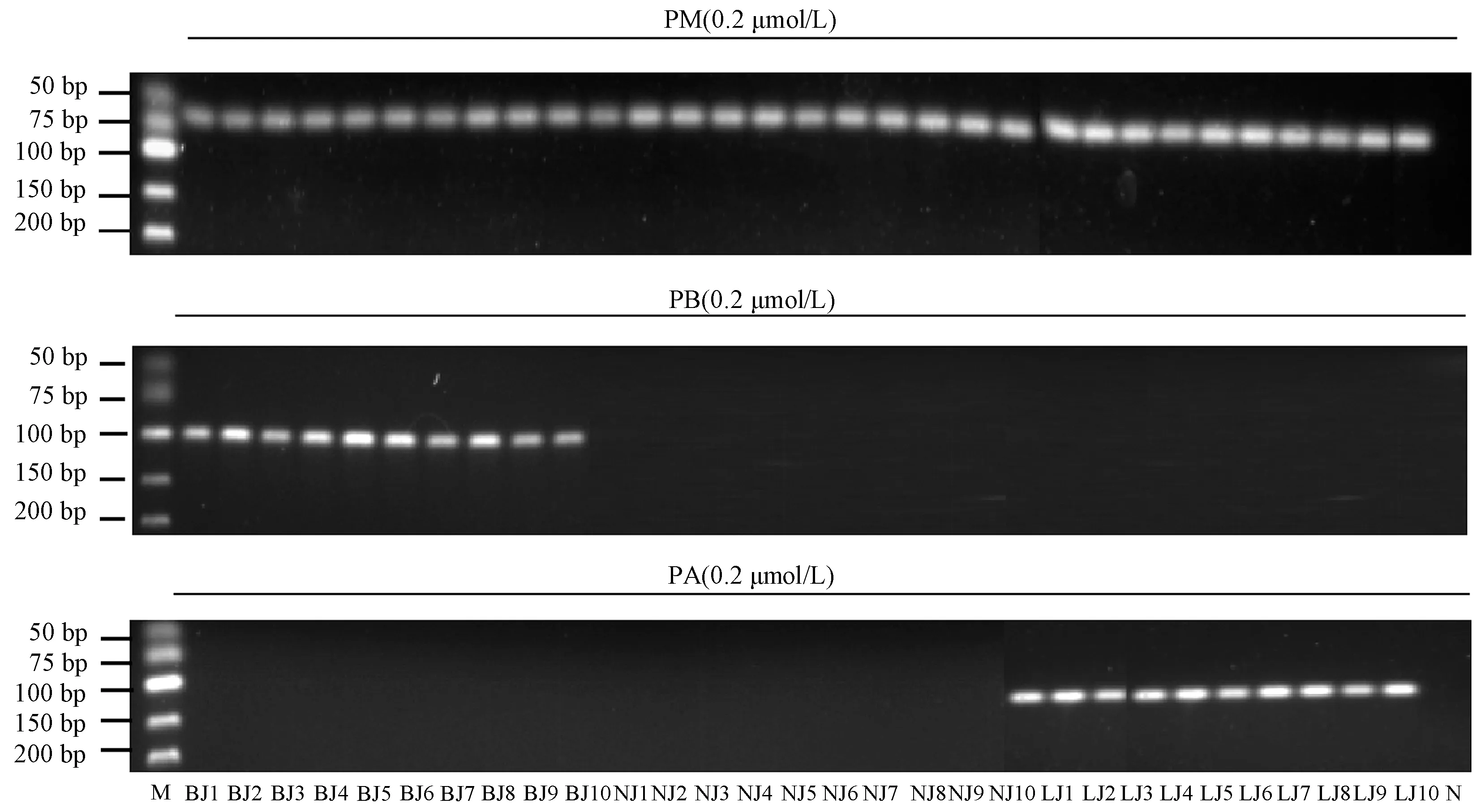
图3 自制僵蛹的检测电泳图
2.7 天蚕片和天蚕胶囊检测 通过本研究所建立的技术对3批天蚕片以及3批天蚕胶囊中的僵蛹成分进行检测,验证标签所示物种是否准确。分别精密称取6批中成药样品粉末20.00 mg,按“2.2” 项下方法提取与纯化DNA,然后在“2.4” 项条件下扩增。由图4、表4可见,这6批市售中成药经均检出了僵蛹的基原家蚕和白僵菌,并且未检测出绿僵菌。
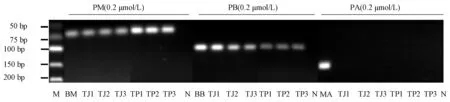
图4 天蚕胶囊及天蚕片的检测电泳图

表4 天蚕片和天蚕胶囊鉴定结果
3 结论与讨论
研究表明生命体中mtDNA较为丰富,比细胞核DNA等其他遗传标记更适合物种鉴定;同时,多拷贝mtDNA在加工产物中比单拷贝核DNA有更高的存活机会,有助于提高分析灵敏度[12-14]。本研究基于mtDNA种间差异设计的特异性引物能同时检出家蚕、白僵菌及其常见伪品基原绿僵菌,且引物间无交叉反应,体现出很强的专属性。
研究表明蛹相比幼虫和成虫的微生物丰富度更高[15],因此开展蛹的质量控制技术研究具有一定意义。本研究利用特异性扩增技术鉴定了天蚕片和天蚕胶囊中的僵蛹成分,该技术准确可靠,且方便快速,有助于监控含僵蚕(蛹)中成药的质量。
本研究考虑到僵蛹与僵蚕的基原一致,而天蚕片和天蚕胶囊仅含有僵蛹,是成分最为简单的临床常用中成药,因而被选择作为研究对象,而没有选择其他较为复杂的含有僵蚕成分的成方制剂。在目前正在进行的工作中,课题组已经选择了含有僵蚕的中成药金嗓清音丸和中风回春丸作为研究对象,这2种中成药的成分复杂,开展专属性鉴定研究更具意义。
中成药中同时含有多种动物药成分,由于制法复杂、辅料干扰,其鉴定难度很大,在后续的工作中将进一步开展相关研究,优化测定条件,建立专属性鉴定技术以期从中成药中同时鉴定多种动物药成分。
本研究的鉴定依据为DNA分子,因而无法实现僵蚕和僵蛹区别,也无法用于鉴别添加染了白僵菌的蚕沙等制伪现象,在后续工作中考虑结合使用差异性蛋白质鉴定技术或者采用DNA定量扩增技术开展进一步研究。