HPLC法同时测定香丹注射液中9种成分
2020-12-13杨凌鉴任莉莉黄九林张胜海金华峰谢娟平贾璞郑晓晖
杨凌鉴 任莉莉 黄九林张胜海金华峰谢娟平贾 璞郑晓晖*
(1.安康学院化学化工学院,陕西安康 725000;2.安康学院秦巴中药资源研发中心,陕西安康 725000;3.安康学院医学院,陕西安康 725000;4.西北大学生命科学学院,陕西西安 710069)
香丹注射液是将丹参水提物和降香饱和芳香水按照一定比例混合精制而成的现代中药制剂,属于国家部颁标准(WS3-B-3289-98)收载的药物[1-3]。现代研究[4-7]显示,该制剂具有扩张血管、增强冠脉血流量等作用,能有效干预心肌缺血、脑缺血、机体缺氧,临床上广泛应用于冠心病、心绞痛、心肌梗死以及脑血管疾病的治疗,疗效显著确切。
中药疗效的发挥是多成分、多靶点协同作用的结果,故开展多成分含有量测定有利于中药材及其相关制剂的全面质量控制[8-9]。前期报道,香丹注射液中丹参所含的酚酸是与该制剂临床疗效密切相关的主要活性物质[10-11],但目前其质量控制方法主要是选择丹参素、原儿茶醛、咖啡酸、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A中的几种[2-3,12]或全部[10-11]进行定量分析,未涉及原儿茶酸、香草酸,而且检测波长均设置为280 nm,可能会影响部分成分的检测灵敏度。因此,本实验在前期采用HPLC-Q-TOF/MS法对香丹注射液化学成分进行定性分析的基础上[13],建立HPLC法同时测定该制剂中丹参素、原儿茶酸、原儿茶醛、香草酸、咖啡酸、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A的含有量,以期为其质量控制的完善提供依据。
1 材料
1.1 仪器 Agilent 1100高效液相色谱仪,配置G1312C二元泵、G1328B手动进样器、G1316A柱温箱、G1315B二极管阵列检测器、Chemstation 5.0化学工作站 (美国Agilent公司);MS105DU型电子天平 (瑞士Mettler-Toledo公司);KQ-250DB型数控超声波清洗器(昆山市超声仪器有限公司);ULUP-I-10型超纯水机(四川优普超纯科技有限公司);QL-901型快速混匀器(海门市其林贝尔仪器制造有限公司)。
1.2 试剂与药物 丹参素、原儿茶酸、原儿茶醛、香草酸、咖啡酸、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A对照品 (批号分别为DST180302-014、DST180428-081、DST180105-011、DST180311-088、DST181018-013、DST170524-028、DST180105-027、DST180128-009、DST180201-008),均购于成都德思特生物技术有限公司,纯度均大于98%。香丹注射液(批号1510201、1510202、1510203,国药准字Z51021309,10 mL×5支),购于四川升和药业股份有限公司;色谱纯甲醇 (德国Merck公司);色谱纯甲酸(美国Sigma Aldrich公司);其他试剂均为分析纯;水为超纯水(电阻率18.25 MΩ),由优普ULUP-I-10超纯水机系统制备。
2 方法与结果
2.1 色谱条件 Agilent TC-C18色谱柱(4.6 mm×250 mm,5 μm);流动相0.2% 甲酸水 (A)-甲醇(B),梯度洗脱(0~25 min,7%~15% B;25~45 min,15%~25% B;45~80 min,25%~50%B;80~100 min,50%~80% B);体积流量0.6 mL/min;柱温30 ℃;检测波长280 nm (0~46、58~100 min,丹参素、原儿茶酸、原儿茶醛、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A)、260 nm (46~52 min,香草酸)、320 nm (52~58 min,咖啡酸);进样量25 μL。
2.2 溶液制备
2.2.1 对照品溶液 精密称取丹参素、原儿茶酸、原儿茶醛、香草酸、咖啡酸、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A对照品适量,置于2.0 mL棕色量瓶中,丹参素、原儿茶酸、原儿茶醛用50%甲醇定容,其余对照品用甲醇定容,制得质量浓度分别为8.00、3.20、2.40、2.60、2.00、3.00、2.80、5.20、2.20 mg/mL的贮备液,分别精密移取0.5 mL,甲醇稀释,即得(444.00、178.00、133.00、144.00、111.00、167.00、156.00、289.00、122.00 μg/mL),在4 ℃下冷藏备用。
2.2.2 供试品溶液 精密吸取注射液1.0 mL,置于5.0 mL棕色量瓶中,超纯水定容至刻度,摇匀,经0.22 μm水系滤膜过滤,即得,在4 ℃下冷藏备用。
2.2.3 阴性样品溶液 按照处方比例和工艺流程,制备缺丹参的阴性样品,按“2.2.2” 项下方法制备,即得,在4 ℃下冷藏备用。
2.3 方法学考察
2.3.1 专属性考察 精密吸取对照品、供试品、阴性样品溶液各25 μL,在“2.1” 项色谱条件下进样测定,结果见图1。由此可知,各成分色谱峰与相邻峰均达到基线分离,理论塔板数按各成分计均大于5 000,阴性无干扰,表明该方法专属性良好。
2.3.2 线性关系考察 将“2.2.1” 项下对照品溶液用甲醇依次稀释至系列质量浓度,在“2.1”项色谱条件下进样测定。以溶液质量浓度为横坐标(X),峰面积为纵坐标(Y)进行回归,分别以S/N=3、S/N=10为检测限、定量限,结果见表1,可知各成分在各自范围内线性关系良好。
2.3.3 精密度试验 精密吸取“2.2.1” 项下对照品溶液,在“2.1” 项色谱条件下进样测定6次,测得丹参素、原儿茶酸、原儿茶醛、香草酸、咖啡酸、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A峰面积RSD分别为0.79%、0.91%、1.60%、0.92%、1.18%、1.39%、0.98%、1.07%、1.40%,表明仪器精密度良好。
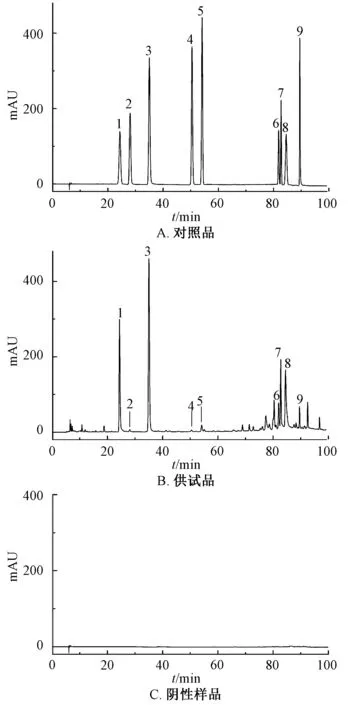
图1 各成分HPLC色谱图Fig.1 HPLC chromatograms of various constituents
2.3.4 重复性试验 取同一批注射液 (批号1510203),按“2.2.2” 项下方法平行制备6份供试品溶液,在“2.1” 项色谱条件下进样测定,测得丹参素、原儿茶酸、原儿茶醛、香草酸、咖啡酸、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A含有量RSD分别为0.92%、2.30%、1.78%、1.98%、0.87%、1.06%、0.76%、0.51%、2.28%,表明该方法重复性良好。
2.3.5 稳定性试验 取同一批注射液(批号1510203),按“2.2.2” 项下方法制备供试品溶液,分别于 0、2、4、8、12、24 h,在“2.1” 项色谱条件下进样测定,测得丹参素、原儿茶酸、原儿茶醛、香草酸、咖啡酸、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A峰面积RSD分别为0.50%、1.99%、1.04%、0.99%、1.12%、1.82%、0.56%、0.60%、1.47%,表明供试品溶液在24 h内稳定性良好。
2.3.6 加样回收率试验 精密吸取各成分含有量已知的注射液(批号为1510203)0.5 mL,置于5 mL棕色量瓶中,按100% 水平加入对照品溶液0.5 mL (丹参素、原儿茶酸、原儿茶醛、香草酸、咖啡酸、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A质量浓度分别为1 510.20、6.15、385.61、3.92、8.09、176.38、325.95、696.46、52.54 μg/mL),按“2.2.2” 项下方法平行制备6份供试品溶液,在“2.1” 项色谱条件下进样测定,计算回收率。结果,丹参素、原儿茶酸、原儿茶醛、香草酸、咖啡酸、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A平均加样回收率分别为100.83%、101.28%、103.14%、98.45%、97.79%、100.31%、99.54%、96.52%、102.69%,RSD分别为2.48%、2.27%、0.97%、1.32%、1.12%、1.79%、1.31%、1.04%、0.88%。

表1 各成分线性关系Tab.1 Linear relationships of various constituents
2.4 样品含有量测定 取3批香丹注射液,按“2.2.2” 项下方法制备供试品溶液,每批平行3份,在“2.1” 项色谱条件下进样测定,计算含有量,结果见表2。
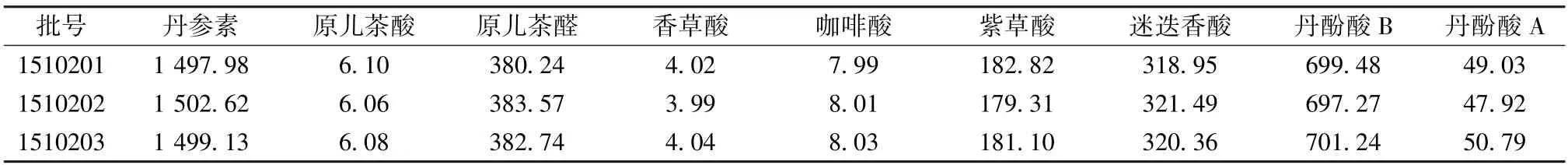
表2 各成分含有量测定结果(μg/mL, n=3)Tab.2 Results of content determination of various constituents (μg/mL, n=3)
3 讨论
3.1 检测指标筛选 研究表明,丹参素、原儿茶酸、原儿茶醛、香草酸、咖啡酸、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A具有抗心脑缺血、抑制血小板聚集、抗炎、保肝肾、抗氧化等多种显著药理活性[14-15]。因此,本实验选择上述9种酚酸类成分作为检测指标。
3.2 色谱条件筛选 在前期研究中,已对流动相种类、洗脱方式、柱温等参数进行了优化[13],故本实验仅需考虑水相添加剂和检测波长即可。所检测的成分均为酚酸类,常用的水相添加剂有甲酸、乙酸[16-17],本实验对其种类和加入量进行了考察,发现0.2%甲酸水洗脱时各成分峰形最好,色谱峰不拖尾。另外,丹参素、原儿茶酸、原儿茶醛、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A在280 nm波长处有最大紫外吸收[18],而香草酸、咖啡酸分别在260 nm[19]、322 nm[20]波长处有最大紫外吸收,为了确保各成分均具有最佳的检测灵敏度,本实验采用分时间段变换波长模式进行分析。
4 结论
本实验建立HPLC法同时测定香丹注射液中丹参素、原儿茶酸、原儿茶醛、香草酸、咖啡酸、紫草酸、迷迭香酸、丹酚酸B、丹酚酸A的含有量,该方法简便准确,稳定可靠,可为该制剂质量控制的完善提供参考依据。
