金属硫化物吸附剂脱除烟气汞研究进展
2020-12-07黄瑞杨阳徐文青张冀翔朱廷钰
黄瑞,杨阳,徐文青,张冀翔,朱廷钰
(1 中国石油大学(北京)机械与储运工程学院,重质油国家重点实验室,北京102249;2 中国科学院过程工程研究所过程污染控制研究中心,北京100190;3 清华大学烟气多污染物控制技术与装备国家工程实验室,北京100084)
汞是一种全球性污染物,具有高毒性、易挥发性、生物积累性,广泛存在于土壤、大气和水中,对植物、动物和人类产生巨大危害[1-3]。汞的化学性质稳定,能在大气中稳定存在长达一年半左右,并且能长距离传输导致跨区域污染[4]。不同形态汞的毒性有所不同,有研究表明单质汞可在微生物的作用下转化为毒性最强的甲基汞[5]。当前人为源大气汞排放来源广泛,主要包括手工和小型金矿开采、燃煤、有色金属冶炼、水泥生产。在人类活动的影响下,目前大气汞浓度比自然水平增加了450%,2015 年全球人为源大气汞排放量已达到2220t,比2010 年大约高出20%,汞污染问题亟待解决[6]。为满足日益严格的汞排放标准,近年来针对汞污染控制开展了大量研究,目前常用的汞污染控制技术主要包括①对燃煤进行洗煤处理将其中的汞进行预脱除;②利用现有污染物控制装置对烟气汞进行协同脱除;③利用氧化态汞(Hg2+)易溶于水的特点,通过加入氧化剂实现汞的形态调控从而将汞脱除;④利用吸附剂的物理吸附或化学吸附作用实现汞的吸附脱除[7]。
从脱汞效率、操作成本等方面考虑,吸附技术被认为是最具有应用前景的脱汞技术。常见的汞吸附剂包括碳基吸附剂[8-10]、钙基吸附剂[11]、矿物吸附剂[12-13]、金属氧化物[14]和分子筛[15]等材料。目前,研究人员针对上述材料已开展了广泛研究,部分吸附剂(如活性炭)已得到工业应用。研究表明,活性炭[16-19]、分子筛[20-22]具有独特的孔结构和大比表面积,对汞的吸附主要是物理吸附,通过改性或负载能有效加强汞吸附性能;金属氧化物由于含有丰富的氧活性位而具有较好的脱汞能力,并且通过载体负载可有效地提高脱汞性能和降低制备成本,其中锰基氧化物[23-26]由于脱汞性能优异而得到学者的广泛关注。上述汞吸附材料的研究主要针对燃煤烟气中汞的脱除,普遍存在对SO2、H2O 等烟气组分抗性差、脱汞性能不高等问题,无法应用于高浓度汞、高浓度SO2的有色金属冶炼烟气中汞的脱除。除上述材料外,近年来研究人员开发出MOFs 材料[27]、金属硫化物[28]、金属硒化物[29]等高性能的新型汞吸附材料,研究发现金属硫化物具有良好的抗SO2、抗H2O 性能,具有脱除有色金属冶炼烟气汞的应用潜力。
本文综述了金属硫化物吸附剂的脱汞性能和影响因素以及不同材料上的脱汞机理;介绍了通过物理或化学改性提高吸附性能的方法;阐述了金属硫化物的再生方法;最后结合当前金属硫化物脱汞的研究进展对后续研究方向提出建议。
1 金属硫化物吸附汞的研究进展
众多研究表明金属硫化物是一种高效的汞吸附剂,并对烟气中H2O、SO2等气体组分具有较好的抗性,但是脱汞性能受温度的影响较大。研究人员通过对金属硫化物进行汞吸附性能评价并结合各种表征方法,阐明了吸附活性位、揭示了汞吸附机理,在此基础上,通过一定手段对金属硫化物活性位和比表面积进行调控,从而提升其汞吸附性能。此外,研究人员针对金属硫化物的再生开展了研究,发现其具有良好的再生性能,可以实现多次循环利用,有效地降低应用成本。
1.1 金属硫化物吸附汞性能

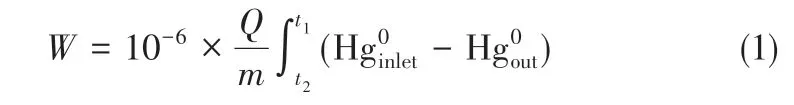
1.2 汞吸附性能的影响因素
1.2.1 反应温度
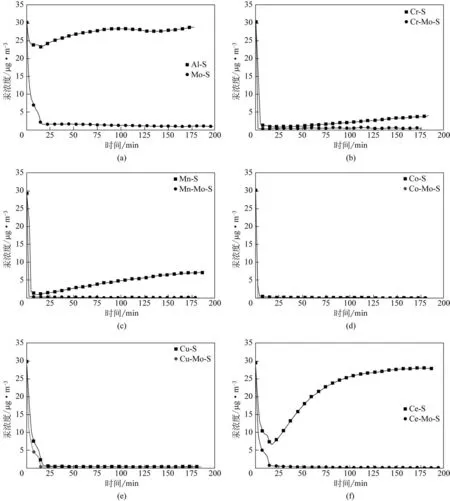
图1 不同金属硫化物的吸附性能比较
Liu 等[32]分别在50℃、100℃、150℃条件下对CoS进行了汞吸附性能评价,结果表明:在50℃和100℃条件下,吸附4h后脱汞效率均接近100%,当反应温度提升至150℃时,脱汞效率显著下降,在吸附4h 后仅为10%,汞程序升温脱附(Hg-TPD)实验结果表明,CoS 上汞的吸附产物在150℃左右开始分解。Zhao 等[41]研究了温度对MoS2吸附性能的影响,结果表明材料在50℃时的脱汞性能最佳,脱汞效率高达100%,同样随着反应温度的升高其脱汞效率逐渐降低。Yang等[36]在不同温度下对CuS进行预处理,图2 为CuS 在不同预处理温度下对Hg0的吸附穿透曲线,结果表明随着预处理温度的升高,汞吸附性能下降。热重和透射电镜(TEM)分析结果表明,当温度高于175℃时,CuS 的结构发生转变,生成吸附性能差的Cu9S8和Cu1.8S,并且高温处理后CuS颗粒发生聚集,结构遭到破坏。因此,温度对金属硫化物吸附性能的影响主要来自两方面。一方面,在高温条件下,生成的吸附产物发生分解,从而影响汞吸附性能;另一方面,在高温条件下,吸附剂结构发生变化,出现颗粒聚集和内在结构遭到破坏的现象,影响吸附性能。如何提高金属硫化物高温下的吸附性能有待进一步研究。
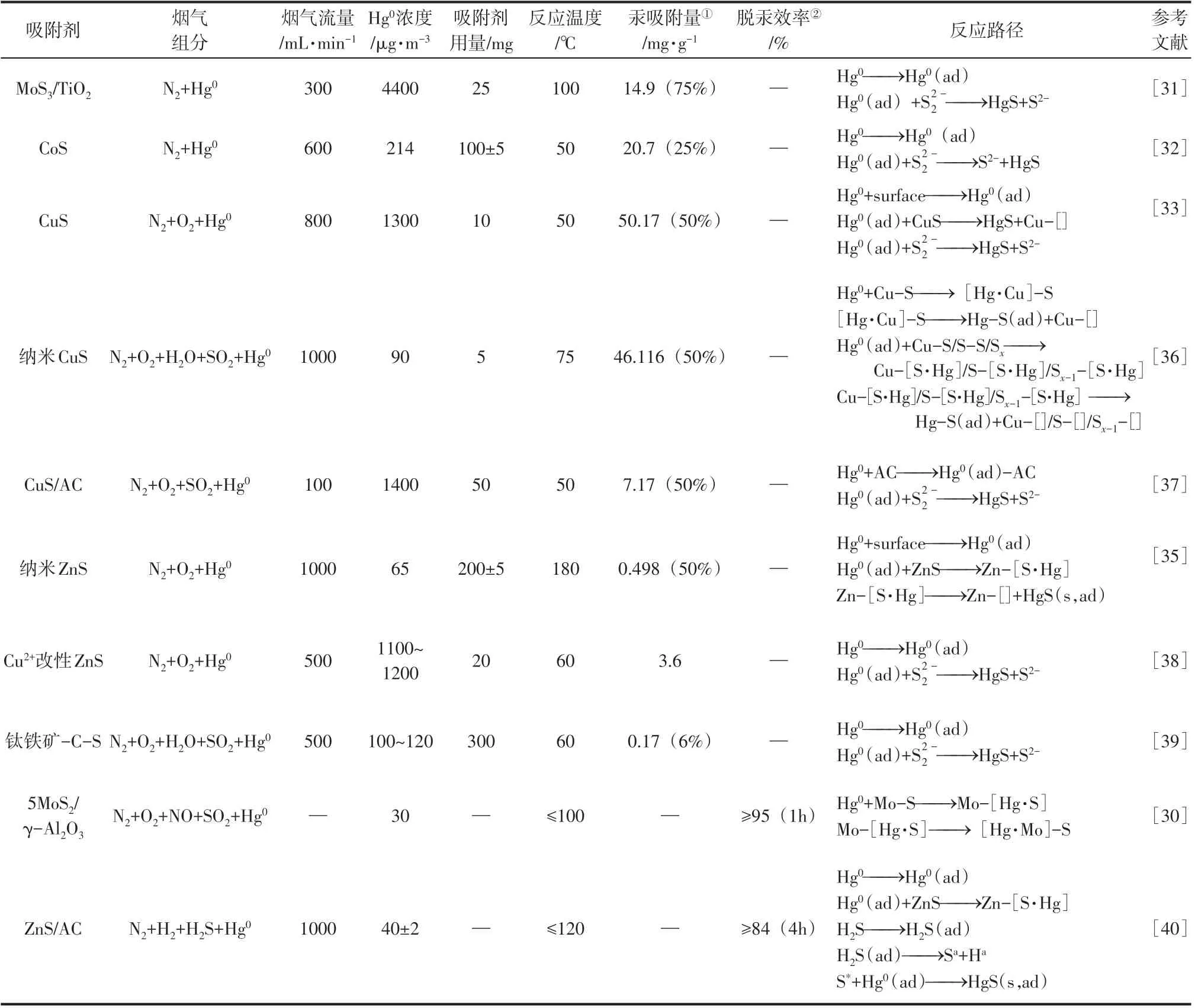
表1 金属硫化物汞吸附材料的研究进展总结
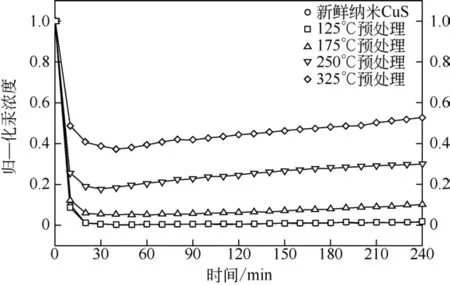
图2 不同温度预处理的CuS样品Hg0吸附穿透曲线[36]
1.2.2 气体组分

此外,Li等[46]研究发现Cl2可在ZnS(100)表面解离成氯离子从而形成含氯ZnS,表面活性氯离子对Hg0的电子有很强的吸引能力,促进Hg0氧化生成稳定的HgCl2和HgCl,因此在Cl2存在的条件下ZnS的脱汞能力得到增强。
1.2.3 空速
空速是影响材料吸附性能的重要参数。Liu等[33]研究了空速对CuS脱汞性能的影响,在空速为8.5×105h-1(远高于实际吸附系统的空速)条件下,汞脱除率可长时间(570min)保持在100%,随着空速的升高脱汞效率降低。Zhao等[41]研究了不同空速对MoS2吸附性能的影响,结果表明当空速为4.5×105mL/(h·g)时,250min 后汞脱除率为66.7%,在空速为4.5×104mL/(h·g)时,吸附2000min 后,汞的脱除率仍然为100%。Zhao等[30]将质量分数为5%的MoS2负载在商业介孔γ-Al2O3上,发现当空速由3.9×104mL/(h·g)提高到7.8×104mL/(h·g)时,其脱汞效率仅由100%下降至95%。金属硫化物在高空速下具有较好的脱汞性能,但是空速不宜过高,将其负载在载体上时有利于提升高空速条件下的汞吸附性能。
1.2.4 光氧化
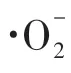

图3 紫外光辐射条件下ZnS吸附汞机理图[47]
1.3 金属硫化物吸附汞机理
1.3.1 吸附活性位点
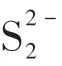

图4 Nano-CuS的汞吸附活性位点分布[36]
1.3.2 吸附机理
金属硫化物对Hg0的吸附作用主要是化学吸附。Yang 等[36]用XRD、Hg-TPD、XPS 表征方法系统研究了汞吸附机理,XRD结果表明,由于CuS在平滑晶面(001)上发生结构重建,有利于形成与Hg0结合力强的聚硫;此外CuS上存在由范德华力结合的二元硫,易发生分解并与烟气中的Hg0反应。Li等[45]通过DFT 证明了Hg0在CuS(001)晶面发生化学吸附,Hg0的结合能表明具有两个硫末端[CuS(001)-S-2]的晶体表面比具有铜和硫末端[CuS(001)-Cu/S]的晶体表面具有更好的Hg0吸附活性,模拟结果与实验结果相符。Li 等[35]对吸附后的ZnS 进行XPS 表征,在100.8eV 观察到明显的Hg 4f 特征峰,但并未发现Hg0在99.9eV 处的特征峰,此外还观察到161eV 和162.2eV 处的S2-特征峰,据此推测Hg0与硫活性位发生化学吸附生成HgS化合物。Mu等[48]利用过DFT研究了Hg0在MoS2上的吸附机理,发现汞原子的d轨道和硫原子的s轨道以及钼原子的p、d轨道发生明显的重叠,导致Hg0与1T-MoS2表面产生强相互作用。
1.4 金属硫化物的改性
目前的研究表明,金属硫化物具有较好的汞吸附能力,具备应用潜力。为降低应用成本,近年来,研究人员就如何提升金属硫化物的吸附性能开展了大量研究。由于金属硫化物的汞吸附性能受自身物理性质、结构以及表面活性位数量的影响,可以采用合适的改性方法调控表面活性位数量,增大比表面积,提高活性位分散程度等方式提高汞吸附性能。
1.4.1 活性位调控
Zhao等[49]发现采用微波辐射处理可以增加MoS2表面活性位数量,相比于传统的制备方法得到的样品,180min 内脱汞效率提高3%,并且微波处理超过3次后的样品其脱汞效率仍明显高于传统制备方法。结合表征和DFT 结果,研究人员推断经过微波处理的MoS2晶体的(001)基面破裂成(100)基面,促进表面形成更多的边界活性位,从而提升了MoS2的吸附性能。由于S1-对Hg0具有更强的亲和力,更有利于汞的化学吸附,Liao 等[38]采用含Cu2+的溶液浸泡ZnS,将S2-可控地氧化成S1-,使其表面生成活化层(如图5所示)而提高界面活性,实验结果表明,处理后的ZnS 样品,其汞吸附量由0.3mg/g提高到3.6mg/g。

图5 Cu2活化后的ZnS样品的HRTEM图及活化前后Hg0吸附量对比[38]
1.4.2 比表面积调控
(1)制备方法 采用合适的制备方法可以得到大比表面积的金属硫化物,有利于活性位点的充分暴露,从而提高吸附性能。Quan 等[50]在150℃下以Co(NO3)2/Na2S、Co(NO3)2/Na2S2O3为前体,通过水热法合成两种硫化钴吸附剂材料,比表面积分别为3.71m2/g(S-1)、23.56m2/g(S-2)。实验结果表明:S-2 样品在200min 内的脱汞效率保持为100%,而S-1 样品在吸附40min 后汞开始穿透,且吸附200min时,汞脱除效率下降至40%。Li等[35]采用液相沉淀法制备ZnS,通过改变陈化时间和十六烷基三甲基溴化铵用量,所得样品的比表面积分别为64.6m2/g、105.9m2/g 和196.1m2/g,均高于商业ZnS(28.3m2/g)。如图6 所示,样品的脱汞性能与比表面积呈现正相关性,其中比表面积最大的ZnS样品在反应4h后汞脱除率仍超过80%。Sun等[51]分别用羧甲基纤维素钠、凝胶和淀粉这3种生物材料作为FeS 的稳定剂,减少FeS 纳米颗粒的聚集。TEM 结果表明,单一FeS 颗粒分布不均匀,发生聚集现象,经过稳定剂处理的FeS颗粒分布更加分散和均匀,未发生明显的颗粒聚集,使得活性位得到充分暴露,进一步通过吸附实验发现,当3种稳定剂与FeS 的质量比为1∶6 时最大的吸附量分别约为1726mg/g、1939mg/g、1989mg/g,是单一FeS 吸附量的两倍多。
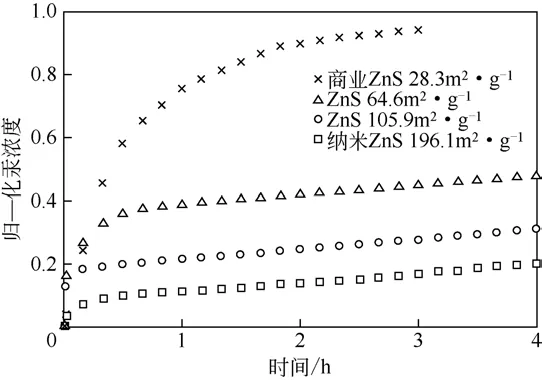
图6 不同比表面积的ZnS样品汞吸附性能对比

1.5 金属硫化物吸附剂再生
1.5.1 热硫溶液/H2S处理再生
金属硫化物具有良好的可再生性,再生后仍能保持较好的汞吸附性能。Quan 等[50]将使用后的吸附剂浸渍在含有S 单质的热混合溶液中进行再生,在5 次吸附-再生实验中,吸附量基本在1.10~1.30mg/g之间,并且穿透曲线十分接近,材料的吸附量和吸附速率均得到有效恢复。Zou 等[39]采用TPD 对吸附的汞进行脱附处理,并采用焙烧加H2S处理的方法对吸附剂进行再生,通过进行5 次吸附-脱附-再生循环实验,发现采用该方法再生的吸附剂汞脱除效率几乎接近100%。
1.5.2 离子溶液浸泡再生
Liao 等[38]研究发现,将使用后的ZnS 浸泡在Cu2+溶液中,其活性可得到恢复,XPS 和高清透射电镜(HRTEM)表征结果表明,经过Cu2+处理后,ZnS表面形成活化层,并生成S-物种。通过对比实验发现,经过Cu2+活化的ZnS 的汞脱附峰出现在250℃,表明材料表面生成了HgS;而经H2O 处理的ZnS 样品,汞脱附峰出现在150℃以下,说明汞以物理吸附形式存在于材料上,在循环实验中,汞的穿透曲线呈现高度的一致性,说明Cu2+溶液浸泡确实可以实现ZnS的再生。
2 结语与展望
本文对金属硫化物脱汞性能、影响因素、脱汞机理、改性和再生方法进行了综述。由于硫化物含有丰富的硫活性物种,可与Hg0发生化学吸附生成稳定的HgS,从而能够实现将烟气中的Hg0高效吸附脱除,烟气中常见的气体组分H2O、SO2对其吸附性能的影响很小,此外硫化物能实现多次再生重复使用而降低成本。目前对金属硫化物吸附脱除烟气汞的研究已获得显著成果,但是还存在一些问题需要进行深入研究:①金属硫化物脱汞的温度窗口一般为50~180°C,高温时脱汞性能显著降低,需要对材料结构或活性位进行调控强化其高温下的性能;②目前一般采用加热法实现汞的脱附,导致高温下金属硫化物结构发生改变从而影响汞吸附性能,而且消耗大量能量,如何实现较低温度下金属硫化物表面汞的脱附也是未来值得深入研究的方向。
