巩膜瓣下应用黏弹剂对青光眼白内障联合术后前房的影响
2020-12-04张庆华
张庆华
0引言
原发性闭角型青光眼(primary angle closure glaucoma,PACG)是一种不可逆的致盲性眼病,其致盲率仅次于白内障,现居世界致盲眼病的第2位,是亚洲最常见的青光眼, PACG合并白内障患者的青光眼急性发作其主要致病因素是房角狭窄与晶状体膨胀,两者在本病的发生与发展过程中相互促进,相互影响。传统的治疗方法为Ⅰ期根据患者房角粘连和关闭情况选择周边虹膜切除术或滤过性手术,Ⅱ期行白内障手术治疗。随着白内障超声乳化技术的快速发展,越来越多的学者支持Ⅰ期通过晶状体摘除手术、加深前房、开放房角来治疗闭角型青光眼[1-2]。若已发生大范围房角关闭或粘连,则可联合滤过性手术[3]。我院采用小梁切除联合白内障超声乳化人工晶状体植入手术方式,术中结合巩膜瓣下使用黏弹剂,治疗38例38眼原发性闭角型青光眼合并白内障患者,效果良好。该方法有效防止了术后浅前房并发症,我们在术后应用OCT对早期前房深度及房角开放情况进行观察,总结报告如下。
1对象和方法
1.1对象选择我院2016-08/2018-08收治的闭角型青光眼急性发作合并白内障患者38例38眼,均为女性和单眼急性发作入院,所有患者既往均已有急性发作病史,房角关闭大于180°以上,使用3种降眼压药物也无法控制眼压,故选择联合小梁切除术而非单纯白内障手术,排除患有其他缺血性眼病或糖尿病、颈动脉疾病等影响前房角的患者。随机分为两组,其中应用黏弹剂组19眼,平均年龄66.10±4.13岁,术前平均眼压43.32±5.21mmHg;常规手术组19眼,平均年龄65.35±6.52岁,术前眼压44.62±4.81mmHg。两组患者年龄及眼压比较差异无统计学意义(P>0.05)。所有入组患者均经过详细的术前谈话,经医院伦理委员会审批通过,接受随机分组手术方案,签署手术意向书及手术知情同意书。
1.2方法
1.2.1术前准备所有患者均于术前给予局部和全身降眼压治疗。手术日眼压均降至30mmHg以下,平均18.30±7.25mmHg,角膜大致恢复透明,可分辨晶状体前囊膜。术前30min快速静滴甘露醇,全部手术由同一经验丰富的医生完成。术前常规应用妥布霉素地塞米松滴眼液滴眼3d。术前30min采用复方托吡卡胺滴眼液散瞳,采用利多卡因球后麻醉并充分按压眼球降低眶压和眼压,奥布卡因进行表面麻醉。
1.2.2手术方法常规手术组患者患眼上方12∶00 ~ 14∶00处穹窿为底的结膜瓣下作3mm×4mm板层巩膜瓣,将棉片浸润0.04%的MMC后放置于巩膜床,约3min再去掉,平衡液彻底冲洗瓣下及结膜囊,上方11∶00位做透明角膜切口,3∶00位做前房穿刺侧切口,注入黏弹剂加深前房,并适当分离周边虹膜与房角,撕囊镊连续环形撕囊(因多伴有晶状体膨胀,应使用足量黏弹剂将前囊膜压平,并及时补充),充分水分离、水分层,超声乳化晶状体核并吸除晶状体核,I/A模式吸除残留晶状体皮质,行后囊膜抛光,在黏弹剂保护下植入可折叠人工晶状体并调正,吸除前房黏弹剂,切口水密。切除巩膜瓣下1.0mm×2.5mm小梁组织,行虹膜周边切除,10-0 尼龙线缝合巩膜瓣两顶角,结扎时松紧适中,连续缝合球结膜,手术结束。
应用黏弹剂组手术方法同上,在完成虹膜周切和小梁切除后,在巩膜瓣、床间向前房方向注入少量黏弹剂,直视下见黏弹剂经滤过口进入前房,虹膜周切口展开并后移,并有少量黏弹剂自巩膜瓣下溢出,瓣呈轻微隆起状态,保留瓣旁结膜下溢出的黏弹剂,缝合结膜,结束手术。
两组术毕均以妥布霉素地塞米松眼膏涂眼。术后常规妥布霉素地塞米松滴眼液滴眼,每日4 次,持续2wk。
1.2.3观察指标检查并记录手术后1、3、7d的房角情况。应用OCT(TOPCON,3D OCT-1)对房角的相关参数进行测量,包括前房深度(anterior chamber depth,ACD)、巩膜突前500μm房角开放距离(angle opening distance,AOD500)、 小梁虹膜夹角(trabecular iris angle,TIA)[4-5]。
统计学分析:采用SPSS11.5统计学软件处理,观察指标计量资料采用均数±标准差表示,比较应用黏弹剂组和常规手术组在术后1、3、7d共3个时间点各项观察指标的差异,采用重复测量数据的方差分析,两组比较采用独立样本t检验,P<0.05 为差异有统计学意义。
2结果
2.1两组患者术后ACD比较两组患者术后ACD比较差异有统计学意义(F时间=21.23,P时间<0.001;F组间=69.58,P组间<0.001;F组间×时间=55.07,P组间×时间<0.001)。术后1、3d,两组患者ACD比较差异有统计学意义(P<0.05);术后7d,两组患者ACD比较差异无统计学意义(P>0.05),见表1。

表1 两组患者术后ACD比较
2.2两组患者术后AOD500比较两组患者术后AOD500比较差异有统计学意义(F时间=15.90,P时间<0.001;F组间=20.95,P组间<0.001;F组间×时间=5.42,P组间×时间=0.015)。术后1、3d,两组患者AOD500比较差异有统计学意义(P<0.05);术后7d,两组患者AOD500比较差异无统计学意义(P>0.05),见表2。

表2 两组患者术后AOD500比较
2.3两组患者术后TIA比较两组患者术后TIA比较差异有统计学意义(F时间=3.84,P时间=0.04;F组间=80.48,P组间<0.001;F组间×时间=13.76,P组间×时间<0.001)。术后1、3d,两组患者TIA比较差异有统计学意义(P<0.05);术后7d,两组患者TIA比较差异无统计学意义(P>0.05),见表3。
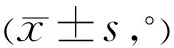
表3 两组患者术后TIA比较
2.4两组患者术后眼压比较两组患者术后眼压均显著降低至20mmHg以下,术后1d应用黏弹剂组眼压高于常规手术组,差异有统计学意义(P<0.05);术后7d两组患者眼压差异无统计学意义 (P>0.05),见表4。

表4 两组患者术后眼压比较
3讨论
OCT作为一种客观的光学检查设备,较其他的房角检查方式有很多优点[6-8]: (1) 患者易于接受非接触性检查,可避免感染、损伤;(2)实时显像,动态观察,便于针对性定位和测量;(3)比超声生物显微镜(UBM)更高的图像分辨率;(4)适用于急性闭角型青光眼,因高眼压性角膜水肿使前房角镜和UBM检查难以进行。非接触性检查的优点在于可减少机械性接触的组织变形而造成前节测量的误差,与UBM和前房角镜相比,OCT 能对眼前段结构尤其是虹膜膨隆状态,房角入口变化以及包含整个角巩膜缘在内的眼前节横截面结构采集图像,进行ACD、AOD、TIA等参数的测量,实现房角形态结构的定量分析,为临床、科研、教学提供更多的便利[9]。既往对于青光眼白内障联合手术的研究,相关报道的侧重点多是疗效指标,对于房角变化这一关键因素的观察则较少,相较于眼压,观察房角的变化,可以更加直观准确地评估手术效果[10]。
统计表明,全球约有6700万PACG患者,而我国50岁以上人群PACG的发病率约为1.1%,其中女性居多。闭角型青光眼的主要发病机制是由于眼前段解剖结构异常,虹膜接近甚至粘连于小梁网,导致房水流出通道关闭,眼压升高,该房角关闭可由反复的瞳孔阻滞引起,而晶状体膨胀则是引起瞳孔阻滞的关键因素。尤其合并白内障的情况下,膨胀的晶状体推动虹膜前移,加剧瞳孔阻滞[11]。传统治疗方法是根据房角关闭及粘连程度选择滤过性手术或周边虹膜切除术,但这并没有清除导致房角关闭的主要原因,仅仅是对症治疗,后期易反复发作,造成多种并发症和视功能的损害。目前超声乳化术已成为治疗闭角型青光眼的主流术式[12-13],手术摘除晶状体,增加眼前节空间,解除了晶状体所致瞳孔阻滞因素,同时在手术过程中,超乳能量传导的冲击及灌注液的压力可使房角增宽和粘连减少,再结合针对性的房角冲洗或黏弹剂分离,能从多方面促进房角的开放,是较传统手术更优胜的对因治疗[14-15]。本文观察患者既往均已有急性发作病史,房角关闭大于180°以上,使用3种降眼压药物也无法控制眼压,故选择联合小梁切除术而非单纯白内障手术,黏弹剂的主要成分玻璃酸钠是构成细胞间质和细胞外基质的重要成分,具有细胞粘合、渗透压调节等生理功能。其生物相容性优良且无毒性,广泛应用于眼科手术中。其粘滞性、假可塑性等特点,在手术中起填充、保护、润滑作用,能提高手术质量和手术治疗的安全性。注入前房内的黏弹剂可经多种房水引流通道清除到眼外[16 ]。
浅前房是青光眼滤过手术后的早期常见并发症,发生率一般在4.8%~70%之间,原因为房水滤过过强、结膜瓣渗漏、脉络膜脱离及房水生成减少等,最常见原因是房水滤过过强,所以防止术后浅前房要从减少术后早期房水滤过量着手。本文研究中,在切除小梁缝合巩膜瓣后,在巩膜瓣下注入黏弹剂,能迟滞房水引流,开放房角,使前房加深,从而避免浅前房发生,减少术后早期低眼压及脉脱的发生[17-18]。巩膜瓣下注入黏弹剂能产生以下作用:(1)加深、稳定前房作用,减少因此而引起的并发症。本研究中,术后3d内,应用黏弹剂组的前房深度、房角开放距离和虹膜小梁角均比常规手术组显著改善。滞留在滤过通道的黏弹剂暂时增加流体阻力,减少房水引流量,使前房压力和深度相对平稳,前房内容量增加,阻止浅前房的发生,也降低了低眼压及脉络膜脱离的风险。术后7d时,滤过道局部滞留的黏弹剂逐渐被房水水化,流动性增加,在房水持续生成和眼压上升作用下,逐渐从滤过口排出到结膜下,解除了黏弹剂维持的暂时性滤过道阻力,逐渐恢复房水的引流,避免眼压进一步增高,同时使黏弹剂的前房效应消失,由此可以解释本文病例观察到术后7d时,两组的OCT检查结果已无显著差异。而前房内仍残留的极少量黏弹剂可通过小梁网排出。(2)巩膜瓣下和结膜下的黏弹剂,使瓣与床之间、瓣与结膜之间被物理隔离,也在术后早期相对增加了房水引流阻力。(3)闭角型青光眼急性发作的白内障病例,同时存在前房炎症反应,房角往往发生粘连和虹膜堆积,少量的黏弹剂通过小梁切口进入前房的过程中,可将嵌于切口的堆叠虹膜推离房角,减少虹膜粘连,使滤过口通畅。同时其弹性还可压迫、阻止术区及虹膜、睫状体的渗血,减少血块堵塞滤过口。
注入黏弹剂的注意点:(1)注入过程需缓慢、均匀,注意保证黏弹剂在巩膜瓣下向小梁切口逐渐推进,防止房水过度流失,同时注意观察根切口变化,使粘连的房角开放,提高手术成功率。注射针头不能进入前房,否则有可能使人工晶状体移位及眼内出血等。(2)注入量不要太多,否则术后易引起高眼压等并发症,一般以直视见虹膜周切口展开并稍后退为宜。(3)进入前房的黏弹剂主要停留在根切口处,在后期大部分水化后经滤过道排出,术后无须使用抑制房水药物,若术后眼压偏高,可予临时药物处理,如静滴甘露醇等。
在青光眼白内障联合术中应用瓣下黏弹剂,无毒副作用,可逆性的改善术后早期房角结构,在不增加并发症的基础上,减少了术后浅前房的发生,能有效促进房角开放、增宽,促进有效滤过泡的形成,加快和改善了术后的恢复,效果确实,值得进一步研究应用。
3陈君毅, 孙兴怀, 陈雪莉. 合理应用晶状体摘除手术治疗原发性闭角型青光眼. 中华眼科杂志 2020;56(1):9-12
