靛红双腙类化合物生物活性的研究进展
2020-12-04余婕于健严国兵
余婕,于健,严国兵
靛红双腙类化合物生物活性的研究进展
余婕,于健,严国兵*
(丽水学院,浙江 丽水 323000)
靛红双腙类化合物是一种重要的靛红衍生物,具有多种生物活性。为了进一步研究靛红双腙类化合物的生物活性与其构效关系,近年来人们对其结构进行了大量的修饰和改造,合成了一些活性较强的化合物。对近年来靛红双腙类化合物的生物活性及构效关系研究进行了综述。
靛红衍生物;靛红双腙;生物活性
靛红双腙是一类靛红衍生物,它具有出广泛的生物活性,如抑菌活性[1]、杀菌活性[2]、抗癌活性[3]、抗结核活性[4],以及对神经系统的作用,如镇痛[5]、抗炎[6]等。除此之外,靛红双腙还可以充当有效的酶抑制剂[7]、缓蚀剂[8]等。HASSAN[9]等将靛红与水合肼在乙醇中回流反应,后将得到的靛红腙与芳香醛在乙醇中进行缩合反应,得到相应的靛红双腙化合物。近年来,人们对靛红双腙类化合物的结构进行了大量的修饰,得到了一些研究成果,本文将对靛红双腙类化合物的生物活性及构效关系进行归纳和总结。
1 靛红双腙类化合物的抗菌活性
YOUSSEF[1]等设计合成了一系列靛红双腙衍生物(化合物1~5),以革兰氏阳性菌和革兰氏阴性菌为试验菌,研究化合物对多种微生物的抗菌活性。使用的细菌有:枯草芽孢杆菌、白色葡萄球菌、铜绿假单胞菌和大肠杆菌。使用纸片技术进行测试,结果表明,所制备的衍生物对所有类型的细菌都表现出一定的活性,抑制率在45%~70%之间。

图1 化合物1~5的结构式
MURUKAN[10]等合成了一系列靛红双腙金属配合物。根据元素分析、摩尔电导率、磁化率数据、紫外吸收可见光谱、红外吸收可见光谱、电子顺磁共振光谱和核磁共振光谱研究,对配合物进行了表征。分析数据表明,镍(II)、铜(II)和锌(II)配合物具有1∶1的金属配位比,锰(II)、铁(II)和钴(II)配合物具有1∶2的配位比。红外光谱数据表明,双腙表现为一元三齿配体。铜(II)配合物的X射线衍射研究表明其为正交晶格。电子顺磁共振光谱数据表明,金属-配体键具很强的共价性。
通过抗菌活性筛选试验,对配体和金属配合物进行了抗菌活性筛选。结果表明,所有金属配合物的抗菌活性都强于配体。这种活性的增强可以根据螯合理论来解释,螯合作用大大降低了金属离子的极性。螯合作用不仅可以降低金属离子的极性,还可以增加螯合物的亲脂性,有利于金属离子与脂质的相互作用。但螯合作用不是抗菌活性的唯一标准,金属离子的性质、配体的性质、配位位点、配合物的几何结构、浓度、亲水性、亲油性和共配体的存在以及空间和药代动力学因素对抗菌活性有重要影响。因此,金属配合物的抗菌性能不仅仅归因于其螯合作用,而是多种作用的复杂混合。
DEVI[11]等合成了一系列Co(II)、Ni(II)、 Cu(II)和Zn(II)靛红双腙金属配合物。通过元素分析、电导研究、磁化率和光谱技术(红外、紫外-可见光谱、核磁共振、质谱和电子自旋共振)进行表征,结果表明配合物为八面体或畸变八面体的单核结构。对革兰氏阳性菌、革兰氏阴性菌和真菌进行体外抑菌试验,结果表明所合成的化合物对多种微生物都有很好的抗菌活性,且其配合物的抗菌活性优于母体配体,其中Cu(LIV)(Q)·H2O(化合物6)是最有效的抗菌剂,在检测其对人体的毒性后,认为可用于食品和制药工业。

图2 化合物6的结构式
PANDEY[2]等合成了一系列新的有机磷衍生物(化合物7~16)。利用红外光谱、核磁共振氢谱和碳谱对其进行了表征。研究了化合物对镰孢炭疽菌、尖孢镰刀菌和淡色弯孢菌的杀菌活性。研究结果表明,化合物在抑制所有试验真菌的菌丝生长方面显示出很好的效果,且抗菌活性与被测化合物的结构特征有关。与磷酸盐相比,硫代磷酸盐的效价更高;与含靛红-3-(取代苯甲酸腙)的化合物相比,含靛红-3-(取代苯氧乙酸腙)的化合物的效价更高;与其他取代物相比,附着在芳香环上的取代氯效价更高。其中,化合物11和14显示出优于商业杀菌剂Bavistin、Bitox-50的杀菌性能,活性是商业杀菌剂的2~4倍。
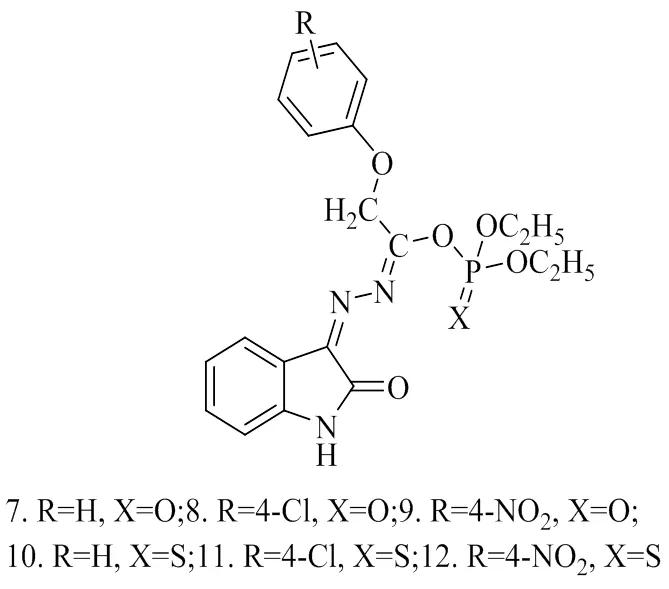
图3 化合物7~12的结构式
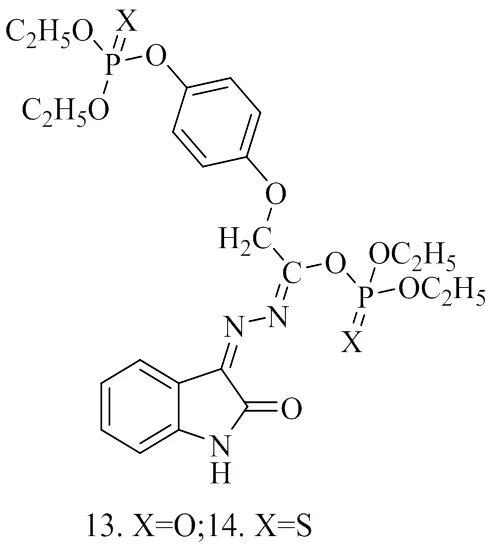
图4 化合物13~14的结构式

图5 化合物15~16的结构式
2 靛红双腙类化合物的神经系统活性
疼痛是机体受到伤害性刺激后产生的一种保护性反应,常伴有恐惧、紧张、不安等情绪活动。镇痛药主要作用于中枢或外周神经系统,选择性抑制和缓解各种疼痛。发炎指生物组织受到外伤、出血、或病原感染等刺激,激发的生理反应,其中包括了红肿、发热、疼痛等症状。抗炎药是用于治疗组织受到损伤后所发生的反应炎症的药物。
KHAN[5]等合成了8个靛红双腙衍生物(化合物17~24),采用涡流热板法对白鼠进行镇痛活性测定。根据基础反应时间的结果记录在表一中,证明该系列化合物具有一定镇痛活性,但效果弱于阿司匹林。

图6 化合物17~24的结构式
KHAN[6]等设计合成了27个靛红双腙化合物(化合物25~32),并对其抗炎活性和细胞毒性进行了评价。其中,化合物25~32表现出不同程度的呼吸爆发抑制活性,IC50值在242.97~652.12 μM之间。与标准消炎药(IC50= 271.12±1.12 μM)相比,化合物26、27、28、29、30、31和32显示出不同的抗炎活性。化合物26(IC50= 242.97±2.24 μM)表现出比标准消炎药更好的活性,化合物27和30表现出一定的抗炎作用,IC50值分别为470.11±2.42和429.97±3.42 μM,而化合物29、31和32分别表现出IC50值492.71±6.12、495.12±2.02、519.12±1.93 μM,其他所有化合物显示出低于50%的抑制作用,被认为是不活跃的。比较化合物26和吲哚美辛的抗炎活性,化合物26的活性更高,表明吲哚骨架是抗炎活性的先决条件,化合物26和27两倍的活性差异是由于萘键的不同,而结构类似于化合物26和27的化合物25完全失活似乎是由于吲哚部分的C-4和C-7处的两个Cl取代基引起的。一般来说,与其他取代基相比,R4的性质似乎对化合物抗炎活性有更大的影响。经卤虫致死试验,对化合物细胞毒性进行评价,结果表明化合物25~32对卤虫无细胞毒性。综上所述,化合物26可作为先导化合物,其更密切相关的合成修饰分子可作为更有效的抗炎药出现。
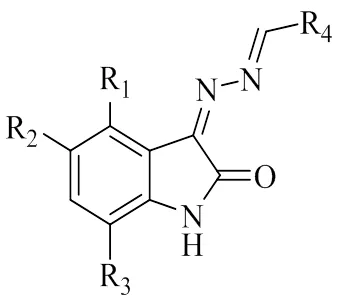
图7 化合物25~32的结构式
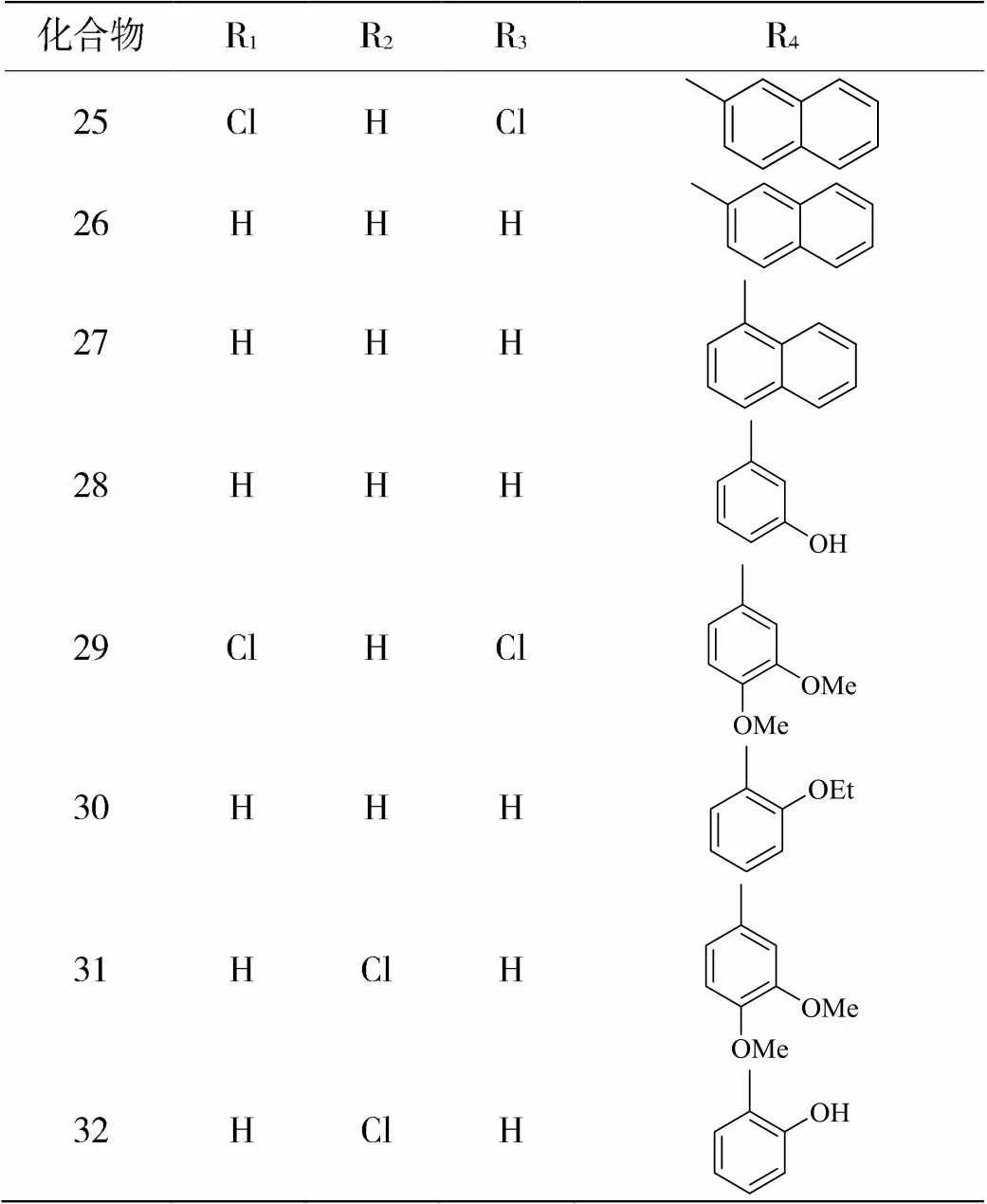
表1 化合物25~32的结构式
3 靛红双腙类化合物抗癌、抗结核活性
癌是指起源于上皮组织的恶性肿瘤,是恶性肿瘤中最常见的一类。结核是一种由结核杆菌感染引起的慢性传染病。
ELDEHNA[3]等采用混合药效团法设计合成了一系列新的靛红双腙-吡啶杂化物(化合物33~36),研究其对HepG2肝癌、A549肺癌和MCF-7乳腺癌细胞的体外抗增殖活性。结果表明,所合成的杂交种对所检测的癌细胞株具有良好的生长抑制活性。化合物33和34的IC50分别为11.5±1.05 μM和 8.7±0.91 μM,对HepG2癌细胞株具有良好的抑制作用。在抗A549活性方面,化合物34的IC50值为10.8±1.15 μM,是活性最强的类似物,它们的效价比阿霉素低了1.4倍(IC50= 7.6±1.37 μM),化合物33和35(IC50= 19.7±2.59和16.8±1.92 μM)对A549表现出良好的活性。根据MCF-7细胞的细胞毒性评价显示,化合物33、35和36的IC50分别为 10.4±1.47、14.7±2.82、14.9±1.04 μM,化合物34对MCF-7细胞系的IC50值为6.3±0.79 μM,几乎与阿霉素(IC50= 6.1±1.95 μM)相等,成为本研究中抗MCF-7最有效的药物。
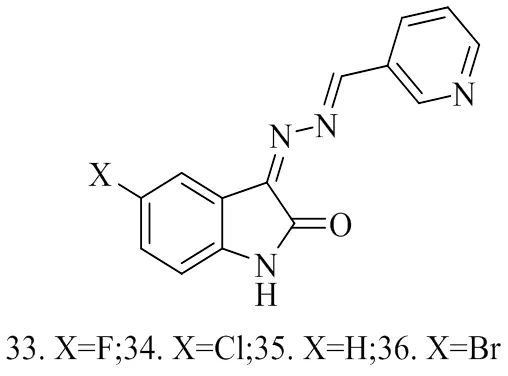
图8 化合物33~36的结构式
KARUNANIDHI[4]等合成了30个靛红双腙衍生物(化合物37~44),并对其进行抗结核活性筛选。结果表明,这些化合物对结核分枝杆菌H37Rv的活性在2.3~200 μM之间,其中,具有杂环的化合物表现出更强的活性。化合物37(MIC= 2.3 μM)和38(MIC= 17 μM)显示出极好的抗结核活性。对两种抗分枝杆菌化合物37和38进行二级筛选,比较了两种化合物在有氧条件下对结核分枝杆菌的耐药菌株、金黄色葡萄球菌和铜绿假单胞菌等的MIC值。被测化合物的数据表明,它们对所有菌株都具有中等至优异的活性。其中,化合物37对耐药菌株(INH-R1和INH-R2)均表现出良好的活性,对利福平耐药株(RIF-R1和RIF-R2)表现出中等的活性,对氟喹诺酮耐药株(FQ-R1)表现出较低的活性,而化合物37对所有菌株均表现出中等的活性。化合物39、40、41、42、43、44也表现出较好的抑制活性。其中,化合物40、41和42表现出较高的抗真菌活性,MIC值分别为7.0、9.0、5.6 μM,IC50值分别为3.9、6.4、3.9 μM。化合物43和44表现出中等活性,MIC值分别为34、77 μM。进一步研究最具活性的化合物40和42对耐药分枝杆菌的抗菌活性。化合物40对INH-R1和INHR2菌株的IC50分别为3.4、5.3 μM,对RIF-R1和RIF-R2菌株的IC50值分别为1.9、8.4 μM,对氟喹诺酮耐药菌株的IC50值为4.9 μM,均表现出较好的活性。化合物42对所有抗性菌株的IC50值在11~27 μM之间,表现出中等活性。
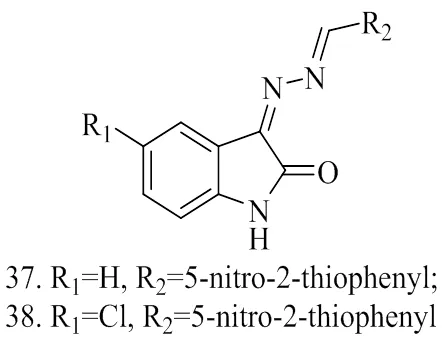
图9 化合物37~38的结构式

图10 化合物39~44的结构式
4 靛红双腙类化合物的其他活性
许多病原微生物依赖于它们的宿主来获得关键的代谢物,例如,所有寄生原生动物(如疟原虫、弓形虫、利什曼原虫、锥虫等)都缺乏从头合成嘌呤核苷酸的能力。取而代之的是,这些生物体依靠补救酶从宿主体内获得嘌呤碱和核苷,并将其转化为相应的核苷酸。因此,通过对补救酶的作用,干扰嘌呤回收可能是杀死这些生物的有效方法之一。
SOMOZA[7]等为了探索这一观点,试图阻断寄生原生动物胚胎三毛滴虫的嘌呤补救途径,胚胎三毛滴虫的嘌呤补救主要依赖于一种酶(HGXPRTase)。SOMOZA等人详细比较了胚胎HGXPRTase和人血红蛋白酶的活性位点,利用对接算法筛选具有HGXPRTase抑制作用的化合物。他们设计合成并分析了22种化合物,其中化合物 45~48为靛红双腙类化合物。这22种化合物中有18种(82%)的IC50低于1 mM筛选阈值,10种(45%)抑制HGXPRTase的效价等于或高于两种原始抑制剂的效价。此外,其中一些化合物对胚胎HGXPRTase的抑制作用明显强于人血红蛋白酶。

图11 化合物45~48的结构式
KHAN[12]等设计合成了一系列靛红双腙化合物(化合物49~51),研究其构效关系,并用光谱技术对所有化合物进行表征。经抗糖化试验,确定了一系列潜在的分子作为抗糖基化剂。结果表明,所有化合物的抗糖化活性IC50值在243.95~634.05 μM之间。其中,化合物49(IC50= 243.95 ± 4.59 μM)、50(IC50= 257.61 ± 5.63 μM)和51(IC50= 291.14 ± 2.53 μM)的抗糖化活性均优于标准品(芦丁,IC50= 294.46 ±1.50 μM)。化合物49和50具有分别位于邻位和对位的硝基,硝基与甲基乙二醛的羰基形成具有很高的抗糖化活性的配合物。类似地,化合物51所具有的高抗糖活性可能是由二羟基类似物与甲基乙二醛的羰基反应生成缩醛所致。
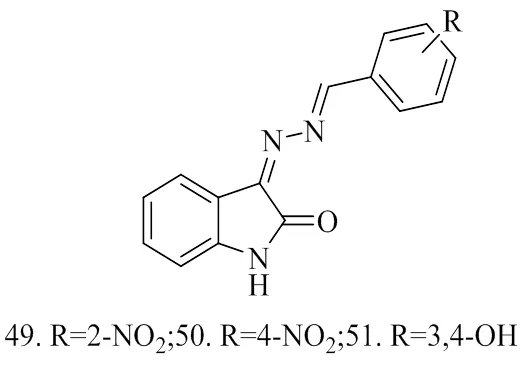
图12 化合物49~51的结构式
KHAN[13]等根据先前的研究发现,氧化应激似乎参与了糖尿病的病理生理学和代谢综合征的心血管并发症。鉴于上述糖尿病与氧化应激之间的关系, KHAN等决定重新合成一系列靛红双腙化合物(化合物52~56),筛选它们的抗氧化潜力,经超氧阴离子自由基清除活性和DPPH自由基清除活性的体外测定,结果显示,有4种化合物表现出不同程度的超氧阴离子自由基清除活性(IC50=156.34~273.15 μM),化合物52(IC50=156.34 ± 0.22 μM),化合物53(IC50=273.15 ± 1.60 μM),化合物54(IC50= 224.12 ± 0.80 μM),化合物55(IC50=225.03 ± 0.73 μM),与标准没食子酸没食子酸酯(IC50=104.04 ± 1.70 μM)相比,它们具有良好的超氧阴离子自由基清除活性,且化合物52和化合物56表现出良好的DPPH自由基清除活性,其IC50值分别46.63 ± 0.26、436.90 ± 0.59 μM。其中,化合物52在其以前的研究中显示出优异的抗糖基化活性,在此次研究中显示出合理的超氧阴离子自由基和DPPH自由基清除活性。他们猜测化合物52清除自由基的活性可能与儿茶酚部分有关。

图13 化合物52~56的结构式

表2 化合物52~56的结构式
2015年同课题组成员KHAN[14]等再次合成了一系列靛红双腙化合物(化合物57~61),并研究了其对利什曼原虫的杀灭作用。在27个化合物中,化合物57、58、59、60和61为潜在的抗利什曼原虫化合物,表现出不同程度的抗利什曼原虫活性,其IC50值分别为44.86±0.66、65.27±0.38、76.58±0.30、46.51±0.36、84.05±0.23 μM,其余化合物IC50值大于100 μM,均无抗利什曼原虫活性。化合物58(IC50=65.27±0.38 μM)较化合物57活性略有下降,可能是邻位甲氧基的羟基质子被甲基保护所致。
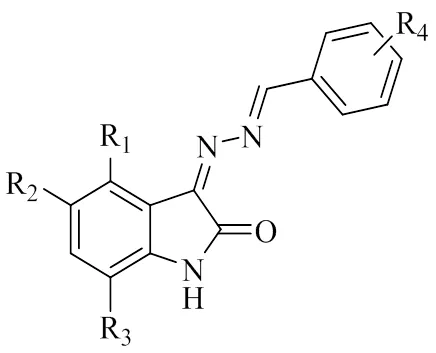
图14 化合物57~61的结构式

表3 化合物57~61的结构式
MUSHARRAF[15]等探索了一类新的靛红双腙作为UV-LDI基质,用于MALDI-TOF-MS分析低分子量肽,并将基质的性能与其化学结构关联起来。化合物的选择标准是基于MALDI基质所需的结构特征,即共轭芳香体系、λmax等,筛选出4种具有必需功能的靛红双腙衍生物作为潜在基质。化合物62在用于分析缓激肽时产生非常高的强度,且在用于分析肾素肽时,显示出类似的结果。总的来说,新开发的基质产生了具有高重复性的分析物的优良信号强度。然而,这些新的基质在低质量区几乎没有观察到背景信号,发现适合用于分析小分子。为了评价新基质在小分子分析中的性能和观察在低质量区产生的背景信号,对两种低相对分子质量化合物胆酸(408.57 Da)和鹅去氧胆酸(392.57 Da)进行了分析。用化合物63作为基质,分析胆酸(0.1 μM)溶液,显示出极好的再现性。
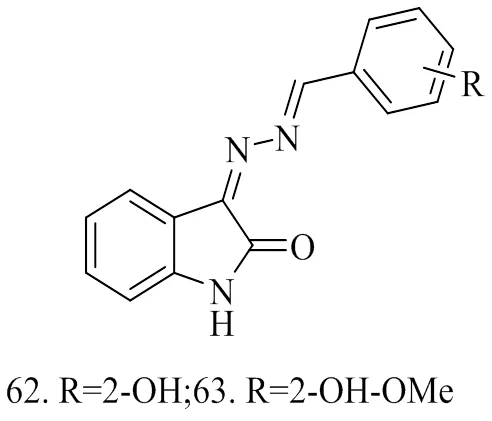
图15 化合物62~63的结构式
软钢是一种重要的工程材料,由于其成本低、力学性能优良,被广泛用作建筑材料。软钢在工业设备酸洗清洗、油井酸化等各种工业用酸溶液中腐蚀严重[16-17]。抑制性酸溶液通常用于减少酸对金属的腐蚀。这些抑制剂通过增加阳极或阴极极化行为、减少离子的移动或扩散以及增加金属表面的电阻来减少腐蚀过程[18]。靛红双腙类化合物不仅表现出广泛的生物活性,还充当有效的缓蚀剂[19-20]。
ANSARI[8]等采用重量法研究了3种靛红双腙化合物(化合物64~66)对1.0 M HCl中碳钢腐蚀的抑制作用,经电化学阻抗谱、动电位极化和量子化学等研究,讨论了其活化能、平衡常数、吸附自由能、活化焓和活化熵的值等。研究发现,3种化合物在1.0 M HCl中均表现出良好的缓蚀性能,缓蚀效率依次为化合物64>化合物65>化合物66,所研究的化合物为混合型抑制剂,且这些化合物遵循Langmuir吸附等温线,通过扫描电子显微镜和X射线能谱观察,证实了金属表面存在由化合物形成的保护性缓蚀剂膜。

图16 化合物64~66的结构式
近年来,纳米II-VI化合物半导体因其优异的性能和潜在的应用前景而备受关注。因此,人们对纳米材料的合成、形貌和相位控制以及物理性质等方面进行了大量研究[21-22]。ZnSe是能带隙为2.8 eV的II-VI纳米半导体材料之一,由于其在短波激光和其他光电子领域的潜在应用,受到了广泛的关注。
FLORENCE[23]等以靛红双腙为配体,在室温下采用湿化学反应法对硒化锌纳米结构进行了形态结构修饰(化合物67),制备所得硒化锌纳米棒相对均匀。

图17 化合物67的结构式
透射电镜观察结果表明,平均直径为100 nm,顶部直径为8~10 nm。在紫外-可见吸收光谱中观察到带隙的强烈蓝移,在390 nm处的吸收最大值。光致发光研究表明,硒化锌纳米棒具有增强的光致发光特性。因此,所制备的硒化锌纳米棒在蓝色发光体、催化剂和气体传感器等方面具有广阔的应用前景。该靛红双腙化合物还可作为配体用于制备其他形貌特殊、性能优异的金属硒化物(CdSe、CuSe)。
5 结束语
靛红双腙类化合物是一类具有多种生物活性的靛红衍生物,目前人们对其结构进行的大量修饰和改造,主要研究方向有:在苯环中引入取代基;在双腙上引入取代基。经过不断的深入研究,将会发现更多结构多样、活性优良的靛红双腙类化合物。
[1]YOUSSEF M S K. Synthesis of antimicrobial heteroaryl-substituted- 1,2,3-triazolines via the reaction of diazomethane with anils and mixed azines of thiophenealdehyde and/or isatin[J]., 1981, 31(1): 363-367.
[2]PANDEY V K, DWIVEDI A, PANDEY O P, et al. Organophosphorus derivatives containing isatin-3-hydrazones as chemotherapeutants against fungal pathogens of sugarcane[J]., 2008, 56(22): 10779-10784.
[3]ELDEHNA W M, ALTOUKHY A, MAHROUS H, et al. Design, synthesis and QSAR study of certain isatin-pyridine hybrids as potential anti-proliferative agents[J]., 2015, 90: 684-694.
[4]KARUNANIDHI S, CHANDRASEKARAN B, KARPOORMATH R, et al. Pharmaceutical compounds: The Republic of South Africa, WO2018100484[P]. 2018-06-07.
[5]KHAN S A, SIDDIQUI A A, BHATT S. Analgesic activity of isatin derivatives[J]. Asian Journal of Chemistry, 2002, 14(2): 1117.
[6]KHAN K M, KHAN M, ALI M, et al. Superoxide respiratory burst inhibitory activity of Bis-schiff bases of isatins[J]. Journal of Chemical Society of Pakistan, 2013, 35(3): 987-993.
[7]SOMOZA J R, SKILLMAN A G, MUNAGALA N R, et al. Rational design of novel antimicrobials: blocking purine salvage in a parasitic protozoan[J]. Biochemistry, 1998, 37(16): 5344-5348.
[8]ANSARI K R, QURAISHI M A. Bis-Schiff bases of isatin as new and environmentally benign corrosion inhibitor for mild steel[J]. Journal of Industrial and Engineering Chemistry, 2014, 20(5): 2819-2829.
[9]HASSAN K M, KHALIL Z H. Studies on Spiro Azetidinones and Spiro Thiazolidinones, III Synthesis of Some New Spiro Azetidinones, Spiro Thiazolidinones, Bis-azetidinones and Bis-thiazolidinones[J]. Zeitschrift für Naturforschung B, 1979, 34(4): 621-623.
[10]MURUKAN B, MOHANAN K S. Characterization, Electrochemical Properties and Antibacterial Activity of Some Transiton Metal Complexes with [(2-hydroxy-1-naphthaldehyde)-3-isatin]-bishydraz- one[J]., 2006, 31(4):441-446.
[11]DEVI J, BATRA N. Synthesis, characterization and antimicrobial activities of mixed ligand transition metal complexes with isatin monohydrazone Schiff base ligands and heterocyclic nitrogen base[J]., 2015, 135:710-719.
[12]KHAN K M, KHAN M, ALI M, et al.Synthesis of bis-Schiff bases of isatins and their antiglycation activity[J]., 2009, 17(22):7795-7801.
[13]KHAN K, KHAN M, AMBREEN N, et al.Bis-Schiff Bases of Isatins: A New Class of Antioxidant. Journal of Pharmacy Research[J]., 2011, 4:3402-3404.
[14]KHAN M, KHAN K M, RAHIM F, et al. Synthesis Leishmanicidal Activities of bis-Schiff Bases of Isatins[J]., 2015, 37(6):520-526.
[15]MUSHARRAF S G, BIBI A, SHAHID N, et al. Acylhydrazide and Isatin Schiff Bases as Alternate UV-Laser Desorption Ionization (LDI) Matrices for Low Molecular Weight (LMW) Peptides Analysis[J]., 2012, 3(12) :779-789.
[16]QURAISHI M A, SARDAR R. Aromatic Triazoles as Corrosion Inhibitors for Mild Steel in Acidic Environments[J]., 2002, 58(9):748-755.
[17]ABD EL-MAKSOUD S A, FOUDA A S. Some pyridine derivatives as corrosion inhibitors for carbon steel in acidic medium[J]., 2005, 93(1):84-90.
[18]EMREGÜL K C, DÜZGÜN E, ATAKOL O. The application of some polydentate Schiff base compounds containing aminic nitrogens as corrosion inhibitors for mild steel in acidic media[J]., 2006, 48(10):3243-3260.
[19]QURAISHI M A, AHAMAD I, SINGH A K, et al. N-(Piperidino- methyl)-3-[(pyridylidene)amino]isatin: A new and effective acid corrosion inhibitor for mild steel[J]., 2008, 112(3):1035-1039.
[20]KHAN K M, KHAN M, ALI M, et al. Synthesis of bis-Schiff bases of isatins and their antiglycation activity[J]., 2009,17(22):7795-7801.
[21]NAVANEETHAN M, ARCHANA J, NISHA K D, et al. Synthesis of wurtzite ZnS nanorods by microwave assisted chemical route[J]., 2012, 66(1): 276-279.
[22]WANG H, TIAN T, YAN S, et al. Large-scale synthesis of ZnSe nanoribbons on zinc substrate[J]., 2009, 311(14): 3787-3791.
[23]FLORENCE S S, UMADEVI M, AROCKIASAMY D L, et al. Tailoring of Morphology and Optical Properties of Bishydrazone- Capped ZnSe Nanorods[J]., 2015, 68(10): 1508-1512.
Research Progress in Bioactivity of Isatin Dihydrazone Compounds
,,YAN Guo-bing
(Lishui University, Lishui Zhejiang 323000, China)
Isatin dihydrazone compounds are important derivative of isatin, which has many biological activities. For further researching the relationship between the bioactivity and the structure-activity of isatin dihydrazone compounds, numerous modifications of isatin dihydrazone compounds have been carried out in recent years, and some compounds with strong activity have been synthesized. In this paper,research progress in biological activities and structure-activity relationships of isatin dihydrazone compounds was reviewed.
Isatin derivatives; Isatin dihydrazone compounds; Biological activity
丽水市科技局高层次人才培养资助项目(项目编号:2017RC12)。
2020-06-11
余婕(1999-),女,浙江省宁波市人,研究方向:含氟药物小分子设计和绿色合成化学。
严国兵(1975-),男,教授,博士,研究方向:绿色有机合成、金属催化和含氟药物小分子设计。
R914.5
A
1004-0935(2020)11-1398-07
