茶多酚对早期龋进展的影响
2020-11-30马丽陈静郭爱花张向宇
马丽,陈静,郭爱花,张向宇△
龋病是发生于牙体硬组织的一种细菌感染性疾病,在导致牙齿缓慢破坏的同时还会对身心健康造成影响[1]。有研究显示,对尚未形成龋洞的早期龋通过改善口腔卫生习惯或化学药物处理(如氟化物、封闭剂)可减缓龋损进展[2-3],寻找能够阻断早期龋进展的药物是预防和治疗龋病的重要方向。天然产物茶多酚(tea polyphenol,TP)由于性质稳定、毒副作用轻微,一直是防龋阻断剂研究中的热点[4]。大量研究发现茶多酚可以抑制致龋菌(如变异链球菌)在牙面上的黏附和聚集,干扰致龋菌获得性薄膜的形成[5-6],但在龋的发展过程中除了致龋菌外,牙齿脱矿及再矿化程度同样会影响龋齿的进展。Hiraishi等[7]研究证实天然产物橙皮苷可通过稳定胶原进而抑制牙本质脱矿。而有关茶多酚在早期龋进展中对牙齿硬组织影响的研究较少,且结论不一。本研究选取天然产物茶多酚为实验药物,通过建立牛牙早期龋模型及体外pH循环实验,模拟口腔环境下牙齿的脱矿及再矿化过程,观察茶多酚对早期龋进展的影响,同时评价其与氟化物的联合作用效果,为今后开发安全有效的天然防龋制剂提供实验依据。
1 材料与方法
1.1 材料收集新鲜拔除的3岁龄黄牛的切牙20颗。茶多酚(产品型号:L30226524;纯度:96%)购自北京索莱宝科学技术有限公司。氟化钠(NaF,分析纯)购自上海生工生物有限公司。前期预实验结果显示茶多酚的最小抑菌浓度为2 g/L,因此选择该浓度作为茶多酚实验药物浓度;氟抑龋的有效浓度为1 mg/L,因此选取该浓度作为NaF实验药物浓度。
1.2 脱矿液、再矿化液及缓冲液的配制参照文献[7]的方法配制脱矿液及釉质再矿化液。脱矿液由50 mmol/L乙酸、1.5 mmol/L氯化钙、0.9 mmol/L磷酸二氢钾配制,用氢氧化钾调整pH值为5.0。釉质再矿化液由1.5 mmol/L氯化钙、0.9 mmol/L磷酸二氢钾、130 mmol/L氯化钾、20 mmol/L羟乙基哌嗪乙硫磺酸(HEPES)缓冲液配制,用氢氧化钾调整pH值为7.0。釉质再矿化液中加入400 mg/L胶原酶Ⅰ配制成牙本质再矿化液。参照文献[8]的方法配制缓冲液,由130 mmol/L氯化钾、20 mmol/L HEPES配制,用氢氧化钾调整pH值为7.0。
1.3 早期龋样本的制备将20颗切牙牙冠制备成6 mm×6 mm×2 mm釉质块[8],经包埋、磨平、抛光后,在10%磷酸溶液中浸泡10 s。釉质边缘涂抹指甲油覆盖,仅留出5 mm×5 mm窗口。另取根部牙体组织,制备成牙本质标本。共制备牙釉质及牙本质标本各24块。将牙釉质与牙本质标本浸入100 mL的脱矿液中,置于37℃台式恒温培养摇床(天津市欧若仪器仪表有限公司,HNY型号)中96 h使其脱矿,以模拟早期龋的病理改变。将制备好的牙釉质龋及牙本质龋标本分别采用随机数字表法分为4组(n=6):空白对照组(DW组)、氟化钠组(NaF组)、茶多酚组(TP组)、茶多酚与氟化钠联合应用组(TP+NaF组)。
1.4 pH循环实验参照文献[7]的方法进行pH循环实验,步骤如下:标本于脱矿液(1 mL)、实验溶液(1 mL)和再矿化液(1 mL)中依次浸泡14 h、2 h、8 h,每次更换浸泡液时在缓冲液中超声荡洗5 min。整个pH循环在37℃恒温培养摇床下保持8 d,pH循环结束后收集脱矿液和再矿化液。其中,DW组的实验溶液为再矿化液,NaF组为含1 mg/L氟化钠的再矿化液,TP组的实验溶液为含2 g/L茶多酚的再矿化液,TP+NaF组的实验溶液为含2 g/L茶多酚及1 mg/L氟化钠的再矿化液。
1.5 脱矿液中钙、磷离子流出值的测定收集第1、8天pH循环后的脱矿液,采用全自动生化分析仪(D320,SINNOWA)测定钙、磷离子浓度。将第1天pH循环后测得的钙、磷离子浓度作为钙、磷流出基线值,pH循环结束后的脱矿液中的钙、磷离子浓度作为总钙、磷离子流出量,钙、磷离子的相对释放量为总钙、磷离子流出量与钙、磷流出基线值的比值。
1.6 表面显微硬度的测定通过显微硬度计(MHV-2000型,上海沪工高峰工具有限公司)检测pH循环后所有样本表面的维氏硬度(surface microhardness,SMH)。每个样本在与表面中线垂直处取6个点,测量其硬度值,取平均值。
1.7 X线能谱分析样本的钙磷比参照文献[9]的方法处理样本,基本操作如下:将pH循环后的标本置于2.5%戊二醛中固定24 h,去离子水超声荡洗,梯度乙醇(50%、70%、90%、100%)逐级脱水各10 min,干燥后喷金。X线能谱分析仪(Oxford Inea Energy300,荷兰)放大500倍检测钙磷原子含量,同一样本不同区域重复测量3次,取平均值,并计算钙磷比。
1.8 羟脯氨酸水平的测定采用羟脯氨酸酶联免疫吸附测定(ELISA)试剂盒(上海笃玛生物科技有限公司)检测牙本质再矿化液中羟脯氨酸水平,严格按照试剂盒说明书进行操作。
1.9 统计学方法采用SPSS 16.0软件进行统计学处理,计量资料以均数±标准差(±s)表示,多组间比较采用单因素方差分析,组间多重比较行LSD-t检验,P<0.05为差异有统计学意义。
2 结果
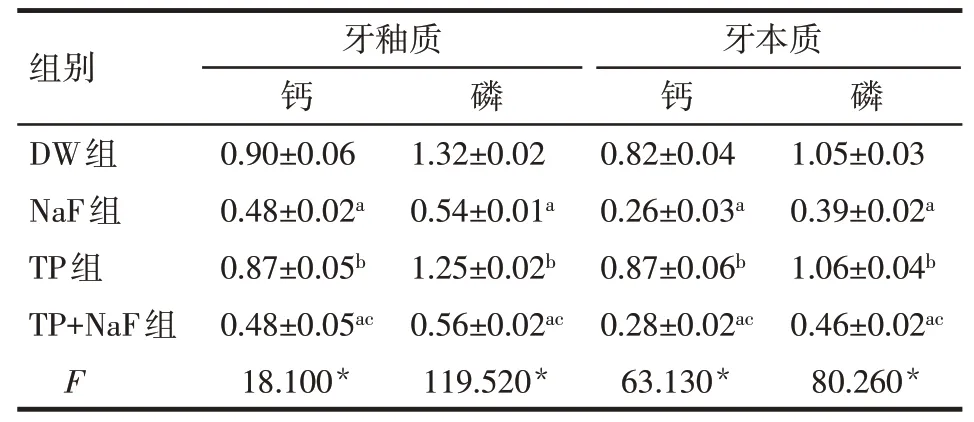
2.1 脱矿液中钙、磷离子相对释放量在牙釉质及牙本质的脱矿液中,NaF组钙、磷离子相对释放量均明显低于DW组(P<0.05);TP组钙、磷离子相对释放量均明显高于NaF组和TP+NaF组(P<0.05),与DW组差异无统计学意义(P>0.05);TP+NaF组与NaF组差异无统计学意义(P>0.05),见表1。
Tab.1 Comparison of the relative amount of calcium and phosphate in demineralized fluids between four groups表1 4组脱矿液中钙、磷离子相对释放量的比较(n=6,±s)
Tab.1 Comparison of the relative amount of calcium and phosphate in demineralized fluids between four groups表1 4组脱矿液中钙、磷离子相对释放量的比较(n=6,±s)
*P<0.05;a与DW组 比 较,b与NaF组 比 较,c与TP组比 较,P<0.05
组别DW组NaF组TP组TP+NaF组F牙釉质钙0.90±0.06 0.48±0.02a 0.87±0.05b 0.48±0.05ac 18.100*磷磷1.32±0.02 0.54±0.01a 1.25±0.02b 0.56±0.02ac 119.520*牙本质钙0.82±0.04 0.26±0.03a 0.87±0.06b 0.28±0.02ac 63.130*1.05±0.03 0.39±0.02a 1.06±0.04b 0.46±0.02ac 80.260*
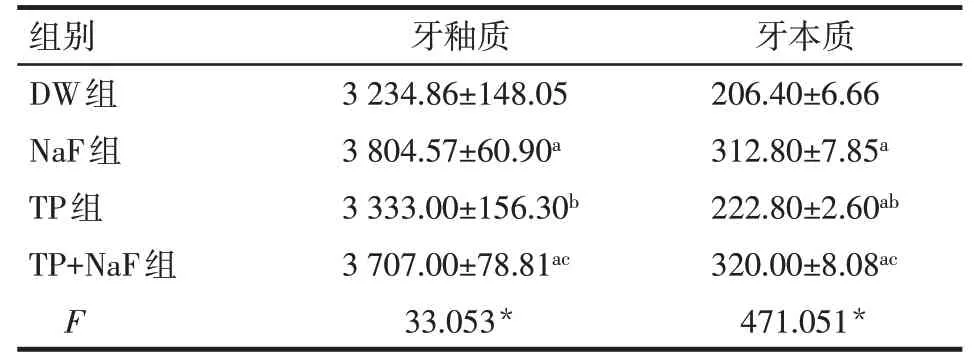
2.2 再矿化后标本表面显微硬度值牙釉质表面显微硬度值NaF组和TP+NaF组均高于DW组和TP组(P<0.05),TP组与DW组以及TP+NaF组与NaF组间差异均无统计学意义;牙本质表面显微硬度值NaF组、TP组和TP+NaF组均高于DW组,NaF组和TP+NaF组高于TP组(P<0.05),TP+NaF组与NaF组间差异均无统计学意义,见表2。
Tab.2 Comparison of microhardness of ename and dentin surface between four groups表2 4组牙釉质及牙本质表面显微硬度值比较(n=6,HV,±s)
Tab.2 Comparison of microhardness of ename and dentin surface between four groups表2 4组牙釉质及牙本质表面显微硬度值比较(n=6,HV,±s)
*P<0.05;a与DW组比较,b与NaF组比较,c与TP组比较,P<0.05
组别DW组NaF组TP组TP+NaF组F牙釉质3 234.86±148.05 3 804.57±60.90a 3 333.00±156.30b 3 707.00±78.81ac 33.053*牙本质206.40±6.66 312.80±7.85a 222.80±2.60ab 320.00±8.08ac 471.051*
2.3 X射线能谱分析样本钙磷比在pH循环结束后的牙釉质表面,NaF组、TP组和TP+NaF组钙磷比均高于DW组(P<0.05),NaF组、TP组和TP+NaF组间差异无统计学意义;在牙本质表面,NaF组、TP组和TP+NaF组钙磷比均高于DW组(P<0.05),TP组低于NaF组和TP+NaF组(P<0.05),TP+NaF组与NaF组差异无统计学意义,见表3。
Tab.3 Comparison of calcium and phosphate ratios of enamel and dentin surface after pH circulation between four groups表3 4组pH循环后牙釉质及牙本质标本表面钙磷比的比较 (n=6,±s)

Tab.3 Comparison of calcium and phosphate ratios of enamel and dentin surface after pH circulation between four groups表3 4组pH循环后牙釉质及牙本质标本表面钙磷比的比较 (n=6,±s)
*P<0.05;a与DW组比较,b与NaF组比较,c与TP组比较,P<0.05
组别DW组NaF组TP组TP+NaF组F牙釉质1.30±0.14 1.65±0.09a 1.57±0.15a 1.62±0.16a 6.272*牙本质1.44±0.13 1.94±0.12a 1.61±0.12ab 1.92±0.15ac 20.352*
2.4 再矿化液中羟脯氨酸水平NaF组和TP+NaF组牙本质再矿化液中羟脯氨酸水平均低于DW组和TP组(P<0.05),TP组与DW组以及TP+NaF组与NaF组间差异均无统计学意义,见图1。
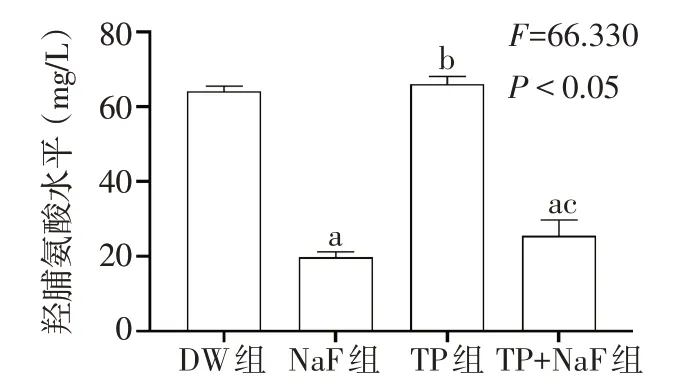
Fig.1 Comparison of hydroxyproline concentrations in dentin remineralization solution between four groups图1 4组牙本质再矿化液中羟脯氨酸水平的比较
3 讨论
龋病是牙体硬组织脱矿与再矿化失衡引发的。在牙体硬组织脱矿阶段,牙菌斑中致龋菌分解碳水化合物产生有机酸,这些酸汇聚在菌斑与牙齿界面,形成一定的浓度梯度[10]。当pH达到临界值(pH=5.5)时,氢离子会扩散至钙化的牙齿组织中,开始较明显的脱钙脱磷过程。在此阶段,若通过药物等途径促使再矿化占优势,矿物离子再沉积于脱矿区表面,就可以避免早期龋洞的形成。本实验通过浸泡脱矿液使牙体组织表面脱矿的方式制备早期龋模型,通过pH循环实验模拟龋的进展过程。结果显示,TP组钙、磷离子相对释放量与DW组无明显差异,提示茶多酚不具有抑制牙体硬组织中钙磷流出的作用,对于早期龋的脱矿无明显影响,此结果与李继遥等[11]的研究结果一致。然而,齐芳芳等[12]的研究结果表明茶多酚可以有效抑制早期人工根面龋中钙离子流出,进而抑制脱矿。进一步探究原因后发现,研究结果不同可能与龋模型的造模方法不同有关。齐芳芳等[12]实验中所用的龋齿模型是在致龋菌的参与下构建的,而茶多酚对于主要致龋菌——变形链球菌的抑制作用是明确的。结合上述实验结果,笔者推测茶多酚可通过抑制致龋菌的生长及相关毒力因子的表达影响牙体硬组织的脱矿。
李继遥等[11]采用测量显微硬度值的方法来衡量牙釉质表面的再矿化情况,结果显示茶多酚对釉质的再矿化无明显的抑制或促进作用,这与本实验中牙釉质表面显微硬度值的结果一致。但是,本研究采用X线能谱分析pH循环结束后牙釉质和牙本质表面钙磷比结果显示,TP组在pH循环结束后的牙釉质和牙本质表面的钙磷比均高于DW组,提示在早期龋的进展过程中,茶多酚可以促进脱矿后牙釉质及牙本质表面钙磷离子的再沉积。分析本实验中pH循环后的牙齿标本表面钙磷比与显微硬度值的结果出现差异的原因,可能是因为检测方法的差异造成的。显微硬度的测量较为粗略,需要再矿化达到一定程度才能被测量出来,而X线能谱分析可以较为准确地分析除氢和氦元素之外的其他各种元素,尤其是钙、磷等元素的含量,其敏感度更高[13]。pH循环实验中,钙、磷离子只是进行了初步、有限的再沉积,因此,敏感度相对较高的能谱分析更能检测这种轻微的变化。
Yu等[14]研究认为多形性茶多酚可通过与牙本质有机物结合来降低牙本质的通透性,从而抑制牙体组织脱矿。张凌琳等[15]研究证实釉质有机质在中药五倍子多酚性化合物(GCE)促进早期釉质龋再矿化过程中发挥着重要作用,当有机质去除或缺失时,GCE促进早期釉质龋再矿化的作用不显著。Hiraishi等[7]提出牙本质胶原作为矿物质沉积的支架,在再矿化过程中可通过增强其稳定性以便于矿物离子的重新沉积。羟脯氨酸是胶原分子特有的氨基酸,对其进行定量检测可以反映基质胶原的水解情况[16]。因此,为了分析茶多酚促进再矿化的机制,本研究进一步检测了再矿化液中羟脯氨酸水平,结果显示,TP组牙本质再矿化液中羟脯氨酸水平与DW组无明显差异,提示茶多酚促进牙本质的再矿化并不是通过抑制胶原水解、稳定胶原蛋白实现的,但是否依赖于有机物的支架作用,尚需进一步研究验证。有学者提出茶多酚所具有的多羟基结构可发生络合反应,与钙、铁等金属离子作用形成环状螯合物并生成沉淀[4]。本研究中牙釉质及牙本质表面钙磷比的增高是否与茶多酚、钙离子之间的反应有关,其机制仍需进一步探究。
氟化物作为一种再矿化剂,可以在釉质晶格中形成氟磷灰石以增强对酸的抵抗力,同时影响唾液和牙齿界面进行的脱矿和再矿化过程[17]。目前,含氟产品已广泛应用于龋齿临床的预防并显现出确切的临床效果。但氟的安全范围较窄,在理想剂量与有毒剂量间的界限较为模糊,高剂量的氟化物会导致牙齿和骨骼氟中毒,甚至诱导出变异链球菌的耐氟菌株[18-19]。因此,如何保持氟化物的理想剂量,使其以长期稳定的速率缓释氟尚待进一步解决。本实验尝试将天然产物与氟化钠联合应用,以期发挥天然产物的优势,在保留氟化物抑制牙齿硬组织脱矿、促进再矿化作用的同时降低其毒副作用,但实验结果未显现有协同增强作用。这可能是由于氟化物先一步作用于牙面进而阻碍其他药物接触牙面发挥作用,联合应用时药物作用的先后顺序对实验结果是否有影响仍需进一步研究。有研究指出,茶多酚与氟混合处理牙面可以促进钙盐沉积,提高釉质的抗酸力[20]。与本研究结果不同,推测原因可能与选择的氟化物、茶多酚剂量不同有关。前者实验中NaF和茶多酚的剂量分别为0.45 g/L和5 g/L,而本实验选择的是1 mg/L的NaF和2 g/L的茶多酚。
综上所述,天然产物茶多酚除了具有抑制致龋菌的作用外,还可通过促进钙磷离子的再沉积干预牙釉质及牙本质的再矿化过程,进而影响早期龋的进展,这为应用茶多酚防龋提供了新思路。
