糖尿病肾脏疾病患者血脂异常与尿蛋白关系的临床研究
2020-11-28杨学萍张岁林曹为刘永峰董生荣王小芳
杨学萍 张岁林 曹为 刘永峰 董生荣 王小芳

[摘要] 目的 研究探讨糖尿病肾脏疾病(DKD)患者血脂异常与尿蛋白关系。方法 回顾性选取该院2013年1月—2017年1月肾内科及内分泌科89例住院的DKD患者,收集基本临床资料,依据24 h尿蛋白定量分为3组,对相关血脂指标进行比较,并行相关性分析。结果 肾病综合征组患者的TC、NHDL-C、Apo-B水平更高;TC、NHDL-C、Apo-B与24 h尿蛋白定量和糖化血红蛋白(HbA1c)相关(P<0.01),LDL-C、TG仅与HbA1c有关联(P<0.01),Apo-A1仅与24 hpro有关联(P<0.05);各血脂指标依据四分位法分组,TC、TG、NHDL-C、Apo-A1、Apo-B数值越高,组内24 h尿蛋白定量≥3.5 g百分比例升高(P<0.05),而组内LDL-C和HDL-C差异无统计学意义(P>0.05)。结论 DKD患者血脂异常与蛋白尿严重程度息息相关。
[关键词] 糖尿病;肾脏疾病;血脂异常;尿蛋白
[中图分类号] R4 [文献标识码] A [文章编号] 1672-4062(2020)09(a)-0183-03
[Abstract] Objective To study the relationship between dyslipidemia and urine protein in patients with diabetic kidney disease (DKD). Methods A retrospective selection of 89 patients with DKD hospitalized in the Department of Nephrology and Endocrinology in the hospital from January 2013 to January 2017, collected basic clinical data, and divided them into three groups based on 24-hour urine protein quantification. The relevant blood lipid indexes were compared and correlation analysis was performed. Results Patients in the nephrotic syndrome group had higher levels of TC, NHDL-C, and Apo-B; TC, NHDL-C, and Apo-B were related to 24-hour urine protein quantification and glycosylated hemoglobin (HbA1c)(P<0.01), LDL-C and TG are only associated with HbA1c(P<0.01), and Apo-A1 is only associated with 24 hpro(P<0.05); each blood lipid index was grouped according to quartiles, TC, TG, NHDL-C, Apo-A1 and Apo-B, the percentage of 24 hours urine protein ≥3.5 g in the group increased(P<0.05), but there was no statistical difference between LDL-C and HDL-C in the group(P>0.05). Conclusion DKD patients with dyslipidemia are closely related to the severity of proteinuria.
[Key words] Diabetes, Kidney disease, Dyslipidemia, Urine protein
糖尿病肾脏疾病(diabetic kidney disease,DKD)是终末期肾病(end-stage renal disease,ESRD)的主要病因之一。刘志红院士早在2012年指出我国ESRD中DKD占16.4%,并有可能成为首位原因。国内外研究相继证明促进肾脏病的进展方面血脂异常也起了作用,包括:促进氧化应激,启动TGF-β途径,加强内皮细胞功能紊乱、促进单核细胞迁移等[1]。国内相关文献[2]提示不同程度的血脂升高均推进DKD的发生发展。该研究通过回顾性选取该院2013年1月—2017年1月肾内科及内分泌科89例住院的DKD患者的临床化验指标,旨在探讨DKD患者血脂代谢指标与蛋白尿水平以及肾脏病进展的关系,为DKD患者血脂的控制提供临床参考依据。现报道如下。
1 资料与方法
1.1 一般资料
选取该院收住在肾病科、内分泌科的2型糖尿病肾脏病患者,共89例,其中女性39例,男性50例。排除酮症酸中毒、糖尿病高渗状态、肝功能严重受损、感染性休克、嚴重营养不良、甲状腺功能异常、已行肾脏替代治疗者、合并其他肾病。根据2017年中国糖尿病肾脏疾病防治临床指南[3]:①大量蛋白尿;②微量蛋白尿伴糖尿病视网膜病变;③Ⅰ型糖尿病病程10年以上出现微量白蛋白尿等情况。即可诊断DKD。以上病例均通过伦理委员会批准,患者及其家属签署知情同意书。
1.2 方法
利用Microsoft Office Excel建立数据库,收集患者的年龄、性别、身高、体重、体重指数(BMI)指标。各指标基线值以入院首次检查数值为准,基线期资料包括:总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、载脂蛋白A1(Apo-A1)、载脂蛋白B(Apo-B)、载脂蛋白A1与B比值(Apo-A1/B),非高密度脂蛋白胆固醇(NHDL-C)=TC-HDLC。空腹血糖(FBG)、餐后2 h血糖(2 hBG)、血肌酐(Scr)、尿素氮(BUN)、血浆白蛋白(ALB)、糖化血红蛋白(HbA1c)。eGFR(mL/min)应用MDRD公式:170×(Scr)-0.999×(年龄)-0.176×(BUN)-0.170×(ALB)×(0.762女性)。
1.3 分组依据
结合24 h蛋白尿定量的不同分为非肾病综合征组和肾病综合征组(24 hpro≥3.5 g),非肾病综合征组包括1 g以下组(24 hpro<1.0 g)及1~3.5 g组(1.0 g≤24 hpro<3.5 g)两个亚组。
1.4 统计方法
采用SPSS 17.0统计学软件进行数据分析,数据用(x±s)表示。多组间比较,符合正态分布采用方差分析SNK检验,不符合应用K-W检验。用χ2检验对性别组成进行比较统计偏离。参数间应用Spearman等级相关分析,以P<0.05为差异有统计学意义。依据四分位法组间比较应用Cochran-Artirrmge趋势检验。
2 结果
2.1 一般资料及不同蛋白尿组间比较结果
89例DKD中,血肌酐随着24 hpro的递增呈递增趋势,血浆白蛋白、eGFR呈递减趋势,3组间差异有统计学意义(P<0.05)。组间比较结果示:24 hpro≥3.5 g组的TC、NHDL-C、Apo-B水平均高于24 hpro<1 g、1.0 g≤24 hpro<3.5 g组(P<0.05),而24 hpro<1 g、1.0 g≤24 hpro<3.5 g組之间差异无统计学意义(P>0.05)。糖尿病病程、TG、HDL-C、LDL-C、Apo-Al,各组间差异无统计学意义(P>0.05)。见表1。
2.2 血脂指标与各影响因素的相关性分析
TC、NHDL-C、Apo-B与24 hpro、HbA1c有关联。LDL-C、TG仅与HbA1c有关联(P<0.01)。Apo-A1仅与24 hpro有关联(P<0.05)。见表2。
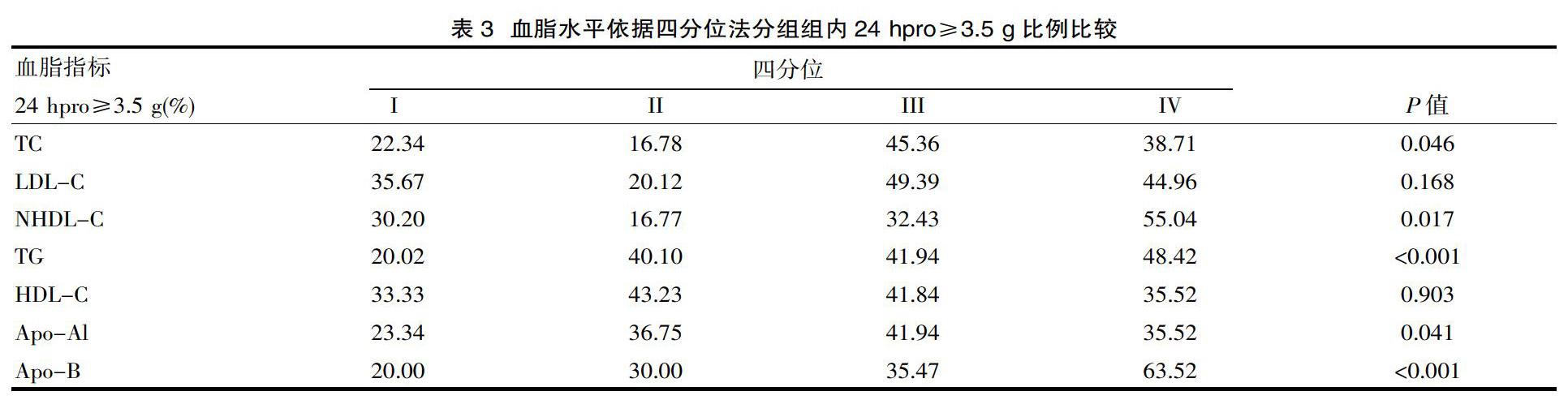
2.3 血脂水平依据四分位法分组
依据四分位法分组,比较各组内24 hpro≥3.5 g的百分比,结果示:随着TC、TG、NHDL-C、Apo-Al、Apo-B数值升高,组内24 hpro≥3.5 g比例逐渐升高(P<0.05)。见表3。
3 讨论
糖尿病肾脏疾病(DKD)在全球范围内基本已成为终末期肾病(ESRD)的最主要病因,预后不佳,也是糖尿病患者最终死亡的原因之一。在美国ESRD患者>2 600万,其中37%的ESRD患者具有糖尿病原发性诊断[4]。其发病机制复杂,越来越多的证据表明其进展的重要原因包括高血压、高血糖、遗传因素及血脂的异常[5]。探索并阐明这些机制为优化DKD的诊断及治疗方案,在临床上及相关研究方面可提供新的思路。
DKD主要特征是尿白蛋白的排泄率增加[6],DKD患者血脂异常反过来会影响到蛋白尿的严重程度。在该研究中,24 hpro≥3.5 g组TC、NHDL-C、Apo-B水平明显高于非肾病综合征组,相关性分析提示TC、NHDL-C、Apo-B、Apo-Al均与24 hpro有关联,证明DKD患者血脂水平与24小时尿蛋白定量密切关联。Wada T等[7]研究发现较传统血脂代谢指标相比,非高密度脂蛋白胆固醇(NHDL-C)与微量蛋白尿存在着非常明显的相关性。就血脂异常与蛋白尿而言,早期学说认为蛋白尿会造成血液中白蛋白的流失,在促进肝脏合成白蛋白的同时脂蛋白也同步增加,继而引发机体血脂水平升高。体内血脂水平越高,脂质成分就越容易在肾小球内沉积,此时就会不同程度促进肾小球基底膜细胞增殖。脂质一旦沉积在肾小球内,巨噬细胞、单核细胞将脂质吞噬,形成泡沫细胞,从而加重肾小球的硬化程度,反过来会进一步引发肝脏的受损,加重蛋白尿的程度。血脂升高还会使纤溶系统功能下降,引起肾小球毛细血管及微血管栓塞,肾小球滤过性增高,进一步加重尿蛋白的排出[8]。另一方面,血脂升高后,内皮细胞分泌舒张、收缩血管的细胞因子释放就会增多,化学介质发生失衡,肾小球前、后血管收缩明显增强,血管张力增高,就不同程度的增加肾脏的通透性,继而加重血浆蛋白的渗漏。从该研究中各血脂指标水平四位法分组比较结果来看,随着TC、NHDL-C、TG、Apo-Al、Apo-B升高,组内24 hpro≥3.5 g比例逐渐升高,进一步验证了血脂异常会加速DKD进展。目前在国内外关于表现为蛋白尿甚至大量蛋白尿的DKD患者血脂水平与其疾病的进展的研究甚少。因此为DKD患者血脂的控制提供临床参考依据。
[参考文献]
[1] Shipra Agrawal, Joshua J, Zaritsky, et al. Dyslipidaemia in Nep-hrotic Syndrome: Mechanisms and Treatment[J].Nat Rev Nephrol,2018,14(1):57-70.
[2] 吕艳红,毛英杰,樊春梅.2型糖尿病与2型糖尿病肾病患者血脂、肾功能指标变化分析[J].中国实用医药,2019,14(33):57-58.
[3] 中华医学会糖尿病学分会.中国2型糖尿病防治指南(2017年版)[J].中华糖尿病杂志,2018,10(1):4-67.
[4] Primary Causes of End-Stage Renal Disease[J].US Pharm,2016,41(8):6.
[5] 陈涧杨,韩飞.糖尿病肾脏病的预防与治疗[J].中华全科医师杂志,2017,16(4):253-257.
[6] 刘睿,刘扬,符庆瑛,等.糖尿病肾脏病与血脂异常相关性研究[J].中国中西医结合肾病杂志,2019,20(4):321-323.
[7] Wada T,Muso E,Maruyama S,et al.Rationale and study design of a clinical trial to assess the effects of LDL apheresis on proteinuria in diabetic patients with severe proteinuria and dyslipidemia[J].Clin Exp Nephrol,2018,22(3):591-596.
[8] 李军辉,程东生,王锋,等.糖尿病肾病患者血脂异常与尿蛋白关系[J].上海交通大学学报:医学版,2016,59(3):478-482.
(收稿日期:2020-06-07)
