氯化锌活化制备澳洲坚果壳活性炭试验
2020-11-28郭刚军马尚玄胡小静付镓榕许文龙黄克昌邹建云
郭刚军,马尚玄,胡小静,付镓榕,许文龙,黄克昌,邹建云
(1.云南省热带作物科学研究所,云南 666100;2.文山学院化学与工程学院,云南 663000)
活性炭(activated carbon,AC)是一种多孔碳质材料,比表面积大、孔结构发达、吸附性能强、可回收利用,在食品、医药、化学工程以及环境保护等领域有着广泛的应用[1-2]。农林副产物(如稻壳、果壳、木屑等)的主要成分为纤维素或者木质素,其固定碳和挥发物含量较高而灰分含量较低,且来源广泛、价格低廉、可再生能力强,是适于制备活性炭的主要原料[3-4]。随着活性炭产业可持续发展理念的不断深入,以农林废弃资源作为原料制备活性炭吸附剂已成为当下研究和开发的热点[5]。
澳洲坚果(Macadamiaspp.),又称夏威夷果,原产于澳大利亚昆士兰东南部和新西兰威尔士东北部的亚热带森林,其可食用部分为果仁,常被用作高级食品原辅料[6]。据云南省坚果行业协会统计:2017年我国澳洲坚果种植面积约为19万hm2,占世界种植面积总量的62%,位居世界第一。澳洲坚果壳是果仁产品加工后的副产物,质量占全果的60%~75%,主要由纤维素和酸不溶木质素组成,是可再生的富碳资源[7],其质地坚硬,具有较高的机械强度,且自然含碳量高、灰分低,具有优质的天然结构,利于形成孔隙结构,是制备活性炭的良好原料[8]。氯化锌活化法制备的活性炭具有产率与比表面积高、过渡孔发达、价廉易得等优点[9]。Dolas等[10]以开心果壳为原料制备了活性炭,分析了氯化锌质量分数、活化时间、活化温度等因素对活性炭的比表面积与孔径结构的影响。刘晓红等[11]采用马弗炉加热法制备了核桃果皮基活性炭,测定了不同实验条件下活性炭的得率、比表面积和碘吸附值。卢辛成等[2]采用正交试验方法探讨了制备杉木屑活性炭的条件,研究了氯化锌质量分数、浸渍比、活化温度和活化时间对其亚甲基蓝与碘吸附值的影响。而以澳洲坚果壳为原料,采用氯化锌活化法制备活性炭工艺优化及其结构表征的研究还鲜见报道。
笔者以活性炭得率、亚甲基蓝吸附值和碘吸附值为考察指标,通过单因素和正交试验法确定了氯化锌活化法制备澳洲坚果壳活性炭的最适宜的工艺条件,并对所制备活性炭的表面官能团与孔结构进行分析,以期为开发和综合利用澳洲坚果壳资源提供一定的技术参考。
1 材料与方法
1.1 试验材料
试验原料为澳洲坚果壳,取自西双版纳云垦澳洲坚果科技开发有限公司,其元素分析(干基)结果为C质量分数(50.24±0.32)%、H质量分数(7.06±1.08)%、O质量分数(39.92±0.40)%和N质量分数(0.28±0.03)%;灰分(干基)质量分数为(1.02±0.06)%。椰壳活性炭对照品(CAS:64365-11-3),购自山东西亚化学工业有限公司。氯化锌、碘、硫代硫酸钠、重铬酸钾、碘化钾、亚甲基蓝、淀粉、盐酸、硫酸、磷酸二氢钾、磷酸氢二钠等试剂均为国产分析纯。
1.2 主要仪器
万能粉碎机,上海比朗仪器有限公司;KSW-4D11型马福炉,上海博迅实业有限公司;BGZ-70型电热恒温鼓风干燥箱,上海博讯实业有限公司;Titrette型数字显示滴定器,普兰德(上海)贸易有限公司;ME4002E型电子天平,梅特勒-托利多仪器(上海)有限公司;DL Ⅲ型智能颗粒强度测定仪,大连鹏辉科技开发有限公司;Vario EL Ⅲ型元素分析仪,德国Elementar公司;Nicolet iS 10型傅里叶变换红外光谱仪(FT-IR),美国Thermo Fisher公司;X射线光电子能谱仪(XPS),美国Thermo Fisher公司;V-Sorb2800型比表面积及孔径分析仪,北京金埃谱科技有限公司。
1.3 试验方法
1.3.1 澳洲坚果壳活性炭制备工艺流程
澳洲坚果壳经洗涤后于105 ℃下干燥12 h,粉碎后过60目(孔径0.250 mm)筛。取一定质量的澳洲坚果壳粉与氯化锌溶液混合并搅拌均匀、浸渍,然后放入高温马弗炉中活化;反应结束后将样品先用0.1 mol/L的盐酸清洗,再用蒸馏水洗涤至中性;置于105 ℃干燥箱中干燥24 h,冷却、研磨、过200目(孔径0.075 mm)筛,制得澳洲坚果壳活性炭样品,备用。
1.3.2 澳洲坚果壳活性炭制备工艺优化
使用氯化锌为活化剂,采用单因素试验方法对比了活化时间(1,2,3,4 和5 h)、浸渍比(g∶mL,1∶3,1∶4,1∶5,1∶6和1∶7)、活化温度(400,500,600,700和800 ℃)、氯化锌质量分数(30%,40%,50%,60%和70%)、浸渍时间(16,18,20,22和24 h)对澳洲坚果壳活性炭的得率、亚甲基蓝吸附值与碘吸附值的影响,以确定每个因素的最优水平。在单因素试验的基础上确定因素水平,以活性炭得率、亚甲基蓝吸附值与碘吸附值为考察指标,采取L16(45)正交试验表确定最优制备工艺组合。
1.3.3 指标分析方法
澳洲坚果壳原料的C、H、O、N含量采用元素分析仪测定;所制备活性炭的亚甲基蓝吸附值按照GB/T 12496.10—1999《木质活性炭检验方法 亚甲基蓝吸附值的测定》检测;碘吸附值按照GB/T 12496.8—2015《木质活性炭检验方法 碘吸附值的测定》检测;水分质量分数按照GB/T 6284—2006《化工产品中水分测定的通用方法》检测;灰分质量分数按照GB 5009.4—2016《食品中灰分的测定》检测;强度按照GB/T 12496.6—1999《木质活性炭检验方法 强度的测定》检测。
1.3.4 澳洲坚果壳活性炭结构表征
1)红外吸收光谱(IR)与X射线光电子能谱(XPS)的测定:IR测定采用溴化钾压片法对活性炭表面基团进行分析,测试条件为扫描累加次数16次,扫描范围为400~4 000 cm-1;XPS测定使用Al Kα作为辐射源,检测活性炭的氧、碳元素。
2)比表面积测定[12]:采用比表面积及孔径分析仪测定样品的比表面积及孔径,其总孔容由相对压力为0.99时的氮吸附量计算为液氮体积得到。采用Brunauer-Emmett-Teller(BET)多点法计算其比表面积,Bavrett-Joyner-Halenda(BJH)法和Saito-Foley(SF)法计算孔体积及孔径参数,t-Plot 法计算微孔和中孔孔容。
1.4 统计分析
正交试验数据采用SAS 9.2软件处理,应用Duncan’s法进行显著性分析,以P<0.05为显著性差异。所有实验均进行了3次重复,结果以平均值±标准差(x±s)表示。
2 结果与分析
2.1 澳洲坚果壳活性炭制备工艺单因素试验分析
2.1.1 活化时间对活性炭得率与吸附能力的影响
活化时间对活性炭得率与吸附能力的影响见图1。随着活化时间的延长,澳洲坚果壳活性炭的得率、亚甲基蓝吸附值和碘吸附值逐渐增加。当时间增加至2 h时,活性炭得率与碘吸附值达到最大值,分别为43.70%与1 752 mg/g,与其他时间相比存在显著性差异(P<0.05);当时间增加至3 h时,亚甲基蓝吸附值达到最大值,为374 mg/g,与其他时间存在显著性差异(P<0.05),而碘吸附值与时间2 h则无显著性差异(P>0.05);随着活化时间继续增加,得率、亚甲基蓝吸附值和碘吸附值呈下降趋势。这是由于在活化反应的开始阶段,活化剂氯化锌除去了炭化后留在空隙中的焦油和无规则碳等物质,暴露出了通过碳原子组合形成的微晶结构的空隙,使其比表面积增大。随着活化剂继续作用,空隙被不断加宽,导致亚甲基蓝吸附值和碘吸附值降低,并且得率也降低[13]。综合考虑,活化时间选择3 h较为适宜。

注:同一指标间字母不同表示差异显著(P<0.05)。下同。图1 活化时间对活性炭得率与吸附能力的影响Fig. 1 Effect of activation time on the yield and the adsorption capacity of the activated carbon
2.1.2 浸渍比对活性炭得率与吸附能力的影响
浸渍比对活性炭得率与吸附能力的影响见图2。随着浸渍比的增大,澳洲坚果壳活性炭的得率、亚甲基蓝吸附值和碘吸附值逐渐增加。当浸渍比增加到1∶5时,得率、亚甲基蓝吸附值和碘吸附值达到最大值,分别为44.90%、368 mg/g与1 848 mg/g,与其他浸渍比存在显著性差异(P<0.05)。随着浸渍比的继续加大,得率、亚甲基蓝吸附值和碘吸附值呈下降趋势。这可能是由于随着浸渍比的加大,越来越多的锌离子伴随着溶液进入纤维孔中,形成更多的孔结构。浸渍比继续加大,活化反应更为剧烈,形成的微孔或中孔被刻蚀成大孔,导致亚甲基蓝吸附值、碘吸附值与得率都有所降低[14]。因此,浸渍比选择1∶5较为适宜。

图2 浸渍比对活性炭得率与吸附能力的影响Fig. 2 Effect of impregnation ratio on the yield and the adsorption capacity of the activated carbon
2.1.3 活化温度对活性炭得率与吸附能力的影响
活化温度对活性炭得率与吸附能力的影响见图3。随着活化温度的升高,澳洲坚果壳活性炭的得率、亚甲基蓝吸附值和碘吸附值逐渐增加,当温度增加至500 ℃时,得率达到最大值,为50.01%,与其他温度存在显著性差异(P<0.05)。当温度增加至600 ℃时,亚甲基蓝吸附值和碘吸附值达到最大值,分别为347和1 706 mg/g,与其他温度存在显著性差异(P<0.05)。随着活化温度的继续升高,得率、亚甲基蓝吸附值和碘吸附值呈下降趋势。这是因为在低温度段范围内,升高活化温度,有助于氯化锌的造孔。但活化温度过高时,由于碳结构过度烧蚀,部分澳洲坚果壳会被直接烧成灰分,使孔径结构破坏较为严重,空隙会变大,导致亚甲基蓝吸附值和碘吸附值降低,并且得率也降低[15]。综合考虑,活化温度选择600 ℃较为适宜。

图3 活化温度对活性炭得率与吸附能力的影响Fig. 3 Effect of activation temperature on the yield and the adsorption capacity of the activated carbon
2.1.4 氯化锌质量分数对活性炭得率与吸附能力的影响
氯化锌作为活性炭常用的活化剂,高温下具有催化脱水作用,在炭化时能起骨架作用,用其制备的活性炭一般具有较丰富的内部孔隙结构以及较高的比表面积[8]。随着氯化锌质量分数的增加,澳洲坚果壳活性炭的得率、亚甲基蓝吸附值和碘吸附值逐渐增加,结果如图4所示。当质量分数增加到50%时,得率、亚甲基蓝吸附值和碘吸附值达到最大值,分别为49.30%、382 mg/g和1 792 mg/g,与其他氯化锌质量分数下存在显著性差异(P<0.05)。随着氯化锌质量分数的继续增加,得率、亚甲基蓝吸附值和碘吸附值呈现下降趋势。这可能是因为大量的氯化锌包围在澳洲坚果壳粉表面,不利于氢、氧的释放,从而减少了吸附能力。另一方面,过量的金属离子使温度升高,炭被严重烧失,微孔或中孔被破坏,部分转化为大孔,使其亚甲基蓝吸附值、碘吸附值与得率都有所下降[16]。因此氯化锌质量分数选择50%较为适宜。

图4 氯化锌质量分数对活性炭得率与吸附能力的影响Fig. 4 Effect of zinc chloride mass fraction on the yield and the adsorption capacity of the activated carbon
2.1.5 浸渍时间对活性炭得率与吸附能力的影响
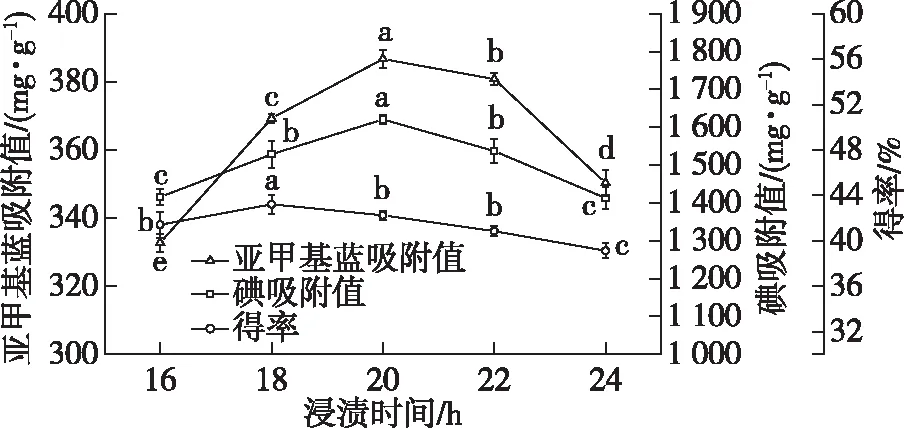
图5 浸渍时间对活性炭得率与吸附能力的影响Fig. 5 Effect of impregnation time on the yield and the adsorption capacity of the activated carbon
浸渍时间对活性炭得率与吸附能力的影响见图5。随着浸渍时间的增加,澳洲坚果壳活性炭的得率、亚甲基蓝吸附值和碘吸附值逐渐增加,当时间增加到18 h时,得率达到最大值,为43.44%,与其他时间存在显著性差异(P<0.05)。当时间增加到20 h时,亚甲基蓝吸附值和碘吸附值达到最大值,分别为387与1 621 mg/g,与其他时间存在显著性差异(P<0.05)。随着浸渍时间的继续增加,得率、亚甲基蓝吸附值和碘吸附值呈下降趋势。这是由于浸渍时间增加使纤维孔隙中间氯化锌溶液增多,有利于形成更多的澳洲坚果壳粉炭化物孔隙结构。但当浸渍时间过长时,纤维孔隙中间的锌离子过量,活化反应剧烈,大量的微孔或中孔被刻蚀成大孔,导致其亚甲基蓝吸附值与碘吸附值下降,得率也下降[17]。综合考虑,浸渍时间选择20 h较为适宜。
2.2 澳洲坚果壳活性炭制备工艺正交试验分析
澳洲坚果壳活性炭制备工艺正交试验结果见表1。由表1可知,澳洲坚果壳活性炭制备工艺各因素对得率影响的主次顺序为:活化时间(A)>浸渍比(B)>浸渍时间(E)>活化温度(C)>氯化锌质量分数(D),最优工艺组合为A2B1C2D3E1;各因素对活性炭亚甲基蓝吸附值影响的主次顺序为A>B>E>C>D,最优工艺组合为A2B2C4D2E4;各因素对活性炭碘吸附值影响的主次顺序为A>B>E>C>D,最优工艺组合为A4B2C1D3E2。
由上述分析可知,指标变动的大小实际上不受因素水平变动的影响,各因素对澳洲坚果壳活性炭得率、亚甲基蓝吸附值与碘吸附值的影响顺序一致,均为A>B>E>C>D,但活性炭制备的最佳工艺条件略有不同。在实际选取最优工艺条件时,需要考虑各因素对得率、亚甲基蓝吸附值和碘吸附值的综合影响,以得到更优的制备工艺条件。由于根据3个试验指标得到的最佳工艺条件不同,将根据得率、亚甲基蓝吸附值与碘吸附值得到的最佳工艺条件制备的活性炭分别标记为AC1、AC2和AC3。其中,AC1活性炭样品的得率、亚甲基蓝吸附值和碘吸附值分别为51.92%、388 mg/g和1 746 mg/g;AC2活性炭样品的得率、亚甲基蓝吸附值和碘吸附值分别为49.35%、413 mg/g和1 773 mg/g;AC3活性炭样品的得率、亚甲基蓝吸附值与碘吸附值分别为49.95%、412 mg/g和1 830 mg/g。一般情况下,活性炭首先应考量其吸附性能,其次是得率[18]。综合考虑,AC3活性炭样品具有最好的碘吸附能力,得率与亚甲基蓝吸附能力也较高,所以选择该实验条件为最佳工艺条件,即为活化时间3.5 h、浸渍比1∶4、活化温度550 ℃、氯化锌质量分数50%、浸渍时间19 h。
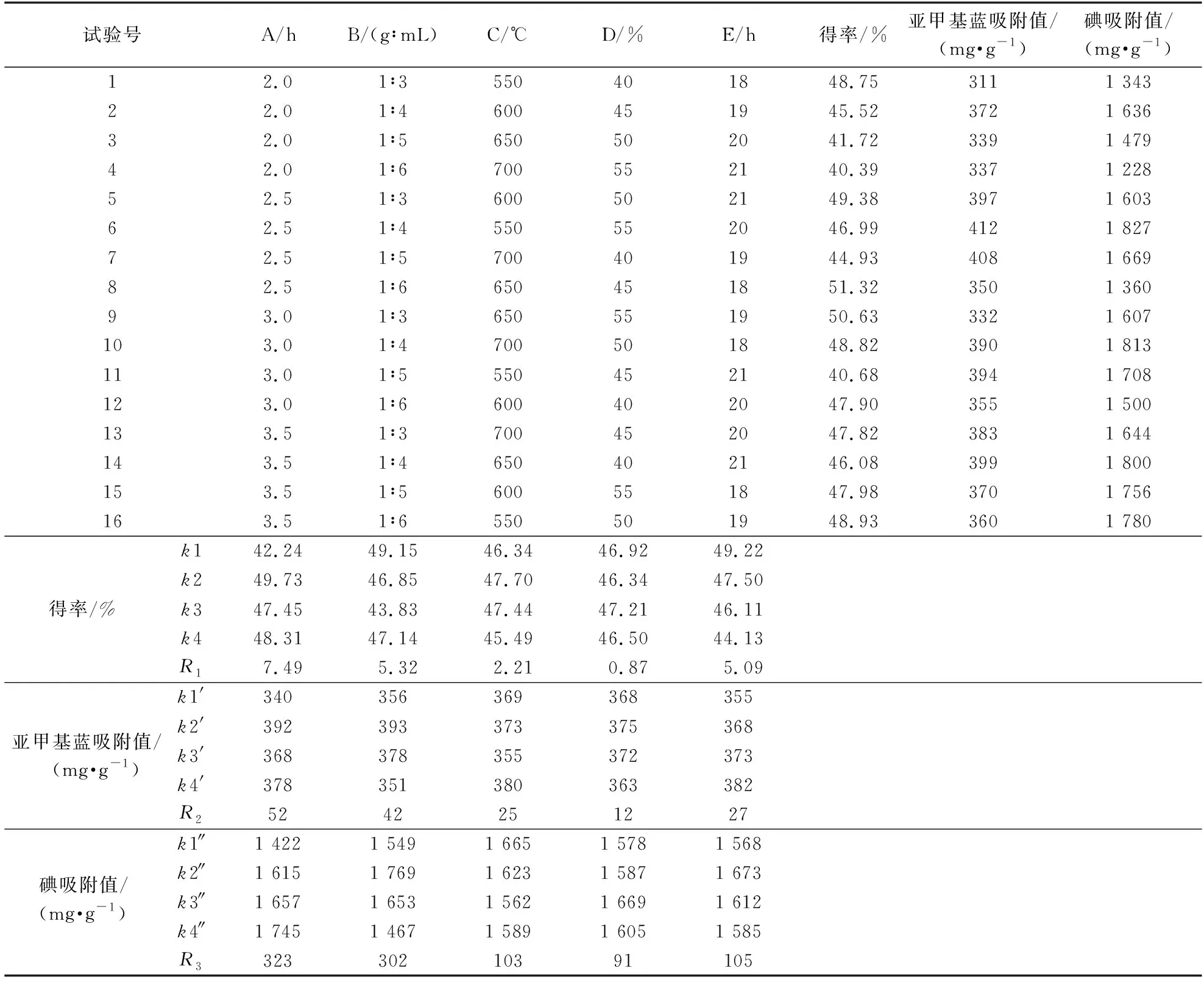
表1 澳洲坚果壳活性炭制备工艺正交试验结果Table 1 Orthogonal array design with experimental results for preparation technology of the activated carbon from Macadamia shell
2.3 澳洲坚果壳活性炭的结构表征
2.3.1 活性炭红外光谱与X射线光电子能谱分析


图6 椰壳活性炭标品与澳洲坚果壳活性炭红外光谱图Fig. 6 Infrared spectrum of activated carbon reference substance of coconut shell and the optimal activated carbon of Macadamia shell


图7 澳洲坚果壳活性炭C1s与O1s的X射线光电子能谱图Fig. 7 X-ray photoelectron spectra for C1s and O1s of the optimal activated carbon of Macadamia shell
2.3.2 活性炭比表面积测定
澳洲坚果壳活性炭吸附-脱附等温线如图8所示,在相对压力为0.4~0.9的范围内出现了明显的吸脱附滞后回环,在相对压力为1.0时,等温线有向上爬升的趋势。按照国际理论与应用化学协会(IUPAC)分类,属于Ⅱ型吸附等温线,等温线形状为IUPAC吸附滞后回线分类中的H3和H4型的结合,表明存在狭缝形孔隙。即在吸附等温线开始部分表明发生了活性炭的微孔填充,在较大相对压力下,平台的倾斜是中孔或大孔以及外表面上的多层吸附的缘故[4]。
为了进一步研究所制备的澳洲坚果壳活性炭孔结构,需要测定其孔径分布,经测定,其比表面积1 174 m2/g,微孔比表面积497 m2/g,中孔比表面积677 m2/g,微孔孔容0.24 cm3/g,中孔孔容 0.58 cm3/g,总孔容0.82 cm3/g,平均孔径2.80 nm。微孔占总表面积的42.33%,中孔占57.67%;微孔占总孔容的29.27%,中孔占70.73%。且从澳洲坚果活性炭孔径分布图9中可以看出,微孔孔径主要集中在0.93~1.61 nm,中孔孔径在2~10 nm,且在4.2 nm附近出现了一个明显的峰,表明样品含有丰富的中孔及较多数量的微孔,与吸附等温线结果一致。综上,制备的澳洲坚果壳活性炭为中孔型活性炭,并拥有较大比例的微孔,因此具备较强的吸附能力,可主要用于液相吸附,同时也可以用于气相吸附[2]。
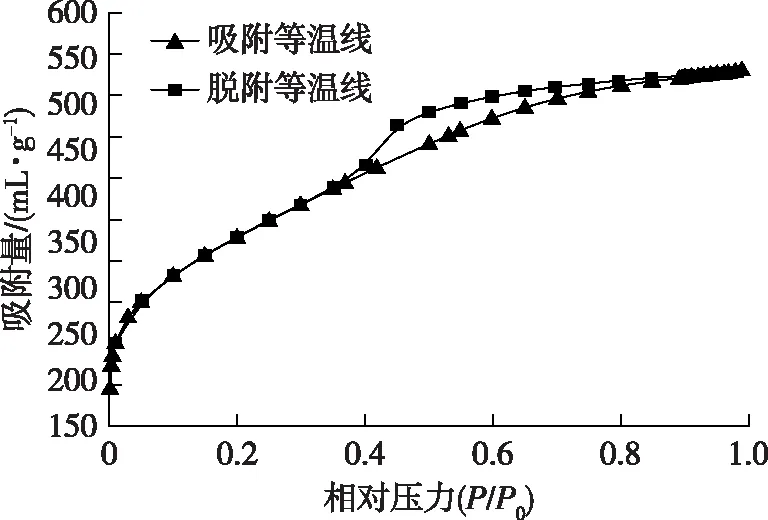
图8 澳洲坚果壳活性炭吸附-脱附等温线Fig. 8 Adsorption-desorption isotherms of the optimal activated carbon of Macadamia shell

图9 BJH 法计算的澳洲坚果壳活性炭孔径分布Fig. 9 Pore diameter distribution of the optimal activated carbon of Macadamia shell by BJH method
2.4 澳洲坚果壳活性炭质量指标分析
澳洲坚果壳活性炭质量指标分析见表2,制备的澳洲坚果壳活性炭的外观为黑色粉末状,水分质量分数、灰分质量分数、强度、亚甲基蓝吸附值与碘吸附值分别为1.45%、0.84%、96.78%、412 mg/g与1 830 mg/g,均符合国家标准GB/T 13803.2—1999《木质净水用活性炭》(一级品)与食品安全国家标准GB 29215—2012《食品添加剂植物活性炭(木质活性炭)》的要求,表明其具有良好的质量与吸附能力。

表2 澳洲坚果壳活性炭质量指标Table 2 Quality indexes of the optimal activated carbon of Macadamia shell
3 结 论
以澳洲坚果壳为原料,采用氯化锌活化法制备活性炭,通过单因素与正交试验确定最佳工艺条件,并对所制备的活性炭进行了结构表征,主要结论如下:
1)澳洲坚果壳活性炭制备的最佳工艺条件为:活化时间3.5 h、浸渍比1∶4(g∶mL)、活化温度550 ℃、氯化锌质量分数50%、浸渍时间19 h。在此条件下,制备活性炭的得率、水分质量分数、灰分质量分数、强度、亚甲基蓝吸附值和碘吸附值分别为49.95%、1.45%、0.84%、96.78%、412 mg/g和1 830 mg/g。
2)制备的澳洲坚果壳活性炭存在发达且孔径分布不均的孔隙结构,其属于中孔型活性炭,并拥有较大比例的微孔,表面存在醇羟基、酚羟基、醚基、羰基、羧基等含氧官能团,具有一定的亲水性及较强的吸附能力。通过与国家相关标准比较,制备的澳洲坚果壳活性炭的质量指标与吸附性能达到活性炭一级品的标准要求。
