Cu-Ce催化剂上CO催化燃烧反应机理研究进展
2020-11-18康润宁魏小林王子兵
康润宁,魏小林,3,宾 峰,3,王子兵
(1.中国科学院 力学研究所 高温气体动力学国家重点实验室,北京 100190;2.中国科学院大学 工程科学学院,北京 100049; 3.中国科学院 洁净能源创新研究院,辽宁 大连 116023;4.华北理工大学 冶金与能源学院,河北 唐山 063210)
0 引 言
21世纪以来,我国对化石燃料的需求量和消耗量与日俱增,致使环境污染和能量浪费问题严重。而工业炉窑(水泥炉窑、烧结炉及燃煤锅炉等)、冶金工业生产过程(高炉、转炉及焦炉等)、机动车尾气排放等造成大量CO排放,严重污染环境,危害人类健康[1-3]。因此,限制并有效消除CO已成为工业节能减排工作面临的重要研究课题之一。
CO催化燃烧方法作为一种新型有效的燃烧方式,具有起燃温度低、燃料消耗少、能耗低及燃烧效率高等优点。应用于CO燃烧反应的催化剂主要分为贵金属催化剂和过渡金属氧化物催化剂2类。由于贵金属储量有限、制备使用成本高和热稳定性较差等原因,其工业应用受到很大限制[4-7],致使过渡金属氧化物催化剂成为主要研究热点。其中CuO作为主催化剂,可为CO提供吸附位,促进CO吸附与转化;CeO2作为助催化剂,自身特有的萤石型结构非常适合做载体,能够有效促进Cu物种在CeO2表面上的分散程度,且CeO2可通过Ce4+/Ce3+之间的价态变换展现出优良的储放氧性能。故Cu-Ce催化剂以其高效的协同特性与活化性能已被广泛应用于CO催化燃烧的基础应用研究[8-11]。
本文立足于Cu-Ce复合金属氧化物催化剂上CO燃烧化学反应,首先介绍了国内外学者近期在Cu-Ce催化剂上CuO与CeO2协同作用机制方面的研究成果,然后针对Cu-Ce系列催化剂上CO微观反应机理进行分类总结,并结合本课题组相关研究成果,进一步阐明广大学者对Cu-Ce催化剂上不同CO催化反应机理的分歧与认知;在此基础上,以工业废气中CO浓度变化特性为切入点,由低浓度拓展到高浓度,介绍了本课题组所提出的CO自持催化燃烧技术,丰富了CO催化燃烧安全控制理论。最后展望了CO催化燃烧反应研究未来的发展方向,为洁净燃烧与污染物控制理论研究与节能减排技术应用提供参考。
1 Cu-Ce催化剂构效关系
目前,针对Cu-Ce基催化剂的制备方法有溶胶凝胶法、浸渍法、水热合成法、共沉淀法等。Avouropoulos等[12]通过柠檬酸水热合成法、共沉淀法、尿素-硝酸盐燃烧法以及浸渍法分别制备了CuO-CeO2催化剂,并研究其在CO选择性催化氧化中的活性,结果表明,尿素-硝酸盐燃烧法制备的CuO-CeO2催化剂低温活性最好,而共沉淀法与浸渍法制备的催化剂活性较差。这主要是由于前者促进了CuO在CeO2上的分散特性,加强了CuxO与CeO2表面的强相互作用,对活性起到关键作用。Gao等[13]通过水热法可控合成不同形貌的CeO2(棒状、立方体与多面体),并通过浸渍法负载不同含量的CuO,深入阐明结构形貌对Cu-Ce反应界面上强相互作用的影响规律,结果表明,负载1% CuO时,CuO/r-CeO2(棒状)活性最好。
Cu-Ce复合氧化物催化剂的构效关系主要体现在化学价态变化、形貌结构以及载体-活性组分等之间的相互作用等方面。在化学价态组成及变化方面,稀土元素铈的外层电子结构为4f15d16s2,在失电子后具有+3和+4两种稳定价态,易通过Ce3+和Ce4+离子之间的相互转换实现氧的储存和释放,是较佳的储氧体[14]。金属铜主要有+1和+2两种价态,其特有的反π键轨道形式极易吸附和活化CO分子[15-16]。Yao等[17]研究了CuO/CeO2催化剂上的CO氧化反应,认为Ce4+/Ce3+和Cu2+/Cu+电子对均参与催化循环(Cu++ Ce4+↔Cu2++ Ce3+),CeO2和CuO是活性氧的主要来源。Moreno等[18]研究发现CuO/CeO2催化剂中,活性位Cu+主要为CO提供吸附位,而CO氧化反应过程中所需活性氧主要由CeO2提供。但Yang等[19]研究发现Ce0.6Zr0.4O2催化剂上负载10% CuO时,活性氧浓度最大,催化剂活性最高,表明活性氧主要来源于CuO与铈锆固溶体之间的协同作用。
纳米CeO2形貌可控合成技术的发展为研究金属氧化物之间的协同效应以及高性能催化剂的研发带来新的契机。Wu等[20]研究表明,CeO2纳米棒主要暴露{110}和{100}晶面,CeO2纳米立方体优先暴露{100}晶面,而CeO2八面体暴露稳定的{111}晶面。因为{110}晶面更易产生氧空位,3种材料实现CO催化燃烧的活性顺序依次为:纳米棒>立方体>八面体。纳米CeO2若被用作CO催化燃烧的催化剂载体,一方面能够为Cu金属提供空间限制,抑制由CuO颗粒烧结导致的团聚及二次长大现象,同时通过控制合成条件能精确调节Cu金属掺杂量、分布以及尺寸等,能够有效提高材料活性位的有效利用率[21];另一方面,由于纳米CeO2{111}、{110}和{100}等晶面处于不同的配位结构和几何对称性,晶面调控技术的应用有助于考察CeO2活性晶面暴露比例对催化活性的影响规律以及CeO2和CuO界面之间协同效应的差异性。
在催化剂载体-活性组分相互作用方面,研究表明CeO2的表面氧与吸附态CO之间极易发生反应,但其自身活性远低于CuO等过渡金属氧化物[22]。CeO2若被用作催化剂载体,不仅可以对Cu活性相起到高分散与稳定作用,还可以提供反应所需的活性氧物种(吸附氧与晶格氧)。顾慧劼等[23]采用柠檬酸络合-浸渍相结合的制备方法研究了CeO2载体掺杂CuO(yCuO/CuxCe1-xOδ催化剂)对CO催化性能的影响。结果表明,载体中掺杂的CuO与CeO2形成铜铈固溶体,有利于CuO在载体表面均匀分散,提高催化剂的低温催化活性。Luo等[24]认为在CO氧化反应过程中,CuO/CeO2催化剂上的表面高度分散时,CuO活性最高,颗粒CuO活性次之,进入CeO2晶格中的Cu2+活性最低。Jia等[25]通过正相CuO/CeO2和反相CeO2/CuO催化剂体系研究发现,活性物种和载体的颗粒大小直接影响CuO与CeO2之间的接触界面,同时具有相同接触界面周长的CuO/CeO2和CeO2/CuO显示出相同的反应更新频率(turn over frequency,TOF),证明CO氧化的活性位处于CuO与CeO2交界面处,产生界面效应。Yan等[26]制备CeO2/Cu颗粒-纳米稳定晶面催化剂,并通过H2还原方式发现分散状态的纳米CeO2可稳定结合在CuO颗粒表面,形成CeO2-Cu反应界面(图1)。因此,通过CeO2载体形貌结构参数控制优化CuO/CeO2催化剂界面,提高载体-活性组分强相互作用,可作为提高CO催化燃烧性能的有效手段。
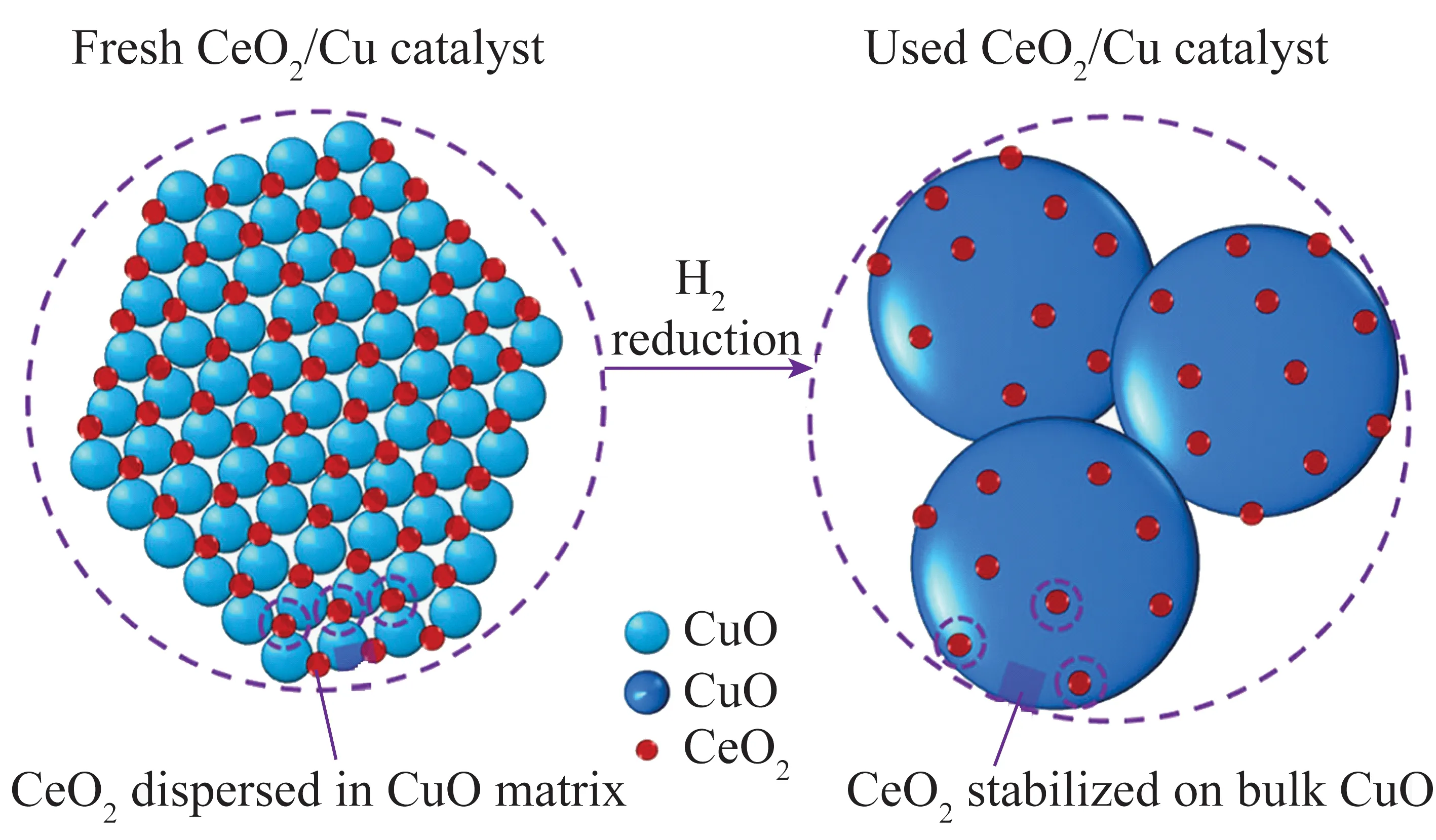
图1 CeO2/Cu催化剂结构演变过程[26]Fig.1 Scheme of structural evolution for CeO2/Cu catalyst[26]
2 Cu-Ce催化剂上催化反应机理研究
目前,CO催化燃烧反应机理主要有Mars-van Krevelen(M-K)机理与Langmuir-Hinshelwood(L-H)机理等。国内外学者基于Cu-Ce催化剂体系,提出了一些合理的反应过程假设,采用试验与相关原位表征技术相结合的方法,对CO催化燃烧反应路径进行了较深入分析,并通过反应动力学模型加以佐证,以期明确CO微观催化反应机理。
2.1 M-K机理
M-K机理可描述为CO吸附在催化剂表面活性位上,与催化剂中的活性晶格氧反应生成CO2,活性晶格氧被消耗后形成氧空位,气相O2进入氧空位重新形成晶格氧,反复循环,保证CO催化氧化反应持续进行。目前,多数学者认为在Cu-Ce系列催化剂上,CO催化氧化反应主要遵循M-K机理。
贾爱萍等[27-28]针对CO低温氧化反应在CuO-CeO2催化剂上进行了较为系统的机理研究,以CuO/Ce1-xCuxO2-δ和Ce1-xCuxO2-δ催化剂为代表,通过多种表征方法及试验研究催化剂结构-性能关系,结果表明,催化剂表面主要存在CuO和Ce1-xCuxO2-δ固溶体这2种活性位,其中CuOx的主要作用是提供CO的吸附位(Cu+-CO),而Ce1-xCuxO2-δ固溶体主要是提供活化晶格氧,CuO与Ce1-xCuxO2-δ之间存在的协同作用促进反应循环进行,同时在CO低转化率(<10%)下建立CuO/Ce1-xCuxO2-δ反应速率表达式为r(CO)=1.42×10-6P(CO)0.74P(O2)0,反应路径同样遵循M-K机理,反应机理如图2所示。Sedmark等[29]研究了Cu0.1Ce0.9O2-y催化剂上CO加氢反应动力学,通过建立典型的动力学模型得到Cu0.1Ce0.9O2-y催化剂上的CO催化燃烧主要遵循M-K机理,即Cu-Ce固溶体中的晶格氧与吸附在CuO上的CO反应生产CO2。Liu等[30]研究了Cu-Pt/CeO2催化剂上CO低温氧化反应,通过X射线吸收精细结构谱(XAFS)以及DFT量子化学计算,发现Cu-O-Ce界面效应促进了Pt的原子级分散,加强了对CO的吸附作用,其中Ptn/CeCu催化剂在30~40 ℃时,吸附的CO可与晶格氧反应生成CO2,实现CO低温高效转化,反应遵循M-K机理。
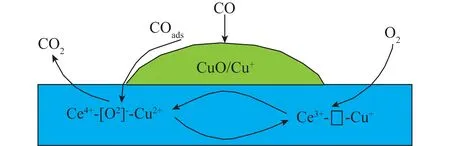
图2 CuO/Ce1-xCuxO2-δ催化剂上CO氧化反应M-K机理[28]Fig.2 Reaction mechanism of CO oxidation over CuO/Ce1-xCuxO2-δ catalyst[28]
2.2 L-H机理
L-H机理主要是指为吸附态CO与吸附态O2在催化剂表面反应生成CO2,而晶格氧却不参与反应。目前在贵金属催化剂上CO催化氧化反应主要是L-H机理[31],但一些学者认为Cu-Ce系列催化剂上的CO催化燃烧反应同样也遵循L-H机理。
Caputo等[32]在CuO/CeO2催化剂上开展了CO催化加氢反应动力学研究,发现反应温度低于110 ℃时,CO氧化反应的反应级数小于1;而反应温度高于110 ℃时,CO氧化反应的反应级数大于1,反应遵循L-H机理。Liu等[33]通过动力学试验及模型计算发现CO催化燃烧过程中,CuO作为CO与O2吸附活性位,在催化剂表面进行反应,由此推断出该反应遵循L-H机理。Lee等[34]认为CuO/CeO2催化剂上CO的催化燃烧主要遵循L-H机理,且主要有2条反应路径:一方面,CuO作为主要活性位会同时吸附CO、O2,进而生成CO2;另一方面,CO吸附在CuO上,而O2吸附在CeO2上,在CuO和CeO2界面处发生化学反应,反应路径如图3所示。
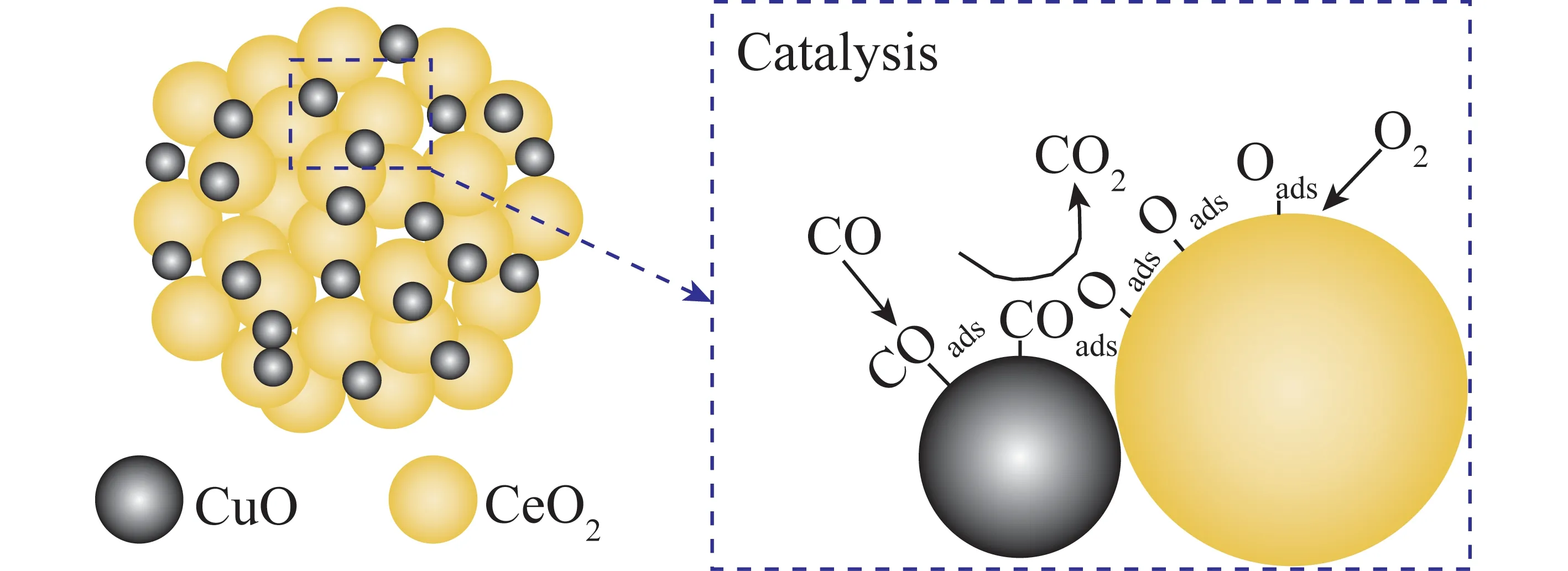
图3 CuO-CeO2催化剂上CO氧化L-H反应机理[34]Fig.3 Reaction mechanism of CO oxidation of L-H over CuO-CeO2 catalyst[34]
综上,针对Cu-Ce系列催化剂,不同学者在催化剂制备、试验条件与方法选取以及表征技术的运用不同,使CO催化燃烧反应机理存在一定差异。
2.3M-K机理与L-H机理
近年来,随着先进原位表征技术的发展,CO催化燃烧反应机理研究趋于完善。李娜[35]研究了不同载体负载CuO系列催化剂上的反应机理,得出CuO/CeO2催化剂上的CO氧化反应遵循M-K机理,还发现CuO/SiO2、CuO/TiO2催化剂上反应遵循L-H机理,氧物种分别吸附在SiO2、TiO2上与吸附在CuO上的CO反应。Zheng等[36]通过原位红外技术(In situ DRIFT)研究了CeO2-ZrO2催化剂上CO氧化的2条反应路径:① CeO2提供CO与O2的吸附活性位,形成碳酸氢盐、单齿碳酸盐和双齿碳酸盐,使CO与O2反应,遵循L-H机理;② 吸附在CeO2上的CO与铈锆固溶体中的晶格氧结合生成桥式碳酸盐,进而生成CO2,反应遵循M-K机理。
上述CO催化氧化反应机理研究是低CO(0.1%~3.0%)浓度条件下开展,主要涉及汽车尾气排放、CO优先氧化等领域。本课题组以冶金工业中转炉放散煤气含有的高浓度CO为切入点,通过制备CuO-CeO2系列催化剂,提出CO自持催化燃烧技术。在转炉炼钢生产过程中,转炉放散煤气(CO≤35%、O2≥2%及CO2≤40%)占整个吹炼期转炉煤气发生量的20%~30%,目前传统的以甲烷燃气直燃排放方式造成了严重的能源浪费和环境污染,形势尤为严峻[37]。CO自持催化燃烧方法能够实现CO的低温高效转化,燃烧反应产生的热量一部分用于维持自身氧化反应,剩余部分有望用于热交换、制热或发电。该方法若作为洁净燃烧与余能回收工艺在炼钢生产中加以应用,不仅能够提高转炉煤气化学热的回收利用率,还可以减少燃气引燃放散煤气带来的环境污染与能量浪费问题。转炉放散煤气中CO自持催化燃烧技术典型的活性曲线如图4所示[38]。高浓度CO/O2混合气体在Cu-Ce/ZSM-5催化剂颗粒表面发生氧化反应并形成局部高温区;高温区随即迅速扩大至相邻的反应活性位,引起热化学飞温,在气固相界面转变为剧烈的自持燃烧状态。在程序升温条件下,高浓度CO催化燃烧过程主要分为3个阶段。以图4中Cu/ZSM-5催化剂为例,第1阶段(CO转化率≤10%)主要是CO在催化剂表面的低温引燃,此时消耗的反应物很快通过内扩散方式进行补充,反应速率主要受本征反应动力学控制。CO转化率随反应温度的升高进一步增大,反应过程中产生的热量大于释放的热量,热量累积促使温度和反应速率继续增加,即进入反应第2阶段。第2阶段为瞬态起燃阶段(通常以CO转化率到达50%时的热点温度定义为起燃温度),高浓度CO在催化燃烧过程中,CO强放热使温度快速升高,形成催化剂床层局部飞温,进而导致其转化率快速升高。此时反应消耗的CO/O2不能完全通过内扩散形式补充,反应速率主要受动力学和外扩散控制。在很短时间内,CO转化率达到近100%,即进入第3阶段(自持燃烧阶段),此时反应速率基本保持不变,温度升高对其影响不大,主要取决于CO和O2向催化剂表面的扩散速率,反应速率主要由气体外扩散控制。同时,由于较高浓度CO燃烧放热较多,即使在不保温隔热的情况下,也可以达到换热平衡,继续维持自持燃烧状态,即可以只依靠反应本身放出的热量维持催化燃烧状态,不需要外界额外提供热量。
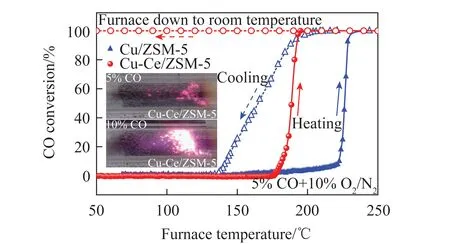
图4 CO自持催化燃烧曲线[38]Fig.4 Self-sustained catalytic combustion curve of CO[38]
Cu-Ce系列催化剂上CO催化氧化反应的研究成果见表1,并与课题组的CuO/Ce0.75Zr0.25O2-δ系列催化剂[39]进行对比,其低温反应性更优异。
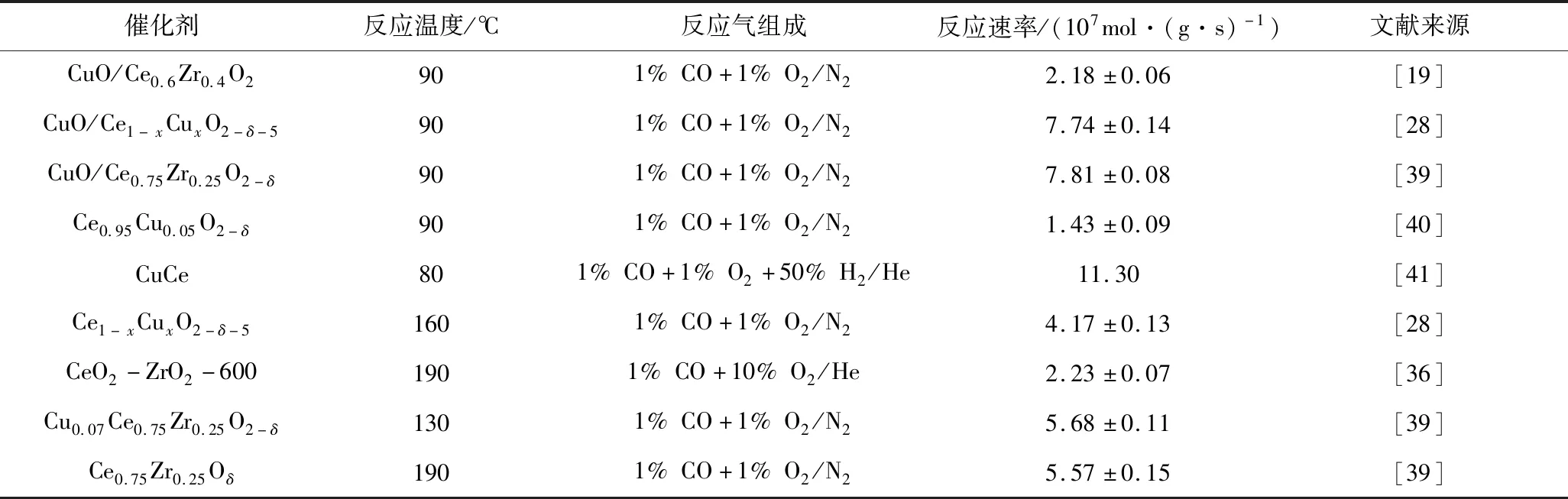
表1 Cu-Ce系列催化剂上CO催化氧化活性结果Table 1 Results of CO catalytic oxidation activity over Cu-Ce series catalysts
通过X射线光电子能谱(XPS)及In situ DRIFT等方法证明Cu-Ce/ZSM-5催化剂CO催化燃烧也存在2条反应路径[38]:① 由于Cu2+离子最外层d轨道电子接近完全充满状态,与Ce离子相比,CO分子更易以反π键轨道形式吸附于Cu2+位,经还原形成Cu+-CO。而O2分子可以接受Ce原子4f轨道上的局域电子并被活化,优先吸附在Ce位上。Cu+-CO物种与CeO2提供的活性氧反应生成CO2。② CO吸附于CeO2表面形成单齿碳酸盐和双齿碳酸盐,所生成的碳酸盐与活性氧反应生成CO2。在CuCe0.75Zr0.25Oy催化剂上,采用In situ DRIFT试验与反应动力学模型相结合的方法,同样得出2条反应路径:CO催化燃烧机理主要以M-K反应机理为主,即CO吸附在Cu+形成Cu+-CO,与催化剂中的晶格氧反应;其次为L-H机理,吸附的CO与吸附在CeO2表面的优先生成中间物种碳酸盐,再进行反应[39,42],反应路径如图5所示。
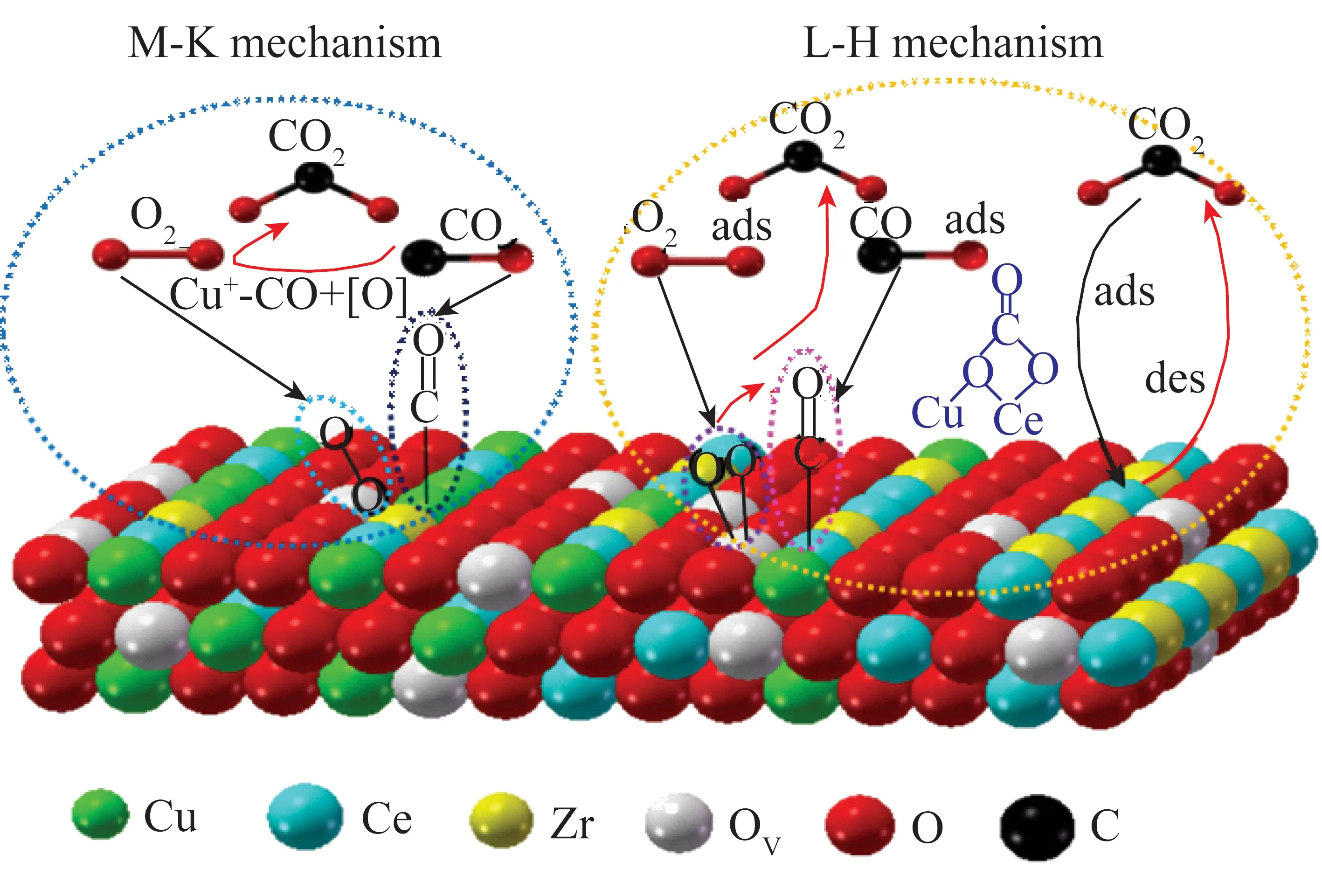
图5 CO催化燃烧反应路径[39]Fig.5 Reaction pathways of CO catalytic combustion[39]
为进一步研发低温高效、高热稳定性催化剂,采用溶胶凝胶法制得CuCe0.75Zr0.25Oy复合氧化物催化剂,其上CO自持催化燃烧的临界条件为3% CO+3% O2/N2,炉温为115 ℃,并通过红外热像仪测定了催化剂床层表面温度场。本课题组正进行CO催化燃烧的定性定量分析研究,并在Cu-Ce-Zr系列催化剂上开展CO程序升温表面反应(TPSR-GC)试验,通过化学吸附仪耦合在线色谱仪初步检测出CuCe0.75Zr0.25Oδ催化剂上CO的总脱附量为286.7 μmol/g,主要以CO2形式脱附,脱附量为280.9 μmol/g,以CO形式脱附的脱附量仅为5.8 μmol/g[43]。在此基础上,通过蜂窝陶瓷(HC)载体涂覆法制得CuCe0.75Zr0.25Oy/HC催化剂,详细探究了不同反应气浓度(CO、O2、CO2)对CO自持燃烧的影响规律,并发现CO反应机理仍以M-K机理为主[44-45],为催化剂工业放大设计奠定基础。
3 CO催化燃烧反应研究未来发展方向
目前针对CO催化燃烧反应机理研究主要集中在Cu-Ce复合氧化物催化剂的结构-性能间作用、表界面效应、尺寸效应及CO与O2反应吸附位的定性分析上,未来还需对以下方面进行深入研究:
1)Cu-Ce催化剂的载体-活性组分强相互作用。采用先进制备方法,如原子沉积法、3D打印法等合成载体形貌可控、活性位点精准锚定的精细催化剂,如单原子催化剂、分子催化剂及特定尺寸的团簇催化剂等。采用先进的原位表征技术(如原位X射线光电子能谱(in situ XPS)、近层扫描隧道显微镜(NAP-STM)、原位X射线吸收光谱(XAS)、扩展X射线吸收精细结构光谱(EXAFS)等)深入研究载体与活性位点的微观相互作用形式,设计优化低温高效Cu-Ce催化剂的合成策略,有助于在纳米尺度水平上理解真实多相反应条件下催化剂结构、活性相形貌变化以及金属氧化物之间的协同效应对催化活性的影响机制。
2)CO催化燃烧机理由定性分析向定量分析拓展。在气固多相催化反应过程中,应充分考虑反应物在催化剂表面吸附-反应-脱附历程,采用原位红外试验、高真空吸附-在线程序升温手段等定量化测定方法,通过考察反应物、中间物种在活性中心上的吸附量对反应路径的影响规律,明确对CO、O2在催化剂表面的覆盖度、催化剂活性位与吸附中间物种对CO催化燃烧反应贡献度的定性定量分析的机理研究。同时,基于量子化学理论,借助VASP、MS等模拟计算软件,在金属氧化物-载体作用模型上计算表面吸附能、搜索反应过渡态等关键信息,为反应机理提供确切的理论指导。
3)CO由低浓度催化氧化向高浓度催化燃烧反应过程的过渡。CO在工业、交通业及生活中的排放浓度不尽相同,导致催化燃烧过程有所不同。目前低浓度CO方面,CO优先氧化、汽车尾气净化等领域一直是研究热点,通过在Cu-Ce基催化剂中添加少量贵金属,可以很好地实现低温CO氧化。鉴于目前CO催化燃烧的微观反应机理研究局限于本征反应动力学阶段,现有研究成果尚能对低温条件下的CO催化燃烧现象做出诠释。但CO催化燃烧处于不同温度段,反应过程与机理可能不同[46],课题组最近研究发现,CO自持催化燃烧实质为反应放出的热量在催化剂床层的局部区域大量累积,放热量远大于散热量,使该部分床层表面出现瞬态热化学飞温直至达到CO完全转化的现象,并以反应物覆盖度随温度变化为依据,初步建立了飞温动力学模型[47],而在反应参数敏感性飞温判据方面仍需完善,由此引起多种反应途径共存,需进一步探讨。
4)研发低成本、规模化低温高效催化剂合成技术,实现工业化应用。目前SCR催化剂在脱硫脱硝方面实现了较好地工业应用,但其长时间高抗硫抗水性能要求阻碍其发展。在CO催化燃烧方面,也应加强产学研结合,让催化剂从实验室走向实际工业应用中,长时间切实考察复杂烟气环境下催化剂的各项性能,针对性地改进、优化催化剂合成策略。
4 结 语
工业炉窑、冶金工业生产过程以及机动车尾气排放等方式造成大量CO排放,催化燃烧技术是有效限制并消除CO的主要技术之一,对推动我国节能减排工作进程具有重要意义。目前Cu-Ce复合氧化物催化剂以其低温高效、寿命长以及廉价等优点成为应用于CO催化燃烧的主流催化剂之一。制备形貌可控、原子利用率高的低温高效催化剂,在明确Cu-Ce催化剂构效关系与载体-活性组分强相互作用的基础上,深入研究CO催化燃烧微观反应机理(M-K、L-H机理),构建反应过程的定性定量描述是实现反应机理精准确定的关键。建立低浓度CO向高浓度CO催化燃烧反应过程的拓展机制,构建本征反应动力学与飞温动力学模型下的CO催化燃烧全过程分析方法。在未来形成一套完善的纳米可控Cu-Ce催化剂上宽CO浓度反应机理的原位定性定量分析方法,并从模型的角度揭示CO自持催化燃烧过程中“起燃”、“自持”和“熄火”本质,为反应器设计提供指导,建立完善的CO催化燃烧安全控制理论,实现实验室试验向工业示范应用的过渡。
