核桃青皮制备高含氧量多孔炭及其对Ni2+的吸附性能
2020-11-13余健星余谟鑫朱博文
余健星,余谟鑫,2,蒯 乐,朱博文
(1.安徽工业大学化学与化工学院,马鞍山243000;2.中钢天源股份有限公司,马鞍山243000)
随着新能源汽车和电动车的普及,动力电池的正极开始广泛使用高镍的三元材料,其中高能量密度的NCM811电池备受关注[1].但是处理废旧的NCM811电池过程中会产生大量高浓度和低浓度的Ni2+,Co2+,Mn2+废液,这些重金属离子可以和生物酶的非活性位点结合,破坏生物酶的活性位点,导致生物重金属中毒,引起炎症、神经衰弱症、系统紊乱和癌症等疾病[2].采取有效、绿色且经济的处理工艺对重金属离子废弃物进行处理,减少废水中重金属污染,并回收利用重金属已成为环境保护领域的重要研究课题.
目前,主要采用化学沉淀法、离子交换法、膜分离法、电化学法和吸附法等对重金属离子的废水进行处理,这些方法中吸附法相对于其它方法具有操作更加简便、吸附容量更大和可再生循环使用等优势,从而备受关注[3]. 吸附法的核心是吸附剂. 沸石[4]、离子交换树脂[5]、壳聚糖[6]和多孔炭[7]等吸附剂对于重金属离子均有一定的吸附能力,其中多孔炭材料吸附剂有更大的吸附容量,易脱附再生且更加经济[8]. 如Huang等[9]利用改性商品炭对有色玻璃废弃物中Ni2+的最大吸附量为35.39 mg/g.Balog等[10]制备的原始和氧化的N掺杂多孔碳纳米管对Ni2+的最大吸附量分别为25.8和29.2 mg/g,说明氧含量的提高有利于提高其吸附量.Arukkani[11]对多孔炭进行改性后对Ni2+的最大吸附量为68.1 mg/g.生物质炭材料具有较大的比表面积、发达的孔隙结构、丰富的含氧官能团等特点,作为炭材料吸附重金属有天然优势. 徐建玲等[12]利用聚乙烯亚胺(PEI)功能化秸秆生物炭对水中Cr6+进行吸附.Kołodyńska等[13]研究了生物质炭(BC)和商业炭(AC)吸附Pb2+,Cd2+,Cu2+,Zn2+和Co2+,虽然BC的比表面积(115.5 m2/g)远远小于AC,但是在pH=5时,BC对上述5种离子最大吸附量分别为37.80,33.90,24.92,23.26和20.23 mg/g,而AC几乎没有吸附效果.BC结构稳定,含有大量的含氧官能团,表面带有负电荷,有很强的离子交换能力.
中国核桃的产量位居世界第一,核桃青皮是生产核桃副产的一种农林废弃物,相对容易收集.核桃青皮含有大量的木质素、纤维素、单宁和色素等[14].利用核桃青皮制备生物质炭材料吸附金属离子具有较好的应用前景.本文将核桃青皮制备成炭材料,考察了其对Ni2+的吸附性能,并通过分析构效关系阐明了吸附机理.
1 实验部分
1.1 试剂与仪器
硝酸镍和硝酸(分析纯),阿拉丁试剂(上海)有限公司;核桃青皮,由河南三门峡炸街果旗舰店提供;纯水,由安徽工业大学提供.
Nicolet is 50型傅里叶变换红外光谱仪(FTIR),分辨率为4.0 cm-1,扫描波长为400~4000 cm-1,美国Thermo ESCALAB公司;250型X射线光电子能谱(XPS),扫描范围为0~1350 eV,美国Thermo ESCALAB公司;ICPS-7510 PLUS型电感耦合等离子体原子发射光谱仪(ICP),日本岛津公司;Nanosem430型扫描电子显微镜(SEM),美国FEI公司;3H-2000PS1型自动氮气吸附仪(BET),将样品在200℃下处理4 h,测定多孔炭的比表面积和孔容等结构参数,并运用BET模型和BJH法进行计算,贝士德仪器科技(北京)有限公司;GSL-1600X型高温真空管式炉,合肥科晶材料技术有限公司.
1.2 核桃青皮炭的制备
将核桃青皮用蒸馏水洗涤数次,去除灰尘和杂质,放入烘箱在100℃下干燥48 h,将干燥后的核桃青皮用电动粉碎机粉碎,过100目筛,得到核桃青皮粉.再称取一定量核桃青皮粉与纯水按质量比1∶5混合,搅拌1 h,放入内衬为聚四氟乙烯的高压反应釜中,于200℃反应16 h,得到核桃青皮炭前驱体.将核桃青皮炭前驱体放入高温真空管式炉,以40 mL/min流速通入高纯氮气作保护气,升温至不同温度(700,750和800℃)并保温180 min,冷却,研磨所得炭材料,过100目筛,得到的核桃青皮炭记为HBCx,其中x代表活化终温度.
1.3 吸附实验
在纯水中溶解硝酸镍,配制不同浓度的Ni2+溶液,用0.1 mol/L HNO3调节pH=6.00,与炭材料HBCx混合,研究其吸附等温线、吸附动力学和动态吸附过程.
1.3.1 吸附等温线 在25℃下,向50 mL不同浓度(25,50,100,200,300,400,600 mg/L)Ni2+溶液中分别添加30 mg HBCx,在1440 min后取一定量溶液,测量吸附后的浓度,研究炭材料吸附等温线.HBCx对金属离子的吸附量qt(mg/g)和去除率η(%)用下式计算[15,16]:

式中,qt为吸附时间t(min)时吸附剂对吸附质的吸附量(mg/g);c0为溶液开始时吸附质的浓度(mg/L);ct为吸附时间t时吸附质的浓度(mg/L);V为吸附质的体积(L);m为吸附质的质量(g).
为了研究单组分体系条件下,炭材料对于金属离子的吸附机理,分别使用Langmuir和Freundlich吸附等温方程进行拟合[16,17]:

式中,ce为吸附质在溶液中的浓度(mg/L);qe为单位质量吸附剂的吸附量(mg/g);Q为吸附达到平衡时单层的最大吸附量(mg/g);KL为表面吸附亲和性常数(L/mg);KF为吸附剂相关的吸附能力常数.
1.3.2 吸附动力学 在25℃下,将300 mg HBCx加入装有500 mL 100 mg/L Ni2+溶液的烧杯中,放入恒温振荡摇床.在10,30,60,120,240,480,960和1440 min时分别取一定量的溶液,测量吸附后的浓度,研究炭材料的吸附动力学;为了研究单组分体系条件下炭材料对于金属离子的吸附机理,分别使用准一级动力学和准二级动力学模型对吸附数据进行拟合[18,19]:

式中,K1为拟一级吸附速率常数(min—1);K2为拟二级吸附速率常数(g·mg—1·min—1).
1.3.3 动态吸附 在25℃,不同流速(1和2 mL/min)条件下研究炭材料HBCx的动态吸附过程.向长10 cm、内径0.8 cm玻璃材质的吸附柱中加入30 mg HBC800,上下两端用脱脂棉花固定,由初始溶液端开始(50 mg/L Ni2+),由蠕动泵将溶液泵入吸附柱,溶液由下端进入吸附柱,从上端流出,再进入收集装置,过滤,测量溶液中金属离子浓度,进行穿透曲线实验.
2 结果与讨论
2.1 SEM分析
图1是HBCx和HBC800吸附Ni2+后的SEM照片.如图1(A)~(C)所示,随着最终活化温度的升高,内部炭骨架被拉伸,孔道被扩大,使其比表面积增大.大量的大孔(约2 μm)均匀地分布在HBCx上,这样的大孔有利于金属离子在炭材料表面和内部的转移.随着活化温度的升高,炭材料表面变得更加粗糙,孔道也更加明显,有更多的活性官能团暴露在炭材料表面,这些均是有利于吸附金属离子的结构[20].另外,HBCx表面呈现出褶皱状形貌,褶皱区域具有较高的表面能,有利于吸附过程[21].如图1(D)所示,HBC800吸附Ni2+后,材料表面显示不同程度的堆积,孔道被堵塞,这种形貌的变化一方面可能是由于炭材料孔道内部吸附大量的Ni2+和炭材料表面的化学基团与Ni2+的络合形成较强的胶黏力;另一方面,炭材料中的无机盐和电离出的OH—会导致金属盐沉积或者是金属氢氧化物的沉淀附着在炭材料表面[22].

Fig.1 SEM images of the samples HBC700(A),HBC750(B),HBC800(C)and HBC800⁃Ni2+(D)
2.2 BET分析
图2为不同活化温度制备的HBCx的吸附-脱附曲线及孔径分布图,由图2(A)可知,在0~0.2相对压力下,HBCx对氮气的吸附量快速增加,说明有小于2 nm的微孔存在;在相对压力较高情况下,吸附和脱附曲线不再重合,二者出现了明显的滞后环现象,为Ⅰ型和Ⅳ型等温线特征的结合,说明存在一定量的微孔和中孔.根据BJH(Barrett-Joyner-Halenda)法计算的孔径分布图说明孔径主要分布于0.5~2 nm和2~10 nm范围内[图2(B)],表明HBCx具有分级的多孔结构.金属离子在水溶液中会形成金属离子的水合物,Ni2+水合半径约为0.4 nm,大微孔和小中孔有利于吸附进行[23].前期研究[24]中未经过水热过程直接高温活化的核桃青皮炭材料比表面积极小,没有微孔和中孔孔容,不利于吸附过程.
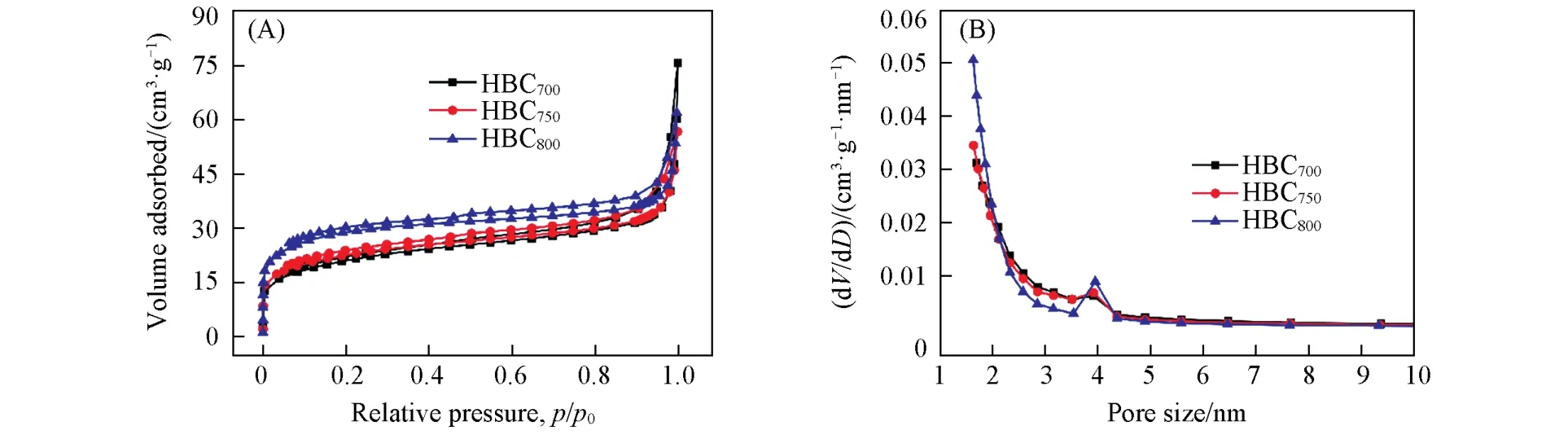
Fig.2 N2adsorption⁃desorption isotherms(A)and pore size distributions(B)of the samples
表1列出了不同HBCx的比表面积(SBET)和平均孔径(Dap).从表1可见,随着最终活化温度的升高,所制备的多孔炭比表面积不断增加,平均孔径减小.其中,HBC800比表面积可达94.39 m2/g.

Table 1 Specific surface area and pore structure parameters of HBCx*
2.3 FTIR分析
图3是HBCx吸附Ni2+前后的FTIR谱图.在FTIR谱图中有大量的吸收峰,说明HBCx上存在大量的化学官能团.图中3420 cm—1处是自由氨基(—NH2)和羟基键(—OH)伸缩振动峰,吸附后样品HBC800的峰强明显减弱,分子间的氢键作用力减弱,可能是—NH2和—OH活性位被Ni2+占据,吸附过程存在离子交换作用;1625 cm—1处的吸收峰对应—C=O键的伸缩振动,吸附前后峰强度有轻微减弱和偏移,可能是—COOH中H+与Ni2+发生离子交换;1448 cm—1处的吸收峰对应芳香族化合物的伸缩振动,吸附前后峰强度均有明显的减弱和偏移,可能是由于芳香族化合物提供的π电子与Ni2+形成能量较小的稳定结构;1070 cm—1处的吸收峰对应脂基、酸酐等官能团的伸缩振动;875 cm—1处的吸收峰对应吡啶和杂环化合物中C—H键的伸缩振动,可能是Ni2+与官能团的离子交换引起的[25~27].

Fig.3 FTIR spectra of HBC700(a),HBC750(b),HBC800(c)and HBC800⁃Ni2+(d)
2.4 XPS分析
图4(A)和(B)为不同活化温度制备的HBCx吸附Ni2+前后的XPS全谱图,HBCx含有大量的C,N和O元素.吸附Ni2+后HBCx的XPS谱图上均出现了明显的Ni2p峰,说明材料对Ni2+有优良的吸附性能.
由表2可知,随着最终活化温度的升高,HBCx的C含量减少,O含量增加,N含量先减少后增加,这可能是由于温度升高,使木质素碳化骨架断裂,损失部分的含N官能团,纤维素和半纤维素碳化组成的填充物暴露在炭材料的表面,其上有更多的含O官能团,从而使O含量增加;随着温度的进一步升高,炭材料内部的填充物更多地暴露,其上的有机官能团更多,同时提高了N,O含量.HBC800的O,N含量最高,分别为21.24%和3.77%,由此可知,HBC800中含N和O官能团较多,有利于吸附.而同类型生物质炭材料氧含量仅为10%~20%[28].
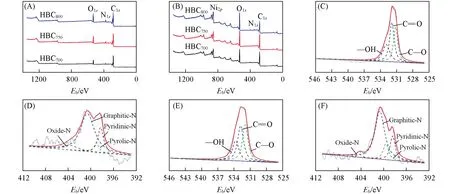
Fig.4 XPS spectra of the samples
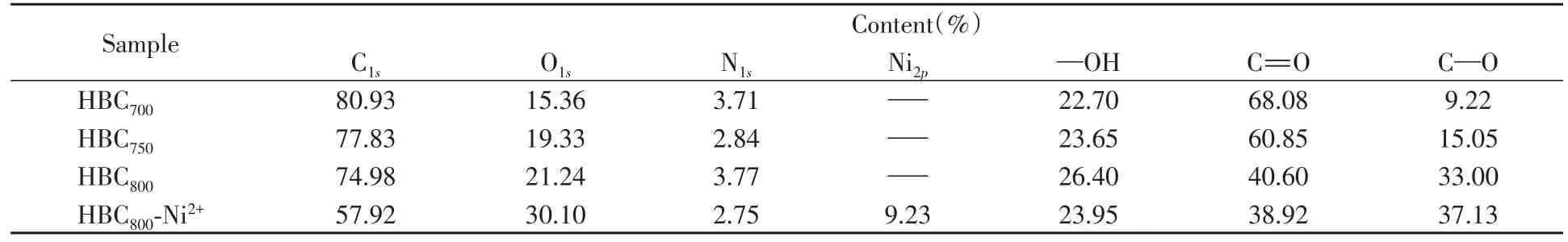
Table 2 Element contents or organic functional groups of XPS analysis
在吸附Ni2+后材料含氧量增加[见图4(C)和(E)],有以下4种可能原因:HBCx有机官能团和Ni2+的水合离子发生了化学吸附,形成较强的作用力;材料中的无机成分与Ni2+反应形成沉淀;炭材料电离出的OH-形成Ni(OH)2沉淀使其附着在材料表面,增加了材料的含氧量;XPS表征主要是表面成分分析,因此表面组分的变化对其结果影响较大.从图4(D)和(F)中可以明显看出,吸附前后N的峰强度差别较大,这主要有以下2种可能:N元素形成的官能团参加了反应,可能是HBCx上—NH2等含氮官能团与金属离子发生离子交换,使材料表面氮元素含量减少[29];由于引入Ni2+,N元素含量相对减少.由表2可知,吸附Ni2+后N元素含量下降到2.75%,说明由N元素组成的基团在Ni2+吸附过程中主要是起离子交换作用.HBC800吸附Ni2+后O1s含量增陋就简加至30.10%,说明由O元素组成的基团在吸附过程中主要起到共沉淀作用,形成络合物和氢氧化物,附着在炭材料表面.在吸附Ni2+后的材料表面镍元素含量增加,说明Ni2+吸附主要依靠材料表面官能团与其进行络合反应或者共沉淀[30].从上述Ni2+吸附前后元素含量的变化,说明HBCx表面官能团的性质有利于吸附Ni2+.
2.5 吸附性能研究
2.5.1 吸附等温线 图5(A)~(C)分别为HBCx对Ni2+的吸附等温曲线、Langmuir模型和Freundlich模型拟合曲线.可见,3种生物质炭材料对Ni2+的吸附均有较好的效果,等温线的初始斜率均比较高.Ni2+初始浓度较低时,生物质炭表面有大量的活性位点,只有部分的活性位点被占据,此时生物质炭对于Ni2+的吸附量相对较低,对Ni2+的去除率接近100%.随着溶液初始浓度的增加,生物质炭表面的活性位点被完全占据,孔道内部的活性位点开始进行吸附,此时生物质炭对于Ni2+的吸附量相对较高,对金属离子的去除率逐渐减小.随着溶液初始浓度的进一步增加,孔道内部的活性位点也被逐渐填满,达到吸附平衡,此时生物质炭对Ni2+的吸附量相对最高,对Ni2+的去除率最小.继续增加Ni2+浓度也不会改变其吸附量,此时的最大吸附量与炭材料自身的结构和性质有关,其中炭材料所含有机官能含量和比表面积为主要因素.
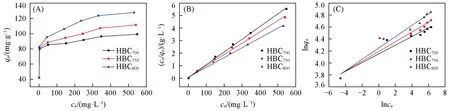
Fig.5 Adsorption isotherm analysis
从表3中Langmuir和Freundlich模型的拟合参数可知,Langmuir模型拟合效果优于Freundlich模型.Langmuir吸附模型拟合的相关性系数(R)皆大于0.995,说明HBCx吸附Ni2+主要为单分子层吸附,即吸附以化学吸附为主,也存在层间扩散的多分子层吸附.HBC800对Ni2+的理论吸附量(qm)高达127.39 mg/g.Freundlich模型拟合的1/n均小于1,说明该吸附过程是一个易于吸附的过程.HBCx对于低浓度(25 mg/L)的Ni2+溶液吸附后通过ICP(对Ni2+检出限为0.008 mg/L)进行检测为未检出,因此,HBCx对Ni2+溶液去除率接近100%,达到国际上含镍废水的可排放标准[31].
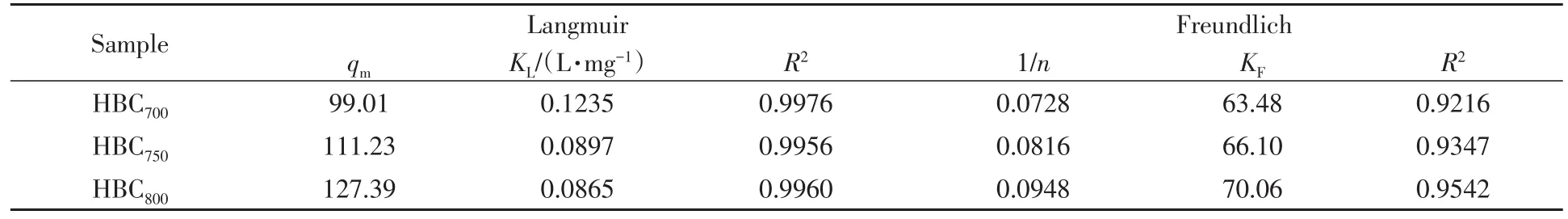
Table 3 Parameters of Langmuir and Freundlich model for the adsorption of Ni2+on HBCx
2.5.2 吸附动力学 图6(A)~(C)分别为HBCx对Ni2+的吸附动力学曲线、拟一级动力学模型和拟二级动力学模型拟合曲线.由图6可知,HBCx对Ni2+的吸附速率很快,在200 min左右基本达到平衡.在吸附初期,因为生物质炭表面有大量的活性位点,只有表面部分的活性位点被占据,此时生物质炭对于Ni2+的吸附量相对较低,对金属离子的去除率较小.随着时间的延长,生物质炭表面的活性位点被完全占据,孔道内部的活性位点开始进行吸附,此时生物质炭对Ni2+的吸附量相对较高,对Ni2+的去除率逐渐增大.随着时间的进一步延长,孔道内部的活性位点也被逐渐填满,此时达到吸附平衡,此时生物质炭对Ni2+的吸附量相对最高,对金属离子的去除率最大,继续延长吸附时间也不会改变其吸附量.
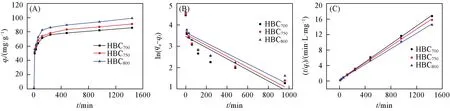
Fig.6 Adsorption kinetics analysis
由表4中的吸附动力学拟合参数可见,准二级动力学模型的相关系数R2远大于准一级动力学模型,从图6中也可见,实验结果能够用准二级动力学模型很好地进行模拟,它们的相关系数R2均大于0.998,且理论计算所得值与实验值十分接近,所以该吸附过程吸附速率主要由化学吸附所控制.

Table 4 Adsorption kinetics parameters for Pseudo-first-order model and Pseudosecond-order model of Ni2+on HBCx
2.5.3 动态吸附 图7为HBC800在不同流速(1,2 mL/min)时对Ni2+的吸附穿透曲线.流速为1 mL/min时HBC800对Ni2+的穿透时间为12 min,耗竭时间为70 min;流速为2 mL/min时,穿透时间为18 min,耗竭时间为128 min.HBC800对Ni2+有优良的吸附性能,有将其用于工业处理Ni2+实践的可能.
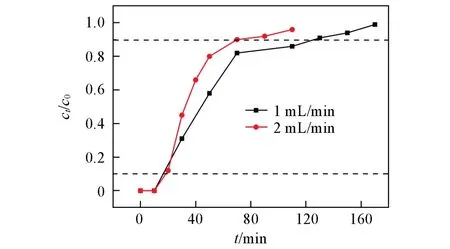
Fig.7 Breakthrough curve for Ni2+dynamic adsorp⁃tion on HBC800
2.6 吸附机理分析
Scheme 1为HBC800对Ni2+吸附机理图.由上面的表征分析和吸附实验可知,HBC800具有高度芳香化和杂环化的结构,金属阳离子与HBC800中的π电子相互作用,一些化学官能团可与Ni2+发生离子交换,形成稳定结构,这与吸附过程主要由化学吸附所控制的结论一致.离子交换、共沉淀和静电吸附等可能是Ni2+在HBC800上的吸附机制,其吸附机理如下式所示:
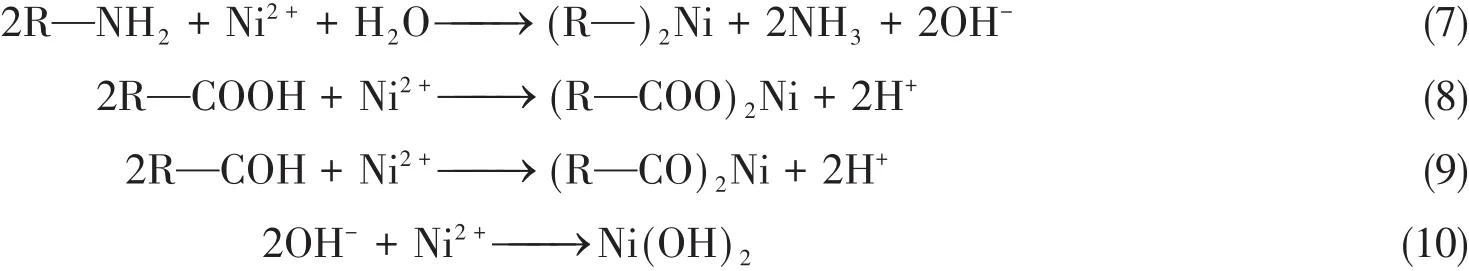
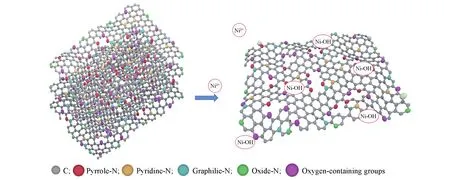
Scheme 1 Adsorption mechanism of Ni2+on HBC800
2.7 与其它吸附剂的比较
表5列出了不同吸附剂在最佳条件下对Ni2+的最大吸附量.与其它炭类吸附剂和合成类吸附剂相比,本文所制备HBC800对Ni2+的最大吸附量是其它吸附剂的2~5倍.所制备的吸附剂为每千克13元,这远远低于其它吸附剂的制备成本.从吸附效果和速率上看,本文所制备的吸附剂实用性要高于其它类吸附剂.因此,本文所制备的炭材料是一种经济、高效且环保的吸附剂.

Table 5 Adsorption capacity of different adsorbents for Ni2+
3 结 论
废旧锂电池处理过程中会产生大量的含镍废水,为了制备廉价的吸附剂,以核桃青皮为原料,先用水热法制备其炭前驱体,然后以不同的最终活化温度得到生物质炭(HBCx).采用SEM,FTIR,BET和XPS等手段对HBCx进行了表征,并考察了其对废旧电池废水中高浓度和低浓度Ni2+的吸附性能.SEM和BET表征结果表明,大量的大孔(约2 μm)均匀地分布在HBCx上,HBCx具有分级多孔结构,当活化温度为800℃,所得HBC800样品的比表面积为94 m2/g,平均孔径为4.07 nm.FTIR和XPS表征结果表明,炭材料表面含氧和含氮官能团丰富,氧含量高达21.24%(摩尔分数),可与Ni2+发生离子交换或共沉淀,这些基团有利于吸附过程.所制备的多孔炭对废液中低浓度的Ni2+去除率接近100%,表现出优异的吸附性能;Langmuir等温模型能很好地描述HBCx对Ni2+的吸附过程,HBC800对Ni2+的最大理论吸附量高达127.39 mg/g.吸附动力学结果表明,该吸附过程遵循准二级动力学方程,表明吸附速率主要受化学吸附控制.离子交换,共沉淀和静电吸附等可能是重金属离子在生物质炭上的吸附机制.以上结果表明,该生物质炭在含镍金属离子废水治理上具有广阔的应用前景.
