不同孕周使用小剂量阿司匹林预防子痫前期的临床应用
2020-11-12郑雯娜邓星梅唐淞源李涛会卢丽萍
郑雯娜,邓星梅,唐淞源,张 瑗,李 涛,李涛会,陈 荣,卢丽萍,付 瑞
(曲靖市妇幼保健院医学遗传与产前诊断科,云南曲靖 655000)
妊娠期高血压疾病(hypertensive disease of pregnancy,HDP) 是人类妊娠期重要的疾病,包括妊娠期高血压,子痫前期(pre-eclampsia,PE),子痫(eclampsia),慢性高血压并发子痫前期及妊娠合并慢性高血压。我国HDP 发病率为5%~12%,其中15%~25%具有子痫前期高危因素的HDP 患者将随妊娠进展发展成子痫[1]。PE 是造成发展中国家和发达国家孕妇死亡的主要原因之一,占妊娠相关死亡率的10%~16%[2-3],也是围产儿病死率升高的主要原因。因此,早期识别子痫前期高危因素并进行有效干预,对该病的防治具有重大意义。近年来,小剂量阿司匹林(low-dose aspirin,LDA) 预防PE 临床应用日渐广泛,但何时启动预防PE 尚存争议[4-5],国内对不同孕周使用LDA 分析比较也少见报道,本研究现对不同孕周启动LDA 预防PE 的临床效果进行评价。
1 资料与方法
1.1 一般资料
选取2018 年5 月至2020 年1 月在曲靖市妇幼保健院产科门诊产检筛查出的具有PE 高危因素的孕妇196 例,其中使用LDA 95 例,未使用LDA的孕妇101 例。高危因素包括:(1) 孕妇年龄大于40 岁;(2) 子痫前期病史;(3) 抗磷脂抗体阳性;(4) 高血压史;(5) 慢性肾炎;(6) 糖尿病或遗传性血栓形成倾向;(7) 初次产检BMI大于35 kg/m2;(8) 子痫前期家族史;(9) 多胎妊娠;10、早孕期收缩压>130 mmHg 或舒张压>80 mmHg。根据首次服用LDA 时间和产检推荐孕周,分为孕11~13+6周、14~19+6周、20~24 周三组干预组。干预组纳入标准: (1) 无用药禁忌;(2) 愿意规律服用LDA;(3) 未服用降压药或抗凝治疗者;(4) 无胎儿畸形。对照组纳入标准: (1) 11~24 周未使用和/ 或未规律使用LDA;(2) 24 周后服用或未服用降压药和/或抗凝治疗。
1.2 干预方法
根据LDA 使用时间不同,将患者分为孕11~13+6周小剂量阿司匹林干预组(31 例),孕14~19+6周小剂量阿司匹林干预组(35 例),孕20~24周小剂量阿司匹林干预组(29 例)。每组干预组给予小剂量阿司匹林100 mg,睡前口服至孕36 周。
1.3 观察指标
比较三个干预组在不同孕周使用LDA 的母儿妊娠结局,包括(1) 子痫前期;(2) 胎儿生长受限(fetal growth restriction,FGR);(3) 胎盘早剥;(4) 产后出血,称重法估算阴道分娩和剖宫产后24 h 内出血量,阴道分娩者出血量>500 mL,剖宫产者>1 000 mL 定义为产后出血;(5) 剖宫产率。
1.4 统计学处理
使用SPSS 软件对患者数据进行统计学分析,结局指标比较采用卡方检验。P<0.05 为差异有统计学意义。
2 结果
2.1 干预组和对照组妊娠结局比较
干预组中均未发生死胎、死产、孕妇死亡等不良结局,用药期间无不良反应。干预组与对照组PE 发生率比较,差异有统计学意义(P<0.05),两组在FGR、胎盘早剥、产后出血率结局中差异无统计学意义(P>0.05)。干预组剖宫产率为54.74%,对照组剖宫产率为74.26%,干预组剖宫产率明显低于对照组(P<0.05),见表1。
2.2 干预组不同治疗时机妊娠结局比较
在对干预组孕11~13+6周、孕14~19+6周、孕20~24 周孕妇分别进行治疗后,PE 发生率分别为12.90%、22.86%、27.59%;FGR 发生率为3.23%、2.86%,20.69%;胎盘早剥发生率为3.23%、2.86%、6.90%;产后大出血发生率为3.23%、5.71%、10.34% ;剖宫产率分别为58.06%、45.71%、62.07%。三个孕周的子痫前期、胎盘早剥、产后大出血、剖宫产率比较P值均大于0.05,差异无统计学意义。经两两比较,孕11~13+6周FGR 发生率低于20~24+6周孕妇(P<0.05),孕14~19+6周FGR 发生率低于孕20~24+6周孕妇(P<0.05)。可表明20 周前使用LDA 能降低胎儿生长受限发生,见表2。
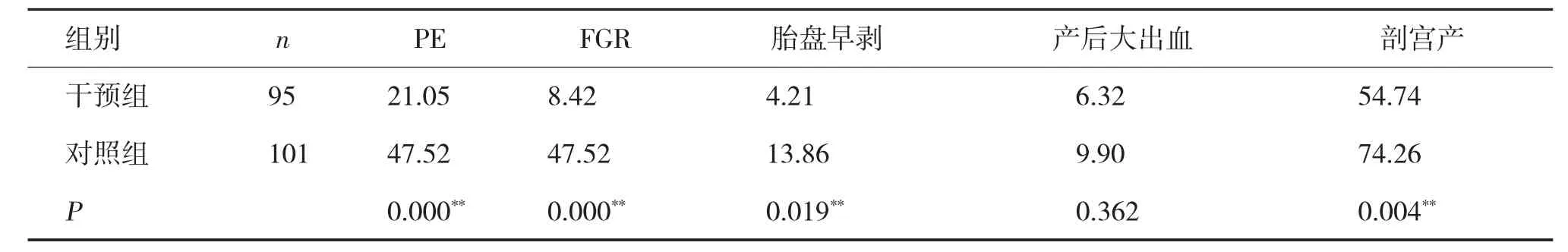
表1 干预组与对照组妊娠结局比较(%)Tab.1 Comparison of pregnancy outcomes between intervention group and control group (%)
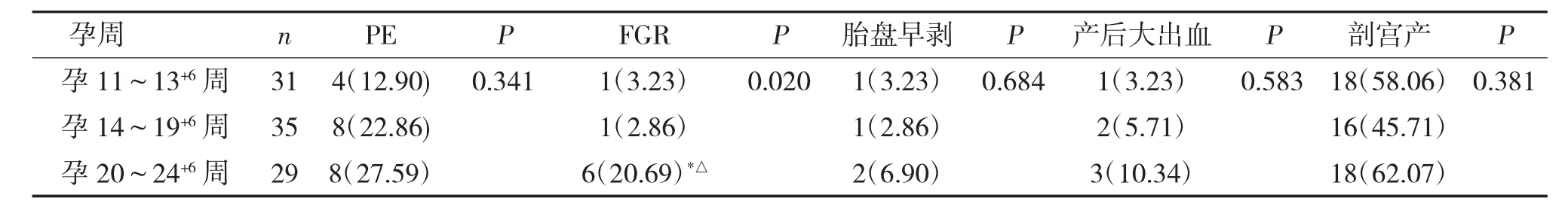
表2 不同治疗时机干预组妊娠结局比较[n(%)]Tab.2 Comparison of pregnancy outcomes in intervention groups with different treatment timing [n(%)]
3 讨论
子痫前期是一种累积多个脏器的复杂综合征,临床可表现为脑组织缺血缺氧,脑出血,昏迷,肝脏水肿坏死,心肾衰竭,危及生命。特别是HELLP 综合征,是子痫前期的严重表现,以溶血,肝酶升高,血小板减少为主要症状,爆发型死亡率100%。子痫前期患者将来罹患慢性高血压、胰岛素抵抗、血脂异常,甲状腺功能减退[6-7]等的风险性亦明显增加。
前列腺素(PG) 在前列腺素合成酶和血栓烷合成酶分别作用下形成血栓素TXA2(thrombinxone-A2,TXA2)和前列环素(prostacyclin,PGI2),TXA2 具有收缩血管、促进附近血小板聚集和诱发血栓形成的作用;PGI2 有抗血小板和舒张血管作用,子痫/子痫前期孕妇中,TXA2 释放增加,PGI2 和内皮舒张因子释放减少,最终导致全身小血管痉挛收缩,血压升高,内皮细胞受损一系列恶性循环[8]。此外,内外源性凝血机制平衡机制被打破[9-10],血小板聚集,血栓形成倾向都是PE 的高危因素。阿司匹林通过乙酰化反应,起到抗血栓以及抗血小板凝聚作用[11],从而可以预防PE。
上世纪80 年代,Wallenburg 等首先报道[12]从孕8 周始服用阿司匹林可使子痫发生率下降,Chiaffarino 等[13]给具有PE 高危因素的孕14 周孕妇服用LDA,得出早期使用阿司匹林有益于降低HDP发病率的结论。Bakhti 等[14]研究发现,自孕8 周~10 周开始口服LDA,妊娠期高血压疾病的发生率下降7%。我国范翠芳等[15]首次对有高危因素的孕妇进行研究发现,18 周起开始口服阿司匹林直至36 孕周停药,孕晚期子痫前期的发生率显著低于对照组。赵应梅等[16]认为有子痫前期高危因素的孕妇13 周~16 周使用可降低PE 发生。2010 年NICE指南提出12 周可开始预防性使用LDA,WHO 推荐12~20 周开始应用LDA[17],段涛等[18]团队认为具有特定PE 高危因素孕妇,可从妊娠11 周,最晚不超过妊娠20 周开始服用LDA。关于LDA 应用最佳时机,一直没有一致结论,在基层临床工作中,一部分孕妇首次产检时间已超过20 周,本研究认为20 周后应用LDA 亦有预防PE 作用,与孙菊英和芮璨等[19-20]报道一致。USPSTF 指南认为对高危孕妇在28 周前仍可使用LDA[21],但本数据表明PE 发生率随着孕周延长有升高趋势,24~28周应用LDA 还需权衡利弊谨慎处之。胎盘早剥、产后出血是妊娠晚期严重并发症,妊娠期高血压疾病是其主要原因之一,由于底蜕膜螺旋小动脉痉挛引起毛细血管缺血坏死,蜕膜静脉床淤血破裂,导致胎盘与子宫壁部分或全部剥离,引起继发性纤溶亢进,最终导致凝血功能障碍,任何原发或继发凝血功能障碍均能造成产后出血。阿司匹林属于抗凝抗栓药物,但小剂量使用不增加胎盘早剥和产后出血率(P>0.05),并能降低剖宫产率(P<0.05),此外20 周前使用LDA 可降低FGR发生率(P<0.05)。
目前,具有高危因素孕妇使用小剂量阿司匹林预防子痫前期虽已得到大部分专家认同,但使用LDA 最佳时机仍无法判定。综上所述,具有PE高危因素的孕妇,在11~24 周启动LDA 治疗能降低PE 发生率,改善妊娠结局。实际工作中,除了提前识别高危因素,对于一部分就诊晚的孕妇,排除用药禁忌后24 周前积极采取预防措施也是大有裨益的。
