高效液相色谱-电感耦合等离子体质谱法测定食用菌中无机汞和甲基汞
2020-11-06陈绍占刘丽萍张妮娜周天慧
陈绍占,刘丽萍,3∗,张妮娜,周天慧
(1.北京市疾病预防控制中心食物中毒诊断溯源技术北京市重点实验室,北京 100013;2.北京市预防医学研究中心,北京 100013; 3.首都医科大学公共卫生学院,北京100069)
汞在自然界中分布很广,汞是对人类和环境最具危害性的元素之一。食品中的汞污染由来已久,汞的测定一直是食品安全关注的问题。汞及其化合物具有很强的毒性,汞对生物的毒性不仅取决于其含量,更与其存在的化学形态及生物本身密切相关,一般来说,烷基汞的毒性比芳基汞和无机汞的毒性大[1]。无机汞易通过生物甲基化作用生成毒性更强的烷基汞,并通过食物链的富集作用进入人体,对环境和人类健康构成极大的安全隐患[2]。相比于绿色植物,蘑菇更易富集高含量的铅、砷、镉和汞等重金属元素,这会给消费者带来严重危害[3-5]。虽然GB/T 2762-2017《食品安全国家标准食品中污染物限量》规定了食用菌及其制品中总汞限量为0.1 mg·kg-1,但仅对水产动物及其制品、肉食性鱼类及其制品中甲基汞的含量进行了规定。我国是食用菌消费大国,也是食用菌出口大国,因此准确测定食用菌中甲基汞的含量对食品安全风险评估具有重要意义。目前关于食用菌中甲基汞测定的报道较少,急需建立相应的测定方法以保障食品安全。
目前,常见的测定汞形态的方法主要有液相色谱-原子荧光光谱法(LC-AFS)[6-8]、液相色谱-电感耦合等离子体质谱法(LC-ICP-MS)[9-11]和气相色谱-质谱法(GC-MS)[12-14]。其中LC-ICP-MS 具有连接简单、灵敏度高、线性范围宽、抗干扰能力强等优点,已成为测定汞形态的主流方法之一。因此,本工作采用高效液相色谱-电感耦合等离子体质谱法(HPLC-ICP-MS)对食用菌中的无机汞及甲基汞进行测定。
1 试验部分
1.1 仪器与试剂
1260型高效液相色谱仪;7700x型电感耦合等离子体质谱仪;Milliplus 2150型超纯水处理系统;KQ-500DV 型数控超声清洗器(可控温20~80 ℃);Universal 32 型高速离心机;8010s 型粉碎机。
无机汞标准储备溶液:100μg·g-1。
甲基汞标准储备溶液:(65.2±2.5)μg·g-1,以甲醇为溶剂。
调谐液:含1μg·L-1的锂、镁、钇、铈、铊、钴。
盐酸、氨水均为优级纯;乙酸铵为分析纯;L-半胱氨酸为生化试剂;甲醇为色谱纯;试验用水为超纯水。
1.2 仪器工作条件
1)HPLC 条件 Agela Technologies Venusil MP C18色谱柱(150 mm×4.6 mm,5μm);流动相为3%(体积分数,下同)甲醇-40 mmol·L-1乙酸铵-1 g·L-1L-半胱氨酸混合液;流量1.0 mL·min-1;进样体积50μL。
2)ICP-MS条件 射频功率1 550 W;采样深度8 mm;雾化室温度2 ℃;载气流量0.85 L·min-1,补偿气流量0.15 L·min-1;监测质量数为202;积分时间为0.5 s;蠕动泵转速为0.3 r·s-1。
1.3 试验方法
称取干食用菌样品0.200~1.000 g置于15 mL塑料离心管中,加入5 mol·L-1盐酸溶液10 mL,在冰水浴中超声提取60 min,期间振摇数次,然后在4℃下以8 000 r·min-1转速离心15 min。移取2 mL上清液至5 mL容量瓶或刻度试管中,在冰水浴中逐滴加入50%(体积分数,下同)氨水,调节样品溶液pH 至3~7,再加入10 g·L-1L-半胱氨酸溶液0.1 mL,最后用水稀释至刻度,经0.45μm 有机系滤膜过滤,在仪器工作条件下进行测定。同时做空白试验。
2 结果与讨论
2.1 流动相的选择
试验初期以甲醇-60 mmol·L-1乙酸铵-1 g·L-1L-半胱氨酸混合液作为流动相,考察了流动相中甲醇的体积分数依次为1%,2%,3%,4%,5%时对无机汞和甲基汞的峰面积和保留时间的影响,结果见图1和图2。
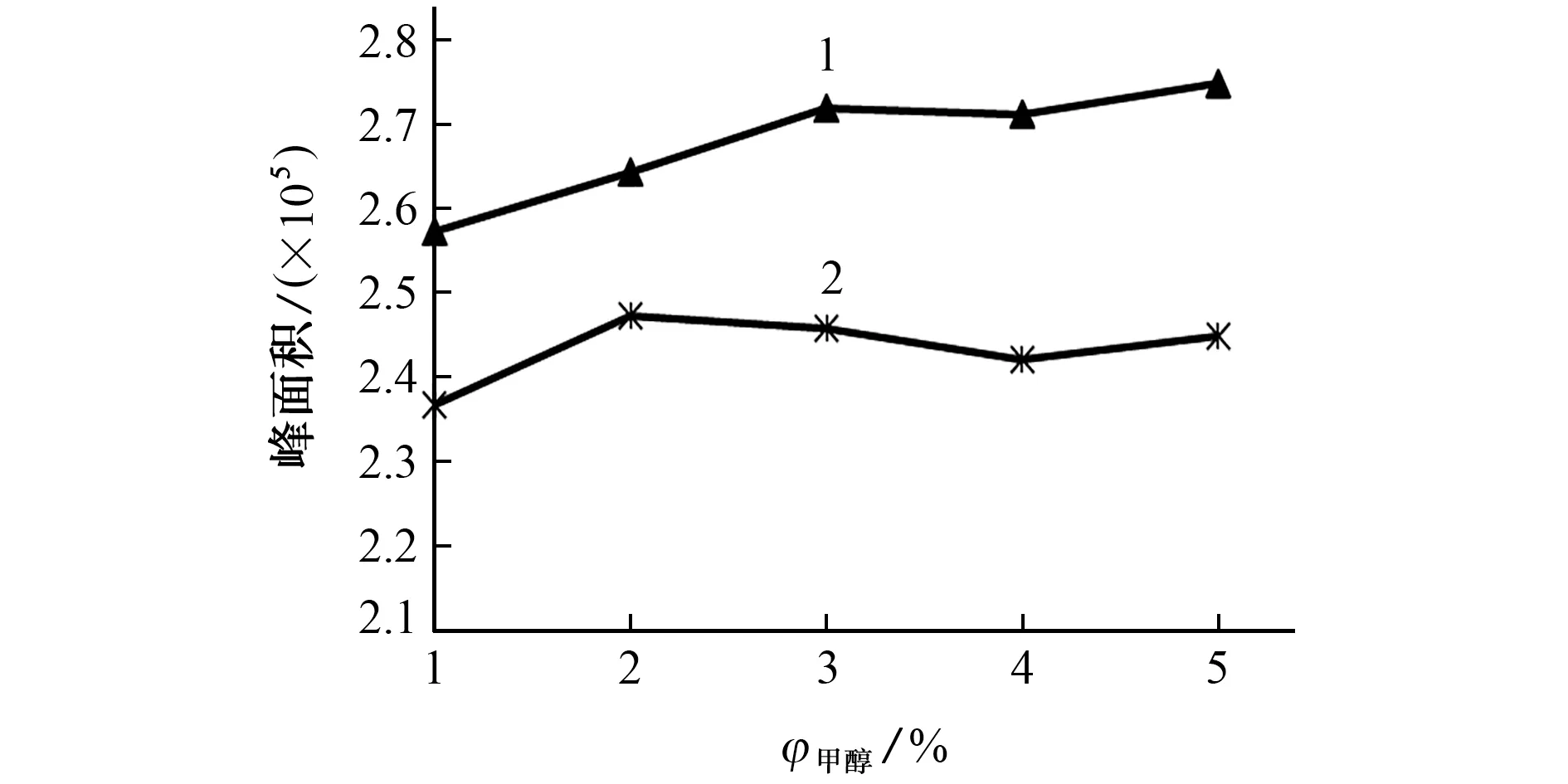
图1 甲醇的体积分数对无机汞和甲基汞峰面积的影响Fig.1 Effect of volume fraction of methanol on peak area of inorganic mercury and methylmercury
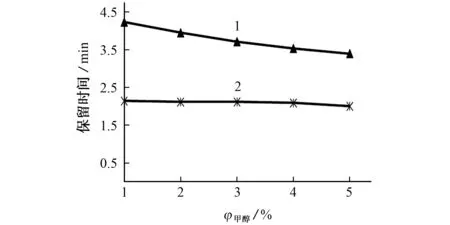
图2 甲醇的体积分数对无机汞和甲基汞保留时间的影响Fig.2 Effect of volume fraction of methanol on retention time of inorganic mercury and methylmercury
由图1可知:流动相中加入甲醇对无机汞、甲基汞的测定具有增敏作用;当甲醇的体积分数超过3%时,增敏作用不再明显增强;甲醇体积分数为2%时,无机汞的信号最佳;随着甲醇体积分数的增加,甲基汞的峰面积逐渐增加。
由图2可知:随着甲醇体积分数的增加,无机汞的保留时间基本不发生变化,甲基汞的保留时间逐渐减小。故甲醇体积分数过大,会导致无机汞和甲基汞分离度变差。
综上所述,同时考虑到长时间将高含量的有机相进入仪器,会在电感耦合等离子体质谱仪的采样锥和截取锥上产生碳富集,进而影响灵敏度,对采样锥和截取锥损耗也较大。试验选择流动相中甲醇的体积分数3%。
在实际样品分析过程中发现:食用菌样品中无机汞含量过高会导致峰拖尾,从而影响甲基汞的测定。为了保证无机汞和甲基汞具有较好的分离度,试验中适当降低流动相中乙酸铵的浓度,同时该操作还可以有效延长色谱柱的使用寿命。综合考虑,试验选择流动相为3%甲醇-40 mmol·L-1乙酸铵-1 g·L-1L-半胱氨酸混合液。
2.2 ICP-MS条件的选择
开机预热后,使用调谐液对仪器各项参数进行调谐,使灵敏度、氧化物、双电荷及背景噪声达到要求,将优化的各项参数保存到分析方法中。
汞在自然界中共有6个同位素,其中丰度比较高的同位素有199Hg、200Hg、201Hg、202Hg,丰度分别为16.87%,23.10%,13.18%,29.86%。上述同位素分别容易受到183W16O、184W16O、185Re16O、186W16O等多原子离子的干扰,然而可能存在干扰的物质几乎不存在于食品基体中。试验选择了丰度最高的202Hg的质量数202 作为监测的质量数,样品基质中无质谱干扰。
试验选择的ICP-MS条件见1.2节。
2.3 前处理条件的选择
目前食品样品的提取多采用5 mol·L-1盐酸溶液作为提取剂。高效液相色谱-原子荧光光谱法测定汞形态可采用氢氧化钠溶液中和盐酸溶液调节酸度。但采用高效液相色谱-电感耦合等离子体质谱法测定时,采用氢氧化钠溶液中和盐酸溶液会引入高含量的钠盐,导致等离子体的电离效率及稳定性降低,影响数据结果的稳定性。试验选用50%氨水调节酸度。
样品溶液酸碱性对无机汞和甲基汞测定的影响见图3。

图3 样品溶液酸碱性对无机汞和甲基汞测定的影响Fig.3 Effect of acidity and alkalinity of sample solution on determination of inorganic mercury and methylmercury
由图3可知:若样品溶液调至弱碱性,无机汞和甲基汞保留时间后移,且在无机汞原出峰位置有个明显的倒峰,影响无机汞的测定,导致无机汞测定结果偏低。试验选择样品溶液为弱酸性。Agela Technologies Venusil MP C18色谱柱属于中等极性柱,适用pH 范围较宽(1.5~8.5)。将pH 控制在3~7即可保证测定结果的准确性,又可有效保护色谱柱。
超声提取时,为避免水分子振荡摩擦使水温升高,可通过加注冰水降温使水温控制在50 ℃以下。
中和反应滴加50%氨水速率不宜太快,避免酸碱中和放热剧烈导致无机汞挥发或甲基汞形态发生转化,影响测定结果。滴加50%氨水时应在冰水浴下逐滴缓慢加入。
2.4 甲基汞标准溶液的稳定性
甲基汞标准储备溶液的溶剂为甲醇,其在冰箱冷冻室(-20 ℃)可保存两年。试验中首先用50%甲醇溶液将甲基汞标准储备溶液稀释成10.00 mg·L-1甲基汞标准溶液,再用流动相将10.00 mg·L-1甲基汞标准溶液逐级稀释至50.00μg·L-1,按仪器工作条件进行测定,监测24 h 内的变化。结果显示:24h 内有0.11%的甲基汞转化为无机汞,为保证测定结果的准确性,甲基汞标准溶液需现用现配。
2.5 标准曲线和检出限
移取适量的无机汞标准储备溶液和甲基汞标准储备溶液用流动相稀释混合配制成0,0.10,0.50,1.00,5.00,10.00,30.00,50.00μg·L-1的无机汞和甲基汞混合标准溶液系列(现用现配)。按仪器工作条件对无机汞和甲基汞的混合标准溶液系列进行测定,以无机汞和甲基汞的质量浓度为横坐标,对应的峰面积为纵坐标,绘制标准曲线。结果表明:无机汞和甲基汞的线性范围均为0.10~50.00μg·L-1,线性回归方程和相关系数见表1。
以3倍信噪比对应的质量浓度为方法的检出限(3S/N),无机汞和甲基汞的检出限见表1。

表1 线性回归方程、相关系数和检出限Tab.1 Linear regression equations,correlation coefficients and detection limits
2.6 精密度和回收试验
按试验方法对食用菌样品进行分析,并进行加标回收试验,平行测定6次,计算回收率和测定值的相对标准偏差(RSD),结果见表2。

表2 精密度和回收试验结果(n=6)Tab.2 Results of tests for precision and recovery(n=6)
由表2 可知:无机汞的回收率为99.4%~103%,RSD 为1.6%~3.0%;甲基汞的回收率为94.6%~96.6%,RSD 为1.7%~4.7%。
2.7 样品溶液的稳定性
向真姬菇样品中加入适量的无机汞和甲基汞混合标准溶液,按试验方法进行分析,监测24 h内测定结果的变化情况,结果见表3。
由表3可知:在监测时间内无机汞的平均回收率为106%,甲基汞的平均回收率为95.5%,说明本方法的稳定性良好。随着监测时间的延长,无机汞的测定值有逐渐增大的趋势,甲基汞的测定值有逐渐降低的趋势,说明甲基汞在样品溶液中存在微量转化的情况。因此,样品提取完成后应在12 h(甲基汞回收率为95.0%)内完成测定,避免长时间放置导致甲基汞向无机汞的转化。

表3 稳定性试验结果Tab.3 Results of test for stability
2.8 方法对比试验
分别按试验方法和GB/T 5009.17-2014《食品安全国家标准食品中总汞及有机汞的测定》中的LC-AFS测定3种食用菌样品中无机汞和甲基汞的含量,结果见表4。

表4 方法对比试验结果Tab.4 Results of test for method comparison μg·kg-1
经配对T检验,3种食用菌样品的P值均大于0.05,说明两种方法的测定结果差异无统计学意义,两种方法测定无机汞和甲基汞的结果一致。
2.9 样品分析
按试验方法对7种食用菌样品中的汞形态进行测定,结果见表5,其中,无机汞、甲基汞总量为无机汞、甲基汞含量的总和,总汞为电感耦合等离子体质谱法测定结果。
由表5可知:样品中无机汞的质量分数为457~1 526 μg·kg-1,甲基汞的质量分数为8.6~134μg·kg-1;无机汞与总汞比值为73.0%~94.4%,甲基汞与总汞比值为1.2%~7.6%;提取效率为80.6%~96.2%。食用菌中汞的形态主要为无机汞,甲基汞的占比较小。

表5 样品分析结果Tab.5 Analytical results of samples
本工作采用高效液相色谱-电感耦合等离子体质谱法测定食用菌中无机汞和甲基汞的含量。方法操作简单、灵敏度高、精密度高、准确度好,与液相色谱-原子荧光光谱法进行对比,结果一致,本方法适用于食用菌中无机汞和甲基汞的测定。
