贝伐珠单抗联合腹腔热灌注化疗治疗结直肠癌并发恶性腹水的临床分析
2020-11-02王会志姜润学
王 霞,王会志,姜润学*
0 引言
恶性肿瘤中结直肠癌男性发病率在全世界范围内居第3位、女性居第3位[1],在我国仅2015年就发现新发病患者37万余,死亡19万余[2],严重威胁着人类的健康。结直肠癌常见的远处转移有肝、肺及腹膜转移等,晚期结直肠癌腹腔内转移并发恶性腹水也是其常见的临床表现,治疗仍然是化疗为首的综合方式。本研究旨在探讨结直肠癌合并恶性腹水患者行贝伐珠单抗(Bevacizumab)联合腹腔热灌注化疗(Hyperthermic intraperitoneal chemotherapy,HIPEC)的临床效果,为临床治疗提供一定的参考依据。
1 资料与方法
1.1 一般资料 依据患者及家属的意愿,对2017年8月至2019年8月期间唐山弘慈医院肿瘤综合治疗科收治的结直肠癌合并恶性腹水患者分别采取Bevacizumab+HIPEC(A组)35例和常规腹腔内注射化疗(B组)60例,两组均联合卡培他滨口服化疗。所有患者实施本治疗前1个月内未实行抗肿瘤治疗,KPS评分>70,预计生存期>3个月,血常规、肝肾功、心电图检查无明显异常。两组患者年龄、性别、体质指数(Body mass index,BMI)、CEA、CA199等一般临床资料比较,差异无统计学意义(P>0.05)。见表1。

表1 两组患者一般临床资料比较
1.2 治疗方法 A组:将腹腔热灌注治疗专用硅胶导管4根(直径5 mm)留置于腹腔内,外接热灌注治疗机,每次应用蒸馏水2 500~3 000 ml+顺铂40 mg+地塞米松5 mg,设置恒温(43±0.5)℃,持续热循环灌注治疗90 min,缓慢放出灌注液,腹腔内注入Bevacizumab 300 mg/m2,在治疗过程中及治疗后预防性应用镇痛、止吐药。B组:行腹腔穿刺置管术留置腹腔导管,引流腹水,在引流结束后,迅速将顺铂40 mg+地塞米松5 mg快速注入腹腔内,夹闭腹腔留置导管24 h再次注药,共实行腹腔内注射药物3次;两组患者均同期行卡培他滨化疗,21 d为1个周期,治疗2个周期后评价临床疗效[3]。
1.3 疗效和不良反应评价标准 临床疗效评价标准:依据WHO肿瘤治疗疗效评价标准将治疗后患者分为4个等级,全部缓解(CR):腹水全部消失,持续不少于4周,症状消除;部分缓解(PR):腹水消失≥1/2但未全部消失,持续不少于4周,症状部分消除;稳定(SD):腹水消失<1/2,症状无明显减缓;进展(PD):腹水未得到控制或者增多,症状加重。缓解率(ORR)=(CR+PR)/总例数,控制率(DCR)=(CR+PR+SD)/总例数。生活质量(Quality of life,QOL)评价标准:QOL改善为KPS评分增加≥10分;QOL稳定为KPS评分增加或减低均不超过10分;QOL降低为KPS评分减低≥10分。治疗导致的毒性反应参见美国国家癌症研究所毒性标准(NCI-CTC)3.0版。

2 结果
2.1 两组患者CEA、CA199水平比较 治疗后,与B组比较,A组患者血清CEA、CA199水平显著降低,差异有统计学意义(P<0.01)。见表2。
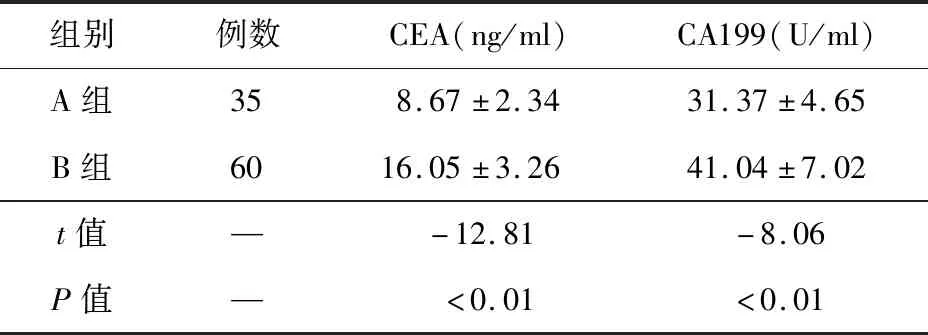
表2 两组患者治疗后CEA、CA199水平比较
2.2 两组患者ORR、DCR比较 治疗后,A组患者ORR、DCR均明显高于B组,差异有统计学意义(P<0.05)。见表3。

表3 两组患者ORR、DCR比较(例)
2.3 两组患者生活质量比较 治疗后,两组患者中共54例QOL改善,A组QOL改善例数明显多于B组,差异有统计学意义(P<0.05)。见表4。

表4 两组患者生活质量比较
2.4 两组患者不良反应发生率比较 两组患者治疗导致的毒性反应主要包括胃肠道反应(恶心、呕吐为主)、骨髓抑制(白细胞、血小板降低为主)及乏力等。两组患者对出现的上述反应均能够耐受,无Ⅲ、Ⅳ度毒副反应,且经对症处理均得到改善。两组患者均未见心脏肝肾功能严重受损、腹腔感染、皮肤感染、肠梗阻、肠穿孔,无不能耐受治疗的患者。两组治疗导致的毒性反应发生率比较,差异无统计学意义(P>0.05)。见表5。
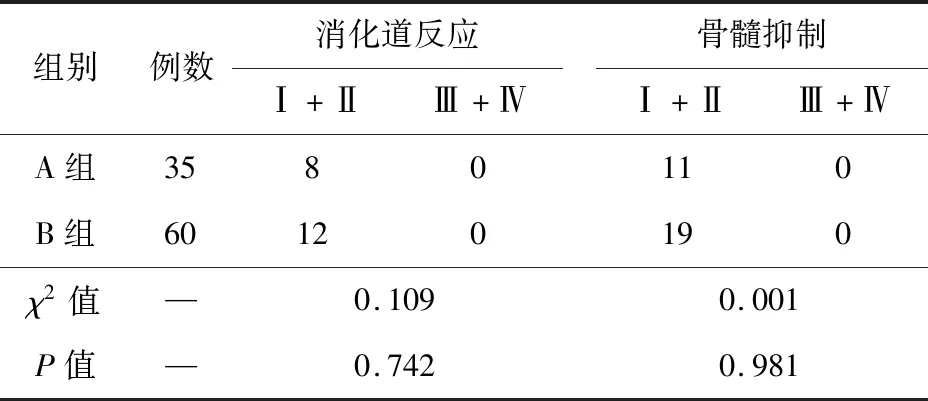
表5 两组患者不良反应发生率比较
3 讨论
恶性腹水是消化道肿瘤常出现的晚期并发症,4%~20%的结直肠癌患者会出现恶性腹水[4]。由于受到大量腹水的影响,患者呼吸和消化等功能降低,生活质量下降,生理及心理的负担加重。若不能对其实施有效、及时的治疗,则会危及其生命,加速患者死亡[5]。针对恶性腹水的治疗,当前以全身与局部相结合的治疗方式为主,全身化疗难以有效抑制腹腔积液生成,局部治疗中腹腔穿刺引流腹水虽然能够在当时减少腹水量,使某些症状短时改善,但是腹腔积液往往会在短期内再次产生。HIPEC是针对恶性腹水所采取的局部治疗措施之一[6-10],并且多位学者通过临床试验已证实HIPEC治疗晚期消化道肿瘤所引起的恶性腹水有效[11-13]。
HIPEC同时应用腹腔热灌注与化疗药物治疗腹腔内肿瘤转移而控制腹水,其40~45 ℃的热疗本身对恶性细胞有直接杀灭作用,可以抑制肿瘤细胞DNA复制、转录、修复等过程,而出现不可逆损伤,甚至导致肿瘤细胞凋亡;热灌注治疗可以使肿瘤细胞膜的通透性增加,从而使化疗药物在肿瘤细胞内分布增多,提高药物和细胞反应率;热疗效应还能提高化疗药物的活性而不增加其不良反应,腹腔热灌注与腹腔内局部化疗具有协同促进的作用;在进行持续腹腔灌注过程中,由于灌注液的循环流动,可以机械性冲洗腹腔内癌细胞和微小病灶,并将部分肿瘤细胞带出腹腔,减少了肿瘤细胞黏附于腹膜的机会[14-15]。
Bevacizumab是抗血管内皮生长因子(Vascular endothelial growthfactor,VEGF)的单克隆抗体,能够特异性结合VEGF,达到抑制肿瘤组织血管增生、诱导癌细胞凋亡的作用,为消化道癌症抗血管生成的重要靶向药物之一[16]。有研究显示,应用贝伐珠单抗联合腹腔热灌注化疗治疗中晚期胃癌合并恶性腹水,与单独应用腹腔热灌注化疗相比,能够显著降低患者血清CEA、CA199水平,提高治疗效果,同时,不增加治疗导致的毒性反应[17]。其机制可能与抑制肿瘤细胞VEGF、肝细胞瘤衍生生长因子和巨噬细胞移动抑制因子的表达有关[18]。在治疗消化道恶性肿瘤时,Bevacizumab能够联合多种化疗药物提高疗效[19]。
本试验中,由于腹腔热灌注治疗系统对腹腔热灌注液温度进行精确控制,使其始终保持在(43±0.5)℃,因此,不但能够保证治疗的有效温度,而且能够确保患者的组织不会被热烧伤,其精确的温控系统保证了在治疗过程中热疗的效果和温度的恒定。治疗2个周期后,与对照组比较,实验组的CEA、CA199水平明显降低,控制率、缓解率明显增高,患者QOL得到显著改善,两组患者的治疗相关毒副反应比较差异无统计学意义。综上所述,实行Bevacizumab+HIPEC治疗结直肠癌合并恶性腹水患者的临床效果较好,此治疗方法值得在临床中推广应用。
