N-特戊酰头孢妥仑匹酯的合成及结构确证
2020-10-31周军荣雷维敏芮立涛江东
周军荣,雷维敏,芮立涛,江东
(浙江东邦药业有限公司,浙江 临海 317016)
头孢妥仑匹酯(Cefditoren pivoxil)是第三代口服头孢菌素,由日本明治制果株式会社首创。1994年4月在日本上市,2001年4月在中国上市,商品名为美爱克(Meiact),用于治疗革兰阳性菌及革兰阴性菌引起的感染[1]。经研究表明,头孢妥仑匹酯对肺炎链球菌、流感嗜血杆菌、化脓性链球菌、金黄色葡萄球菌、卡他莫拉菌五大主要致病菌引起的社区获得性呼吸道感染治疗显著[2-4]。该药物作用机制为抑制细菌细胞壁合成,具有抗菌谱广、疗效显著、安全稳定、口服吸收好等特点,临床应用广泛[5]。
对于药物的研究和开发过程中,其质量是衡量药物品质的一个重要标准,药物的质量首先决定于药物自身的疗效和毒副作用。而药物中存在的杂质直接影响到药物的疗效并可能导致毒副作用的产生,因此必须控制。其中有相关资料[6-7]公布头孢妥仑匹酯中已知杂质,主要包括:头孢妥仑钠、头孢妥仑开环物、头孢他美酯、头孢妥仑匹酯δ3异构体、头孢妥仑匹酯甲氧基甲基化合物、头孢妥仑匹酯E型异构体、头孢妥仑二匹酯、N-特戊酰头孢妥仑匹酯、头孢妥仑匹酯二聚体以及头孢妥仑匹酯开环二聚体。因此为了更好地分析头孢妥仑匹酯的杂质,设计合成出高纯度的已知杂质是很有意义的。N-特戊酰头孢妥仑匹酯作为其中的重要已知杂质,但目前关于它的合成及结构确证报道很少。
参考相关文献资料[8-10],设计出了一条合成N-特戊酰头孢妥仑匹酯的工艺路线,具体路线如图1所示。
该工艺路线:首先以头孢妥仑匹酯为起始原料,与特戊酰氯进行酰胺化反应得到产物N-特戊酰头孢妥仑匹酯。该工艺得到的N-特戊酰头孢妥仑匹酯收率及纯度较高,且原料易得。
1 实验部分
1.1 仪器与药品
实验仪器:Agilent Cary 100紫外可见光谱仪、Agilent Cary 630 FT-IR红外光谱仪、6200 series TOF/6500 series质谱仪、Bruker 500M核磁共振仪、Agilent 1260高效液相色谱仪,以及AR1140电子天平等。
主要原料:头孢妥仑匹酯(浙江东邦药业有限公司),特戊酰氯(上海阿拉丁生化科技股份有限公司),其它溶剂与试剂均来源于上海国药集团。
1.2 N-特戊酰头孢妥仑匹酯的合成过程
在常温下,向一个洁净的反应瓶中加入500mL丙酮,再加入35g(0.056mol,1eq)头孢妥仑匹酯,搅拌溶解。将物料逐渐降温,并控制温度在5~10℃下,加入特戊酰氯10.9g(0.090mol,1.6eq),搅拌均匀。再控制温度在5~10℃下,缓慢滴加9.7g(0.096mol,1.7eq)三乙胺。加毕,控温5~15℃搅拌反应5h(展开剂为甲苯:乙酸乙酯:甲醇(体积比)=4:3:1,TLC跟踪监测反应)。反应结束后,物料控温20℃以下进行减压浓缩,浓缩至无馏分滴出。往浓缩残留物中加入乙酸乙酯400mL,搅拌10min,溶解澄清。再往乙酸乙酯料液中加入1.5%稀盐酸溶液220mL,控温10~15℃,搅拌洗涤5min,静置分液30min。分液时弃掉水层,收集有机层。再往有机层中加入200mL饱和食盐水,控温10~15℃,搅拌洗涤5min,静置分液30min。分液时弃掉水层,收集有机层。将有机层料液进行减压浓缩,至料液体积约为120mL。停止浓缩,然后将料液进行缓慢降温至-5~0℃,保温析晶2h。析晶结束后,过滤,得到的湿品置于真空干燥箱内,并控温25~30℃干燥。烘干后,得到34.6g产物N-特戊酰头孢妥仑匹酯,摩尔收率约为87.8%,HPLC检测(条件是色谱柱:YMCPack ODS-AM C18150mm×4.6mm/5μm;检测波长:254nm;柱温:25℃)纯度为98.2%。
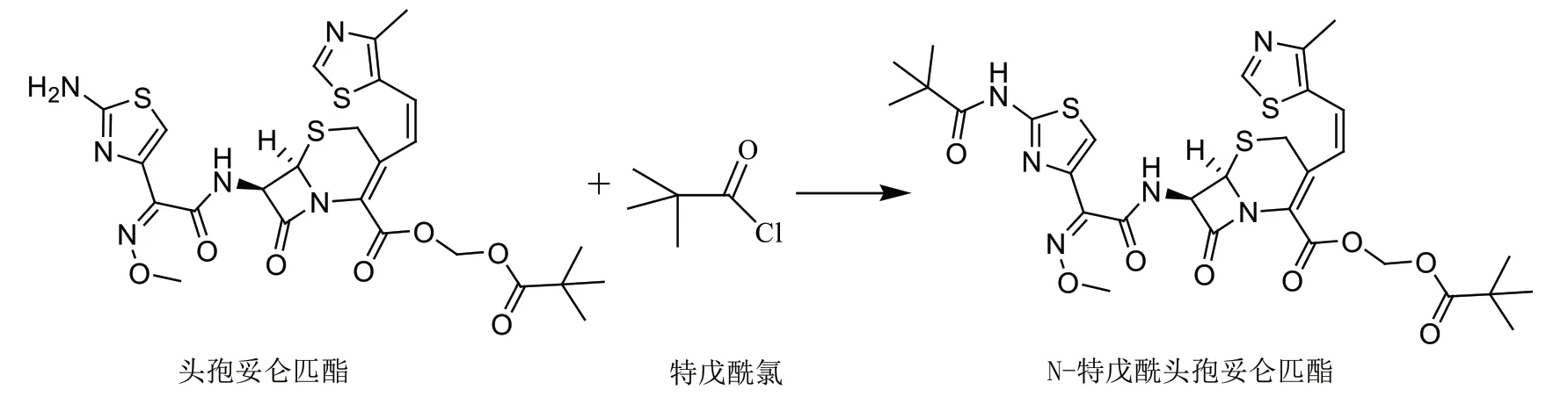
图1 N-特戊酰头孢妥仑匹酯的合成路线
2 分析讨论
将通过1.2步骤得到的N-特戊酰头孢妥仑匹酯进行结构确认分析,分析如下。
2.1 紫外吸收光谱(UV)
由N-特戊酰头孢妥仑匹酯紫外吸收光谱数据可见(见表1)。
ε= A/(c×b)
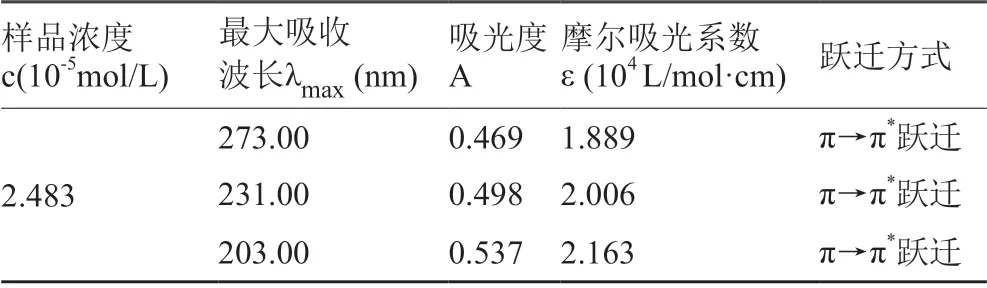
表1 N-特戊酰头孢妥仑匹酯紫外吸收光谱数据
式中:c—溶液的浓度(mol/L);b—吸收池长度(cm)。
N-特戊酰头孢妥仑匹酯有三条紫外吸收带(273.00 nm,ε = 1.889×104L/(mol·cm);231.00 nm,ε = 2.006×104L/(mol·cm);203.00 nm,ε =2.163×104L/(mol·cm)),均为芳香环的π→π*跃迁,与分子中芳环结构相吻合。
2.2 红外吸收光谱(IR)
N-特戊酰头孢妥仑匹酯红外吸收光谱数据见表2,解析:(1)3268、3197/cm为氨基的N-H不对称和对称伸缩振动吸收峰,1091、1044/cm的吸收峰C-O伸缩振动吸收峰,1792、1755、1685 /cm为羰基的C=O伸缩振动,可知该化合物中存在酰胺,酯等结构;(2)1541、1482、1462/cm处较强的吸收峰为双键C=C的伸缩振动,可知分子中含有双键;3)2975、2939、2874/cm为烷烃的C-H伸缩振动吸收峰,1369、1294、1219、1154、1118/cm为烷烃的C-H弯曲振动吸收峰,949/cm为烷烃C-H面外弯曲振动吸收峰,可知分子中存在烷烃。由以上分析结果可知:红外吸收光谱表明样品分子中含有酰胺、酯、双键以及烷烃等特征官能团。
2.3 高分辨质谱(HR-MS)
N-特戊酰头孢妥仑匹酯的高分辨质谱分析如下:其分子式:C30H36N6O8S3,绝对分子量:704.1757。由样品检测图谱可知,正离子模式下,在m/z 705.1862处较强的离子峰对应样品的[M+H]+信号;负离子模式下,在m/z703.1713处较强的离子峰对应样品的[M-H]-信号;以上分析结果与样品的分子量及分子式相符。
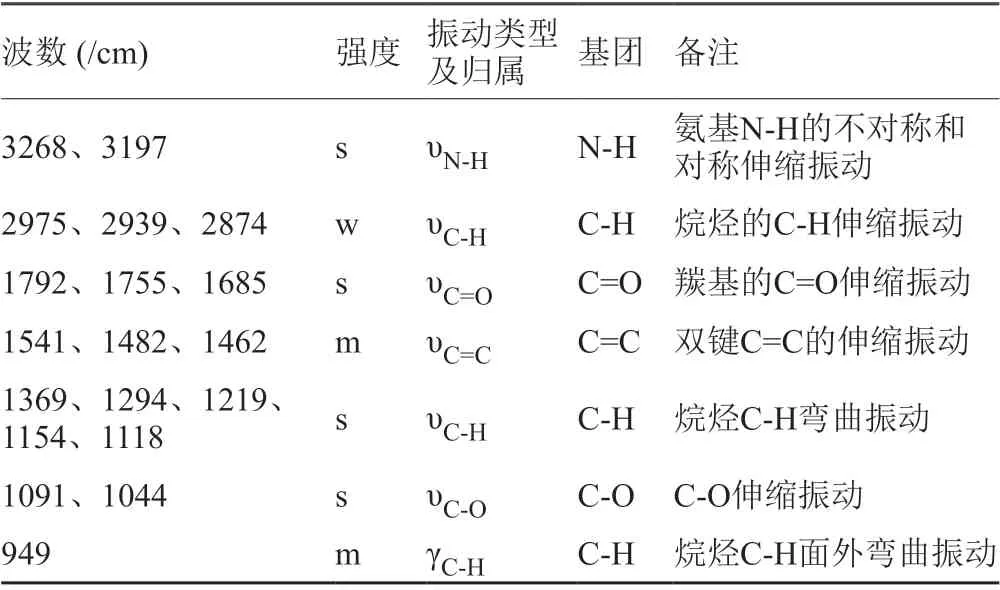
表2 N-特戊酰头孢妥仑匹酯红外吸收光谱数据
2.4 核磁共振波谱(NMR)
对于N-特戊酰头孢妥仑匹酯的核磁共振氢谱(1H-NMR)和碳谱(13C-NMR)数据分析,为了更方便地说明其结构中的各原子的位置,对其化学结构式进行标记,如下图2所示。其中测定结果及解析见表3与表4。
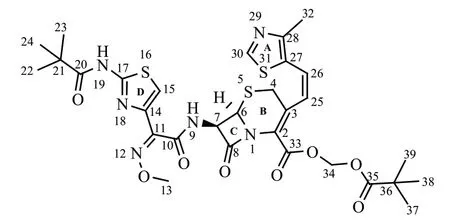
图2 N-特戊酰头孢妥仑匹酯的化学结构式

表3 N-特戊酰头孢妥仑匹酯1H-NMR数据
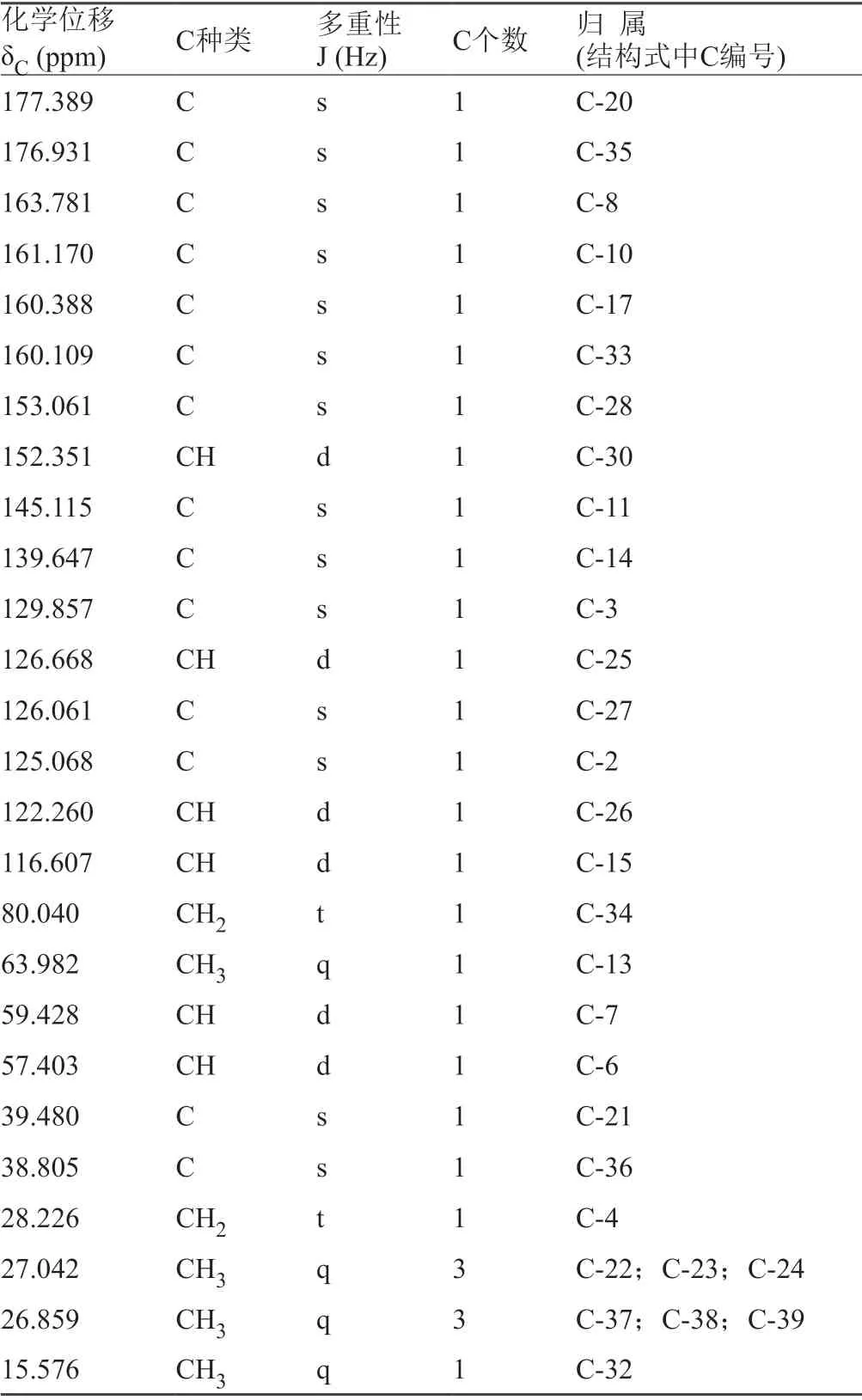
表4 N-特戊酰头孢妥仑匹酯13C-NMR数据
解析:(1)1H-NMR谱(表3)出现的15组质子信号,根据其积分面积比可知该样品中至少含有35个氢原子(其中N-19位上活泼氢未出),包括1组A杂环中无耦合的单峰次甲基(δH8.641,s,1H,H-30)以及1组杂环上取代单峰甲基(δH2.433,s,3H,H-32),2组顺式双键上相互耦合的次甲基(δH6.6 7 3-6.650,d,J=11.8Hz,1H,H-25;δH6.375-6.325,d,J=11.8Hz,1H,H-26);2组B杂环存在同碳耦合裂分的亚甲基信号(δH3.552-3.512,d,J=18.8Hz,1H,H-4a;δH3.321-3.284,d,J=18.8Hz,1H,H-4b)以及1组裂分为双峰的次甲基(δH5.195-5.185,d,J=4.9Hz,1H,H-6);1组C环上的H-6和氨基H-9耦合为双重峰次甲基(δH6.036-6.008,dd,J=8.7,4.9Hz,1H,H-7);1组D环上单峰次甲基信号(δH7.409,s,1H,H-15)以及1组含氧单峰甲基(δH4.150,s,3H,H-13)、1个存在AB系统耦合的含氧亚甲基(δH5.839-5.829,d,J=5.6Hz,1H,H-34a;δH5.786-5.775,d,J=5.6Hz,1H,H-34b)和2组异丁基质子信号(δH1.321,s,9H,H-22/H-23/H-24;δH1.134,s,9H,H-37/H-38/H-39)。以上分析结果与样品N-特戊酰头孢妥仑匹酯分子结构一致;(2)13C-NMR谱(表4)显示该样品含有30个碳信号,其中A环上4个碳信号(δC153.061,C-28;δC152.351,C-30;δC126.061,C-27;δC15.575,C-32),1对双键信号(δC126.668,C-25;δC122.260,C-26);B环和C环上6个碳信号(δC163.781,C-8;δC129.857,C-3;δC125.068,C-2;δC59.428,C-7;δC57.403,C-6;δC28.226,C-4);D环3个碳信号(δC160.388,C-17;δC139.647,C-14;δC116.607,C-15)。此外,还包括2个酰胺羰基碳信号(δC177.389,C-20;δC161.170,C-10)、1个亚胺碳信号(δC145.115,C-11)、2个酯羰基碳信号(δC176.931,C-35;δC160.109,C-33)、1个含氧甲基(δC63.982,C-13)、1个含氧亚甲基(δC80.040,C-34)以及2个异丁基碳信号(δC39.480,C-21;δC38.805,C-36;δC27.042,C-22/C-23/C-24;δC26.859,C-37/C-38/C-39)。以上分析结果与样品N-特戊酰头孢妥仑匹酯分子结构相符。根据核磁共振氢谱(1H-NMR)、碳谱(13C-NMR)可确证N-特戊酰头孢妥仑匹酯的结构,如图2所示。
2.5 结构确证小结
N-特戊酰头孢妥仑匹酯的核磁共振氢谱(1H-NMR)、碳谱(13C-NMR)确证C、H归属符合样品分子结构式,综合紫外、红外以及高分辨质谱结果信息,证实了该结构的正确性。
3 结论
本文将起始原料头孢妥仑匹酯与特戊酰氯进行酰胺化反应得到产物N-特戊酰头孢妥仑匹酯。该工艺得到的N-特戊酰头孢妥仑匹酯收率及纯度较高,且原料易得。通过结构确证(紫外吸收光谱、红外吸收光谱、高分辨质谱以及核磁共振波普)证实了N-特戊酰头孢妥仑匹酯化学结构式的正确性。
