抗真菌药物不良反应文献分析
2020-10-31唐炯刘颖
唐炯,刘颖*
(四川省第二中医医院,成都 610031)
随着现代医学的发展与医疗水平的提高,近年来,由于免疫抑制剂、广谱抗生素、糖皮质激素等药物的广泛使用,肿瘤化放疗、实体器官移植等技术的广泛开展,真菌感染的患者大大增加[1]。自1955年第一个抗真菌药两性霉素问世以来[2],各类抗真菌药物成为治疗真菌感染的重要“武器”。但随着抗真药物在临床的广泛应用,其药品不良反应(Adverse Drug Reactions,ADR)也逐渐增多,本文对2000年—2019年有关抗真菌药物的不良反应文献报道进行回顾性综述分析,旨在为临床合理应用抗真菌药物提供参考依据。
1 资料与方法
1.1 资料来源
依据《新编药物学》主要指治疗系统性真菌感染的4大类即多烯类、三唑类、棘白菌素类、嘧啶类常用抗真菌药物的药品名称(包括药品通用名和常见名称)如“两性霉素”及“二性霉素”为主题词,“不良反应”、“不良事件”、“副作用”、“副反应”、“安全性”为副主题词检索2000年—2019年内《中国期刊全文数据库》、《万方数字化期刊全文库》、《中文科技期刊全文数据库(VIP维普)》中的相关文献。下载原文,按照预先设定的标准和内容进行记录。
1.2 资料入选标准
详尽记录单个或数个病例使用抗真菌药物后发生ADR的病例报道或医疗机构一段时间内使用抗真菌药物的患者发生ADR的分析报告。筛除重复发表文献(仅保留发表日期排在前面的文献)。
1.3 资料收集及纳入
按“1.1”项检索方法得到有关文献3702篇,符合“1.2”项入选标准并考虑排除标准后的文献有235篇 。
1.4 统计分析方法
根据文献提供资料,分类整理抗真菌药物发生ADR的例数,应用Excel对数据进行汇总筛选,对ADR情况进行归类并分析其发生情况。
2 结果
2.1 年龄与性别
共计报道药物不良反应565例,所报道的ADR病例中,年龄最小患者为20d,年龄最大患者为96岁,平均年龄为48.6岁,年龄分布见表1。565例ADR患者中,其中男性患者超过一半,为304例,性别分布见表2。
2.2 不良反应发生时间
抗真菌药所致的ADR,发生时间各不相同。报道的病例中使用抗真菌药物后发生ADR时间最短的不到1min(过敏性休克),而报道发生ADR时间最长的为超过两个月(月经紊乱、皮肤色素沉着等),文献中给出具体不良反应发生时间的病例中,不良反应发生在用药的1~3d比例最大。抗真菌药物所致ADR发生时间见表3。
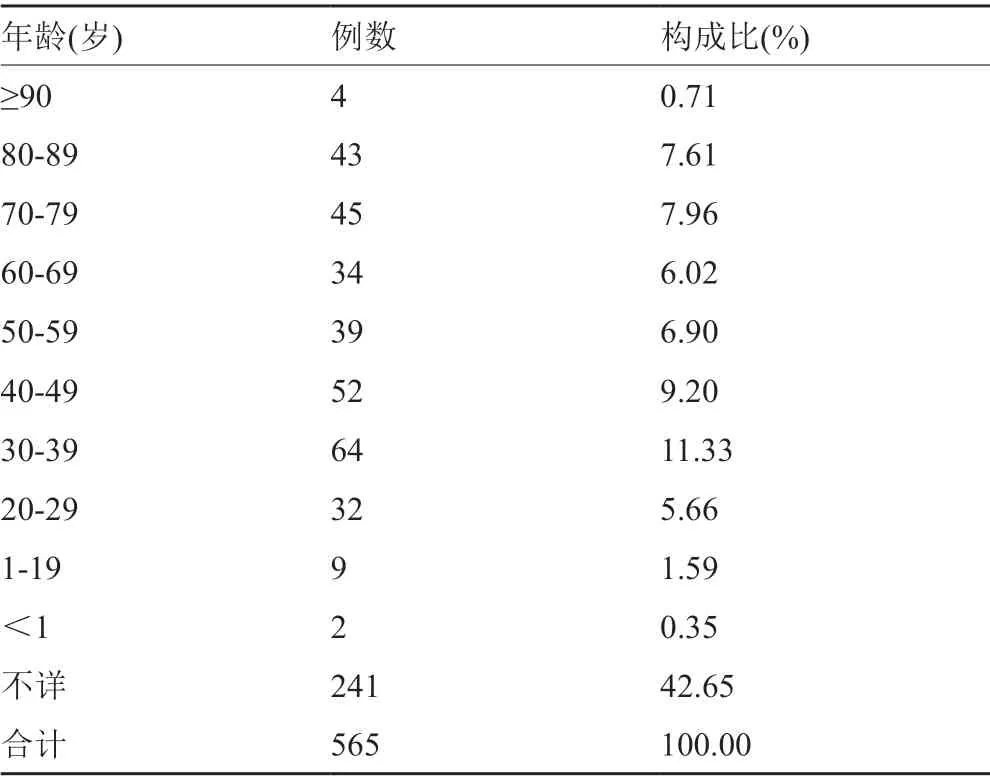
表1 ADR患者的年龄分布
2.3 抗真菌药物致ADR的发生率、发生类型及构成比
报告使用抗真菌药物出现药物不良反应565例,其中三唑类抗真菌药ADR个案报告最多,为407例;其次多烯类为108例;棘白菌素类为14例。各类抗真菌药ADR例数见表4。抗真菌菌药物不良反应以肝胆胰系统、过敏反应、神经系统不良反应多见,分别为130例(占23.01%)、83例(占14.69%)、82例(占14.51%)。报告ADR累及系统/部位、构成比及临床表现见表5。
3 结论与讨论
从年龄分布上看,抗真菌药导致的ADR在20岁~49岁的青中年年龄段例数较多,推测其原因可能为青中年的生理机能、免疫应答等是人体一生中最强阶段,因而是某些药物不良反应的“易感人群”。这也提醒我们医务人员,在老年患者中使用全身性抗真菌药时需密切监护患者用药的安全性的同时也需警惕抗真菌药在青中年患者上使用时发生不良反应的可能。而从性别分布上看,男性患者比例多于女性,可能因为免疫功能低下如HIV感染患者[3]、慢阻肺患者[4]男性比例多于女性,故男性患者真菌感染的比例大于女性,造成使用抗真菌药物的男性患者比例多于女性,进而反映出男性患者出现ADR的比例大于女性。此外,男性患者比例多于女性可能是因为男性吸烟的比例往往大于女性,而长期吸烟可能影响肝脏中的药物代谢酶的数量、活性,导致抗真菌药物在机体内的暴露量发生变化[5],最终导致发生不良反应的男性比例大。

表2 ADR患者的性别分布
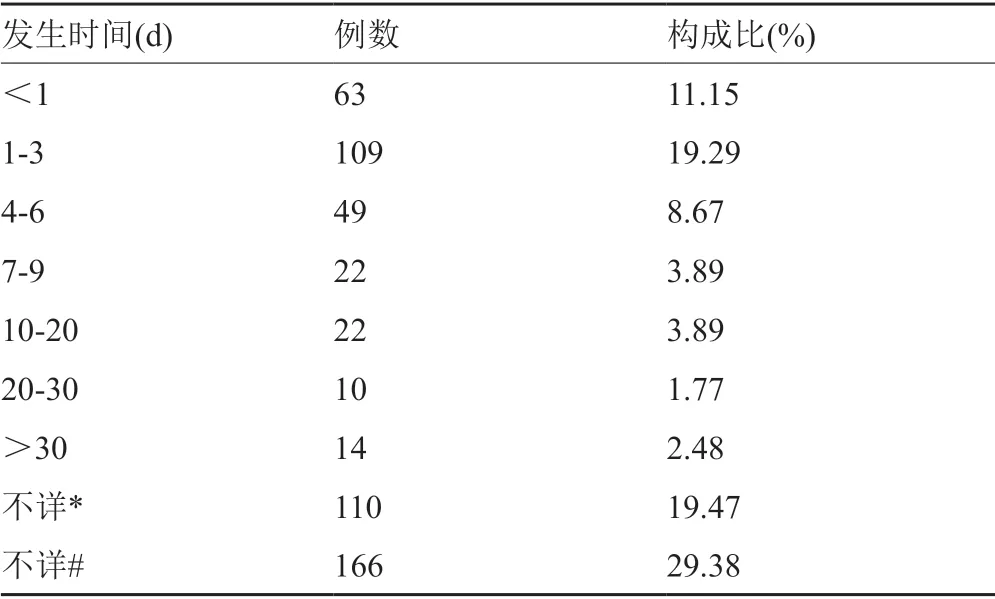
表3 抗真菌药所致药物不良反应发生时间

表4 ADR累及系统/部位、构成比及临床表现
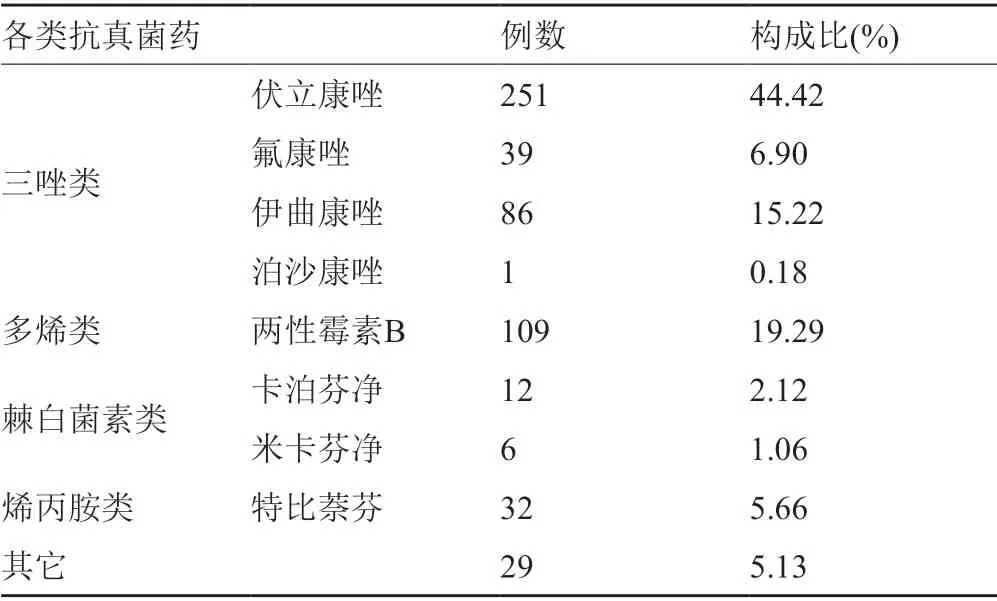
表5 各类抗菌药物致 ADR 例数
抗真菌药物引起各类ADR的时间有所差异,一般情况下过敏性休克、皮疹、瘙痒等症状能够在应用的早期出现,但由于抗真菌药如伏立康唑在人体内通过肝酶系统代谢具有饱和性,呈非线性药代动力学特征,且因为相关药物代谢酶有基因多态性导致的快慢代谢之分[6],导致个体差异较大。此外,抗真菌药在体内往往还受年龄、生理病理状态、营养状态、合并用药等因素的影响,故发生ADR的时间较难预测。建议有条件的医院可对部分高危患者进行治疗药物血药浓度监测,甚至基因检测,以个体化的调整抗真菌药物的给药剂量,而并非仅仅通过体重来制定给药剂量。
本研究中,各类抗真菌药的ADR报道的例数中以三唑类最多,尤其以伏立康唑最多见,分析其原因为所纳入的文献为2000年以后的文献,而两性霉素、特比萘芬、氟胞嘧啶包括伊曲康唑等在2000年以前使用较多;而像卡泊芬净等棘白菌素类抗菌真菌药由于上市时间比较晚,加之药物可及性等因素,其使用目前并不是十分广泛,故其ADR报道的例数也较少。
抗真菌药引起的ADR类型较多的是肝损伤/肝功能异常、神经系统症状、过敏反应。有文献报道,抗菌药物导致的肝功能异常的发生率在药物性肝损伤中约占1/10左右,而其中抗真菌药相关性肝损占到抗菌药物的三成以上[7-8]。抗真菌药引起的肝损伤/肝功能异常的机制尚不明确,目前认为可能是由于药物剂量偏大时,或者在体内代谢异常时,活性基团和自由基等大量消耗肝脏内的谷胱甘肽的物质,导致氧化应激、钙-ATP的自稳性遭到破坏,从而引起肝功能异常甚至损伤[9]。而像伏立康唑、氟康唑等药物既是CYP450的底物又是其抑制剂,容易导致药物在体内剂量波动及出现与其他药物的相互作用,引起肝功能异常。抗真菌药物引起的肝损伤的危险因素有:年龄,老年药物清除速率减慢;营养状况,低蛋白饮食可降低CYP450酶的活性;基础疾病,有糖尿病、病毒性肝炎等[9]。抗真菌治疗一般疗程较长,故需定期监测肝功能指标,如有相关危险因素,更应引起医务人员的重视。
抗真菌药物引起的神经/精神症状如幻视、幻听、精神亢奋等症状的机制可能与药物穿透血脑屏障的浓度相关,从而影响神经系统兴奋性神经递质和/或抑制性神经递质的释放[10],其具体机制还需进一步深入研究。故在制定给药方案时,应避免给药剂量过大。
过敏反应也是抗真菌药报道最多的ADR之一,由于免疫系统的参与而导致的药物过敏反应约占药物不良反应发生率的1/6[11]。药物诱发过敏反应的机制十分复杂,包括一些列细胞因子、淋巴细胞、补体等引起的炎症瀑布。过敏反应不仅仅累及皮肤,也可累及肝脏、心脏、肾脏、造血系统等各种器官和组织,故在使用抗真菌药物前应详细询问患者及其家族的过敏史,并对用药的全过程进行监护。抗真菌药物引起的其它ADR类型如低血糖、低钾血症、阵发性室性心动过速等虽不及肝损伤、过敏反应多见,但可能引起患者死亡或器官功能不可逆损伤等严重后果,也需引起医务工作者的重视。
本研究中的相关数据均来自国内医院或ADR监测中心,从结果来看,同国外系统性抗真菌药的ADR相关研究结果基本一致。一项由巴西东南部教学医院进行的回顾性横断面研究[12]显示,183例接受全身抗真菌治疗(治疗药物主要包括两性霉素、氟康唑、伏立康唑)的患者,其中53例患者出现抗真菌药引起的ADR,出现ADR的患者平均年龄为43岁,ADR出现频率较高的分别为过敏反应(45%)和肝功能异常(30%)。法国的Girois等研究者对治疗侵袭性真菌感染的抗真菌药物的不良反应进行了系统评价和meta分析[13],共纳入54项研究及近1万研究者,研究结果中的不良反应类型也同国内相关文献报道基本一致。
鉴于现有传统的抗真菌药物的安全性问题及不断增加的耐药性,临床迫切需要新的高效低毒的抗真菌药物满足治疗需求。三唑类抗真菌药物目前是使用最为广泛的一类抗真菌药,近年来泊沙康唑和艾沙康唑先后通过FDA批准上市,而正处于研究阶段的雷夫康唑(Ravuconazole)、阿巴康唑(Albaconazole)及 VT-1161阶段,这些新的三唑类抗真菌药可能的优势有:(1)改进药动学特性使血药浓度更具稳定性和可预测性;(2)通过药物的修饰与改造减少对人类 CYP450的影响从而减少药物间相互作用;(3)拓宽抗真菌谱[14],从而成为治疗真菌感染的理想选择。除了正处于研究阶段的几种三唑类药物外,目前,一种长效棘白菌素类抗真菌药,CD101 也正处于研究中,在众多实验中,CD101 表现出对其他棘白菌素敏感或耐药的菌株均具有良好抗菌活性[14-15]。传统的抗真菌药物在真菌感染治疗中占有重要地位,但限于开发全新抗真菌药物耗时周期长、研发经费高,迫切需要新思路、新途径来探寻安全有效的治疗真菌的方法。而免疫疗法(包括真菌疫苗、抗体疗法、细胞免疫治疗)和光动力疗法可能成为抗真菌治疗新的答案[16,17]。
4 结语
抗真菌药物所致药物不良反应,涉及全身多器官、多系统,可能给患者带来严重后果,如器官机体功能的障碍,严重时可能危及生命。且由于抗真菌药使用疗程往往较长,因此,抗真菌药物的合理应用与监护十分重要,医生应严格掌握抗真菌药物的使用指征,药师需对患者制定严格药物监护计划,做好抗真菌药物不良反应的预见、预防,早发现、早处理,保证患者用药安全。
