早产儿万古霉素治疗34 例药物监测与用药分析
2020-10-25姜孙旻徐银莹陆子红袁媛沈丽梦周勤鲍俊峰姚荧
姜孙旻,徐银莹,陆子红,袁媛,沈丽梦,周勤,鲍俊峰,姚荧
新生儿特别是早产儿机体各系统发育不完善,机体免疫力低下、抵抗力差,容易诱发细菌感染,进而导致病儿的住院时间延长,病死率升高。根据研究显示早产儿感染的主要菌群[1]是革兰阳性菌,特别是金黄色葡萄球菌、凝固酶阴性葡萄球菌等。万古霉素是糖肽类抗菌药物,主要作用于革兰阳性球菌,且效果明显。多年来,治疗甲氧西林耐药葡萄球菌(Methicillin-Resistant S.Aureus,MRSA)等多重耐药革兰阳性菌所致的重症感染仍首选万古霉素[2]。
万古霉素抗菌治疗“治疗窗窄”,药物剂量不足导致疗效欠佳且大大增加耐药风险,药物剂量过高会显著增加耳肾毒性等药品不良反应(Adverse Drug Reaction,ADR)的发生率。由于早产儿机体发育不完善,组织器官尚未完全成熟,各种酶系统发育不健全,影响万古霉素体内代谢,上述情况发生率大大提高。本研究参考万古霉素药品说明书及相关文献[3-5],对万古霉素在早产儿中的应用及治疗药物监测(Therapeutic Drug Monitoring,TDM)情况进行分析与评估,对于建立临床药师药学服务新模式具有重要指导意义。
1 资料与方法
1.1 一般资料采用回顾性调查方法,收集南京医科大学附属无锡妇幼保健院新生儿科2016—2018年收治的应用万古霉素[VIANEX S.A.(PLANT C),进口药品注册证号H20140174]抗感染治疗的早产儿共计34例。通过查阅病历,获取病儿的相关临床信息。
纳入标准:①住院期间病儿使用万古霉素抗感染治疗;②病儿进行TDM 至少1 次;③临床药师对万古霉素TDM干预至少1次;④应用万古霉素前后均有病儿相关化验室检查结果;⑤病儿监护人或其近亲属知情同意,本研究符合《世界医学协会赫尔辛基宣言》相关要求。
排除标准:病历资料不完整者和(或)用药前后检查记录不全者。
1.2 用药方案万古霉素初始剂量为临床医师依据药品说明书每次10~15 mg/kg,给药频次参考病儿日龄、体质量、化验室指标、感染程度等情况而定,所有病儿均使用静脉泵静脉给药,持续时间为1 h。1.3 血药浓度测定及临床药师干预采用高效液相色谱法(HPLC)进行测定万古霉素血药浓度,系统由FLC 全自动二维液相色谱耦合仪(湖南德米特仪器有限公司)及岛津LC-20A 液相色谱部件构成,万古霉素质控品由湖南德米特仪器有限公司提供。血药谷浓度为第5 剂给药前30 min 静脉血样浓度,血药峰浓度为第5剂给药后1 h静脉血样浓度。根据相关文献[3-5]临床药师将目标谷浓度定为10~20µg/mL。若病儿血药谷浓度<10µg/mL且临床疗效欠佳者或血药谷浓度>20µg/mL,根据相关文献[6]临床药师将建议调整用药;若病儿血药谷浓度在10~20 µg/mL,根据相关文献[6]临床药师将建议维持目前剂量继续治疗,且注意用药期间控制液体滴入速度及监测ADR。所有临床药师通过TDM报告单,将建议告知临床医生,并进行相关干预。
1.4 实验室指标通过查阅病历获得病儿的各项实验室检验指标结果。在治疗过程中密切监测病儿使用万古霉素治疗前后,感染指标[降钙素原(PCT)、C反应蛋白(CRP)]、肾功能[血肌酐(Cr)、胱抑素C(CysC)、尿素(Urea)]、肝功能[丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、白蛋白(Alb)]等各项指标变化情况。
1.5 临床疗效评价本研究参考相关文献[7-8]对临床疗效进行痊愈、显效、进步、无效4级评定。痊愈:治疗后病儿症状消失、体征平稳、实验室检查恢复正常、致病菌检查阴性。显效:治疗后病情显著好转,但上述4项中有3项恢复正常、有1项未完全恢复正常。进步:治疗后病情有所减轻,但未显著好转。无效:治疗后病情无好转或较前加重。治愈和显效合计为有效,并据此计算有效率。
1.6 ADR监测在诊疗过程中医师与临床药师予以严密监测,用药前后分别检查病儿肾功能进行对比以判断是否发生肾毒性。判断为万古霉素导致的肾毒性[9]是指经过万古霉素治疗后监测肾功能显示血肌酐2~3次连续升高(增加44.2µmol/L,或从基线增幅>50%,以较高者为准),且需排除其他原因后。判断耳毒性是在治疗前、停药后48 h分别进行新生儿耳声发射检查。判断万古霉素导致的“红人综合征”是指万古霉素治疗过程中病儿出现皮肤潮红、心动过速、血压下降等现象。
1.7 统计学方法全部数据采集应用Excel 2019,将数据导入SPSS 21.0专业统计软件进行组别间数据差异性的分析。计量资料表示为±s,计数资料用例(%)表示。计量资料组别间差异性分析选择t检验,计数资料组数差异采用χ2检验或Fisher确切概率法检验。以P<0.05为差异有统计学意义。
2 结果
2.1 病儿基本情况
2.1.1基本情况 研究过程中纳入符合标准的病儿34例(男18例,女16例);体质量(1.58±0.59)kg;4例胎龄低于28周,余30例胎龄范围为28~37周;万古霉素临床介入治疗起始日龄为(19.15±12.27)d,体质量(1.75±0.57)kg;全部纳入病例的住院天数为(39.06±19.88)d。
2.1.2疾病分布 纳入病例的临床诊断,23例为脓毒血症病儿,比例最高,占疾病分布的48.94%;其次为新生儿肺炎,共8例(占17.02%);其余包括中枢、尿路、肠道感染等。
2.2 病原学检查34 例病儿在接受抗菌药物治疗前,均进行了病原学检查,结果显示,26例(76.47%)病例细菌检查为阳性,其中的4 例为混合性感染。根据表1 数据可以看出,革兰阳性菌共25 例次,占全部病例的83.33%;而实验数据也提示了19 例次之多的多重耐药革兰阳性菌感染,占革兰阳性菌株的76.00%,且均对万古霉素具有高度敏感性。

表1 采用万古霉素治疗早产儿34例病原学检查中革兰阳性菌25 例次结果
2.3 TDM结果及临床药师干预情况研究过程中34 例病儿共进行了47 次TDM,其中进行1 次TDM的23例,进行2次TDM 为10例,而进行4次TDM 为1 例。如表2 数据,临床药师干预前,谷浓度达标率仅为26.47%,且有2 例病儿谷浓度高于20 µg/mL(5.88%),增加了发生ADR的风险;余病儿谷浓度普遍低于10µg/mL,治疗效果差,且易发生耐药。临床药师充分对病儿药物代谢、分布状况进行评估,根据TDM 结果对临床用药的剂量做出个体化的调整45例次,临床医师根据药师建议综合评估后采纳38例次(84.44%)。调整后再次进行TDM,结果显示达标率达76.92%,临床药师有效的干预能够显著提高谷浓度达标率(P<0.05)。

表2 临床药师干预前后万古霉素谷浓度监测结果/例(%)
2.4 万古霉素治疗疗程全部病儿万古霉素治疗时间分布于3~21 d,药物平均使用时长为(9.91±4.22)d,其中以连续用药8~14 d 者最多,共计18 例(52.94%),此项数据同临床指南中所推荐的新生儿脓毒血症抗菌药物治疗时间相符。
2.5 联合用药入组病例,单用万古霉素病儿4例,其余30例(88.24%)病儿治疗中均联合应用其它品种的抗菌药物,且7例危重病儿治疗中先后联合2种不同抗菌药物,1 例极危重病儿的治疗中采用三联广覆盖用药。
研究结果如表3,联合用药中,主要为碳青霉烯药物如美罗培南(占43.59%),其次是加酶抑制剂复合制剂。

表3 早产儿30例抗生素联合用药的品种
2.6 实验室指标实验数据如表4,病儿经万古霉素治疗,PCT、Urea、Cr、CysC、AST 降低幅度显著(P<0.05),而 CRP、ALT 及 ALb 治疗前后的变化不明显(P>0.05)。
2.7 临床疗效34 例研究对象,临床治疗后29 例有效,有效率85.29%。此项数据充分显示出万古霉素治疗早产儿病例中的确切效果。将病儿依据是否有效划分为两个研究组,进一步探寻对治疗效果具有影响性的因素,见表5。
表5 显示的预测模型同临床实际状况相符度较高(预测正确率85.3%)。结果提示联合用药、万古霉素谷浓度及疗程长短、临床药师干预采纳度等对疗效无显著影响(P>0.05)。除了样本量有限的原因外,还可能由于早产儿疾病严重程度、合并症等情况存在差异,上述因素难以成为影响预后的独立因素。
表4 采用万古霉素治疗早产儿34例用药前后实验室指标/±s
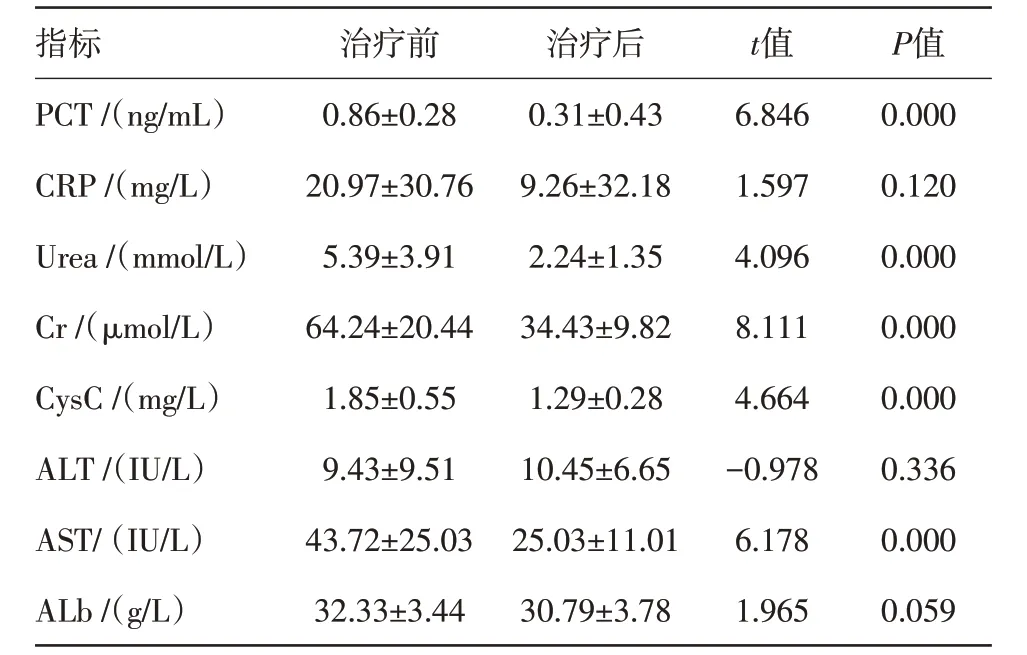
表4 采用万古霉素治疗早产儿34例用药前后实验室指标/±s
注:PCT为降钙素原,CRP为C反应蛋白,Urea为尿素,Cr为血肌酐,CysC 为胱抑素C,ALT 为丙氨酸氨基转移酶,AST 为天冬氨酸氨基转移酶,Alb为白蛋白
指标PCT/(ng/mL)CRP/(mg/L)Urea/(mmol/L)Cr/(µmol/L)CysC/(mg/L)ALT/(IU/L)AST/(IU/L)ALb/(g/L)治疗前0.86±0.28 20.97±30.76 5.39±3.91 64.24±20.44 1.85±0.55 9.43±9.51 43.72±25.03 32.33±3.44治疗后0.31±0.43 9.26±32.18 2.24±1.35 34.43±9.82 1.29±0.28 10.45±6.65 25.03±11.01 30.79±3.78 t值6.846 1.597 4.096 8.111 4.664-0.978 6.178 1.965 P值0.000 0.120 0.000 0.000 0.000 0.336 0.000 0.059
2.8 ADR 监测根据表4 数据,本研究中的病儿均未出现同万古霉素相关严重的儿、肝、肾毒性,亦未出现研究报道中所描述的“红人综合征”等过敏反应。分析原因与临床药师在万古霉素使用过程中实施了TDM 及严密的药学监护,如控制滴注速度有关。
3 讨论
3.1 万古霉素的抗感染治疗本研究纳入的早产儿病例以脓毒血症等严重感染病例为主,这些病例的普遍特点是在起病早期无显著特异性临床表现,然而,往往出现病情突然加重而危及生命的现象。所以,疾病的早期诊断和介入处理尤为重要。病原菌的检出往往作为感染性疾病确诊的“金标准”,但其细菌培养和药敏时间耗时相对较长,而白细胞计数(WBC),会随着早产儿日龄增加发生改变,且易受到非感染性因素影响,特异性较低[12]。大量研究表明[12-13],PCT 作为诊断早产儿细菌性感染的价值高于WBC 及CRP,敏感性和特异性较高,可较为准确的评价早产儿感染状态及严重程度。表4 数据显示出,临床治疗后实验组中各病例PCT 呈现显著降低趋势(P<0.05)、同时CRP 水平也有所降低(P>0.05),结合病儿的临床症状,可从一个方面说明使用万古霉素治疗后细菌感染得到了有效控制。
3.2 万古霉素的血药浓度监测表2结果显示,研究中在临床药师干预之前血药谷浓度达标率仅26.47%,且监测值普遍偏低。谷浓度检测结果显著低于目标范围的原因可能同本次研究对象为早产儿相关,此类病儿往往病情比较严重,存在较大的细胞外液积蓄,因此,万古霉素表观分布容积(Vd)显著增加,血药浓度偏低[14-15]。加之,目前临床经验用药主要是选择日龄、体质量两个因素以计算药物剂量,而未能将病儿胎龄、机体病理状况等因素纳入考虑。医师采纳临床药师干预建议,调整剂量进一步复测后,显著提高了谷浓度的达标率(P<0.05)。

表5 采用万古霉素治疗的早产儿34例疗效与各因素的相关性分析
3.3 ADR 监测本研究中无一例病儿出现万古霉素相关性ADR,一些统计学研究也证实了正常谷浓度下的万古霉素对早产儿没有显著的耳、肾毒性,临床用药相对较安全[16-18]。首先,可能与本研究谷浓度高于20µg/mL 的病例较少有关;另外,本研究中纳入的病例均为早产儿,存在大量输液及营养不良等状况,导致Cr 值偏低,可能干扰了对病儿肾毒性的判断[17]。因此,万古霉素在使用过程中是否会对早产儿肾功能产生严重影响,仍需进一步的研究。
4 结论
本研究结果显示出万古霉素在治疗由革兰阳性菌所导致的早产儿危重感染病例中的确切治疗效果,但是临床经验性给药情况下普遍存在谷浓度达标率低的情况,此时极易出现细菌耐药,建议临床应用中严格掌握适应证,同TDM相结合。临床药师与医师密切配合,共同参与早产儿病例的万古霉素临床个体化应用的全过程,形成一种新的药学服务模式,有效地避免治疗效果不佳、临床耐药情况的发生,减少ADR,保障治疗效果及用药安全。
