FisetinCu&Zn配合物和嘌呤分子相互作用的理论研究
2020-10-21罗冬梅李雪刚姚娜谭冬远靳瑞发肖文敏辛景凡孙菱翎余杰
罗冬梅 李雪刚 姚娜 谭冬远 靳瑞发 肖文敏 辛景凡 孙菱翎 余杰


摘 要:本文采取量子化学中的DFT(密度泛函)法,用Gauss09程序包优化的了Fisetin及Fisetin和Cu2+,Zn2+形成的可能的配合物與嘌呤分子相互作用后的几何结构.得出相对应的优化的之后的结构参数、相互作用能量等,计算结果显示,所优化的体系均无虚频,结构稳定.所得相互作用能表明,鸟嘌呤(Guanine)与所设计络合物之间有明显相互作用.
关键词:Fisetin(漆黄素);Zn2+,Cu2+;嘌呤;量子化学
中图分类号:O642.0 文献标识码:A 文章编号:1673-260X(2020)03-0028-05
1 引言
漆黄素(Fisetin,属于黄酮类化合物的一种,非人工加工过的黄酮化合物类存在生物活性、药理功能和抗氧化能力,并用于某些疾病的预防及治疗,如癌症,肿瘤等,对于新创造的的药物的设计有很重要的意义.)[1]是科学家从漆树木质部的一些水提炼物中提取出的,它能够保护血管、防止脂质过氧化.大量的生命必须要含有微量的元素中,Cu2+和Zn2+是不可或缺的,所以其络合物的一些生理以及药理作用是我们的研究目标之一[2].Fisetin或者铜的络合物也同样能够呈现出好的抗氧化性或者增强药性,铜元素是一种常见的微量元素,在呼吸中发挥着重要作用,在光合作用中同样的发挥着作用,而且它在很多的酶中能够发现[3].锌能够让我们发育、提高食欲、增强智力和免疫力,参和体内300多种酶和功能蛋白的组成等,食物摄取来源主要为水产品和肉类及谷物.[4]
Fisetin添加到营养补充剂中,有多种药理作用.同时四类碱基是生命体DNA的组成单元,任何药理和生理过程都会和其有关[5].黄酮类化合物有一些金属离子配合物能够提高药效而且存在药理机能,有望为中药物质基础研究提供一些好的新的途径,也是Fisetin的一个研究方向和目标[6].本文选取漆黄素分子和Cu2+,Zn2+,按照理论和计算上可能的配合方式,研究设计出三种络合物,络合方式为碱基分子采取N或者O原子位置,和络合物中的金属离子中心直接接触,结果表明,只有鸟嘌呤和该类络合物有明显相互作用.
2 计算细节
论文所涉及到的有计算均采用高斯09[7]程序包,在B3LYP[8]水平上完成.非金属元素C、H和O采用6-31++g**[9]基组,金属铜、锌离子采用LANL2DZ[10]基组,得到了全优化的的分子、配合物体系以及该配合物体系和四个碱基相互作用体系,能量数据,结果表明Fisetin铜、锌络合物只对鸟嘌呤有明显的相互作用.
3 结果和讨论
3.1 腺嘌呤络合体系
由表1知,在2Fisetin-Cu1+-A分子中,结合Cu+之后,Cu+离子和O的键长R(O13,Cu)为2.560A,是最长的键,是不稳定的,Cu+离子和O的键长R(O14,Cu)为2.104A,是最短的键,相对稳定的.C-N的键长R(C63,N75)为1.377A;N-H的键长R(H70,N71)为1.040A;C-O的键长R(C8,O13)为1.253A.在2Fisetin -Cu2+-A-opt分子中,结合Cu2+之后,Cu2+离子和O的键长R(O43,Cu)为2.270A,是最长的键,是不稳定的,Cu2+离子和O的键长R(O44,Cu)为2.037A是最短的键,稳定.C-N的键长R(C63,N75)为1.348A;N-H的键长R(H70,N71)为1.014A;C-O的键长R(C8,O13)为1.260A.在2Fisetin-Zn2+-A-opt分子中,结合Zn2+之后Zn2+和O的长R(O43,Zn)为2.164A是最长的键,是不稳定的,Zn2+和O的长R(O44,Zn)为2.05A,是最短的键,是相对稳定的.N-H的键长R(H70,N71)为1.014A;C-N的键长R(C63,N75)为1.363A;N-H的键长R(H70,N71)为1.014A;C-O的键长R(C8,O13)为1.397A.结合碱基后,2Fisetin-Zn2+-A-op相比较2Fisetin-Cu2+-A-opt,2Fisetin-Cu1+-A的键长减小,所以Zn2+结合Fisetin在几何参数上看更加稳定.
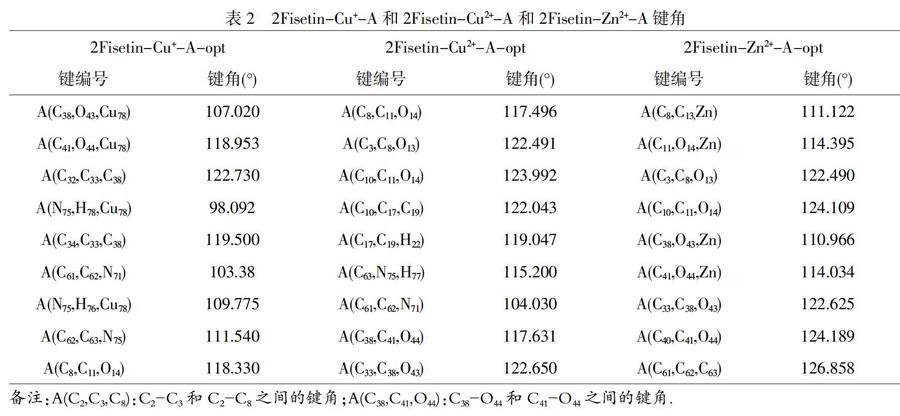
如图1 Fisetin和Adenine大体上是平面的机构,Fisetin和碱基Adenine(腺嘌呤)结合后,Cu+为中心原子,在2Fisetin-Cu+-A-opt中,原Fisetin中的键角A(C2,C1,C6)由119.62°变化到122.31°变化了2.69°;原Adenine中的键角A(C2,C1,C13)由108.26°变化到126.86°变化了21.60°.Fisetin和碱基Adenine(腺嘌呤)结合后,Cu2+为中心原子,在2Fisetin-Cu2+-A-opt中原Fisetin中的键角A(C2,C1,C6)由119.62°变化到122.04°变化了2.44°;原Adenine中的键角A(C2,C1,C13)由108.26°变化到121.92°变化了13.67°.Fisetin和碱基Adenine(腺嘌呤)结合后,Zn2+为中心原子,在2Fisetin-Zn2+-A-opt中原Fisetin中的键角A(C2,C1,C6)由119.62°变化到126.86°变化了7.24°;原Adenine中的键角A(C2,C1,C13)由108.25°变化到122.62°变化了14.37°说明平面结构被打破.
3.2 鸟嘌呤络合体系
根据表3、表4知,在2Fisetin-Cu+-GO-opt分子中,结合Cu之后,Cu+离子和O的键长R(O44,Cu)为1.943A,是最长的键,是不稳定的,Cu+离子和O的键长R(C64,N71)为1.315A,是最短的键,是相对稳定的.C-N的键长R(C64,N72)为1.376A;C-H的键长R(C65,H67)为1.082;C-O的键长R(C40,O42)为1.382A.在2Fisetin-Cu2+-GO-opt分子中,结合Cu之后,Cu2+离子和O的键长R(O13,Cu)为3.658A,是最长的键,是不稳定的,Cu2+离子和O的键长R(O44,Cu)为1.923是最短的键是相对稳定的,C-N的键长R(C61,N62)为1.451A;N-H的键长R(N66,H74)为1.472A;C-O的键长R(C38,O43)为1.261A.
在2Fisetin-Zn2-GO-opt分子中,Zn2+和O的长R(O43,Zn)为2.146A是最长的键,是不稳定的,Zn2+和O的长R(O44,Zn)为2.039A,是最短的鍵,是相对稳定的.N-H的键长R(H70,N71)为1.042A;C-N的键长R(C63,N75)为1.363A;N-H的键长R(H70,N71)为1.042A;C-O的键长R(C38,O43)为1.272A.结合碱基后,2Fisetin-Cu2+-GO-opt相比较2Fisetin-Cu+-GO-opt,2Fisetin-Zn2+-GO的键长减小,所以Cu2+结合Fisetin更加稳定.
根据表5知,如图所示Fisetin和Guanine大体上是平面的机构,Fisetin和碱基Guanine结合后,Cu+为中心原子,在2Fisetin-Cu+-GO-opt中,原Fisetin中的键角A(C2,C1,C6)由119.62°变化到119.78°变化0.16°;原Guanine中的键角A(C2,C1,C4)由118.56°变化到110.464°变化了-8.10°.Fisetin和碱基Guanine结合后,Cu2+为中心原子,在2Fisetin-Cu2+-GO-opt中原Fisetin中的键角A(C2,C1,C6)由119.62°变化到120.47°变化了0.85°;原Guanine中的键角A(C2,C1,C4)由118.56°变化到122.62°变化4.06°.Fisetin和碱基Guanine结合后,Zn2+为中心原子,在2Fisetin-Zn2+-GO-opt中原Fisetin中的键角A(C2,C1,C6)由119.62°变化到126.86°变化了7.24°;原Guanine中的键角A(C2,C1,C4)由118.56°变化到122.06变化了3.50°则说明平面结构被打破.
通过吉布斯自由能计算相互作用能,公式:
△G=Gcom-basic-Gcom-Gbasic
其中Gcom-basic为络合物与碱基体系的吉布斯自由能,Gcom为络合物的吉布斯自由能,Gbasic为碱基分子的吉布斯自由能.结果表明,只有鸟嘌呤的相互作用能为负值,因此为相对稳定络合体系.
4 结语
从铜、锌的Fisetin络合物与碱基作用的计算结果知,只有鸟嘌呤的相互作用能为负值,与几何结构参数相一致,其他的体系优化出的结构相对较为松散.说明鸟嘌呤分子与铜和锌离子相互作用较强,络合体系较为稳定.
参考文献:
〔1〕李想.黄酮醇类化合物ESI-ITMSn质谱裂解规律的量子化学研究[A].药物分析实验室,2015(6):1-5.
〔2〕师帅,黄曦,艾洪齐.DNA碱基(对)及其Zn2+复合物对CO2,N2,H2小分子的吸附[A].机实验室,2014(2):1492-1494.
〔3〕Maher P, Dargusch R, Bodai L, et al. ERK activation by the polyphenols fisetin and resveratrol provides neuroprotection in multiple models of Huntington\"s disease[J]. Human Molecular Genetics, 2011, 20(2):261-270.
〔4〕于凤池.铁、锌生理功能及稻米中铁、锌含量分布和测定方法的比较研究[J].农业科技通讯,2011(11):87-88.
〔5〕刘青,蒋小岗.在激酶抑制剂DRB在骨髓瘤细胞中调控锌指转录因子IKZF1的机制研究[A].药学院抑制剂实验室,2016(6):847-848.
〔6〕陈宏霞,王成章.漆树黄酮类化合物研究进展[A].生物质化学利用国家工程实验室,2013(7):1754-1752.
〔7〕Frisch M. J., Trucks G. W., Schlegel H. B., Scuseria G. E., Robb M. A., Cheeseman J. R., Montgomery J. A., Jr., Vreven T., Kudin K. N., Burant J. C., Millam J. M., Iyengar S. S., Tomasi J., Barone V., Mennucci B., Cossi M., Scalmani G., Rega N., Petersson G. A., Nakatsuji H., Hada M., Ehara M., Toyota K., Fukuda R., Hasegawa J., Ishida M., Nakajima T., Honda Y., Kitao O., Nakai H., Klene M., Li X., J. E., Hratchian H. P., Cross J. B., Bakken V., Adamo C., Jaramillo J., Gomperts R., Stratmann R. E., Yazyev O., Austin A. J., Cammi R., Pomelli C., Ochterski J. W., Ayala P. Y., Morokuma K., Voth G. A., Salvador P., Dannenberg J. J., Zakrzewski V. G., Dapprich S., Daniels A. D., Strain M. C., Farkas O., Malick D. K., Rabuck A. D., Raghavachari K., Foresman J. B., Ortiz J. V., Cui Q., Baboul A. G., Clifford S., Cioslowski J., Stefanov B. B., Liu G., Liashenko A., Piskorz P., Komaromi I., Martin R. L., Fox D. J., Keith T., Al-Laham M. A., Peng C. Y., Nanayakkara A., Challacombe M., Gill P. M. W., Johnson B., Chen W.
〔8〕Tirado-Rives J., Jorgensen W. L., Performance of B3LYP density functional methods for a large set of organic molecules, J. Chem. Theory and Comput., 2008, 4:297-306.
〔9〕McLean A. D., Chandler G. S., Contracted Gaussian-basis sets for molecular calculations. 1. 2nd row atoms, Z=11-18, J. Chem. Phys., 1980,72 (5639):48.
〔10〕Dunning Jr.T. H.,Hay P. J., in Modern Theoretical Chemistry, Ed. H. F. Schaefer III, 1977, 3:1-2.
收稿日期:2019-12-21
基金项目:国家自然科学基金(21563002);内蒙古科技厅自然科学基金(2019MS02030);内蒙古自治区高等学校科学研究项目(NJZY20199,NJZY18205,NJZY20202);内蒙古自治区光电功能材料重点实验室基金
通讯作者:罗冬梅(1976-),女(汉族),黑龙江克东人,赤峰学院副教授,博士,从事量子催化和天然产物分子研究
