水热法制备Mn掺杂ZnO及其光催化性能研究
2020-10-21刘方华李香兰彭小英冯胜雷
郭 慧,刘方华,2,付 翔,2,李香兰,彭小英,2,冯胜雷
(1.江西科技学院城市建设学院,南昌 330098;2.江西科技学院绿色建筑研究所, 南昌 330098; 3.河北工程大学土木工程学院,邯郸 056038)
0 引 言
在工业经济快速发展的同时,改善环境污染问题迫在眉睫,在提高人民生活水平的前提下,如何保持青山绿水需要科研工作者从科学的角度给出解决方案。工业废水污染是环境污染中重要的一类[1],特别是印染厂、制革厂、化工厂排出的偶氮类、蒽醌类和杂环类有机废水,色度深、毒性大、有机物含量高、降解难度大[2]。光催化技术是新兴起来的一种先进氧化技术,因其具有绿色、无污染、降解彻底的优点,而在工业废水处理领域具有广阔的应用前景[3-5]。
光催化材料在光催化技术中处于核心的地位,目前应用最为普遍的光催化材料是TiO2及其复合物,但是TiO2成本较高[6]。相比之下,ZnO与TiO2带隙结构相似,而且具有毒性低和价格低廉的优点[7-8],特别是在降解某些污染物的时候呈现出比TiO2更优越的光催化性能,因此,ZnO成为光催化领域一种具有潜在应用价值的新材料[9]。但是,纯ZnO存在光谱响应范围窄,光生载流子复合率高等缺点,为此,人们通过半导体复合、非金属/金属掺杂和贵金属表面负载等形式来改善其光催化性能,提高光催化效率[10-13]。Mn在地壳中含量丰富(约占0.1%),廉价易得,且毒性低,更为重要的是Mn与Zn离子半径相近,如果将Mn掺杂入ZnO的晶格中,就可以引入掺杂能级、降低禁带宽度、拓宽光响应范围和提高光催化效率。
本研究拟采用水热合成法来制备Mn掺杂ZnO粉体,通过物相分析、孔隙结构和光学性质研究来表征该粉体,以有机染料为降解对象,研究该粉体的降解性能、降解选择性和降解寿命,以期为工业有机废水处理提供技术支撑。
1 实 验
1.1 原材料
醋酸锌((CH3COO)2Zn·2H2O)购自于天津市大茂化学试剂厂,水合硫酸锰(MnSO4·H2O)和氢氧化钠(NaOH)购自于西陇科学股份有限公司,有机染料刚果红(CR, C32H22N6Na2O6S2)、罗丹明B(RhB, C28H31ClN2O3)和亚甲基蓝(MB, C37H27N3Na2O9S3)购自于国药集团化学试剂公司,以上化学试剂均为分析纯。
1.2 粉体合成
称取4.95 mmol醋酸锌和一定量的水合硫酸锰溶解于20 mL去离子水中。将100 mL 0.05 mol/L的氢氧化钠溶液边搅拌边加入到上述的溶液中,继续搅拌30 min。然后倒入反应釜中,在恒温干燥箱中,200 ℃条件下反应2 h。反应后,用去离子水和无水乙醇对所得到的沉淀分别清洗3次,最后在60 ℃下烘干得到Mn掺杂ZnO粉体。当Mn/(Mn+Zn)的比值为0.01和0.05时,制得的粉体分别记为Mn0.01Zn0.99O和Mn0.05Zn0.95O。
1.3 粉体表征
粉体的物相组成通过X射线粉末衍射仪(XRD, Bruker D8, 德国Bruker公司)进行测试,采用石墨单色器,波长λ=0.154 18 nm 的Cu靶为辐射源,工作电压和电流分别设置为40 kV和30 mA,扫描角度的范围为5°~60°。使用美国Micromeritics公司生产的ASAP2460仪器,对粉体在77 K温度下进行氮气吸附脱附和比表面积(BET)分析,测试前先在60 ℃ 干燥12 h。使用日本Hitachi公司的F4600荧光分析仪对粉体进行光致发光分析(PL),激发波长为325 nm。使用美国PerkinElmer公司生产的Lambda950光度计对粉体进行紫外-可见光漫反射(UV-Vis DRS)分析,以BaSO4作为参考样。
1.4 光催化测试
取试样0.5 g粉体放入装有250 mL浓度为10 mg/L的有机染料水溶液中,超声分散5 min,搅拌暗吸附30 min后,置于紫外灯(ZF-1,8 W,365 nm,上海精科仪器厂)下20 cm处进行光催化反应。每隔10 min吸取3 mL降解液,在转速为10 000 r/min的台式高速离心机(H/T16MM型,湖南赫西仪器装备有限公司)上离心1 min,在可见光分光光度计(721型,上海精科仪器厂)上测试溶液的吸光度值,根据标准曲线计算出相应的浓度,测试完后液体倒回烧杯中。用C/C0(C0为有机染料溶液初始浓度,C为光照t时间后的浓度) 来记录溶液浓度的变化。有机染料刚果红、亚甲基蓝和罗丹明B最大的吸收波长分别设置在448 nm、665 nm和554 nm。
有机染料溶液降解完后,测试溶液的COD(化学需氧量)值以评价其矿化率[14]。根据GB11914—89《水质 化学需氧量的测定 重铬酸盐法》,取降解后并经高速离心的溶液5 mL,加入 5 mL 重铬酸钾标准溶液(0.025 mol/L)和 15 mL 浓H2SO4-Ag2SO4溶液,加热回流 2 h 后,冷却至室温,以试亚铁灵为指示剂,用0.1 mol/L的硫酸亚铁铵标准溶液滴定,溶液由黄色经蓝绿色至红褐色即为终点。根据消耗的硫酸亚铁铵体积来计算COD 值,以公式(1-COD/COD0)×100%计算COD去除率,其中COD0和COD分别为降解前后溶液的COD值。
为了测试粉体的光催化寿命,用同样的Mn0.05Zn0.95O粉体按照上述步骤连续降解4次刚果红溶液,每次降解完后,更换溶液,粉体离心60 ℃烘干后继续使用。用吸附30 min后的(1-C/C0)×100%来表示吸附率,用光照70 min后的(1-C/C0)×100%来表示降解率。
2 结果与讨论
2.1 性能表征
图1(a)为Mn掺杂ZnO粉体的XRD图谱。粉体的XRD图谱与六方纤锌矿ZnO的标准衍射谱(JCPDS No. 36-1451)相一致,无新相的出现,说明合成的粉体较纯。粉体的XRD各衍射峰较尖锐,说明粉体结晶良好。Mn 掺杂 ZnO 粉体的XRD图谱中没有出现杂峰,说明Mn离子代替了 ZnO 晶格中Zn的位置。图1(b)的局部放大XRD图显示Mn掺杂ZnO的XRD相对于纯相ZnO向大角度方向偏移,并且Mn掺杂量越多,偏移角度越大,这说明Mn进入了ZnO的晶格中,并且Mn掺杂ZnO后晶粒尺寸变小,这是因为Mn4+半径(0.060 nm)和Mn3+半径(0.066 nm)小于Zn2+半径(0.074 nm),当Mn代替晶格中的Zn位置后,晶格体积变小。
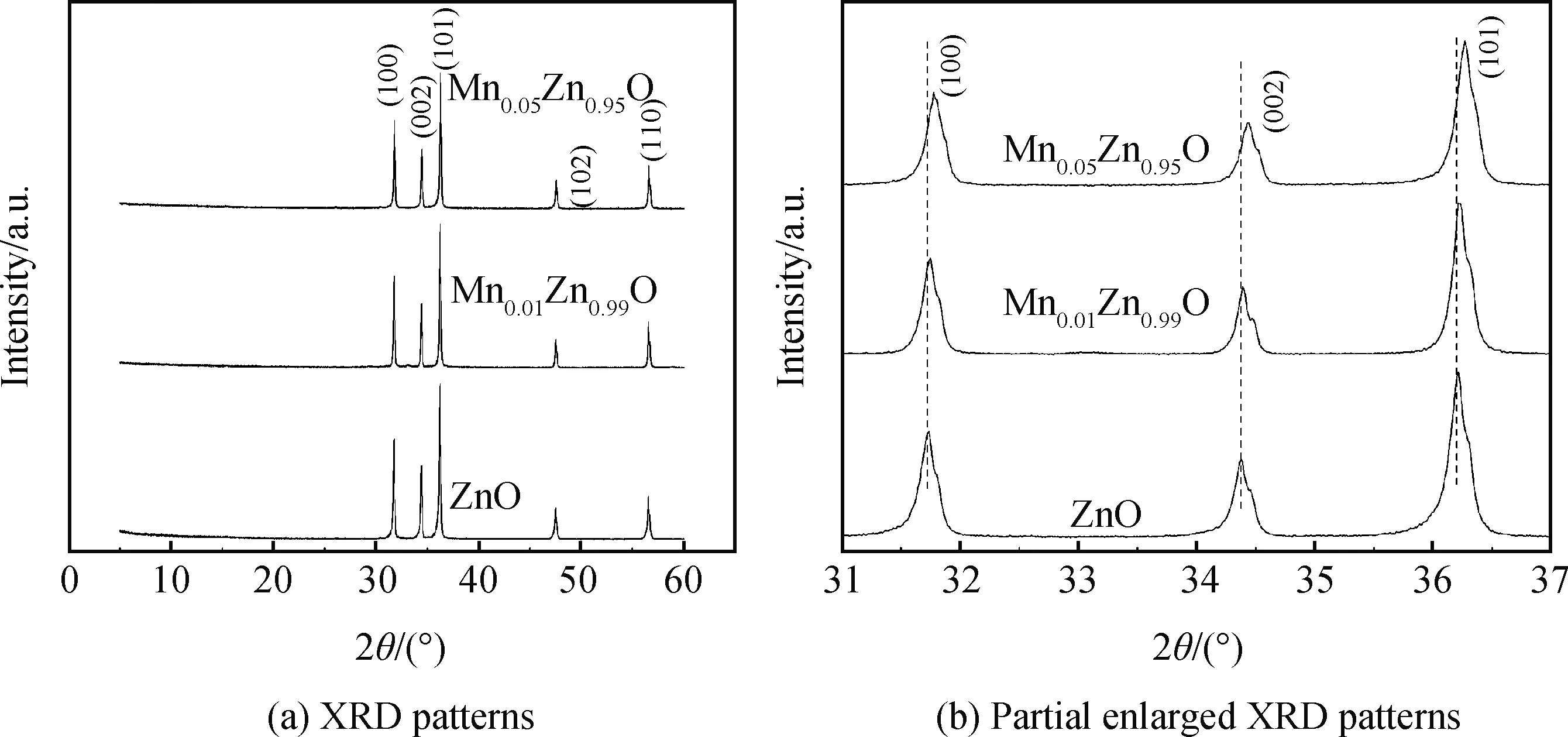
图1 Mn掺杂ZnO粉体的XRD图谱Fig.1 XRD patterns of Mn doped ZnO powders
图2为Mn掺杂ZnO的氮气吸附脱附曲线。三种粉体的氮气吸附脱附曲线均为IV型吸附等温线(BDDT分类法)和H3型滞后回线,粉体中的孔尺寸为介孔(2~50 nm)范围,并且Mn0.05Zn0.95O中的孔体积最大。测试出的孔结构参数如表1所示,可以看到Mn0.05Zn0.95O比表面积和孔容积最大,粉体粒径最小。

表1 Mn掺杂ZnO粉体的孔结构参数Table 1 Pore structure parameters of Mn doped ZnO powders
图3是Mn掺杂ZnO的光致发光图。从图上可以看出,所有样品在473 nm处有一个尖锐的蓝光发射峰,在525~600 nm处出现了一个较宽的绿光发射峰。在ZnO晶体中容易形成锌填隙Zni缺陷,该缺陷能级到价带顶的能量约为2.90 eV,所以电子从锌填隙Zni缺陷能级到价带顶的跃迁产生了蓝光发射峰[15]。而绿光发射峰来自于ZnO 晶格内部的氧空位或锌填隙等本征缺陷形成的深能级跃迁。Mn 掺杂ZnO后,形成的Mn离子能够捕获电子,抑制了光生载流子的复合,增加了非辐射过程,从而导致发射峰强度降低[16]。Mn0.01Zn0.99O和Mn0.05Zn0.95O的荧光发光强度相比于纯ZnO明显减弱,说明其光生载流子的复合率降低,从而有更多的光生载流子迁移到材料表面发生光催化反应,提高了材料的光催化活性。
图4为Mn掺杂ZnO粉体对紫外-可见光漫反射谱和禁带宽度。在图4(a)中,ZnO在可见光区几乎没有吸收,Mn0.05Zn0.95O相对于ZnO在紫外区和可见光区对光的吸收均有所加强,这与潘会等[17]的报道类似。从图中还可以看到,Mn0.01Zn0.99O和Mn0.05Zn0.95O的吸收边相对于ZnO发生红移,这使得粉体能够吸收更多的光,产生更多的光生载流子。根据Kubelka-Munk公式[18],αhυ=A(hυ-Eg)n,可以得到半导体的禁带宽度,其中α为吸收系数,h为普朗克常数,υ为光的频率,A为常数,Eg为禁带宽度。对于ZnO这样的间接间隙半导体,n=2[19]。如图4(b)所示,ZnO的禁带宽度分别为3.18 eV,Mn掺杂ZnO后禁带宽度有所减小,Mn0.01Zn0.99O和Mn0.05Zn0.95O的禁带宽度分别为3.13 eV和3.16 eV,这是由于Mn掺杂替代Zn后产生的局域化3d电子恰在费米能级附近,它与能带电子间的sp-d交换耦合引起带隙变化,其中s-d和 p-d交换相互作用分别使得导带边变低和价带边升高,从而使Eg变窄[16]。禁带宽度的减小有利于拓宽光谱的响应范围,吸收更多的光用于光催化反应。
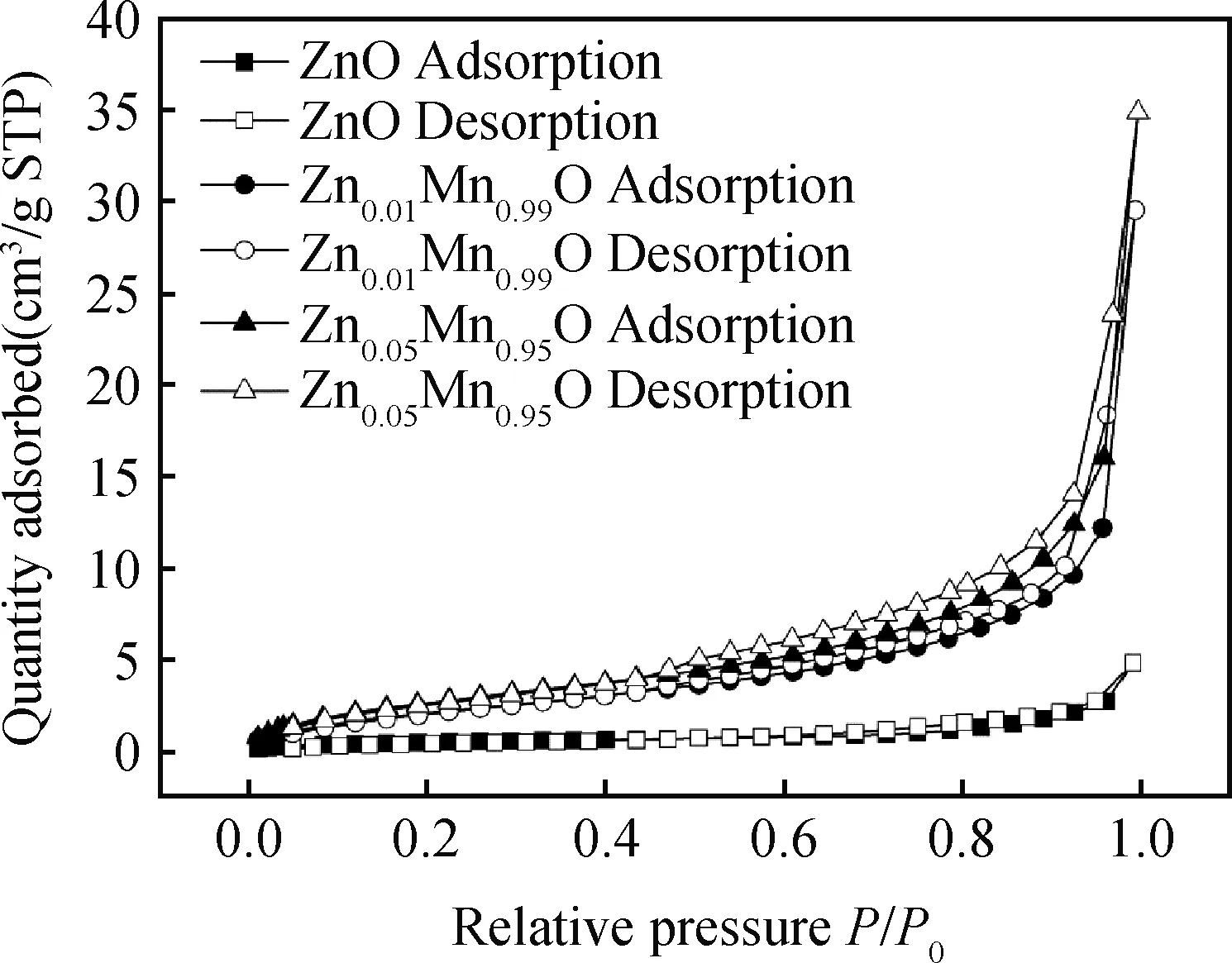
图2 Mn掺杂ZnO粉体的氮气吸附脱附曲线Fig.2 N2 adsorption-desorption curves of Mn doped ZnO powders
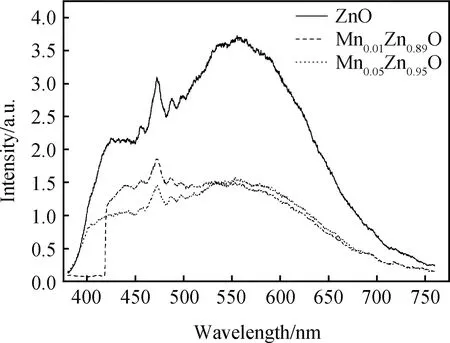
图3 Mn掺杂ZnO粉体的光致发光谱Fig.3 Photoluminescence spectra of Mn doped ZnO powders
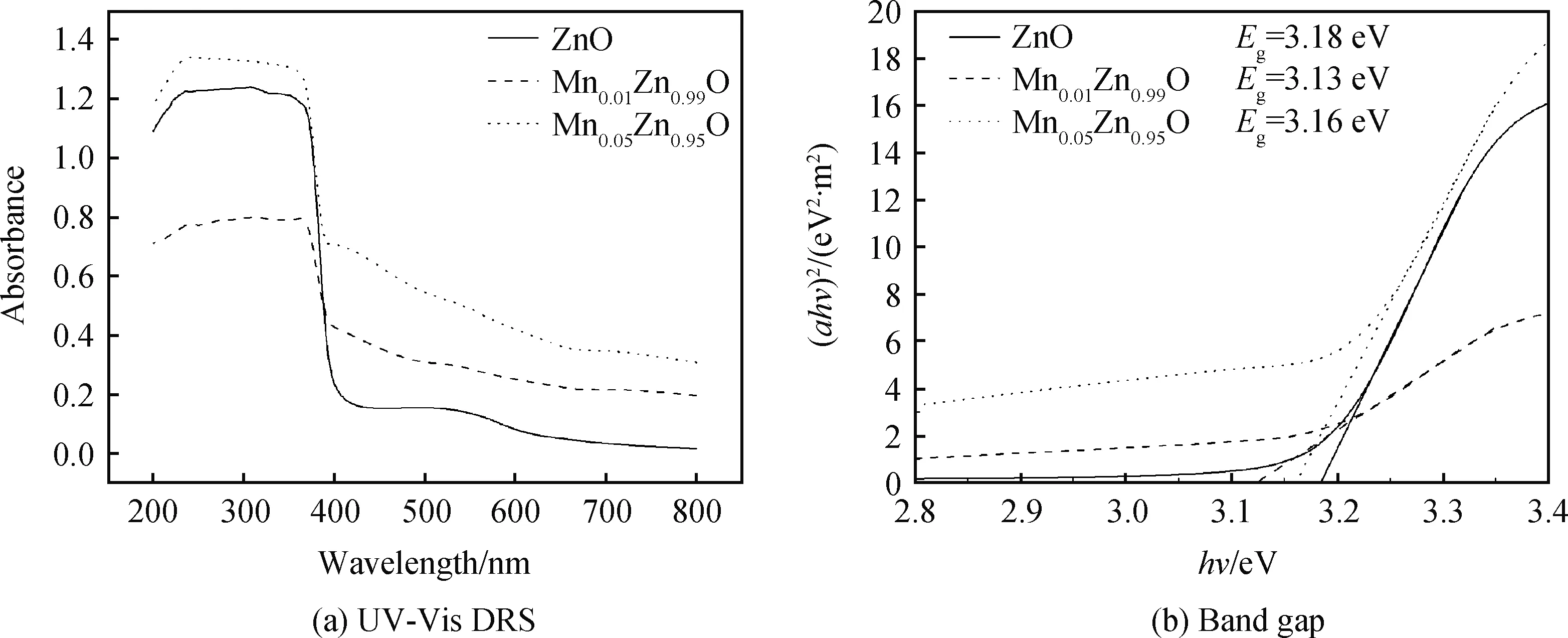
图4 Mn掺杂ZnO粉体的紫外-可见光漫反射谱(a)和禁带宽度(b)Fig.4 UV-Vis DRS(a) and band gap(b) spectra of Mn doped ZnO powders
2.2 光催化降解性能
图5为Mn掺杂ZnO粉体对刚果红的降解曲线和COD去除率。从图5(a)可以看到,在吸附30 min后,ZnO、Mn0.01Zn0.99O、Mn0.05Zn0.95O对刚果红溶液的吸附率分别为2.91%、5.22%和7.35%,这与粉体的孔隙率有关,Mn0.05Zn0.95O的孔容积最大,吸附性能最佳。在光照70 min后,刚果红自降解率仅为1.17%,说明在8 W、365 nm的紫外光照条件下,刚果红难以降解。光照70 min后,在ZnO、Mn0.01Zn0.99O、Mn0.05Zn0.95O的刚果红溶液C/C0值分别0.089、0.066和0.026,Mn0.05Zn0.95O对刚果红的降解效率最高,这是因为Mn掺杂到ZnO晶格中后,引入了掺杂能级,降低了禁带宽度,产生了更多的光生载流子,这些光生载流子迁移到晶体表面,和吸附的刚果红分子发生了氧化还原反应,将刚果红分子降解为CO2、H2O等小分子,提高了降解效率。从图5(b)可以看出,在刚果红COD去除率方面,光解过程产生的COD去除率几乎为零,光照70 min后,ZnO、Mn0.01Zn0.99O和Mn0.05Zn0.95O对刚果红溶液的COD去除率分别为70.78%、72.47%和76.34%,进一步说明了Mn掺杂ZnO后促进了刚果红溶液的矿化,其中Mn0.05Zn0.95O对刚果红的矿化率最高,降解最为彻底。矿化率低于降解率说明刚果红降解后产生的中间产物相当稳定,难以矿化[20]。
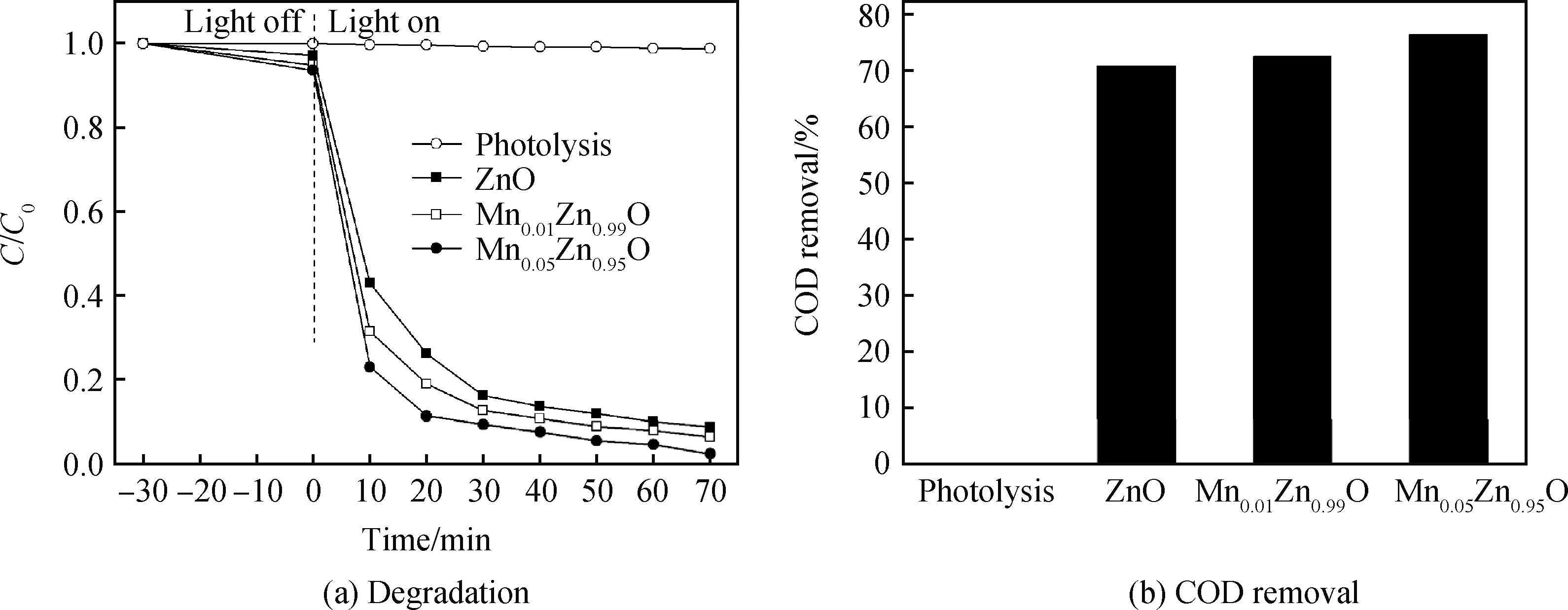
图5 Mn掺杂ZnO对刚果红的降解曲线(a)和COD去除率(b)Fig.5 Degradation curves(a) and COD removals(b) of Mn doped ZnO over Congo red
图6为Mn0.05Zn0.95O对不同染料的降解曲线和COD去除率。从图6(a)可以看到,暗吸附30 min后,Mn0.05Zn0.95O对刚果红、罗丹明B和亚甲基蓝的吸附率分别为7.35%、11.75%和8.87%,Mn0.05Zn0.95O对罗丹明B吸附最好,对刚果红吸附最差,这是因为在染料溶液中,罗丹明B带正电荷,刚果红和亚甲基蓝带负电荷,ZnO及其掺杂物的等电点在9.6左右[21],所以中性染料中Mn0.05Zn0.95O带负电荷,在静电作用下,Mn0.05Zn0.95O吸附罗丹明B分子而排斥刚果红和亚甲基蓝分子,而刚果红和亚甲基蓝分子结构的差异使得排斥作用略有不同。光照70 min后,刚果红、罗丹明B和亚甲基蓝的自降解率分别为1.17%、7.66%和16.16%,说明这三种染料在此光照条件下比较稳定,自降解困难,自降解率的差异与染料分子结构相关。尽管Mn0.05Zn0.95O对刚果红、罗丹明B和亚甲基蓝的吸附不同,但是在光照50 min后亚甲基蓝溶液完全降解,60 min后罗丹明B完全降解,70 min后刚果红溶液的C/C0值为0.026,说明亚甲基蓝最容易降解而刚果红最难降解,它们分子结构的差异性在光催化降解过程中起着更为重要的作用[22]。经过70 min光照后,取降解后的溶液测试其COD去除率,结果如图6 (b)所示。刚果红、罗丹明B和亚甲基蓝的COD去除率非常低,分别为0.007%、0.05%和0.12%,说明光解难以使得有机染料矿化。经过70 min光照后,Mn0.05Zn0.95O对刚果红、罗丹明B和亚甲基蓝的COD去除率分别为76.34%、82.19%和88.59%,矿化率的差异与分子结构的差异性相关。
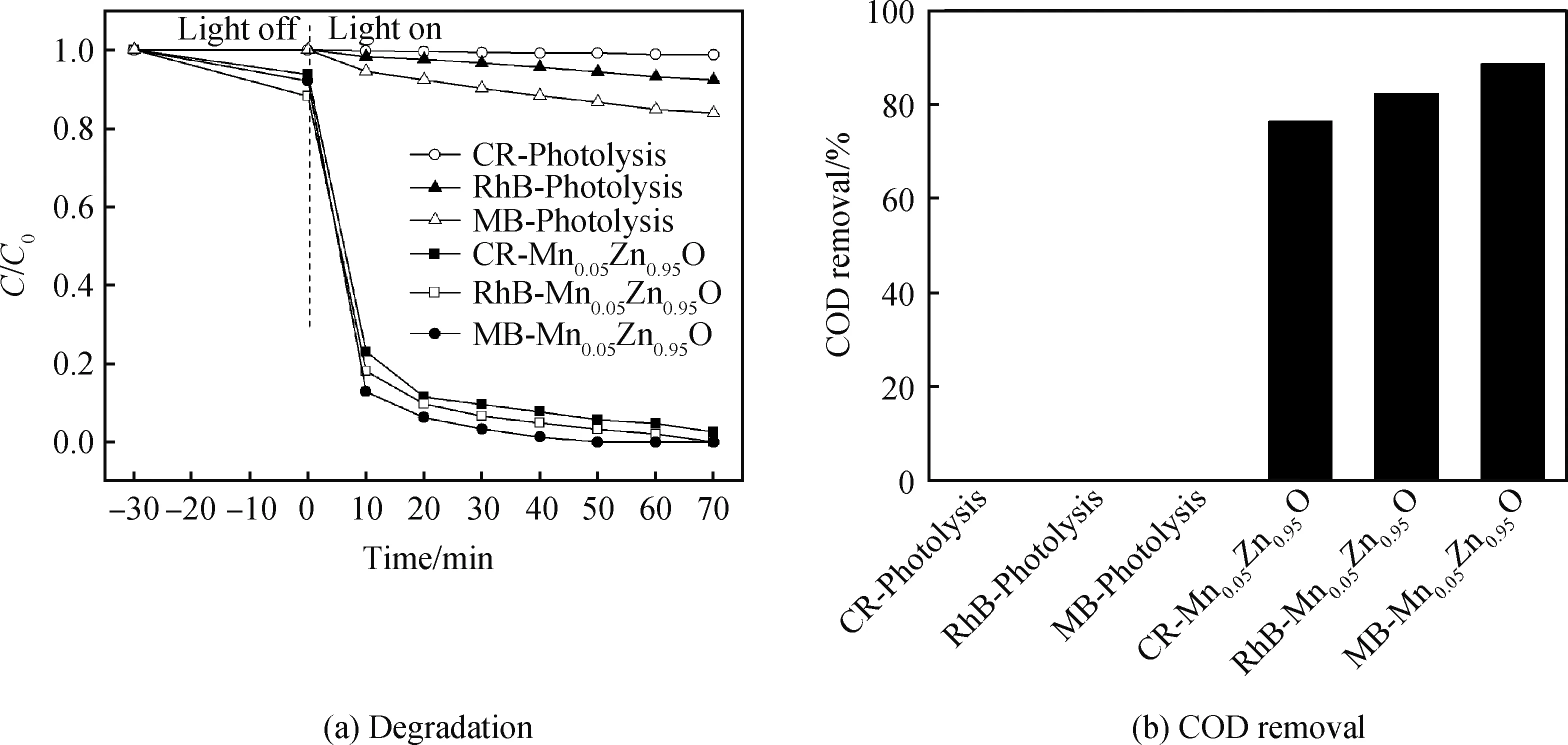
图6 Mn0.05Zn0.95O对不同染料的降解曲线(a)和COD去除率(b)Fig.6 Degradation curves(a) and COD removal(b) of Mn0.05Zn0.95O over different dyes
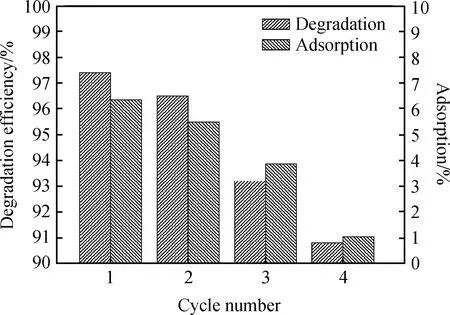
图7 Mn0.05Zn0.95O对刚果红的降解寿命和吸附率Fig.7 Degradation life and adsorption of Mn0.05Zn0.95O over Congo red
图7是Mn0.05Zn0.95O对刚果红的降解寿命和吸附率曲线。连续降解后,降解率由第1次的97.4%降到第4次的90.8%,降解率减少了6.6%,这是因为一方面粉体吸附的有机染料分子及降解过程的中间产物遮挡了活性位点,降低了对染料的吸附,如图7所示从第1次到第4次,吸附率依次为6.35%、5.49%、3.87%和1.04%,吸附率的降低印证了活性位点的减少;另一方面尽管在每次循环降解后,尽量回收粉体,但是在离心过程中还是造成了少量的粉体损失,这是粉体光催化剂不可避免的缺点,Mishra等[23]也报道了类似的结论,他们将制备的g-C3N4/TiO2/膨润土复合光催化剂5次连续降解活性艳红染料后,降解率由90%降到75%。董海军等[24]使用TiO2/g-C3N4粉体连续5次降解甲基橙后,降解效率降低了约40%,其认为是由于光催化降解产物吸附在了催化剂表面,减少了催化活性位点,但是通过适当热处理后光催化剂的活性又能得到恢复。粉体光催化剂这一缺点有望在后续的负载型光催化剂上得到解决。
3 结 论
(1)当Mn替代0.5%的Zn时,Mn占据了ZnO晶格中Zn的位置,粉体粒度小、比表面积大,抑制了光生载流子的复合,降低了禁带宽度,拓宽了光的响应范围。
(2)在8 W、365 nm紫外光条件下光照70 min后,制备的Mn0.05Zn0.95O粉体对刚果红降解率达到了97.4%,COD去除率达到了76.34%;Mn0.05Zn0.95O对罗丹明B吸附最好,对亚甲基蓝降解最好;对刚果红连续降解4个循环后,降解率降低了6.6%。
