基于网络药理学与分子对接法探寻双黄连口服液治疗新型冠状病毒肺炎的有效成分及机制研究
2020-10-17谢丽华蔺晓源胡国恒
谢丽华,蔺晓源,何 飘,刘 瑛,胡国恒*
(1.湖南中医药大学,湖南 长沙410208;2.湖南中医药大学第一附属医院,湖南 长沙410007)
新型冠状病毒肺炎(Coronavirus Disease 2019,COVID-19)是一种由2019 新型冠状病毒(SARSCoV-2)感染引起的流行性肺炎,其传染性强,人群普遍易感,临床症状以发热、乏力、干咳为主,严重者并发急性呼吸窘迫综合征。针对COVID-19,西医主要以抗感染、对症支持治疗为主[1],中医药作为祖国医学的宝贵遗产,在治疗与预防疫病方面具有丰富的临床经验,在整体观念及辨证论治思想的指导下,可通过驱邪外出、扶助正气实现整体调节,以改善临床症状、延缓疾病发展。
2020 年1 月31 日,中国科学院初步发现双黄连口服液可抑制SARS-CoV-2,双黄连口服液由金银花、黄芩、连翘3 味中药组成,具疏风解表、清热解毒之效。 金银花、连翘疏散风热、清热解毒,配以苦寒之黄芩以清中上焦湿热、泻上焦实火,主要用于以发热、咳嗽、咽痛为主的外感风热之症,对病毒感染所致的上呼吸道感染、肺炎等具有一定疗效[2]。 研究表明,双黄连口服液可通过减少炎性细胞浸润、抑制病毒复制,减轻肺损伤,对流感病毒(H1N1、H5N1)、呼吸道合胞病毒、轮状病毒具有明显的抗病毒效应[3-6]。刘菊等[7]通过总结中药抗病毒及抗COVID-19 临床推荐用药的研究发现,抗病毒中药使用频率前5 的为金银花、板蓝根、鱼腥草、连翘、黄芩,中医药防治COVID-19 推荐用药多含金银花、连翘、板蓝根、黄连、黄芪、人参等,而在多次COVID-19 临床诊疗方案中并未推荐双黄连制剂。故本文采用网络药理学对双黄连口服液主要化学成分及其靶点进行功能及通路富集分析,预测双黄连口服液防治COVID-19的有效成分及潜在作用机制,并采用分子对接的方法,对主要活性成分与SARS-CoV-23CL 水解酶(Mpro)、ACE2、2019-nCoV RBD/ACE2-B0AT1complex进行筛选,为寻找COVID-19 的药物治疗或新药研发提供依据。
1 材料与方法
1.1 材料
中药系统药理学数据库和分析平台(TCMSP,http://lsp.nwu.edu.cn/tcmsp.php);DAVID 6.8 数据库(https://david.ncifcrf.gov/);RCSBPDB 数 据 库(http://www.rcsb.org/);Swiss Target Prediction 数据库(http://www.swisstargetprediction.ch/);PubChem 数据库(https://pubchem.ncbi.nlm.nih.gov/);GeneCards 数据库(https://www.genecards.org/);CTD 数 据 库(http://ctdbase.org/);BioGPS 数据库(http://biogps.org/#goto=welcome);Venny 2.1 在线软件作图工具平台(https://bioinfogp.cnb.csic.es/tools/venny/);在线绘图平台Omicshare(https://www.omicshare.com/);Chemoffice 软 件;AutoDockVina1.1.2 软 件;PyMOL 软 件;Cytoscape 3.6.1 软 件;GraphPad Prism 8 软件。
1.2 方法
1.2.1 双黄连口服液化学成分的收集 以“金银花”“黄芩”“连翘”为关键词通过TCMSP 数据库搜索其成分,以口服生物利用度(oral bioavailability,OB)≥30%、药物相似性(drug-likeness, DL)≥0.18为标准进行筛选,并结合相关文献数据确定化学成分,使用Pubchem 数据库下载化学成分的分子结构并保存各成分的Canonical SMILES 格式。
1.2.2 双黄连口服液靶点的预测 将SMILES 格式导入Swiss 数据库,以“人类”为研究对象,得到相应化学成分的作用靶点,整合去除重复后得到双黄连口服液的作用靶点。
1.2.3 COVID-19 靶点的获取 使用GeneCards、CTD 数据库,以"novel coronavirus"为关键字进行搜索,每个数据库选择相关度前300 的靶点作为COVID-19 的相关作用靶点[8],整合去除重复后得到COVID-19 作用靶点。
1.2.4 潜在作用靶点的获取 将双黄连口服液靶点及COVID-19 靶点分别导入Venny 2.1 在线作图工具平台,绘制韦恩图,得到两者的交集,即为双黄连口服液抗COVID-19 的潜在作用靶点,即成分-疾病靶点。
1.2.5 网络构建 将化学成分及所得到的潜在作用靶点导入Cytoscape 3.6.1 软件, 构建双黄连口服液抗COVID-19 的“中药-成分-靶点-疾病”关系网络,使用Network Analyzer 功能对药物中的化学成分及靶点进行分析,节点大小颜色深浅代表度(degree)值的大小,根据节点度值筛选主要活性成分及关键靶点。将关键靶点录入STRING 数据库获取蛋白相互作用信息,运用Cytoscape 3.6.1 软件进行可视化分析,并通过BioGPS 数据库对关键基因进行组织定位分析,得到其作用组织。
1.2.6 通路富集分析 将成分-疾病靶点以Gene Symbol 的格式导入DAVID 6.8 数据库,分别选择生物过程(biological process, BP)、分子功能(molecular function, MF)和细胞成分(cellular component, CC)进行基因本体(GO)富集分析,选择KEGG 进行靶点基因通路注释分析,并且使用GraphPad Prism 8 软件将GO 富集分析满足P<0.05 的结果做成可视化条形图。 使用Omicshare 平台将KEGG 分析满足P<0.05 的结果制成可视化气泡图。
1.2.7 分子对接验证 将主要活性成分的分子结构导入Chemoffice 软件对其进行分子结构能量优化,保存;应用RCSBPDB 数据库下载SARS-CoV-2 3CLMpro(PDB ID:6LU7)、ACE2(PDB ID:1R42)、2019-nCoVRBD/ACE2-B0AT1complex(PDB ID:6M17)的晶体结构,运用Mgltools 1.5.6 进行加氢、计算电荷后保存为*pdbqt 文件,选择3CLMpro、ACE2、complex 特有的小分子配体作为活性中心,最后运用AutoDockVina 对其进行分子对接,利用Pymol 进行分析作图。
2 结果
2.1 潜在化学成分
根据OB≥30%,DL≥0.18,通过TCMSP 检索到双黄连口服液中3 味中药去除重复的化学成分后共74 个,金银花23 个,黄芩36 个,连翘23 个,其中,汉黄芩素为黄芩、连翘所共有,豆甾醇、黄烷酮为黄芩、金银花所共有,槲皮素、木犀草素、山奈酚为连翘、金银花所共有,β-谷甾醇为3 者共有。 研究表明,金银花中的齐墩果酸、木犀草苷、异绿原酸A 和连翘中的连翘酯苷具有潜在的抗SARS-CoV-2 作用[9],虽然这些成分不满足OB≥30%,DL≥0.18 的标准,亦纳入研究,故共收集到78 个化学成分。
2.2 抗COVID-19 潜在作用靶点
将Swiss 数据库中得到的化学成分作用靶点去重复后得到629 个靶点,中药-成分-靶点统计见图1。通过Genecards、CTD 数据库查找COVID-19 相关作用靶点,去重复后得到330 个。将化学成分潜在作用靶点及疾病相关靶点导入Venny 2.1 在线作图工具平台,绘制韦恩图,见图2,共得到两者交集靶点72 个,表明双黄连口服液可能通过调节多个潜在靶点发挥作用。
2.3 中药-成分-靶点-疾病网络构建
将双黄连口服液化学成分与72 个潜在作用靶点导入Cytoscape 3.6.1 软件,除去无靶点关联的孤立成分,绘制中药-成分-靶点-疾病关系网络,见图3。 使用Network Analyzer 功能对关系网络进行分析,度值代表该成分与潜在靶点的关联数,度值越大表明该成分在疾病网络中越重要,根据度值筛选活性成分,其中7-O-甲基汉黄芩素、1,2-苯二甲酸二(2-乙基己基)酯、刺槐素、汉黄芩素、黄芩素、5,7,4'-三羟基-8-甲氧基黄酮、鼠尾草素、去甲汉黄芩素、5,2'-二羟基-6,7,8-三甲氧基黄酮、金圣草素、千层纸素A、黄芩黄酮、黄烷酮、木犀草素等14 个成分度值均大于成分度值中位数(成分度值中位数=13),且均能与18 个及以上靶点相关联,预测这14 个成分是双黄连口服液抗COVID-19 的主要活性成分。
2.4 PPI 网络构建及组织定位分析
根据靶点度值≥2 倍中位数(靶点度值=4)筛选关键靶点[10],得到PTGS2、SRC、MMP2、EGFR、APP等28 个关键靶点,将关键靶点录入STRING 数据库得到蛋白之间相互作用关系,并导入Cytoscape 3.6.1软件进行可视化分析,构建PPI 网络,结果见图4。PTGS2 为前列腺素内过氧化物合成酶的一种亚型,其主要产物前列腺素对RNA 病毒、DNA 病毒均有抗病毒活性,可在病毒复制的早期抑制细胞中的病毒复制[11]。 SRC 蛋白激酶在多种病毒感染过程中被激活并在病毒复制、侵袭过程中具有重要作用[12-13]。EGFR 是受体酪氨酸激酶(RTKs)家族成员之一,其可介导病毒入侵,并在病毒延长存活时间及逃避宿主免疫监控等过程发挥重要作用[14]。
为明确双黄连口服液发挥抗病毒功效与人体组织之间的关系,将关键靶点导入BioGPS 数据库进行定位,见图4,其中,各组织类型分别为呼吸系统的肺及气管,消化系统的胃肠,神经系统的脑,免疫系统的血小板、T 细胞、B 细胞、浆细胞、中性粒细胞等,不同颜色代表对应不同的组织。由图可知,13 个靶点作用于肺组织,为最多,依次为大脑10 个,T 细胞9 个,胃肠8 个,血小板8 个,中性粒细胞6 个,B细胞5 个,浆细胞3 个。表明双黄连口服液活性成分抗COVID-19 的关键基因主要在肺组织和免疫细胞中表达。
2.5 GO 富集分析及KEGG 通路注释分析
将72 个潜在靶点导入DAVID 数据库进行GO富集分析(P<0.05),共得到169 个条目,包含121 个生物过程,23 个细胞成分,25 个分子功能,见图5。生物过程主要涉及分解代谢、RNA 转录调控、血管再生、IL-6 的表达与调控等;在细胞成分中,主要涉及细胞溶质、胞外基质、溶酶体、RNA 聚合酶II 转录因子复合物等;分子功能主要包括ATP 结合、血红素结合、转录因子活性等。KEGG 分析(P<0.05)共富集到100 条信号通路,见图6,主要集中在癌症相关通路、缺氧诱导因子-1 信号通路(HIF-1 signaling pathway)、雌激素信号通路(Estrogen signaling pathway)、磷脂酰肌醇3-激酶(PI3K)/蛋白激酶B(Akt)信号通路(PI3K-Akt signaling pathway)、肿瘤坏死因子信号通路等(TNF signaling pathway)等,可见上述生物功能及信号通路可能与双黄连口服液治疗COVID-19 密切相关。
2.6 主要活性成分的分子对接验证

图4 关键基因PPI 筛选网络及组织定位分析图
一般结合能小于0 说明配体可与受体自发结合,目前对于活性分子靶点筛选尚无统一标准,根据文献报道,此处选取结合能≤-5.0 kcal/mol 作为活性分子与SARS-CoV-2 存在较强结合活性的评价标准[15]。研究表明,SARS-CoV-2 与SARS-CoV 感染途径均通过其表达的S-蛋白与人体内ACE2 相结合构成SARS-CoV-2-RBD-ACE2 复合物,再通过S蛋白膜融合作用释放病毒核酸进入细胞内[16]。SARS-CoV-2 属于RNA 病毒,3CLMpro 在其复制过程中发挥重要作用[17],影响3CLMpro、ACE2 结合活性或影响病毒与ACE2 结合复合物结构的稳定性干扰病毒感染宿主细胞及复制过程,可能是抑制SARS-CoV-2 感染人体的方式[18]。 故将网络药理学分析中度值前14 的活性成分与3CLMpro、ACE2 及2019-nCoVRBD/ACE2-B0AT1 complex 进行分子对接,结果见表1 及图7。 结果显示,14 个主要活性成分与3CLMpro、ACE2 及complex 结合能均<-5.0 kcal/mol,可知双黄连口服液主要活性成分与这3 个蛋白结合构象能量低,结构稳定,具有较好的结合能力。
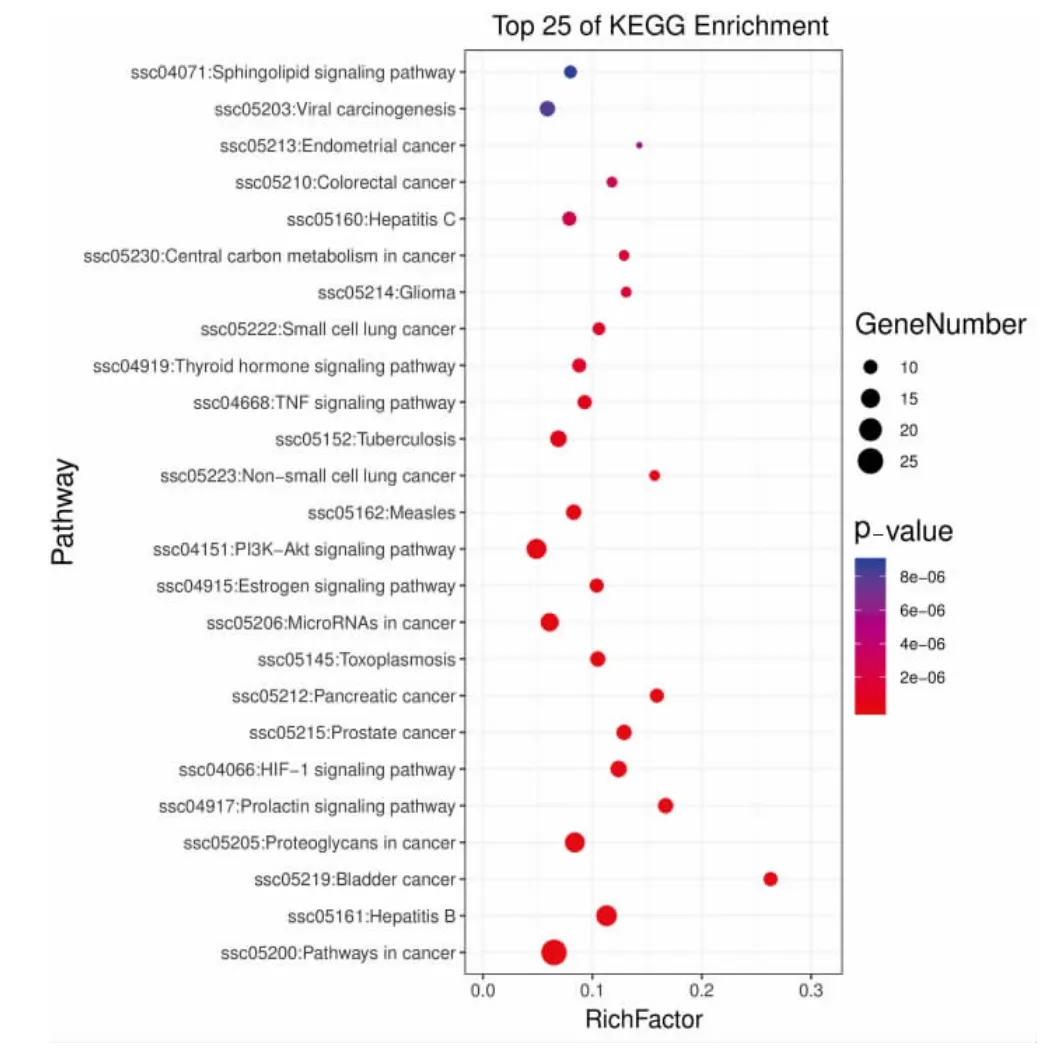
图6 潜在靶点KEGG 通路注释分析气泡图
3 讨论

表1 双黄连口服液主要活性成分的结合能
自推行中西医结合治疗COVID-19 后,我国疫情逐渐被控制下来,而中医药发挥至关重要的作用,数据表明,中西医结合治疗临床治愈率(91.2%)较单纯西医治疗(61.1%)有明显提高[19-20]。 根据此次疫情发生的特点,COVID-19 属于中医学“疫病”范畴,“寒湿疫毒”为其重要病因[21]。《新型冠状病毒感染的肺炎诊疗方案(试行第三版)》[22]将COVID-19 分为寒湿郁肺、邪热壅肺、邪毒闭肺、内闭外脱4 类,治以化湿解毒、宣肺透邪,或清热解毒、宣肺透邪,或宣肺解毒、通腑泄热,或开闭固脱、解毒救逆。双黄连口服液具疏风解表、清热解毒之效,可明显降低邪热壅肺型支气管肺炎患者血象及降钙素原等感染指标,改善患者发热、咳嗽、气急及肺部啰音等症状及体征[23]。目前,双黄连口服液广泛用于流感、肺炎的临床治疗[24-25]。 虽在多次修订的《新型冠状病毒感染的肺炎诊疗方案》 中并没有明确推荐双黄连口服液治疗,但通过对全国各地区治疗COVID-19 的中药数据挖掘发现,金银花、黄芩、连翘使用次数较为频繁[26],因此其物质基础及作用机制的研究具有一定意义,也为COVID-19 的中医药治疗提供参考。
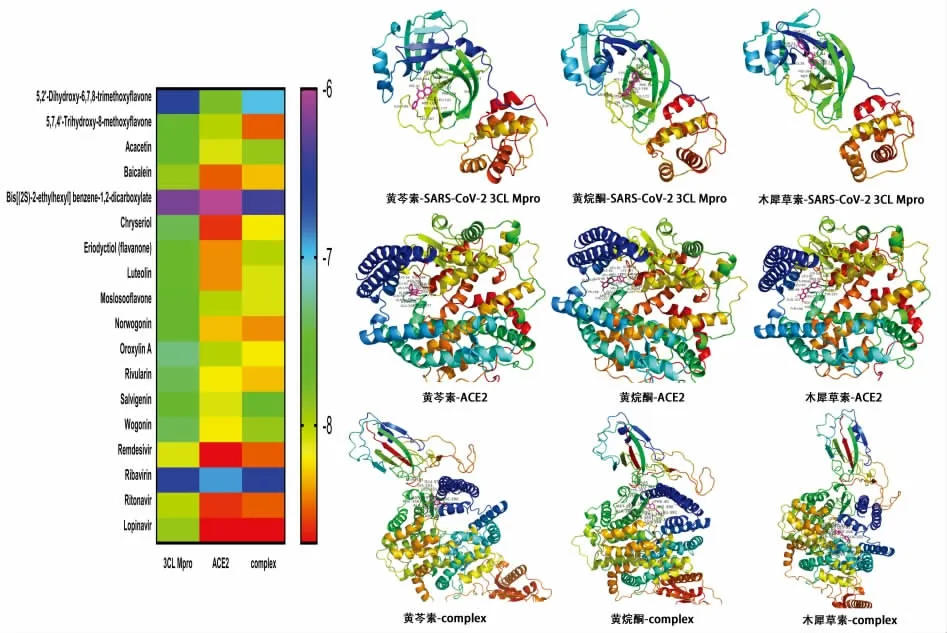
图7 分子对接热图和黄芩素、黄烷酮、木犀草素与3CLMpro、ACE2、complex 分子对接模式
本研究通过网络药理学进行研究,共得到双黄连口服液化学成分78 个,化学成分靶点629 个,COVID-19 相关靶点330 个,最终得到化学成分-疾病靶点72个。 对成分-疾病靶点进行GO 富集分析发现,双黄连口服液活性成分可参与RNA 转录及转录因子活性、IL-6 的表达与调控、ATP 结合、血红素结合等生物功能发挥抗COVID-19 作用。 研究表明,SARS-CoV-2 属于RNA 病毒,RNA 转录可调控其复制增殖过程[17]。 黄芩素、木犀草素可抑制H5N1病毒复制,并可干扰N5N1 诱导巨噬细胞IL-6、TNFα 产生[27]。IL-6 是一种促炎性因子,是形成细胞因子风暴中的关键因素,在加速COVID-19 发生发展中发挥重要作用[28]。 黄芩苷可明显降低IL-6、TNF-γ等细胞因子抑制炎症反应[29],连翘可通过降低核因子-κB(NF-κB)、Toll 样受体4(TLR4)表达水平,减少IL-10、IL-6 等细胞因子分泌,发挥抗炎及免疫调节作用[30]。血红素为铁卟啉化合物,是血红蛋白的辅基,其可与氧结合参与机体载氧、贮氧过程,当组织得不到充足的氧,或不能充分利用氧时,则可导致机体缺氧,严重COVID-19 患者可见呼吸困难和低氧血症,其发生机制可能与IL-2、IL-10、TNF 等诱发炎症反应,缺氧诱发活性氧(ROS)的产生,进而引起弥漫性肺泡损伤、肺水肿,导致呼吸困难,甚至引发急性呼吸窘迫综合征(ARDS)[31]有关。黄芩苷可下调百草枯中毒大鼠肺组织转化生长因子-β1(TGFβ1)、HIF-1α 表达,改善肺纤维化及缺氧症状[32]。
KEGG 通路注释分析结果显示,双黄连口服液主要通过调节癌症相关通路、HIF-1、PI3K-Akt、TNF信号通路等途径来干预COVID-19。 HIF-1 通路主要通过调控ROS 产生、能量代谢、线粒体呼吸等过程参与机体缺氧反应[33],去甲汉黄芩素可降低缺氧细胞内ROS 的产生,下调HIF-1α、Caspase-3 表达,增加Bcl-2 表达水平,保护细胞膜完整性[34]。 TNF 信号通路主要与炎症反应相关,金银花提取物可抑制H1N1 病毒核酸RNA 表达,抑制病毒复制,还可降低TNF-α、IL-1β 水平抑制炎症反应[35]。 PI3K/Akt 通路可调控细胞增殖、分化、凋亡、能量代谢等过程,还参与调节TNF-α 诱导的炎症反应及ROS 介导的氧化应激反应[36-37]。黄芩苷可抑制PI3K/Akt 通路激活,抑制NF-κB 转导,减少TNF-α、IL-6 等细胞因子的分泌,发挥抑制炎症反应作用[38]。连翘苷可通过调控NF-κB 通路以抑制IL-1β 诱导的细胞凋亡[39]。因此,双黄连口服液活性成分可能通过干预癌症相关通路、HIF-1、PI3K-Akt 及TNF 信号通路,发挥抗病毒、抗炎、抑制氧化应激、抑制细胞凋亡作用,从而达到治疗COVID-19 的目的。
PPI 网络构建发现干预COVID-19 的关键靶点主要为PTGS2、SRC、MMP2、EGFR、APP 等28 个。进一步对关键靶点进行组织定位分析,可知其基因主要映射在肺组织和免疫细胞中。SARS-CoV-2 感染早期主要通过与肺中气道上皮细胞、肺泡上皮细胞、血管内皮细胞和巨噬细胞表达的ACE2 结合而侵入机体[40-41]。SARS-CoV-2 感染和肺组织损伤可触发免疫反应,募集巨噬细胞、单核细胞,释放细胞因子,诱发T 细胞免疫反应及B 细胞免疫反应[31],可见肺组织及免疫细胞较易受累。 PTGS2 主要产物是前列腺素(PG),黄芩苷、黄芩素、汉黄芩素等黄酮类化合物可通过抑制脂多糖(LPS)激活的小鼠巨噬细胞对PGE2 的产生发挥抗炎作用[42]。木犀草素可抑制PI3K/Akt 通路激活,减少直肠癌细胞诱导的小鼠肺组织中MPP9 表达[43]。连翘可以抑制H1N1 肺炎小鼠模型中促炎细胞(巨噬细胞、淋巴细胞、白细胞等)释放TNF、IL-6 等细胞因子发挥抗炎作用[44]。 黄芩素可显著抑制免疫细胞对巨噬细胞迁移抑制因子(MIF)的释放,抑制PARP1 激活,保护线粒体功能,减少细胞凋亡[45]。
通过构建“中药-成分-靶点-疾病”关系网络发现,双黄连口服液活性成分主要有木犀草素、千层纸素A、黄芩素、汉黄芩素、黄芩黄酮等14 个,该14 个 成 分 均能与SARS-CoV-2 3CLMpro、ACE2 及2019-nCoVRBD/ACE2-B0AT1 complex 结合,表明双黄连口服液对COVID-19 具有一定的潜在治疗作用。其中,黄芩素、黄烷酮、木犀草素与3CLMpro结合能力较好,而3CLMpro 抑制剂可有效阻断病毒复制;金圣草素、黄芩素、黄烷酮、木犀草素和ACE2 具有较好的结合能力,可竞争性结合ACE2,抑制SARSCoV-2 感染宿主细胞;5,7,4'-三羟基-8-甲氧基黄酮、去甲汉黄芩素、黄芩素、黄芩黄酮与complex 有较好的结合能力,可影响SARS-CoV-2 S 蛋白受体与ACE2 结合复合物结构的稳定性以抑制病毒核酸进入宿主细胞。结合分子对接结果,黄芩素、黄烷酮、木犀草素与3 个蛋白结合能均较低,且与瑞德西韦及《新型冠状病毒肺炎诊疗方案(试行第7 版)》[46]中推荐的利托那韦、洛匹那韦具有相似的结合能力。 黄芩素、木犀草素等黄酮类化合物可通过抑制病毒复制、降低细胞因子产生发挥抗病毒作用[27],故推测黄芩素、黄烷酮、木犀草素可能在抗SARSCoV-2 中发挥重要作用。
综上所述,通过对双黄连口服液中化学成分、作用靶点及其主要活性成分与3CLMpro、ACE2、complex 结合能力进行网络药理学及分子对接技术研究,可以发现双黄连口服液可通过多成分、多靶点、多途径协同发挥抗COVID-19 的作用。 然而,“整体观念、辨证论治”是中医诊治疾病的基本特点,临证处方之时还需考虑患者体质阴阳偏盛之别、发病地域寒温之异、病情发展阶段不同等情况因证施治。双黄连为苦寒清解之品,易损伤脾胃,易耗伤人体阳气,故不可盲目服用。且根据2015 版《中华人民共和国药典》[47],黄芩苷、绿原酸、连翘苷为双黄连口服液的质量控制成分,在制备过程由于成分的富集及丢失,致黄芩素、黄烷酮、木犀草素等含量较低,故双黄连口服液抑制SARS-CoV-2 具有一定限制性。此外,网络药理学及分子对接技术本身具有一定的局限性,其预测的结果还需进一步的实验验证其有效性,为防治COVID-19 及药物研发提供科学依据。
