脂肪酸糖醇酯制备脂质纳米载体对姜黄素的包裹及释放性能的研究
2020-10-15金青哲王兴国
程 洋,韦 伟,金青哲,王兴国
(江南大学 食品学院,江苏省食品安全与质量控制协同创新中心,江苏 无锡 214122)
姜黄素因存在于姜黄中而得名,是目前世界上销量最大的天然食用色素之一,被世界卫生组织及美国食品药品管理局等多个组织列为准许使用的食品添加剂。除此之外,姜黄素因具有抗癌、抗炎、抗氧化等功能[1-3],被医学研究广泛关注。细胞毒性实验表明,姜黄素可以被人类安全摄入[4],但是其低水溶性[5]、易氧化、中/碱性环境下不稳定及对肠部细胞低渗透性[6]等缺陷限制了其作为生物活性物质在食品、药品领域的应用。因此,现在主要面临的挑战是保护这类具备多重功能的生物活性物质免遭不利因素的影响并增加其生理益处。
纳米载体能够有效提升药物生物活性、控制药物释放并抑制药物副作用,成为了目前医药领域研究的热点。纳米载运系统[7]被越来越多地参与危重病症的治疗,尤其是对于肿瘤、癌症这类致病机理复杂的病症,智能性纳米载体可有效抵达靶向区域,有针对性地辅助治疗。目前纳米载药材料以多聚物居多,主要包括多糖、蛋白质等,这些物质结构相对复杂,赋予纳米载药体表面更多修饰位点,以期提供更为智能的靶向载运效果。但复杂的结构也导致其合成、纯化等生产过程相对困难,尤其是对多聚物聚集程度进行有效控制是一大难题[8],除此之外,多聚物自身毒理性缺陷也成为了多聚物纳米颗粒应用受限的一大阻碍[9]。
本研究以具有高生物相容性的脂肪酸糖醇单酯为脂质纳米载体制备原料,包载疏水性模型药物姜黄素,在此过程中探究载体在包埋药物前后粒径、表面电势变化,进行形态学表征,利用体外消化系统,探索消化过程中该材料包载姜黄素的变化,同时利用体外释放实验研究脂质纳米载体的温敏性,分析其作为纳米载体在生物医药领域的应用空间。
1 材料与方法
1.1 实验材料
1.1.1 原料与试剂
月桂酸乙二醇单酯(纯度>95%)、肉豆蔻酸赤藓糖醇单酯(纯度>95%),经酶法合成、纯化得到;姜黄素(纯度97%),购自上海阿拉丁生化科技股份有限公司;胃蛋白酶、胰脂酶及胆汁盐,购自上海百灵威科技有限公司;氯化钾、磷酸二氢钾、碳酸氢钠、六水合氯化镁、氯化钠、碳酸铵、盐酸及二水合氯化钙,均购自上海国药集团试剂有限公司;实验用水通过Milli-Q系统(Millipore,MA)过滤得到。
1.1.2 仪器与设备
JY92-llN型超声波细胞粉碎机,多角度粒径与高灵敏度Zeta电位分析仪(美国布鲁克海文仪器公司),TGL-16B高速台式离心机,T-6V型可见分光光度计,FE20型pH计,S-1型水浴摇床,XW-80A型旋涡混合器,BQ 100-1A型蠕动泵驱动器。
1.2 实验方法
1.2.1 脂质纳米载体的制备
脂质纳米载体的制备在Wei等[10]的方法基础上稍作调整。将0.4 mg姜黄素与10 mg脂肪酸糖醇单酯(质量比90∶10的肉豆蔻酸赤藓糖醇单酯和月桂酸乙二醇单酯复配物)在高于脂肪酸糖醇单酯熔点5℃的温度下熔化,并加至10 mL冷水中,通过1 000 r/min磁力搅拌5 min的方式加速其在水中的分散进而初步形成水包油(O/W)型乳液。然后利用超声波细胞粉碎机在20 kHz、500 W条件下进行超声从而进一步促进分散。超声过程中每10 s暂停2 s,重复3次,共超声30 s,得到包载姜黄素的脂质纳米载体乳液。
1.2.2 粒径及表面电势测定
样品乳液的粒径和表面电势均利用多角度粒径与高灵敏度Zeta电位分析仪测定。在粒径测定模式下,将25℃、173°入射光作为测定条件,将乳液样品放入比色皿置于仪器中进行检测。在表面电势(Zeta电位)测定模式下,利用pH 7.4缓冲液进行适当的浓度调整,乳液样品被放入比色皿并插上电极置于仪器中测定。粒径及表面电势至少测定3次,结果以“平均值±标准差”表示。
1.2.3 姜黄素含量的测定
模型药物姜黄素含量的测定参考Wei[10]、Tan[11]等的方法并在此基础之上进行调整。取1 mL脂质纳米载体乳液至1.5 mL EP管中,12 000 r/min高速离心5 min以分离纳米载体。取上清液加入5 mL 二氯甲烷并旋涡振荡2 min,静置至水相与有机相完全分开,取下层包含姜黄素的有机相利用乙醇进行适当稀释,在波长422 nm下利用可见分光光度计测定吸光度,参考标准曲线(y=0.078 46x,R2=0.999 94,其中y表示吸光度,x表示姜黄素质量浓度)计算姜黄素含量。 每个样品至少测定3次,结果以平均值表示。按下式计算脂质纳米载体包载药物的包载率及姜黄素释放率。


式中:药物总量为包载药物的载体制备过程中加入的姜黄素质量,0.4 mg;剩余药物量为载体制备后乳液体系中游离的姜黄素质量,mg;药物释放量为释放过程中乳液体系中游离的姜黄素的质量,mg。
1.2.4 形态学表征
1.2.4.1 扫描电子显微镜(SEM)观察
将质量浓度为1 mg/mL、体积为5 μL的包载姜黄素的脂质纳米载体乳液滴于锡箔纸光面部分,利用双面导电胶将锡箔纸固定在托盘上,放置在真空干燥器中过夜干燥。样品镀金后利用SU8100型冷场发射扫描电子显微镜观察。观察条件:二次电子检测器加速电压5 kV,距离4~5 mm。
1.2.4.2 原子力显微镜(AFM)观察
将质量浓度为10 μg/mL的包载姜黄素的脂质纳米载体乳液滴于刚刚剥离的云母片表面,并放于空气中自然干燥过夜。利用Dimension ICON型原子力显微镜进行观察。观察条件:扫描频率1 Hz,分辨率512像素×512像素,扫描尺寸300 nm×300 nm;每个样品在不同位置进行观察以保证重复性。
1.2.5 体外释放实验
脂质纳米载体的体外释放实验参考Wei等[10]的方法,并在此基础上进行调整,实验分别在4、25、37℃及42℃下进行。将新鲜制备的7.5 mL包载姜黄素的脂质纳米载体与等体积的1%SDS溶液加入玻璃试管中,置于指定温度下的摇床中,转速设置为240 r/min,分别于15、30、60、120、240 min取样500 μL,在12 500 r/min下离心5 min,取上清液测定其中姜黄素含量,并计算释放率。
1.2.6 体外模拟消化
利用体外模拟消化实验,研究包载姜黄素的脂质纳米载体在进入消化道后的变化。体外模拟消化模型参考文献[12],并在其基础上稍作调整。根据Minekus等[13]的方法配制模拟口腔消化液(Simulated saliva fluid,SSF)、模拟胃消化液(Simulated gastric fluid,SGF)及模拟小肠消化液(Simulated intestinal fluid,SIF),具体见表1。

表1 模拟消化液的制备
1.2.6.1 口腔消化
向50 mL样品乳液中加入10 mL SSF,预热至37℃,并以100 r/min恒温搅拌10 s,以模拟口腔消化[14]。
1.2.6.2 胃部消化
将60 mL口腔消化产物(50 mL包载姜黄素的脂质纳米载体+10 mL SSF)排入预留有12 mL SGF的胃部反应容器进行消化,在消化过程中维持胃部环境pH为2,具体流速条件见表2。分别于反应5、15、30、60 min及90 min取样1 mL,对所取样品按1.2.3操作(不需分离纳米载体)测定姜黄素含量,并计算姜黄素释放率。
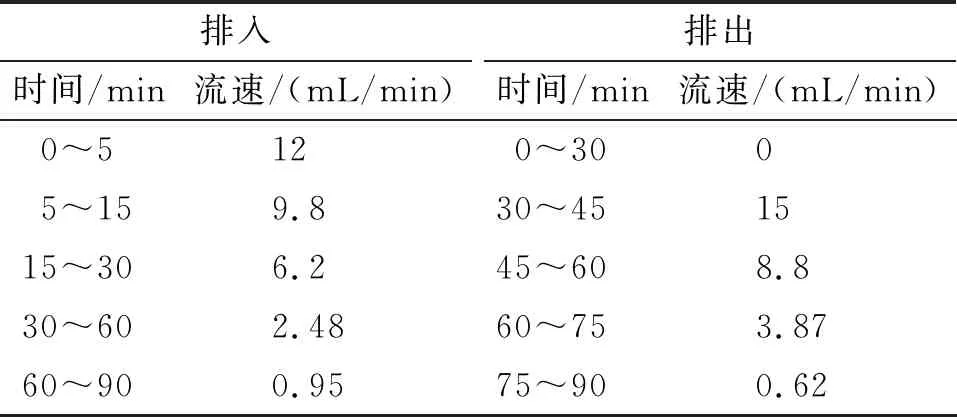
表2 胃部模拟消化过程流速控制条件
1.2.6.3 肠部消化
将200 mL胃部消化产物(乳液与SSF、SGF混合物)排入预留有36 mL SIF的肠部反应器进行进一步消化,消化过程中维持pH为7,具体肠部消化液流速条件见表3。分别于反应5、10、30、69、90 min及120 min取样1 mL,对所取样品进行姜黄素含量的测定。

表3 肠部模拟消化过程流速控制条件
1.2.7 数据统计分析
实验数据利用Origin 9和IBM SPSS Statistics 25软件进行数据处理并分析作图。以p<0.01为差异极显著,p<0.05为差异显著的判断标准。
2 结果与讨论
2.1 脂质纳米载体粒径与表面电势
将经溶解-超声法得到的空脂质纳米载体、包载姜黄素的脂质纳米载体及姜黄素溶于乙醇溶液,发现均无可见颗粒,且都均一稳定存在。空脂质纳米载体无色澄清,包载姜黄素的脂质纳米载体呈透明的淡黄色,颜色较姜黄素自身颜色浅,这一点直观证明了脂质纳米载体对于姜黄素的包载具有一定效果。
利用多角度粒经与高灵敏度Zeta电位分析仪对空脂质纳米载体和包载4%姜黄素的脂质纳米载体进行粒径及表面电势表征,结果见表4。

表4 脂质纳米载体粒径及表面电势
由表4可见,脂质纳米载体包载姜黄素后,粒径由250.63 nm增加到265.42 nm,PDI由0.29增加至0.30,Zeta电位由 -39.87 mV变为-45.44 mV,粒径大小、分布及表面电势绝对值均略微增加,并未因包载姜黄素而发生显著性变化,这表明在利用溶解-超声法制备包埋姜黄素的脂质纳米载体过程中,两种脂肪酸糖醇单酯与姜黄素相互混合均匀,并结合紧密,在水相中达到了较好的亲水亲脂性平衡。当脂肪酸糖醇单酯进入水中后,由于具备特别的两亲结构而发生自组装,使得亲水性糖醇头基端朝向外部水相,脂肪酰基端朝向内部成疏水性空间,同属疏水性的姜黄素与脂肪酰基端通过疏水力的相互作用结合填补了内部疏水性空间,进而使包载姜黄素的脂质纳米载体较原空脂质纳米载体粒径稍大。
在包载前后表面电势均呈负电,表明脂肪酸糖醇单酯的糖醇头基端对脂质纳米载体的制备产生很大影响,这一点同Wei等[10]的研究结果一致,而Zeta电位绝对值的增加表明疏水性药物与原有空脂质纳米载体的有机结合,提高了体系的稳定性。脂肪酸糖醇单酯作为脂质纳米载体包载姜黄素得到的包载率为94.60%,高于Tan等[11]包载姜黄素的研究结果,表明本研究包载结果较优,这一点同粒径和电位结果相符。
2.2 脂质纳米载体形态
利用SEM对包载4%姜黄素的脂质纳米载体进行形态学表征,结果见图1。

图1 包载姜黄素脂质纳米载体的SEM图
由图1可见,包载姜黄素脂质纳米载体为分布均匀的较小纳米颗粒(箭头处),粒径大小与分布情况同表4测定结果一致。颗粒呈圆形,具有较为光滑的表面。由于脂质自身不导电,在测试时对样品表面喷金,但喷金厚度可能在一定程度上改变样品表面形态,影响表征结果,使测定结果无法呈现样品表面原貌。因此,又采用了AFM进行观测,结果见图2。

图2 包载姜黄素脂质纳米载体的AFM图
与SEM相比,AFM前处理更方便,只需隔夜自然风干与环境达到湿度饱和,即可进行观测,无需喷金,不会对样品表面形态造成改变。同时,不仅可以提供二维图,还能够提供粒子高度的信息。由图2(a)可见,颗粒为均匀的圆形,粒径大小及分布与表4测定结果一致,这一点由3D图(图2(b))也可清晰看出。图2(c)显示了其代表性颗粒高度为7.97 nm,说明包载姜黄素的脂质纳米载体直径(265.42 nm)远大于高度,表明颗粒在云母表面以扁平的圆盘状存在。脂质纳米颗粒虽然在云母片表面结构不会发生变化,但由于与环境存在湿度差而导致内部水分蒸发,发生塌陷形成了圆盘状粒子[15]。
2.3 脂质纳米载体在体外释放过程中的变化
将包载姜黄素的脂质纳米载体分别置于4、25、37℃及42℃摇床中,研究不同温度下姜黄素释放率随时间的变化情况,结果见图3。

图3 不同温度下包载姜黄素的脂质纳米载体药物释放率
由图3可见,包载姜黄素的脂质纳米载体在4种温度环境下,释放率均呈现先快速增加后趋于平稳的趋势。其中在4℃反应体系中,姜黄素释放率在实验开始15 min后达到2.14%,之后基本不变;在25℃下,姜黄素释放率在实验开始30 min后达到29.92%,之后基本稳定;在37℃及42℃下,姜黄素释放率在开始15 min后达到96%左右,之后基本稳定。随着温度的升高姜黄素的释放率呈现升高趋势,在37、42℃下,姜黄素的释放率显著高于其他两种温度环境,且释放率达到98%以上,这证明了脂质纳米载体具备高于37℃的温度敏感性。对于37℃的敏感性被认为对生物医药领域应用十分重要[16],证明了制备的脂质纳米载体在生物医药领域具有很大的应用潜力。
2.4 脂质纳米载体在体外模拟消化过程中的变化
在本研究中,脂质纳米载体呈液态,不同于固态样品在消化初期具备咀嚼过程,且不会在口腔中长期逗留,同时结合文献[17]可知,口腔并不是脂质体主要的释放场所,原因在于其不具备特定酶活性且消化持续时间短。但这些并不能排除口腔消化液对胃肠部消化过程产生影响,因而仅进行口腔消化步骤并未取样。
通过姜黄素释放率及含量分别反映包载姜黄素的脂质纳米载体在胃部及肠部释放过程中的变化,结果见图4、图5。

图4 包载姜黄素的脂质纳米载体在胃部的药物释放率
由图4可知,包载姜黄素的脂质纳米载体进入胃部后即发生了药物释放,且释放速率较高。仅5 min姜黄素释放率就达到92.53%,随着消化过程的继续,释放率继续升高,15 min后达到97.81%,随后趋于稳定。这一点同其他包载药物的纳米载体在胃部消化过程中呈现的现象不同[18],它们往往能够保证药物在胃部以包载形式存在,但释放率较低。同样以姜黄素为包载对象,Tan等[11]以多糖为纳米载体材料研究姜黄素在消化过程中的释放情况,结果其在胃部的释放率仅为16%,这同本实验结果差异较大,主要在于本研究制备的脂质纳米载体的较高临界溶解温度(UCST)为37℃。当温度低于37℃时,载体材料脂肪酸糖醇单酯因自身相对分子质量较小且具备疏水基团而在分子内部发生缔合现象[19],因而形成不溶于水的纳米颗粒;当脂质纳米载体进入37℃的模拟环境后,脂肪酸糖醇单酯的糖醇部多羟基结构受热而展开,与水结合形成分子间氢键促使分子内发生解缔合现象,进而溶于水,致使姜黄素直接暴露,释放率升高。胃部为强酸环境,且不存在脂类水解酶,因此姜黄素能够稳定存在[20],并未发生分解。

图5 包载姜黄素的脂质纳米载体在肠部的药物含量变化
包载姜黄素的脂质纳米载体经过模拟胃部消化后进入模拟小肠继续消化。由图5可知,在进入肠道消化前姜黄素含量为98.63%,但在消化30 min后便基本分解殆尽。这一现象表明肠部是姜黄素的主要分解场所。肠部在酶种类、离子强度及pH等环境因素方面与胃部差异很大,接近中性的pH致使姜黄素无法稳定存在而分解成阿魏酸和阿魏酰甲烷[6];胰脂酶会促进水解;胆汁盐则在消化过程中辅助氧化分解[21]。
3 结 论
以质量比90∶10的肉豆蔻酸赤藓糖醇单酯和月桂酸乙二醇单酯复配物为原料,制得粒径(265.42 nm)较小、分布均匀(PDI为0.30)的包载姜黄素的脂质纳米载体,其包载效果优良,包裁率为94.60%。SEM与AFM形态学表征结果与粒径分析仪分析结果一致;体外消化实验表明,在胃部消化过程中,姜黄素释放率快速上升,15 min达到97.81%,而小肠是姜黄素的主要分解场所;体外释放实验证明了包载姜黄素的脂质纳米载体具备对37℃的温度敏感性,表明制备的包载姜黄素的脂质纳米载体在医药领域具备很大的应用空间。
