胃癌患者癌组织中赖氨酸去甲基化酶3A的表达及临床意义*
2020-10-13杜天明王向阳何承志
杜天明, 严 群, 王向阳, 何承志, 王 辉△
1华中科技大学同济医学院附属武汉中心医院胃肠外科,武汉 430014 2华中科技大学同济医学院附属同济医院胃肠外科,武汉 430030
胃癌是全球第5大常见癌症和癌症死亡的第3大主要原因[1-2]。早期胃癌无症状,晚期胃癌患者的预后较差,中位生存期约为1年[3-5]。赖氨酸去甲基化酶3A(lysine demethylase 3A,KDM3A),是含有组蛋白去甲基酶家族成员,其通过促进二甲基化组蛋白H3(H3K9me2)或单甲基化溶素-9(H3K9me1)上的组蛋白去甲基化而促进基因表达[6-7]。研究发现其可促进乳腺癌[8]、宫颈癌[9]肿瘤细胞侵袭和转移,但其在胃癌中的作用尚未见研究报道。本研究通过免疫组织化学法检测100例胃癌组织中KDM3A表达水平,分析KDM3A表达与临床病理学参数之间的关系,及KDM3A表达对胃癌患者临床结局的影响。
1 材料与方法
1.1 胃癌组织样本
本研究纳入2012年1月到2014年12月间于武汉市中心医院胃肠外科收治并行手术治疗的胃癌患者手术标本100例。纳入标准:①经胃癌切除术后,病理确诊为原发性胃癌的患者;②患者按NCCN指南原则行胃癌治疗;③除胃癌外不存在其他部位肿瘤;④病历资料完整且具有完整随访资料者。本研究经医院伦理委员会批准。
1.2 患者临床资料收集和随访
从患者病历中获取临床参数和病理资料。其中临床参数包括:年龄、性别、肿瘤部位、浸润深度、淋巴结转移等。根据国际癌症控制联盟(UICC)和美国癌症联合委员会(AJCC)胃癌肿瘤-淋巴结-转移(TNM)分期系统推荐的TNM分类系统(第8版)[10]对病理切片进行再评估。评估由2位对患者临床资料不知情的病理医生对肿瘤样本进行独立评估。随访方案如下:患者从手术后第1天开始随访,随访通过定期门诊和电话随访方式进行,每半年随访1次。无瘤生存时间为患者手术当天到随访期间肿瘤首次复发或随访截止时间之间的时间间隔。总生存时间为患者手术当天到随访期间死亡或随访截止时间之间的时间间隔。随访截止于2019年1月,共失访2人。
1.3 免疫组化检测
使用抗生物素蛋白-生物素-过氧化物酶复合物法检测胃癌组织切片中KDM3A表达情况。方法简述如下:将4 μm组织切片脱石蜡并通过二甲苯和梯度乙醇水合,用微波炉加热进行抗原修复,然后用3%H2O2在37℃阻断内源性过氧化物酶活性。采用第一抗体为KDM3A抗体(1∶300稀释),用0.01 mol/L PBS代替一抗处理病理切片作为阴性对照。KDM3A抗体购自Abcam公司(Cambridge,UK)。将切片与过氧化物酶缀合的二抗一起温育。组织切片用苏木精复染,然后在显微镜下观察。
1.4 免疫组化评分和患者分组
本研究对胃癌组织病理切片中免疫组化结果进行半定量评分。胃癌组织中KDM3A表达水平免疫组化评分标准:染色强度评分:0分=无染色,1分=弱染色,2分=中等染色,3分=强染色;染色细胞百分比评分:0分=细胞无染色,1分=1/3以下细胞染色,2分=1/3至2/3细胞染色,3分=2/3以上细胞染色。病理标本最终评分结果为染色强度和染色细胞百分比评分的乘积。根据免疫组化结果将患者分为两组:总评分为0~未满3分为KDM3A低表达组;总评分为3~9分为KDM3A高表达组。
1.5 统计学方法
用GraphPad Prism(GraphPad,San Diego,CA,USA)进行统计学分析,卡方检验和Fisher精确概率法检验用于评估KDM3A表达与胃癌临床病理特征之间的关系。使用Log-rank检验评估KDM3A高低表达两组患者无瘤生存率和总生存率差异。以P<0.05为差异有统计学意义。
2 结果
2.1 胃癌组织中KDM3A的表达
免疫组化检测结果显示KDM3A主要定位于胃癌细胞的细胞核及胞质内。全部患者中,KDM3A高表达组有58例(58.0%),KDM3A低表达组有42例(42.0%),KDM3A在胃癌组织中代表性免疫组化染色结果见图1。

A:KDM3A低表达;B:KDM3A高表达图1 免疫组化检测显示胃癌癌组织中KDM3A的表达(苏木精染色,×200)Fig.1 Immunohistochemical staining of KDM3A expression in gastric cancer tissues(Hematoxylin staining,×200)
2.2 胃癌组织中KDM3A表达与临床病理参数间的关系
KDM3A的表达与患者性别、年龄、分化程度、静脉浸润和淋巴管浸润及T分类无统计学相关性(均P>0.05),KDM3A表达与胃癌患者TNM分期(P=0.006)和N分类显著相关(P=0.010),见表1。
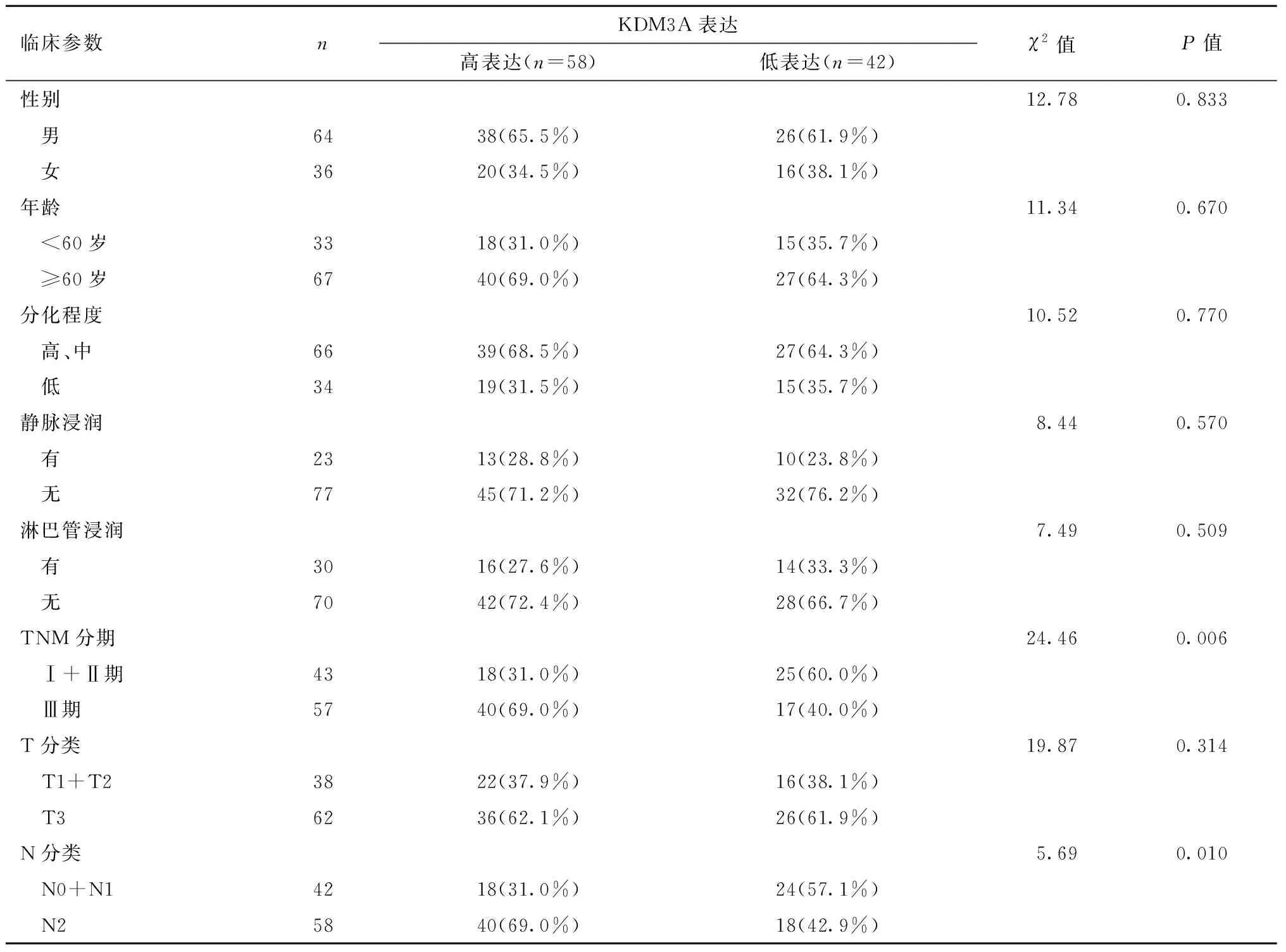
表1 KDM3A的表达与胃癌患者的临床病理学参数之间的相关性Table 1 Correlation between the expression of KDM3A and clinicopathological parameters in patients with gastric cancer
2.3 KDM3A表达与胃癌患者无瘤生存率和总生存率的关系
Kaplan-Meier生存曲线显示KDM3A高表达组患者5年无瘤生存率为18.7%,KDM3A低表达组5年无瘤生存率为28.5%,KDM3A高表达组患者5年无瘤生存率低于KDM3A低表达组,P=0.009,见图2A;KDM3A高表达组患者5年总生存率为21.4%,KDM3A低表达组5年总生存率为33.2%,KDM3A高表达组患者5年总生存率低于KDM3A低表达组,P=0.003,见图2B。

图2 KDM3A高低表达组患者无瘤生存率(A)和总生存率(B)曲线比较Fig.2 Comparison of tumor-free survival rate(A)and overall survival rate (B)in patients with gastric cancer with high and low KDM3A expression
2.4 影响胃癌患者无瘤生存率的单因素和多因素分析
Cox比例风险模型中单因素分析结果显示:TNM分期、T分类、N分类和KDM3A表达是影响胃癌患者无瘤生存率的危险因素(均P<0.05);多因素分析显示TNM分期(P=0.010)及KDM3A表达(P=0.037)是胃癌患者无瘤生存率的独立危险因素,见表2。
2.5 影响胃癌患者总生存率的单因素和多因素分析
Cox比例风险模型中单因素分析结果显示:TNM分期、N分类、组织学分化和KDM3A表达是影响胃癌患者总生存率的危险因素;多因素分析显示组织学分化(P=0.038)及KDM3A表达(P=0.002)是影响胃癌患者总生存率的独立危险因素。见表3。

表2 患者术后无瘤生存率的单因素和多因素分析Table 2 Univariate and multivariate cox regression analyses for overall survival in gastric cancer patients

表3 患者总生存率的单因素和多因素分析Table 3 Univariate and multivariate cox regression analyses for overall survival in gastriccancer patients
3 讨论
胃癌是消化道最常见的肿瘤,发病率高,居我国各种恶性肿瘤发病率的首位,近年来随着饮食结构的改变、工作压力增大及幽门螺杆菌的感染等原因,我国胃癌呈现年轻化倾向[11]。多种因素影响胃癌的预后,鉴定与胃癌预后相关分子标志物对了解胃癌发病机制和制定治疗策略尤为重要[12]。
KDM3A是组蛋白H3赖氨酸9脱甲基酶,体外实验发现其可促进肿瘤增殖、转移和肿瘤的耐药性[13-14]。KDM3A在乳腺癌[8]、宫颈癌[9]、肺癌[15]和卵巢癌[16]中表达,且癌组织中表达增加,而在鼻咽癌中其表达水平较邻近非癌组织表达下调[17]。目前尚未见报道胃癌中KDM3A表达水平和临床意义。
本研究免疫组化检测结果显示KDM3A主要定位于胃癌细胞的细胞核及胞质中。研究结果与宫颈癌[9]结果类似,在80例宫颈癌患者中发现KDM3A高表达46例,低表达34例,且KDM3A主要定位于宫颈癌细胞的细胞核中。KDM3A高表达与患者TNM分期和N分类相关,文献报道[9]KDM3A过表达与宫颈癌患者的淋巴结转移和晚期FIGO分期有关。KDM3A过表达是口腔和口咽鳞状细胞癌患者淋巴结转移和晚期肿瘤分期的危险标志[18]。KDM3A表达与乳腺癌[8]临床病理特征之间没有统计学关联。提示KDM3A表达及在肿瘤中的作用和意义因肿瘤类型而异。
进一步行生存分析发现,KDM3A高表达组患者无瘤生存率和总生存率均显著低于KDM3A低表达组患者。已发现KDM3A高表达与宫颈癌[9]、口咽鳞状细胞癌[18]不良临床结果密切相关。本研究通过Cox比例风险回归分析,KDM3A表达水平是影响胃癌患者无瘤生存率和总生存率独立的危险因素。
本研究结果显示,KDM3A表达与胃癌患者预后密切相关且为预测胃癌预后新的分子标志物。尽管如此,KDM3A表达如何影响胃癌预后的分子机制尚不清楚。综合文献分析KDM3A影响肿瘤预后可能存在如下3种潜在机制:首先,在结直肠癌中[19],研究报道KDM3A表达可能促进结直肠癌细胞迁移和侵袭能力,其机制可能与KDM3A表达影响癌细胞上皮间质转化和基质金属蛋白酶代谢有关。其次,在尤文氏肉瘤[20]中,KDM3A基因启动子受到microRNA-22调节,且KDM3A酶蛋白在尤文氏肉瘤组织中表达水平高于正常组织,体外实验中发现KDM3A高表达与癌细胞高侵袭和转移能力密切相关。最后,最近研究发现,体外的宫颈癌细胞实验中发现KDM3A可调节JAK2/STAT3信号通路而促进肿瘤发生和侵袭能力[21];而在胃癌细胞体外实验中发现JAK2/STAT3信号是胃癌发生和进展一个重要分子调节机制,采用miRNA干扰JAK2/STAT3信号通路可抑制胃癌增殖和侵袭[22]。尽管如此,本研究并未探知KDM3A表达影响胃癌预后的潜在机制,尚需要进一步研究。
本研究存在如下不足:由于是单中心回顾性研究,需要多中心前瞻性大样本研究来证实本结论,KDM3A表达影响胃癌进展的分子机制尚需要进一步探讨。
总之,本研究发现KDM3A表达与胃癌患者TNM分期和N分类密切相关,是影响胃癌患者无瘤生存率和总生存率的独立危险因素,其可能是判断胃癌患者预后新的重要生物标志物。
