用t-BAMBP从锂云母沉锂废液中萃取碱金属
2020-10-12汪金良季柏仁
汪金良,季柏仁
(1.江西理工大学 材料冶金化学学部,江西 赣州 341000;2.江西省闪速绿色开发与循环利用重点实验室,江西 赣州 341000)
铷和铯在许多领域有着重要用途[1-5]。当前,主要从花岗伟晶岩中提取铷和铯,主要工业矿物有锂云母和铯榴石。江西宜春锂云母矿中含有丰富的铷和铯[6-7],这些铷和铯在提取锂过程中被富集到沉锂废液中。
从溶液中提取铷、铯,主要有沉淀法、离子交换法和溶剂萃取法。沉淀法较为成熟,主要采用四苯硼钠法[8]、亚铁氰化锌法[9]等进行复盐沉淀,但流程冗长、分离效果差、产品纯度不高、收率低、生产成本高。离子交换法用的较少,因为离子交换剂的交换容量小、溶液浓度低,且分离效果相对较差[10-11]。溶剂萃取法研究较多,应用较广[12-13],其中,酚醇类4-叔丁基-2-(α-甲苄基)酚(t-BAMBP)萃取剂,具有选择性强、反应迅速、易于反萃取、毒性小、价格较便宜等优点,得到较为广泛认可[14-16]。
用t-BAMBP从溶液中萃取铷、铯的研究已有相关报道,但从高钾钠溶液中分离萃取铷和铯的研究尚未见有报道。试验研究了用t-BAMBP+磺化煤油体系从锂云母沉锂废液中萃取分离铷和铯,为实现锂云母资源的综合利用提供参考信息。
1 试验部分
1.1 试验原料与试剂
试验所用沉锂废液取自宜春某碳酸锂企业,为锂云母经硫酸盐焙烧—浸出—净化—沉淀等工序提取碳酸锂后的沉锂废液,pH=7.8,主要成分见表1。
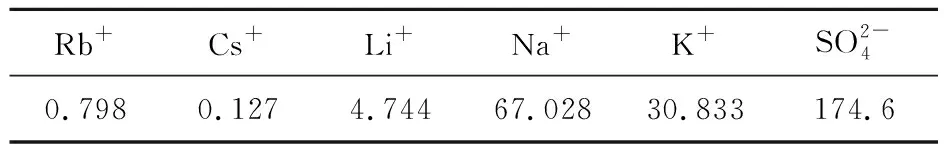
表1 锂云母沉锂废液的主要成分 g/L
试验所用试剂:t-BAMBP,磺化煤油,氢氧化钠,盐酸,均为分析纯。试验用水为重庆阿修罗公司AXLB1020-1型纯水机制备的去离子水。
1.2 试验原理与方法
碱性条件下,t-BAMBP酚羟基上的酸性质子H+容易发生解离,解离后的质子H+与废液中的碱金属离子(以M+表示)发生交换反应,生成疏水性极强的酚盐而进入有机相。反应式为
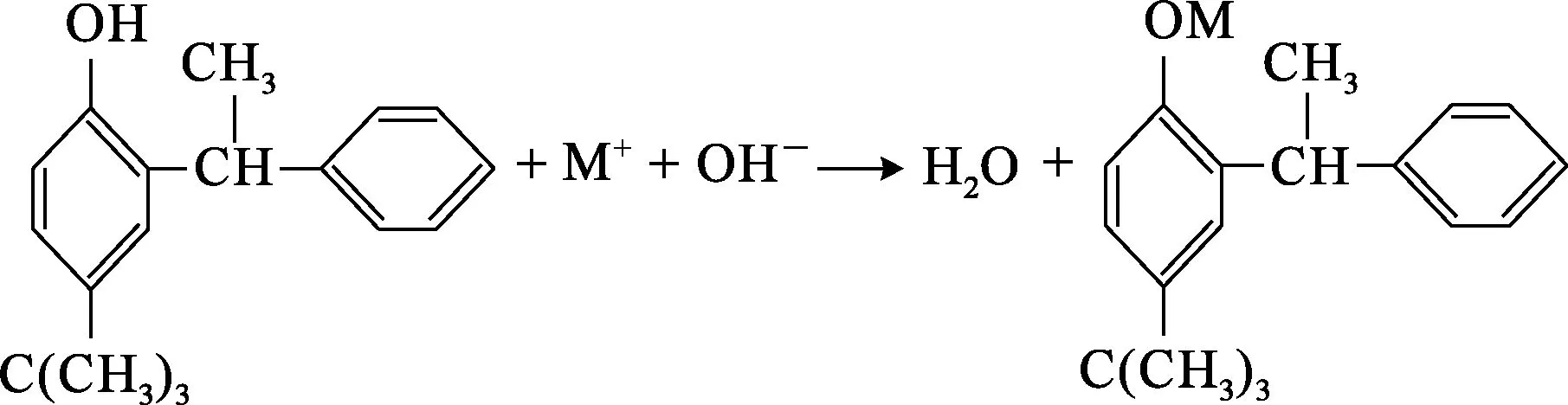
t-BAMBP为黏稠状有机物,可用磺化煤油稀释[17]。
t-BAMBP萃取剂对碱金属离子的萃取能力随碱金属离子半径增大而递增,即Cs+>Rb+>K+>Na+>Li+[18]。
用氢氧化钠溶液将含碱金属元素废液调至一定碱度。准确移取一定体积废液和有机相至125 mL梨形分液漏斗中,并置于恒温振荡器(SHZ-88型,常州金坛市万华实验仪器厂)中,控制一定温度,反应一定时间后,静置、分层;定量移取一定萃余液,用原子吸收光谱仪(TAS990型,北京普析通用仪器有限责任公司)测定碱金属质量浓度,用差量法计算有机相中对应碱金属质量浓度,计算相应萃取率、分配比D和分离系数β。
2 试验结果与讨论
2.1 萃取剂质量浓度对碱金属萃取率的影响
在pH=14.0、萃取相比Vo/Va=1.0、振荡速度200r/min、温度25 ℃、萃取时间5.0 min条件下,萃取剂t-BAMBP质量浓度对碱金属萃取率的影响试验结果如图1所示。

—■—Rb+;—●—Cs+;—▲—Li+;—▼—Na+;—◆—K+。图1 t-BAMBP质量浓度对碱金属萃取率的影响
由图1看出:t-BAMBP质量浓度对碱金属萃取率影响较大,随t-BAMBP质量浓度升高,各碱金属萃取率均升高;t-BAMBP对碱金属的萃取顺序为Cs+>Rb+>K+>Li+>Na+。Na+半径比Li+的大,Na+萃取率本应高于Li+萃取率,但因体系中Na+质量浓度(90.03 g/L)远高于Li+质量浓度(4.75 g/L),从而使Li+萃取率反而高于Na+萃取率;t-BAMBP质量浓度提高到0.5 g/mL时,Cs+萃取率达98.43%,Rb+萃取率达63.14%。继续升高t-BAMBP质量浓度,Rb+萃取率提高幅度不大,而其他元素萃取率仍在提高,尤其是K+萃取率升高明显,这将造成后续铷、铯分离困难;另外,萃取剂质量浓度太高会降低萃取体系的流动性,造成分层困难。综合考虑,确定萃取剂质量浓度以0.5 g/mL为宜。
2.2 废液碱度对碱金属萃取率的影响
在萃取剂质量浓度0.5 g/mL、萃取相比Vo/Va=1.0、振荡速度200 r/min、温度为25 ℃、萃取时间5.0 min条件下,废液碱度对碱金属萃取率的影响试验结果如图2所示。
由图2看出:碱金属萃取率与废液碱度(pH)呈正相关,pH越高,金属萃取率越大,但pH过高,两相乳化现象加重,从而导致分层时间大大延长;当pH提高到14.0时,Cs+萃取率达98.43%,Rb+萃取率达63.14%;继续升高废液pH,Cs+和Rb+萃取率均提高不明显,而其他碱金属的萃取率都有所提高。t-BAMBP酚羟基上的酸性质子H+在碱性条件下易发生解离,解离后的质子H+与溶液中的碱金属离子发生交换反应,生成疏水性极强的酚盐而进入有机相,而碱金属离子与H+之间的交换能力不同,故而可实现元素间的分离。综合考虑,确定废液pH以14.0为好。
2.3 萃取相比对碱金属萃取率的影响
在萃取剂质量浓度0.5 g/mL、废液pH=14.0、振荡速度200 r/min、温度25 ℃、萃取时间5.0 min 条件下,萃取相比Vo/Va对碱金属萃取率的影响试验结果如图3所示。

—■—Rb+;—●—Cs+;—▲—Li+;—▼—Na+;—◆—K+。图3 萃取相比对碱金属萃取率的影响
由图3看出,碱金属萃取率与Vo/Va正相关。萃取剂对碱金属有一定饱和容量,即相比Vo/Va越大,萃取的碱金属越多;随Vo/Va增大,各碱金属萃取率均有所提高,Vo/Va增至1.0时,Cs+萃取率为98.43%,Rb+萃取率为63.14%;继续增大Vo/Va,Rb+和Cs+萃取率虽略有升高,但生产成本也会相应增加。综合考虑,确定相比Vo/Va以1.0为好。
2.4 振荡速度对碱金属萃取率的影响
在萃取剂质量浓度5 g/mL、废液pH=14.0、 萃取相比Vo/Va=1.0、温度25 ℃、萃取时间5.0 min条件下,振荡速度对碱金属萃取率的影响试验结果如图4所示。

—■—Rb+;—●—Cs+;—▲—Li+;—▼—Na+;—◆—K+。图4 振荡速度对碱金属萃取率的影响
由图4看出,振荡速度对碱金属萃取率影响不大。试验中发现,振荡速度较高时,两相分相时间大大延长,且出现轻微乳化现象。综合考虑,确定振荡速度以200 r/min为宜。
2.5 温度对碱金属萃取率的影响
在萃取剂质量浓度0.5 g/mL、废液pH=14.0、萃取相比Vo/Va=1.0、萃取时间5.0 min条件下,温度对碱金属萃取率的影响试验结果如图5所示。
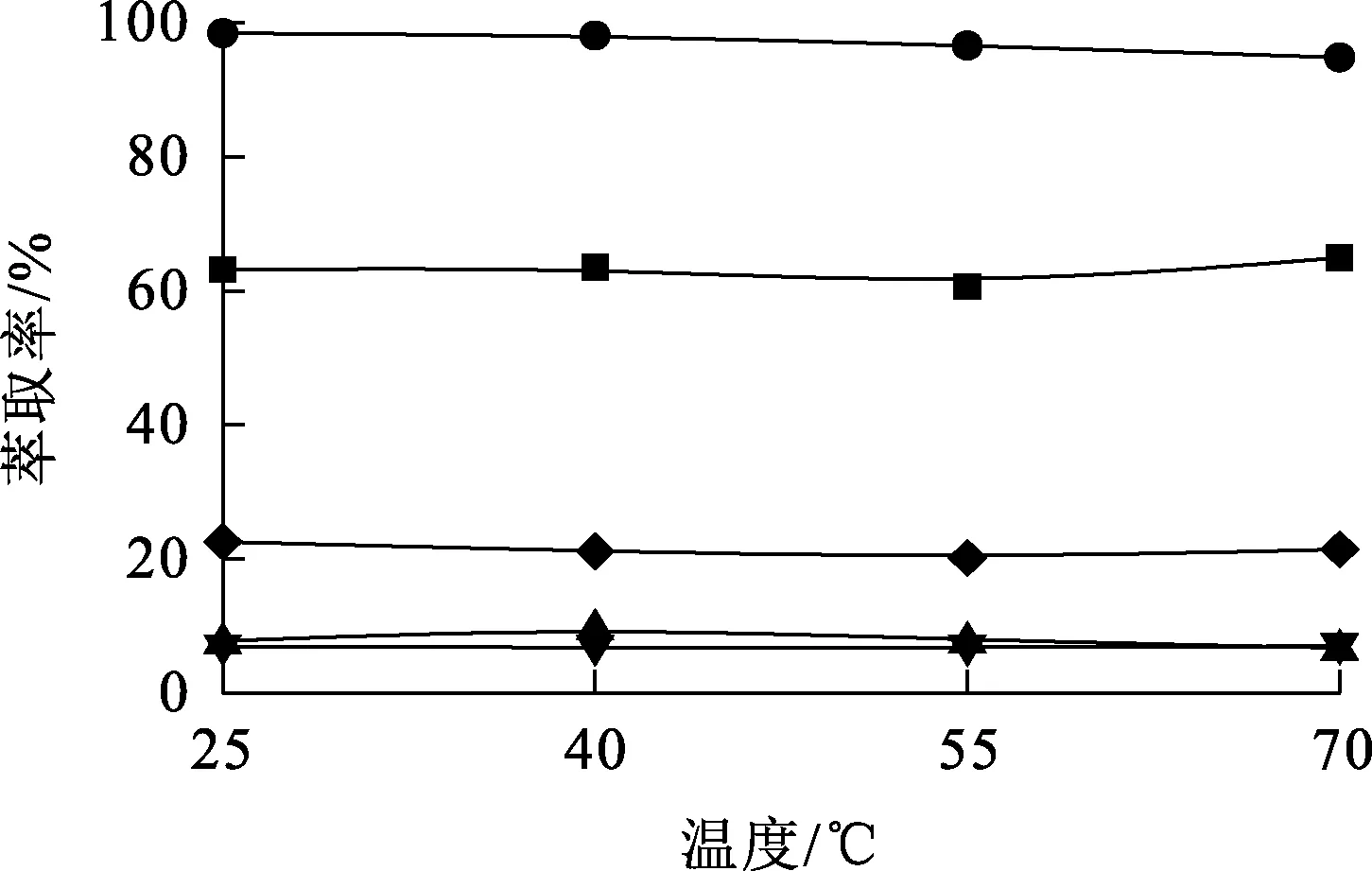
—■—Rb+;—●—Cs+;—▲—Li+;—▼—Na+;—◆—K+。图5 温度对碱金属萃取率的影响
由图5看出,温度对碱金属萃取率影响不大,随温度升高,碱金属萃取率略有下降,但变化不大。这是由于t-BAMBP萃取碱金属的过程放热,温度升高不利于萃取。综合考虑,确定在常温(25 ℃)下萃取最佳。
2.6 萃取时间对碱金属萃取率的影响
在萃取剂质量浓度0.5 g/mL、废液pH=14.0、萃取相比Vo/Va=1.0、振荡速度200 r/min、温度25 ℃条件下,萃取时间对碱金属萃取率的影响试验结果如图6所示。

—■—Rb+;—●—Cs+;—▲—Li+;—▼—Na+;—◆—K+。图6 萃取时间对碱金属萃取率的影响
由图6看出,t-BAMBP萃取碱金属离子的反应速度很快,5.0 min即达萃取平衡。
2.7 优化条件下的萃取
根据单因素试验结果,用t-BAMBP+磺化煤油体系从沉锂废液中萃取碱金属。试验条件:t-BAMBP质量浓度0.5 g/mL,废液pH=14.0、萃取相比Vo/Va=1.0、振荡速度200 r/min,温度25 ℃, 萃取时间5.0 min。试验结果如图7、8所示,萃取后水相和有机相化学组成见表2,pH约为14.0。

图7 优化条件下的碱金属的分配比
由图7看出:Cs+的分配比最大,其次是Rb+,均大于1;而Li+、Na+、K+的分配比均小于1。这表明,采用t-BAMBP+磺化煤油萃取体系可有效分离废液中的Cs+、Rb+与K+、Li+、Na+。
由图8、表2看出:碱金属离子之间的分离系数大小为β(Cs+/Rb+)≫β(Rb+/Na+)>β(Rb+/Li+)>β(Rb+/K+)>β(K+/Li+)>β(Li+/Na+)>1。其中β(Cs+/Rb+)最大,这表明:采用t-BAMBP+磺化煤油体系进行萃取,可将Rb+和Cs+有效分离;萃取后,废液中的Cs+几乎全部进入有机相,Rb+大部分进入有机相,而Li+、Na+和K+大部分留在水相。但由于废液中Na+、K+含量高,虽只有少量进入有机相,但其在有机相中的含量仍远高于Rb+和Cs+。因此,须经过多级逆流萃取进一步分离。
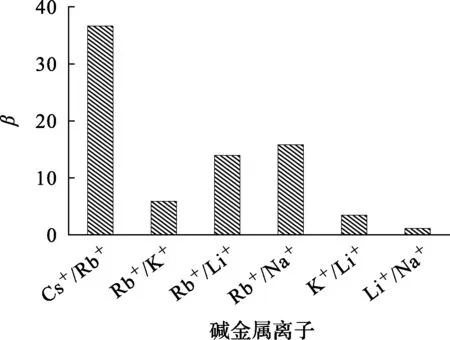
图8 优化条件下碱金属之间的分离系数

表2 单级萃取平衡后水相和有机相的化学组成
3 结论
针对高钾钠锂云母沉锂废液,用t-BAMBP+磺化煤油体系进行萃取,可以将溶液中Cs+、Rb+与K+、Li+、Na+分离;t-BAMBP萃取碱金属的顺序为Cs+>Rb+>K+>Li+>Na+,碱金属间的分离系数大小为β(Cs+/Rb+)≫β(Rb+/Na+)>β(Rb+/Li+)>β(Rb+/K+)>β(K+/Li+)>β(Li+/Na+)>1,该体系对Cs+、Rb+有很强的萃取分离能力。
在萃取剂质量浓度0.5 g/mL、废液pH=14.0、 萃取相比Vo/Va=1.0、振荡速度200 r/min、温度20 ℃、萃取时间5.0 min最佳条件下,Cs+、Rb+、Li+、Na+和K+萃取率分别为98.43%、63.14%、 7.77%、6.89%和22.58%。
溶液中存在大量K+和Na+,对Rb+、Cs+的分离有较大影响,应采取多级逆流萃取方式提高Rb+、Cs+的富集度和分离程度。
