超高效液相色谱-质谱法测定卤肉制品中四环素类药物残留及分析
2020-10-10黄代文
陈 艳 黄代文
乐山市产品质量监督检验所 四川乐山 614000
四环素类抗生素药物包括四环素、土霉素、金霉素和强力霉素,它是由放线菌产生的一类广谱性抗生素,是我国应用时间最长、应用范围最广的动物抗生素[1,2],四环素类药物广泛的应用于兽药和饲料添加剂方面[3],它可以较强的抑制多种病原菌,可用于大范围的畜禽疾病的预防与治疗[4]。由于食品中残留的四环素类抗生素可破坏人体正常的肠道菌群平衡[5],另外还具有溶血或肝毒作用,对胃肠、肝脏的损害较大[6],更严重的是四环素类抗生素具有致突变性和潜在的致癌性[7,8]。
液相色谱-质谱联用法(LC-MS/MS)将色谱法对复杂组分的高分离能力与质谱法具有高选择性、高灵敏度及能够提供相对分子质量与结构信息的优点结合起来,使用质谱作为检测器,对化学组分进行定量和定性分析,在食品、环境、医学等许多分析分离的领域得到了广泛的应用[9]。
LC-MS/MS检测灵敏度高、前处理简单、定性定量准确,近年来已成为食品药品以及农产品中痕量药物残留分析的关键技术[10~15]。而超高效液相色谱-串联技术(UPLC-MS/MS)相比较传统的LC-MS/MS,检测的灵敏度、准确性和重复性均有显著的提高,检测时间缩短,适用于兽药多残留的快速检测[16]。
本论文采集了乐山市及周边地区市售的不同品种卤肉制品,在GB/T 21317-2007《动物源食品中四环素类兽药残留检测方法》[17]的基础上,对样品提取方式、提取液的选择、流动相的选择、固相萃取柱和色谱柱的选择进行了研究及讨论,建立一套灵敏度高、检测准确的分析方法,实现对市售卤肉制品中的四环素类药物同时提取和检测,并对乐山市及周边地区市场上卤肉制品中的四环素类抗生素进行了检测和质量安全评价分析。
1 材料与方法
1.1 仪器与试剂
Waters超高效液相色谱一四极杆串联质谱仪(I-Class&Xevo,TQD),配有电喷雾离子源(ESI)和Masslynx 4.0工作站、Waters Oasis HLB固相萃取柱(200mg/6mL),购自美国Waters公司;
OA-SYS氮吹仪购自Organomation Associates,Jnc;
电子分析天平(TLE204/02),购自瑞典梅特勒托利多公司;
湘仪H1850医用离心机,购自长沙高新技术开发区湘仪离心机仪器有限公司;
四环素、土霉素、金霉素和强力霉素标准品(纯度均大于99.0%),购自德国Dr.Ehrenstotfer;
甲醇、乙腈(色谱纯),购自美国Fisher公司;
柠檬酸、磷酸二氢钠二水化合物、乙二胺四乙酸二钠、盐酸、氢氧化钠(分析纯),购自成都科隆化学品有限公司。
试验用水为经UP净化系统0.22μm过滤膜过滤的纯化水。
1.2 标准溶液的配制
1.2.1 EDTA-Mcllvaine缓冲液
称取11.8g柠檬酸-水合物、13.72g磷酸氢二钠二水合物、33.62g乙二胺四乙酸二钠(EDTA-2Na))溶解于1L水中,用稀盐酸及氢氧化钠调pH值至4.1,用作四环素类抗生素提取液。
1.2.2 标准储备液
将四环素、土霉素、金霉素和强力霉素标准品用甲醇配制成100μg/mL的标准储备液,在-18℃避光保存。
1.2.3 工作液
将上述标准储备液用流动相稀释成0.1、0.5、1.0、2.5、5.0、10.0μg/mL的系列标准溶液,现配现用。
1.2.4 流动相的配制
0.1%甲酸水,0.50mL甲酸(色谱纯)加入500mL经过0.22μm过滤膜过滤的纯水中,现配现用。
1.3 样品前处理
1.3.1 样品处理
准确称取经组织粉碎机粉碎的样品5g(精确到0.001g)于50mL塑料离心管中,加入20mL EDTA-Mellvaine缓冲溶液,涡旋振荡混合1min,超声提取20min,6 000r/min离心5min,经滤纸过滤后收集上清液于离心管中。残渣再加入20mL EDTA-Mellvaine缓冲溶液,重复提取一次,合并提取液。用6mL甲醇、6mL水活化HLB固相萃取柱,取10mL样品提取液过固相萃取柱,控制流速为1滴/s左右,再用5mL水和5mL甲醇洗涤小柱,抽干,用10mL甲醇+乙酸乙酯(1+9)溶液洗脱,收集洗脱液,旋蒸发至干后,用1mL 0.1%甲酸-水溶液溶解残渣,经0.22μm水相滤膜过滤后,进行LC-MS/MS分析。采用阴性样品基质加标外标法定量计算。
1.3.2 空白基质标准曲线制备
称取与待测样品基质相同或相近的空白样品,分别加入一定量的混合标准工作液,按1.3.1处理,制成一定浓度的空白基质混合标准曲线溶液,绘制空白基质标准曲线。
1.4 色谱条件
1.4.1 液相色谱条件
Waters ACQUITY-UPLCTM BEH C18色谱柱(100mmx2.1mm,1.7μm)。
流动相:乙腈(B)—0.1%甲酸水溶液(A)。
流速:0.4mL/min。
进样体积:5μL。
柱温:40℃。
按照表1进行梯度洗脱。

表1 梯度洗脱程序
1.4.2 质谱条件
离子源:电喷雾电离(ESI),正离子模式。
毛细管电压:4.5kV。
萃取电压:3V。
离子源温度:150℃。
脱溶剂气温度:500℃。
脱溶剂气流量:650L/h。
碰撞气为氩气,采用多反应监测(MRM)模式,质谱参数见表2。

表2 质谱条件
2 结果与讨论
2.1 样品提取方式的选择
实验中对样品常用的提取方式分别作出了比较。将样品匀浆制备后加入标准品,分别采取静置提取、振荡提取和超声波提取三种提取方式,提取相同时间后进行检测。实验结果表明:采用三种提取方式分别提取时,超声波提取的回收率最高,振荡提取第二,静置提取的回收率最低;其原因在于静置提取和振荡提取时,由于溶剂介质分子活性较低,对样品的渗透不充分,因此降低了提取效果;而采用超声波提取样品时,由于超声波具有机械效应、热效应和空化效应,可以增强介质穿透力、加快介质分子运动速度,使得目标物的溶出加快,从而使提取效率提高[18,19]。因此,在实验中均选取超声波提取作为目标物的提取方式。
2.2 样品提取液的选择
样品提取方式参考GB/T 21317-2007《动物源食品中四环素类兽药残留检测方法》,考察了分别使用纯水、EDTA-Mcllvaine缓冲液、5%高氯酸溶液[20]、乙腈四种提取溶剂,提取溶液对四环素类药物回收率的影响如图1所示。由于四环素类药物容易发生降解,并且可以结合蛋白质形成不溶性络合物,在碱性条件下则容易生成同分异构体;而这类药物在弱酸性溶液中则比较稳定,所以在实验中应该选择含金属络合剂的弱酸性提取液。实验结果表明:EDTA-Mcllvaine缓冲液有利于药物在HLB固相萃取小柱上保留,并且可以减少四环素类药物与金属离子的螯合反应[21],从而提高提取效率,提取效果最好。因此在实际实验过程中,均采用EDTA-Mcllvaine溶液进行样品的前处理提取[22]。

图1 提取溶液对4种四环素类平均回收率的影响
2.3 固相萃取条件的选择
实验比较了常用的中性氧化铝小柱、PEP固相萃取柱、Oasis HLB小柱以及C18小柱等固相萃取柱对四种四环素类药物的净化效果。Oasis HLB柱是一种新型的亲水亲脂平衡柱,广泛应用于食品中兽药残留的前处理,如动物源性食品中四环素类、氯霉素类、硝基呋喃类、喹诺酮类兽药残留的前处理。它具有良好的水可浸润性和化学稳定性,表面同时具有亲水性和疏水性官能团,从而对各类极性、非极性化合物具有均衡的吸附作用。其吸附能力大,样品容量高,对大部分有机物的吸附容量增大,回收率也更高,且在吸附后有机物容易被定量洗脱。实验结果表明:HLB柱利用非极性相互作用将四环类抗生素保留在柱上,能有效去除极性较大的杂质,相对保留容量较传统C18柱高,吸附性较强,对基质的净化效果较好,目标物受杂质的干扰较小,可保留更多的分析物,提高固相提取方法的回收率。所以实验选择Oasis HLB小柱作为样品提取溶液的净化和富集柱。
本实验选用了甲醇-乙酸乙酯混合液作为洗脱剂[23],试验比较了不同洗脱液体积比,分别采用V(甲醇)∶V(乙酸乙酯)=5∶95、10∶90、20∶80、30∶70,对提取后的基质加标样品进行洗脱并测定,通过比较回收率,最终确定V(甲醇)∶V(乙酸乙酯)=10∶90作为洗脱液比例。
2.4 流动相的选择
实验比较了甲醇—水、甲醇—0.1%甲酸水、甲醇—乙腈—0.1%甲酸水[25]和乙腈—20mmol/L草酸[25]作为流动相进行梯度洗脱。实验结果表明:流动相中未加入0.1%甲酸的情况下,四环素类药物的电离效果较差,峰型对称性差,加入一定比例的0.1%甲酸后,增加离子化效率,改善了峰形利于分析。
2.5 色谱柱的选择
实验考查了不同色谱柱在四环素药物分离上的效果,包括Waters ACQUITY BEH C18柱(100mm×2.1mm,1.7μm)和Waters Atalantis T3(150mm×2.1mm,3μm)色谱柱[26~28]。实验结果表明:C18柱在本次实验研究中无论从分离效果和峰形均优于T3柱,因此在实验中选择使用C18柱作为色谱分离柱。
通过以上各种条件优化,实验最终采用EDTA-Mcllvaine缓冲液超声提取,Oasis HLB小柱净化,甲醇—乙酸乙酯混合液(10∶90)洗脱,乙腈—0.1%甲酸水作为流动相梯度洗脱,选用Waters ACQUITY BEH C18色谱柱(100mm×2.1mm,1.7μm),测得四环素、土霉素、金霉素和强力霉素总离子流图,如图2所示。

图2 4种化合物总离子流图(1.0μg/mL)PHam
2.6 标准曲线
四种化合物标准溶液线性关系见表3。

表3 四种化合物标准溶液线性关系
浓度分别为0.1、0.25、0.5、1.0、2.5、5.0、10.0μg/mL的空内基质标准溶液,分别以四环素、土霉素和金霉素峰面积为纵坐标,质量浓度为横坐标绘制标准曲线,其回归方程及相关系数见表3,相关系数均大于0.99,线性关系良好。
2.7 回收率和精密度实验
选择卤牛肉、卤猪肉、卤爪翅、卤鸭四种样品,在空白基质中加入50、100、200μg/kg三个浓度添加水平,进行加标回收实验,每个水平重复测定6次,四环素、土霉素、金霉素、强力霉素平均回收率分别为81.8%~103.7%、78.5%~99.4%、78.2%~101.6%、76.7%~97.1%,平均相对偏差分别为3.2%、1.9%、4.6%、3.3%(n=6),结果见表4。

表4 回收率及精密度实验结果(n=6)
3 样品测定及质量安全分析
采用本实验方法,采集了乐山及周边地区市售的220份卤肉制品,对其进行四环素类药物残留量的测定,以及对测定结果进行质量安全性分析。
实验结果表明:乐山及周边地区卤肉制品中四环素类药物残留均符合国家标准,220份样品中,四环素类检出9份,其中四环素3份,强力霉素5份,土霉素1份,检出值最大为33.8μg/kg,总检出率4.1%;检出值均符合中华人民共和国农业部公告第235号[29]、GB 31650-2019《食品安全国家标准食品中兽药最大残留限量》[30]中规定的含量要求,无超标产品。具体检测分析结果见表5。
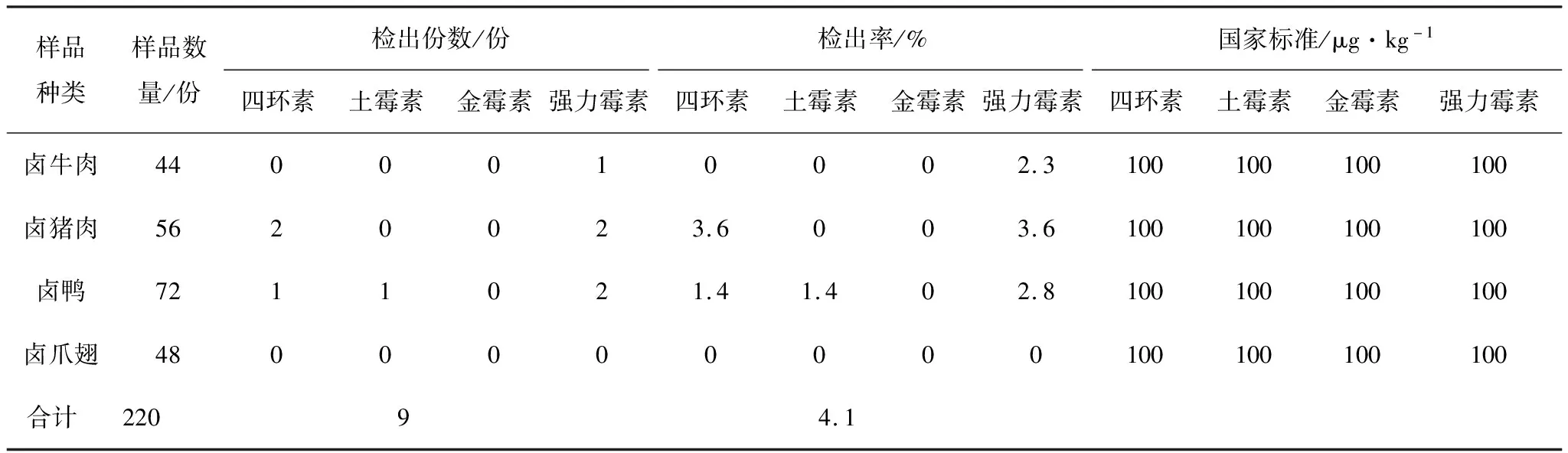
表5 卤肉制品中四环素类药物残留检测情况
4 结论
本次实验建立一种超高效液相色谱-串联质谱(UPLC-MS/MS)检测卤肉制品中的四环素类药物残留的方法。通过优化样品、提取方式、提取条件和仪器条件,确立了卤肉制品四环素、金霉素、土霉素抗生素残留的UPLC-MS/MS分析方法。四环素、土霉素、金霉素、强力霉素在0.1~10μg/mL浓度范围内具有良好的线性关系(r2>0.99)。在50、100、200μg/kg三个浓度添加水平,四环素、土霉素、金霉素、强力霉素平均回收率分别为81.8%~103.7%、78.5%~99.4%、78.2%~101.6%、76.7%~97.1%,平均相对偏差分别为3.2%、1.9%、4.6%、3.3%(n=6);该方法准确、快速、灵敏度高、重复性好、线性范围宽、适用范围广,能够准确、快速、有效地进行卤肉制品中四环素、土霉素、金霉素、强力霉素的残留检测分析。另外,本次实验对乐山及周边地区卤肉制品四环素类药物残留进行了检测,并进行了食品质量安全性分析,检测结果均符合国家标准要求。
