高效液相色谱-四极杆-飞行时间质谱法快速筛查保健食品中10种雄性激素类非法添加物
2020-09-29张虹艳邱国玉石晓峰王行智王小乔许晓辉李晨曦潘秀丽
张虹艳,邱国玉,石晓峰,2*,王行智,王小乔,许晓辉,李晨曦,潘秀丽
(1.兰州市食品药品检验所,甘肃 兰州 730050;2.甘肃省医学科学研究院,甘肃 兰州 730050)
保健食品,是指具有特定保健功能或能补充维生素、矿物质的食品,适宜于特定人群食用,不以治疗疾病为目的,不对人体产生任何急性、亚急性或慢性危害[1]。不法商贩为了达到其宣称的保健功效,而在保健食品中非法添加化学药物,不可避免地会危害人体健康。近年来出现了许多增强体力、改善生长发育类的保健食品,除了添加以西地那非为代表的磷酸二酯酶5抑制剂以外,添加雄性激素类药物的情况也时有发生。雄性激素主要指由性腺(睾丸)合成的一类内分泌激素,消费者在不知情的情况下长期不合理地摄入雄性激素会引起内分泌失调、新陈代谢紊乱,以及增加罹患癌症的风险[2-3]。
目前我国发布的相关检验标准多为补充检验方法,检测对象包括改善睡眠类、降血糖类、降血脂类、降血压类、减肥类、缓解体力疲劳类等非法添加物,有关雄性激素类非法添加物的检测鲜有报道,且缺乏保健食品中雄性激素类非法添加物的检测标准。国内外报道的食品中性激素类非食用添加物的检测方法主要有气相色谱-三重四极杆质谱法[4-5]、液相色谱-三重四极杆质谱法[6-13]、高效液相色谱法[14-16],但上述方法均存在分辨率低、验证手段少和定性分析不准确的问题。高效液相色谱-四极杆-飞行时间质谱(HPLC-Q-TOF MS)法可对化合物的结构和裂解规律加以确证,大幅提高定性筛查能力,动态扩充筛查范围,提前发现潜在风险,被国内外广泛应用于非法添加物检测领域。
本研究基于高效液相色谱-四极杆-飞行时间质谱法,建立了固体基质、液体基质和油性基质保健食品中10种雄性激素类非法添加物的快速筛查技术,可为完善国家标准提供依据,同时为打击保健食品行业非法添加行为、规范保健食品市场提供有力的技术支撑。
1 实验部分
1.1 仪器、试剂与材料
Agilent 1290-6545高效液相色谱-四极杆-飞行时间质谱仪(美国安捷伦公司);5810R冷冻离心机(德国艾本德公司);VORTEX KB-3涡旋振荡器(海门其林贝尔仪器制造有限公司);MS105DU电子天平(美国梅特勒公司),Milli-Q超纯水系统(美国Millipore公司)。
标准品:丙酸诺龙(纯度98.6%,下同)、诺龙(96.7%)、去氢睾酮(98.8%)、氟甲睾酮(98.0%)、表睾酮(98.0%)购于德国Dr.Ehrenstorfer公司;甲睾酮(99.5%)、美雄诺龙(99.9%)、苯丙酸诺龙(99.1%)、丙酸睾酮(99.8%)、睾酮(96.6%)购于中国食品药品检定研究院;乙腈、正己烷(色谱纯,默克公司)。固体基质、液体基质和油性基质分别选取具有代表性的片剂、口服液、软胶囊剂为研究对象,实际检验样品均随机购于兰州市药店、成人用品店,于阴凉处存放。
1.2 标准溶液配制
标准品储备液:准确称取10种雄性激素标准品各10.00 mg,分别用乙腈溶解并定容于10 mL容量瓶中,配制成质量浓度为 1.0 mg/mL的各标准品储备液,于 4 ℃冰箱中保存。
混合标准溶液:分别精密移取各标准品储备液0.1 mL 置于100 mL容量瓶中,用乙腈稀释并定容至刻度,配制成质量浓度均为1.0 μg/mL的混合标准溶液,于4 ℃冰箱中保存。
1.3 样品前处理
1.3.1 固体、液体基质称取固体基质、液体基质的样品各0.5 g,置于10 mL离心管中,准确加入10 mL乙腈,涡旋振荡5 min后,于40 ℃水浴超声10 min,以4 000 r/min离心5 min,取上清液过0.22 μm滤膜,待测。
1.3.2 油性基质称取油性基质的样品0.5 g,按上述方法操作,所得上清液置于10 mL离心管中,加入5 mL乙腈饱和正己烷溶液,涡旋振荡1 min,静置分层,弃去上层正己烷溶液,下层溶液过0.22 μm滤膜,待测。
1.4 仪器条件
1.4.1 色谱条件色谱柱:安捷伦ZORBAX Eclipse Plus C18色谱柱(3.0 mm×150 mm,1.8 μm);流动相:A为0.1%甲酸溶液(含10 mmol/L乙酸铵),B为0.1%甲酸乙腈溶液;流速:0.3 mL/min;柱温:35 ℃;进样量:5 μL。梯度洗脱:0~2.0 min,20% B;2.0~4.0 min,20%~35%B;4.0~6.0 min,35%~40% B;6.0~12.0 min,40%~70% B;12.0~14.5 min,70%~85%B;14.5~17 min,85% B;17~18 min,85%~20% B;18~20 min,20% B。
1.4.2 质谱条件离子源:电喷雾离子源(ESI),正离子模式;干燥气温度:320 ℃;干燥气流速:8 L/min;雾化气压力:241 kPa;鞘气温度:350 ℃;鞘气流速:11 L/min;毛细管电压:3 500 V;全扫描范围:m/z50~1 000;参比离子:m/z121.050 9和922.009 8(用于实时校正),碰撞能量:20 eV。
1.4.3 质谱库的建立按上述仪器条件,在全扫描模式(MS mode)下对质量浓度均为1.0 μg/mL的10种待测药物混合标准溶液进行分析,获得化合物的精确相对分子质量、同位素信息和保留时间,建立一级谱库。然后在HPLC-Q-TOF MS的MS/MS模式(Targeted MS/MS mode)下分析,得到不同碰撞能量(10、20、30、40 eV)下碎片离子的质谱图,建立二级谱库。最后将两次数据采集的化合物精确相对分子质量、保留时间和碎片离子的质谱图导入PCDL软件,完成质谱库的建立。10种雄性激素的分子式、分子离子理论质荷比、分子离子实际质荷比、产物离子、碰撞能量(CE)等质谱参数见表1。
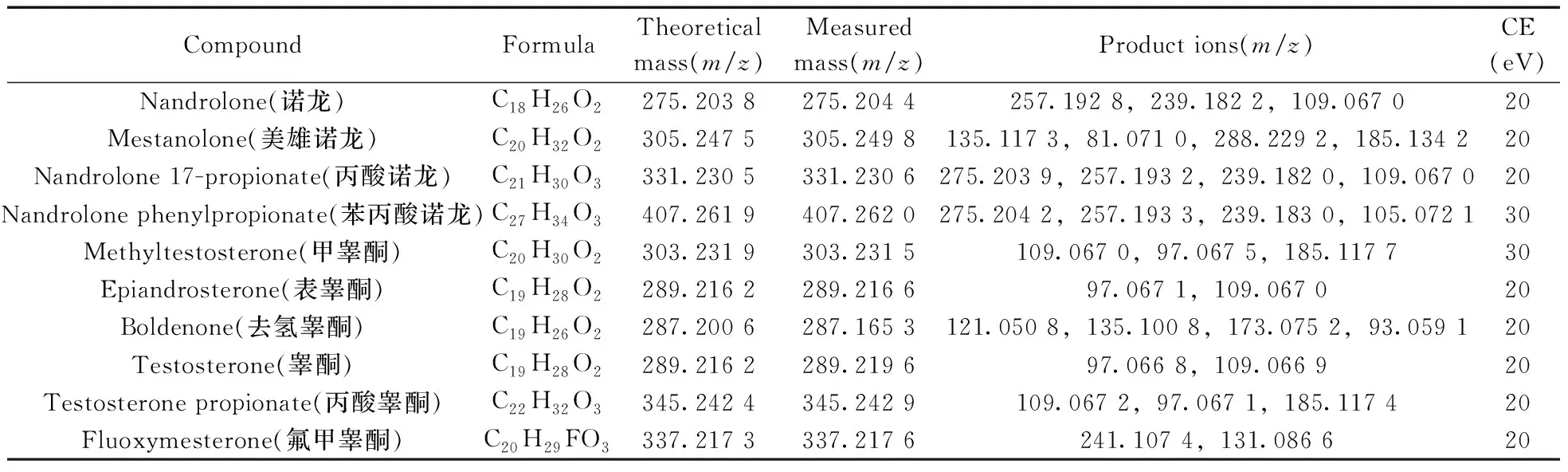
表1 10种雄性激素的质谱参数Table 1 Mass parameters of the 10 androgen drugs
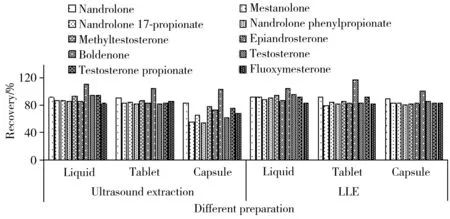
图1 2种前处理方法的平均回收率Fig.1 Average recoveries of two sample preparation methods
2 结果与讨论
2.1 样品前处理方法的优化
选取具有代表性的片剂、口服液、软胶囊剂,对比了超声提取法、液液萃取(LLE)法2种前处理方法的适用性。片剂研磨均匀后取样,口服液直接取样,软胶囊剂取其内容物,精密移取混合标准溶液0.5 mL至以上3种样品的空白基质中,按“1.3”进行超声处理和液液萃取。
在2种不同前处理条件下,10种雄性激素的回收率如图1所示。结果显示,固体基质和液体基质使用超声提取法和液液萃取法的回收率均较高,且超声法操作简便,基本无损失。油性基质使用超声提取法的回收率较差,推测是由于油脂未除去导致基质效应增强,因此用正己烷液液萃取将油脂除去,回收率得到很大提升。综上,固体基质和液体基质前处理选择超声提取法,油性基质选择液液萃取法。
2.2 基质效应评价
将质量浓度均为100 ng/mL的基质标准溶液和溶剂标准溶液分别进样3针,采用下式评价基质效应(ME):ME=基质标准溶液的平均响应值/溶剂标准溶液的平均响应值。ME=1.0表示不存在基质效应,0.8
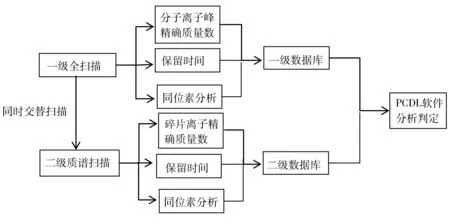
图2 10种雄性激素的TOF MS筛查流程Fig.2 Screening process of 10 androgen drugs by TOF MS
2.3 快速筛查方法的建立
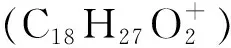
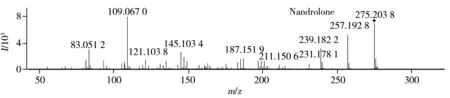
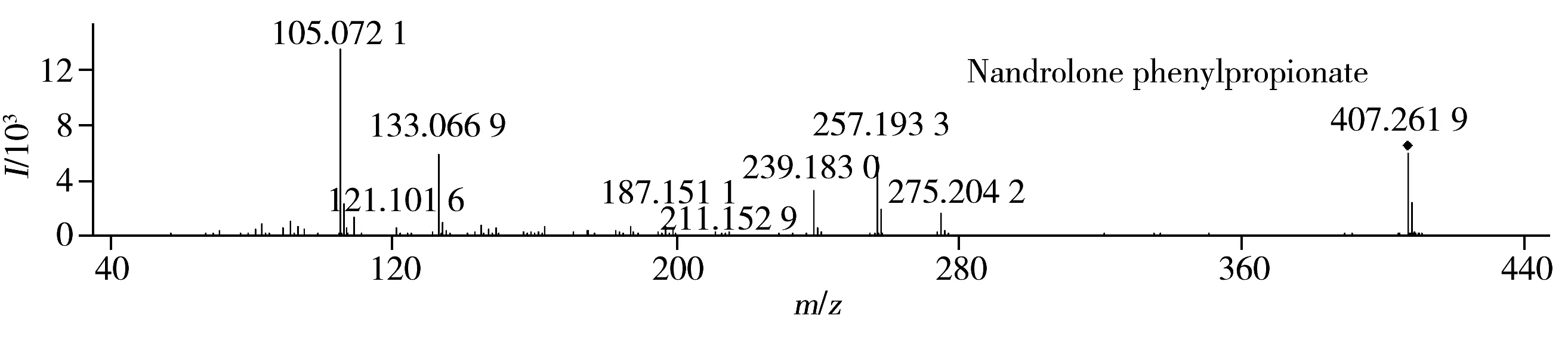

图3 诺龙、苯丙酸诺龙和未知化合物的二级质谱图Fig.3 MS/MS spectra of nandrolone,nandrolone phenylpropionate and unknown compound
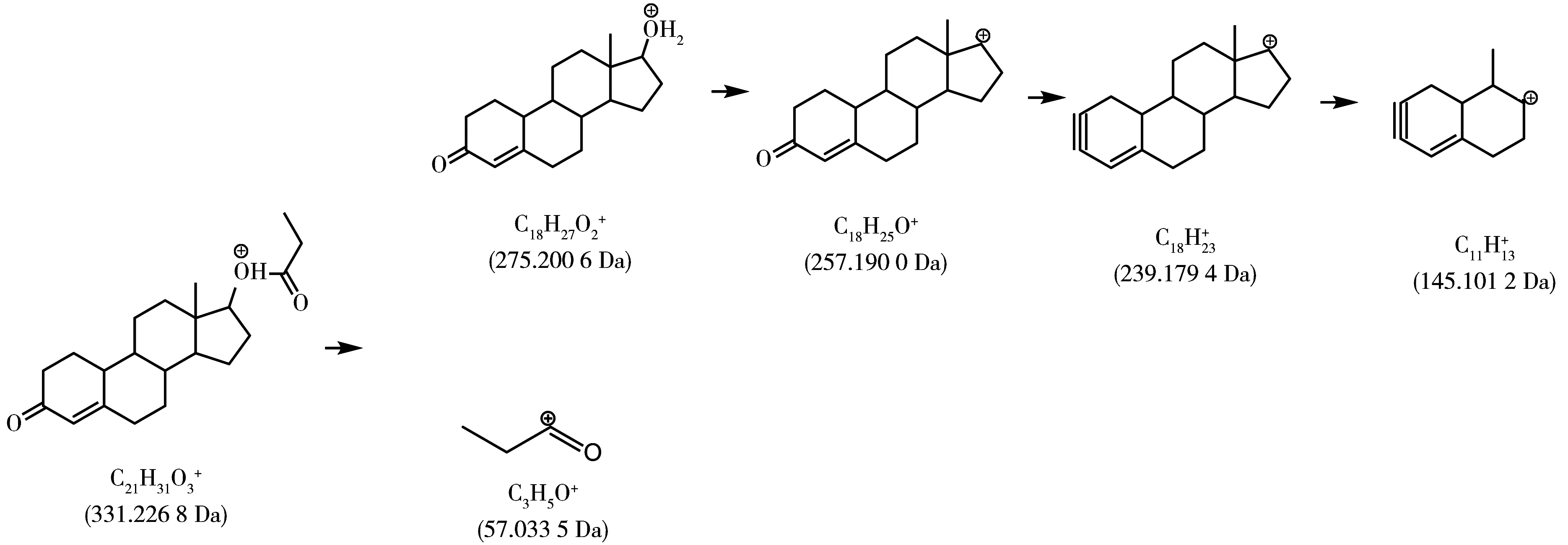
图4 丙酸诺龙的裂解路径Fig.4 The fragment patterns of nandrolone 17-propionate
因此,通过丙酸诺龙对照品建立其一级以及二级谱库,将样品按本方法进行前处理后,进行一级质谱全扫描,与PCDL软件中已建立的数据库进行自动检索,通过精确质量数、保留时间、同位素分布和同位素比例4个指标进行匹配度打分,匹配度为90.3分。再对筛查出的丙酸诺龙可疑化合物进行二级质谱匹配,给予分子离子峰一定能量,通过碎片离子的准确质量数和丰度比进行确认,将PCDL二级数据库导入定性分析软件,进行匹配度打分,碎片离子与二级数据库匹配良好,检索得分为92.9,因此确证该可疑化合物为丙酸诺龙,同时将其信息添加到初期建立的谱库中。
使用建立的非法添加物谱库对未知物进行筛查,可通过与已建立谱库中的化合物二级质谱对比,推断出可能的未知化合物,并将此未知化合物进行确认后扩充到已建立的谱库中,不断更新谱库对未知物的筛查能力。
2.4 方法学验证
2.4.1 专属性取空白的固体基质、液体基质、油性基质保健食品按“1.3”进行样品前处理,再按“1.4”条件进行测定,结果均未检出待测10种雄性激素,表明空白基质对检测无干扰。
2.4.2 线性范围、检出限与定量下限精密移取混合标准溶液适量,配制成质量浓度分别为2、10、20、50、100、200、500 ng/mL的系列标准曲线溶液,以各化合物的质量浓度(X,ng/mL)为横坐标,对应峰面积(Y)为纵坐标,绘制标准曲线。结果表明,10种雄性激素在2~500 ng/mL范围内线性关系良好,相关系数(r2)均大于0.999。将混合标准溶液加入空白基质中,加标浓度逐级递减,按“1.3”进行样品前处理,以3倍信噪比时计算检出限(LOD),10倍信噪比时计算定量下限(LOQ)。固体基质、液体基质和油性基质中的检出限为0.01~0.06 mg/kg,定量下限为0.03~0.2 mg/kg(见表2)。
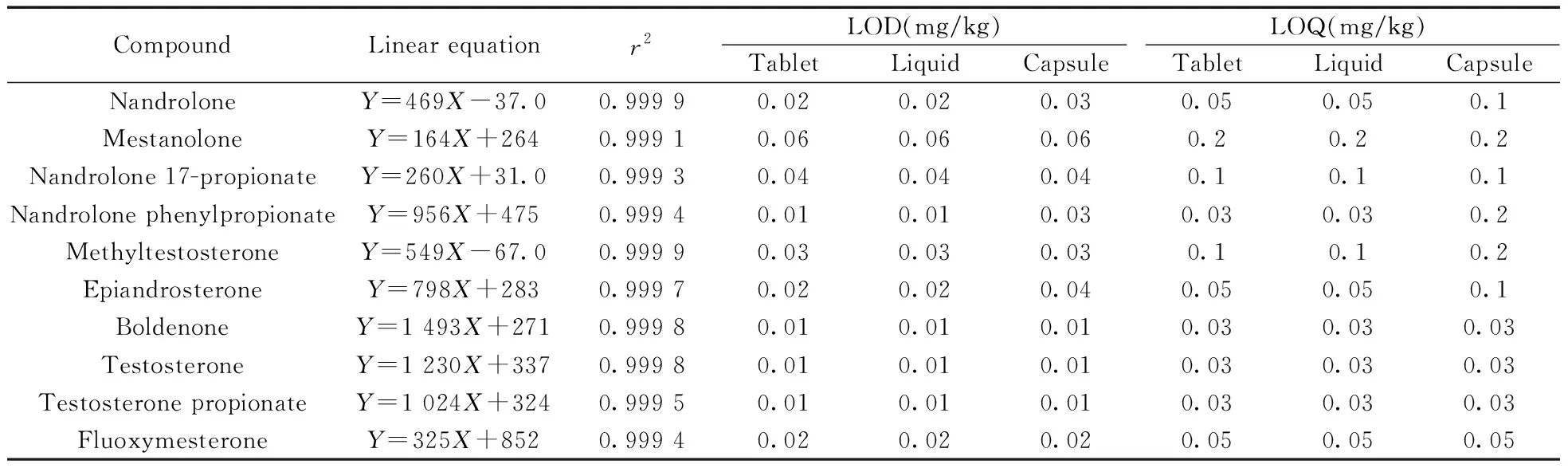
表2 10种雄性激素的线性方程、相关系数、检出限与定量下限Table 2 Linear equations,correlation coefficients,LODs and LOQs of the 10 androgen drugs
2.4.3 回收率与相对标准偏差分别在片剂、口服液、软胶囊剂的空白基质中加入低、中、高3个不同浓度水平的混合标准溶液,每个浓度平行测定6次,加标回收率和相对标准偏差(RSD)结果见表3。结果显示,10种雄性激素的平均回收率为74.3%~113%,RSD为1.2%~7.7%。
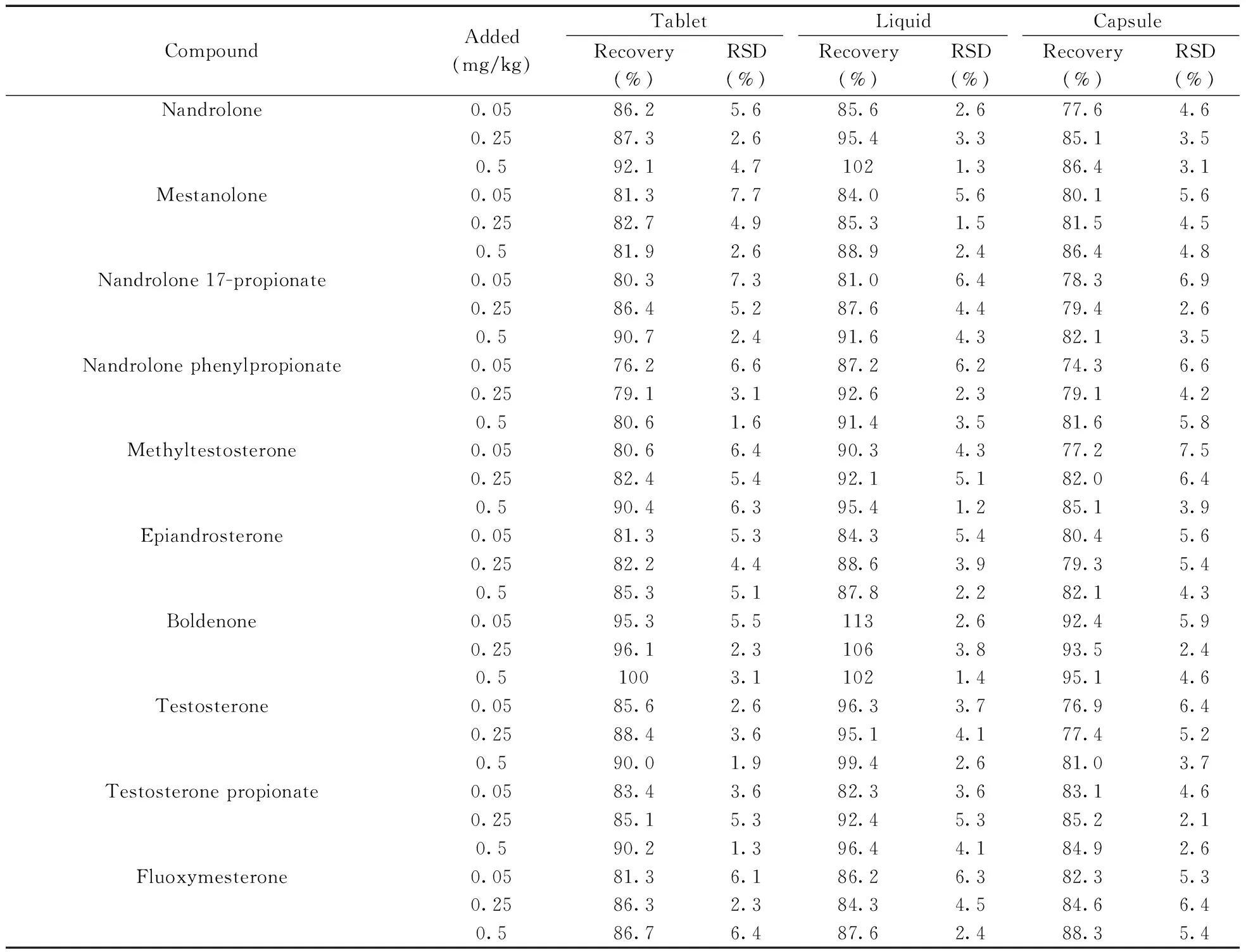
表3 10种雄性激素在3种保健食品基质中的回收率和相对标准偏差Table 3 Spiked recoveries and relative standard deviations of the 10 androgen drugs in three kinds of health food matrices
2.5 实际样品检测
应用本方法检测50批次市售保健食品,按上述方法进行快速筛查,发现1批次样品含有可疑未知化合物,利用碎片离子进行质谱裂解路径的推断,确认该非法添加物为丙酸诺龙,含量为0.13 mg/kg,其色谱图及质谱图如图5所示。丙酸诺龙的检出量较低,推测该化合物与其他增强体力、改善生长发育类药物可通过协同作用以增强药效,减小药物用量。
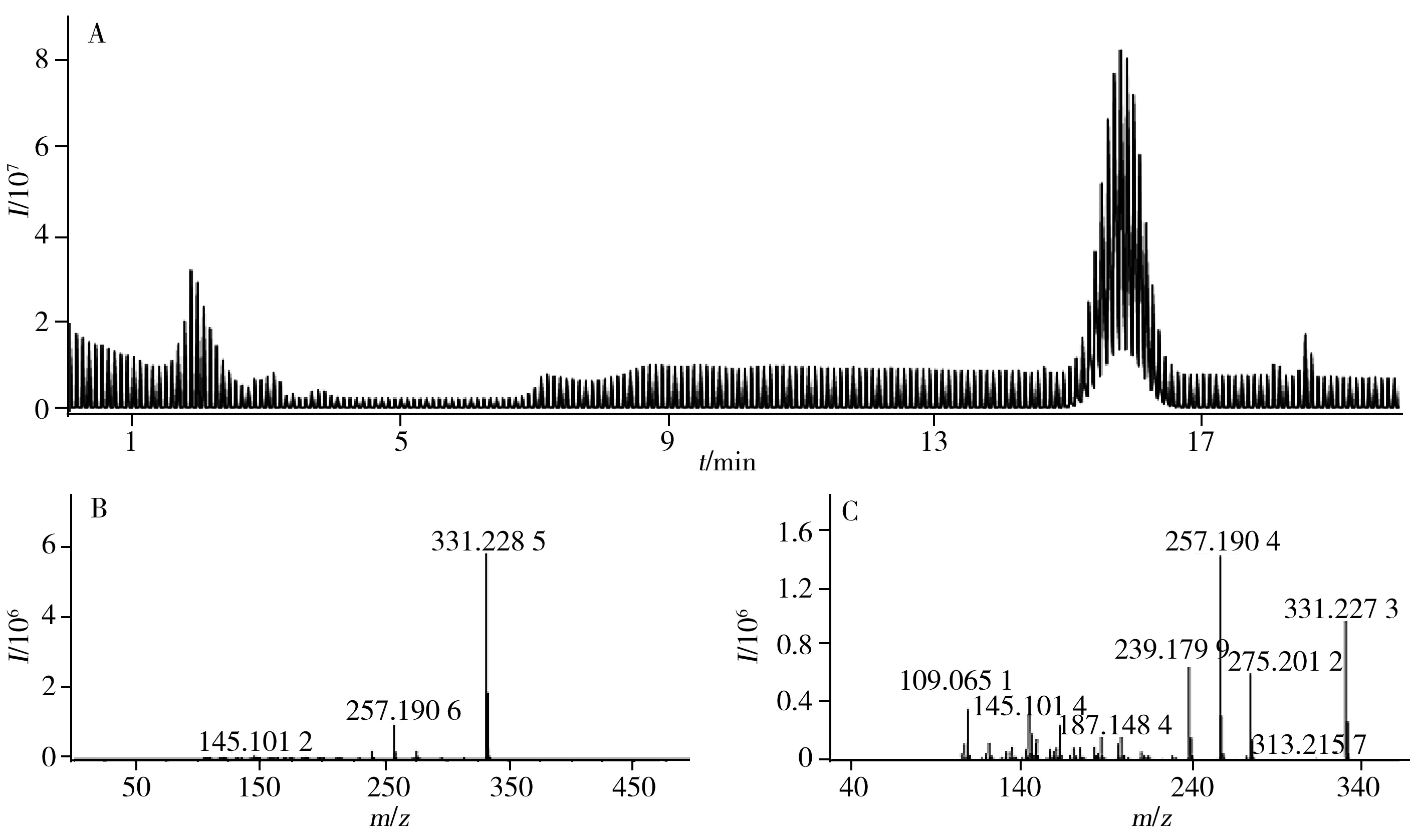
图5 阳性样品的色谱图和质谱图Fig.5 Chromatogram and mass spectra of a positive sampleA.TIC;B.MS spectrum;C.MS/MS spectrum
3 结 论
本研究针对3种具有代表性的保健食品基质,对比了2种前处理方法,通过自行构建的高效液相色谱-四极杆-飞行时间质谱的一级精确质量数据库和二级谱库,建立了快速筛查10种雄性激素的检测方法。该方法操作快速、灵敏、准确,可及时有效地发现保健食品市场中非法添加行为,打击虚假宣传行为,降低保健食品安全风险,为行政监管提供有力的技术支持。
