岱海沉积物内源磷释放特征的研究
2020-09-24陈俊伊郑朔方王书航
黄 威, 刘 星, 赵 丽, 陈俊伊, 郑朔方, 姜 霞, 王书航*
1.中国环境科学研究院, 湖泊水污染治理与生态修复技术国家工程实验室, 北京 100012 2.东华大学环境科学与工程学院, 国家环境保护纺织工业污染防治中心, 上海 201620
磷以多种形态(钙、铁、铝等金属结合态磷及有机态磷)存在于沉积物中,部分磷吸附在矿物质表面作为植物细胞中结构和生物化学作用的重要组分[1-2]. 尤其是湖泊沉积物作为上覆水体的“源-汇”角色,对湖泊富营养化起着决定性作用. 因此,了解沉积物-水界面磷释放特征显得尤为重要.
当沉积物与水环境接触时,沉积物磷与水体中的磷会进行相互交换,直至达到交换平衡. 在一般的吸附过程中,经典的吸附模型可以用来描述这种平衡,如经典的吸附模型曾用来描述土壤或底泥对磷和有机物的吸附过程[3-4]. 但是,完整地诠释含磷沉积物对磷的吸附解吸过程必须考虑到沉积物中NAP (native adsorbed phosphorus,吸附解吸态磷)的含量[5]. NAP能够直接参与磷释放吸附过程,从而影响沉积物对磷的吸附容量. 学者们通常用WA-Pi (弱吸附态磷)代替沉积物中NAP,通过计算EPC0(equilibrium phosphorus concentration, 平衡磷浓度)与间隙水中SRP (soluble reactive phosphorus, 可溶性活性磷)的浓度梯度,进一步判定沉积物的“源-汇”角色[6-7]. 但是,参与沉积物磷释放吸附过程的NAP可能受沉积物组成、环境条件(如湖泊化学性质)等因素的影响而改变[2,8]. 因此,现阶段通常综合吸附解吸试验与模型计算的方法确定NAP含量和EPC0.
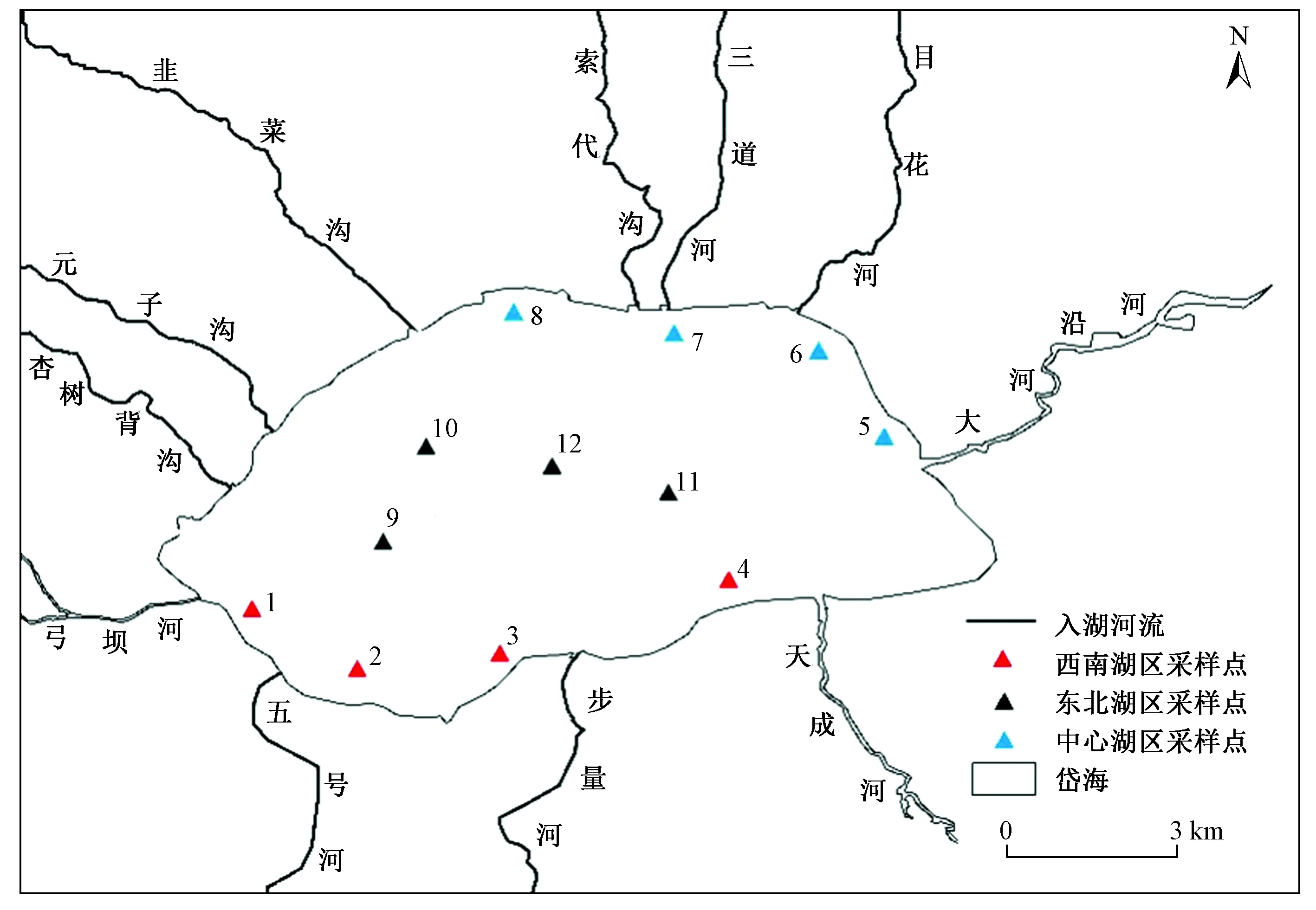
图1 岱海沉积物采样点分布Fig.1 Distribution of sediment sampling sites in Daihai Lake
岱海是一个典型的内陆封闭流域湖泊,属内蒙古自治区中部生态环境核心保护区,其生态环境保护具有典型性和代表性[9]. 近年来,岱海湖水咸化程度逐渐增加,其水体及沉积物中营养盐浓度不断升高,富营养化程度加剧. 在外源营养盐输入得到有效控制的前提下,沉积物营养盐的内源释放成为湖泊水体营养盐浓度升高的主要原因之一[10-11]. 磷作为岱海沉积物主要营养盐之一,其释放风险对岱海水体营养盐浓度有着重要影响. 该研究通过分析岱海西南湖区、东北湖区及中心湖区沉积物对磷的吸附解吸特征,计算沉积物吸附解吸的相应参数,确定岱海各湖区沉积物磷的“源-汇”角色,以期为岱海水体富营养化的综合防治提供理论依据.
1 材料与方法
1.1 研究区域及样品采集
岱海(40°29′27″N~40°37′06″N、112°33′31″E~112°46′40″E)位于内蒙古自治区中部凉城县境内,东西长约25 km,南北宽约10 km,平均水深7 m,蓄水量达13.3×108m3,湖水矿化度2.5 gL左右,流域面积约 2 084.4 km2[9]. 该研究在西南湖区、东北湖区及中心湖区共设置12个沉积物采样点(见图1),于2019年5月使用彼得森挖泥器进行表层沉积物采集. 每个采样点进行多次采泥,每次采集表层底泥2~4 L,放入干净盆中混匀,并装袋置于保温箱,24 h内带回实验室进行预处理.
1.2 试验设计
沉积物的吸附动力学试验在室温(25±2)℃下进行. 磷溶液采用KH2PO4配置,-4 ℃下避光保存,且每次均使用24 h内配置的新鲜溶液. 取不同采样点的沉积物样品(1 g)于150 mL锥形瓶中,并加入50 mL 5 mgL的磷溶液,同时设置4个离子强度梯度. 整个系统用保鲜膜密封,并在恒温 (25±2)℃摇床上以200 rmin的转速进行振荡. 在不同时刻(0.5、1、2、5、10、20、60、120、240和480 min)进行取样,离心过滤,测定溶液中磷的浓度. 试验设置3组平行,假设沉积物与溶液质量的比值在整个试验周期保持不变.
沉积物对磷的吸附等温线通过设置不同初始磷浓度进行绘制. 取不同采样点的沉积物样品(1 g)于150 mL锥形瓶中,加入50 mL不同浓度梯度(0、0.5、1、2、5、10、和20 mgL)的磷溶液. 整个系统用保鲜膜密封,并在恒温(25±2)℃摇床上以200 rmin的转速振荡8 h后进行取样,离心过滤,测定溶液中磷的浓度. 试验设置3组平行,假设沉积物与溶液质量的比值在整个试验周期保持不变.
1.3 样品测试
水样及间隙水中磷素浓度均参考文献[12]方法测定. 测定沉积物间隙水中SRP浓度时,样品高速离心(>10 000 rmin、15 min)后取上清液,测定上清液中磷浓度. 沉积物中WA-Pi(弱吸附态磷)含量采用连续提取法测定[13].
沉积物采集完后直接带回实验室冷冻干燥,研磨过100目(孔径0.15 mm)筛,得到粒径均匀的沉积物颗粒. 测定沉积物TP含量时,称取0.2 g预处理制样后的沉积物样品(经冷冻干燥研磨后的干样),在450 ℃下灰化3 h,冷却后加入20 mL 3.5 molL的HCl,振荡离心16 h后,测定上清液中SRP浓度,得到TP浓度[14]. 测定上清液中的磷浓度,即为沉积物TP含量[14]. 沉积物的pH通过质量与体积比为 1∶2.5 的泥和水混合后测定[15];底泥中OM(有机质)含量则通过样品在550 ℃下煅烧4 h后的质量差进行测定;沉积物的氧化物成分通过X射线荧光分析仪(BRUKER Q4 MOBILE, 德国)测定.
1.4 数据处理
不同沉积物样品不同时刻磷的吸附量(Qt, mg/g)通过式(1)得出:
Qt=(C0-Ct)VW
(1)
式中:C0为初始磷的质量浓度,mg/L;Ct为空白矫正后t时刻磷的质量浓度,mg/L;t为时间,min;V为溶液体积,L;W为样品质量,g.
为了研究沉积物在吸附磷过程中的动力学行为及吸附质在固-液相中、固-液表面和固体内部的扩散机理,一般采用准一级动力学模型〔见式(2)〕、准二级动力学模型〔见式(3)〕进行研究[16-17].
Qt=Qe(1-eK1t)
(2)
(3)
式中:Qe为平衡状态时磷的吸附量,mg/g;Qt为t时刻磷的吸附量,mg/g;K1为准一级动力学模型常数,h-1;K2为准二级动力学模型常数,g/(mg·h).
吸附等温线通常采用经典的Langmuir等温吸附模型和Freundlich等温吸附模型来进行绘制,分别如式(4)(5)所示.
(4)
Qe=KFCen
(5)
式中:Qmax为Langmuir等温吸附模型理论最大吸附量,mg/g;K为吸附剂对吸附质的亲和力,L/mg;Ce为平衡状态时磷的浓度,mg/L;KF为吸附系数,L/g;n为常数,表示吸附剂吸附强度和表面的多相性.
式(4)引入[NAP]与[EPC0],Langmuir等温吸附模型变形为
(6)
(7)
(8)
式(5)引入[NAP]与[EPC0],Freundlich等温吸附模型变形为
Qe=KFCen-KF(Ce0)n-Qe0
(9)
[NAP]=KF(Ce0)n+Qe0
(10)
(11)
式中:Ce0为初始磷浓度为0的条件下,吸附平衡时的溶液磷浓度,mg/L;Qe0为初始磷浓度为0的条件下,吸附平衡时沉积物的磷吸附量,mg/g;[EPC0]为吸附体系处于动态平衡时溶液中磷浓度,mg/L;[NAP]为平衡溶液中可交换态磷与吸附在底泥表面上的可交换态磷的总和,mg/g.
2 结果与讨论
2.1 岱海沉积物磷释放动力学特征分析
岱海3个湖区沉积物对磷的吸附动力学行为可用准一级动力学模型和准二级动力学模型描述. 关于吸附动力学行为,该研究主要探究了3个过程:①吸附质(PO43-或H2PO4-)从液相向固-液相边界层扩散;②吸附质从固-液相边界层向固体表面扩散;③吸附质向沉积物颗粒内部扩散[18]. 岱海3个区域、12个不同采样点的沉积物对磷的吸附动力学行为通过准一级动力学模型和准二级动力学模型进行拟合,结果见图2. 在此次吸附动力学试验中,假设沉积物样品在480 min时达到吸附平衡. 如图2所示,沉积物样品在初期的0~60 min内,吸附速率较快,在后期的60~480 min内,吸附速率逐渐减小,且逐渐趋于平衡,这与早期关于沉积物磷吸附速率的研究结果一致[19-20]. 产生该现象的可能原因是,吸附初期沉积物表面具有较多的活性吸附点位,且这些活性吸附点位迅速被PO43-或H2PO4-离子占领;而在吸附后期,沉积物表面活性吸附点位数量迅速下降,导致磷的吸附速率也随之下降;尤其是在240 min以后,吸附可能达到平衡,并且可能伴随着磷的解吸.
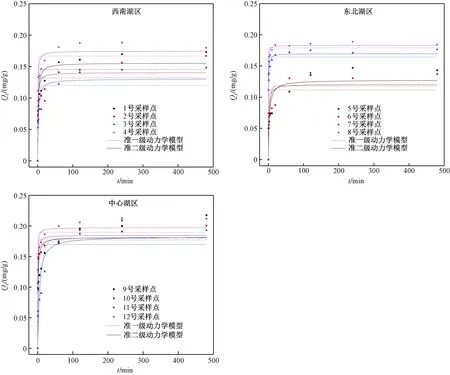
图2 岱海3个湖区沉积物对磷的吸附动力学Fig.2 Sorption kinetics of phosphorus on the sediments from three regions of Daihai Lake
准一级动力学模型和准二级动力学模型拟合结果如表1所示. 结果表明,准二级动力学模型能够更好地描述沉积物对磷的吸附动力学行为〔相关系数(R2)为0.728 8~0.993 8〕,且吸附速率较快,最高达11.45 g/(mg·min). 中心湖区沉积物平衡吸附量Qe的值显著较大,表明中心湖区沉积物具有更好的磷吸附能力. 这主要是因为中心湖区沉积物(9号和11号采样点)的Al、Ca氧化物含量相对较高(见表2). 一方面,可进一步推动Al、Ca与P的化学沉淀作用;另一方面,Al、Ca氧化物增加了沉积物的比表面积,有利于沉积物对磷的吸附[7]. 研究[21]表明,沉积物样品中高含量的OM有利于磷的吸附. 中心湖区沉积物的OM含量相对较高(见表2),使其具有较高的Qt值和吸附速率常数K2值,这也与已有研究结果[22-23]一致. 此外,有研究[24-25]指出,湖库环境中pH较低的沉积物对磷的吸附能力较大,这主要是因为pH的升高促使H2PO4-转化成HPO42-,使Al、Ca和Fe氧化物的表面电荷发生改变,导致这些氧化物对磷的吸附能力降低. 也有研究[26-27]表明,较低的pH可促进吸附态磷向Ca结合态磷(Ca-P)转化,而沉积物中Ca-P、Fe-P、Al-P等结合态磷均具有磷“汇”的潜在功能,可提升沉积物对磷的吸附能力. 从表2可以看出,对比其他湖泊[28-30],岱海沉积物pH普遍偏高(pH>8),沉积物对磷的吸附能力较其他湖库也普遍偏弱. 表1所示动力学吸附数据Qe也表明岱海沉积物对磷的吸附能力较低[28,31]. 对比岱海3个湖区,pH较低的中心湖区沉积物对磷的吸附能力较大,但在一定程度上也加大了中心湖区沉积物磷的释放风险.
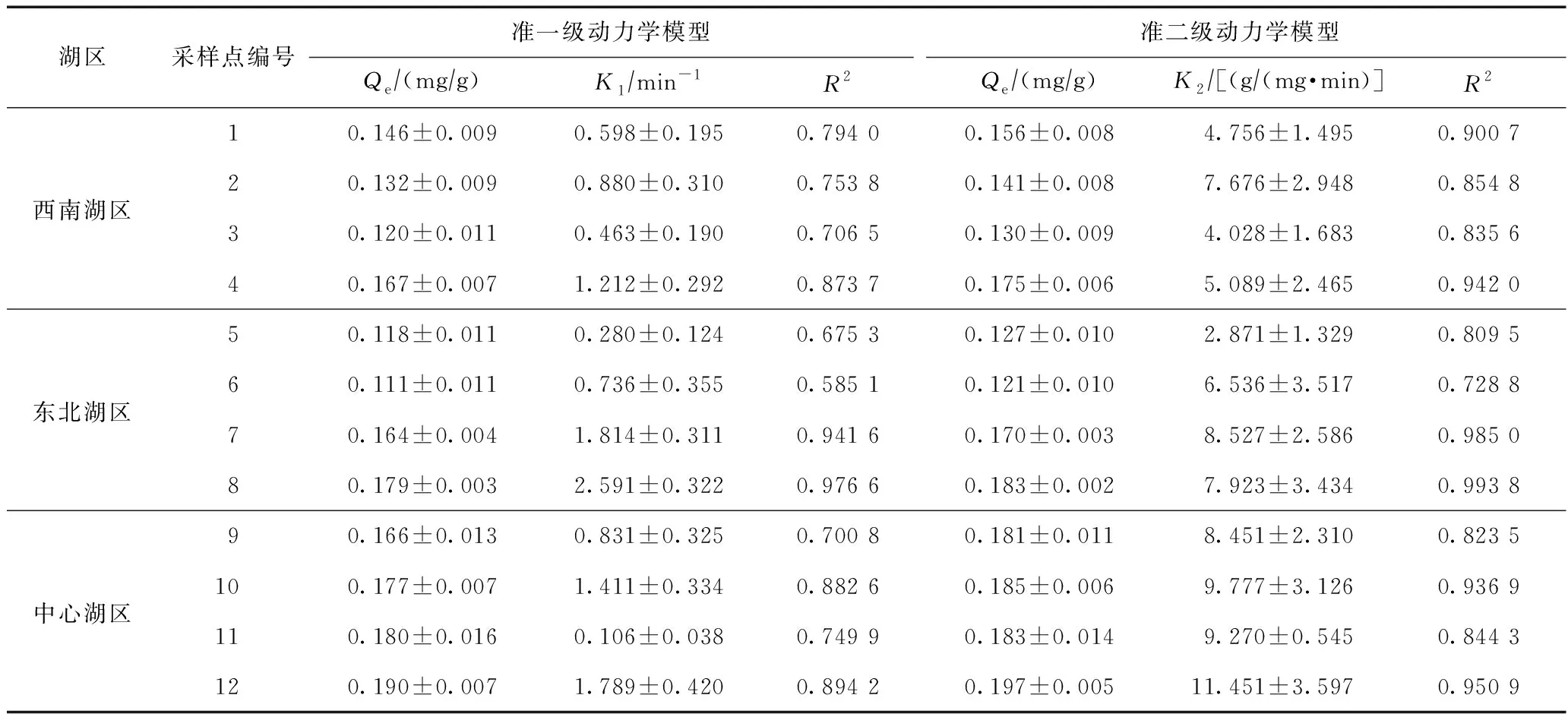
表1 准一级和准二级动力学模型动力学参数
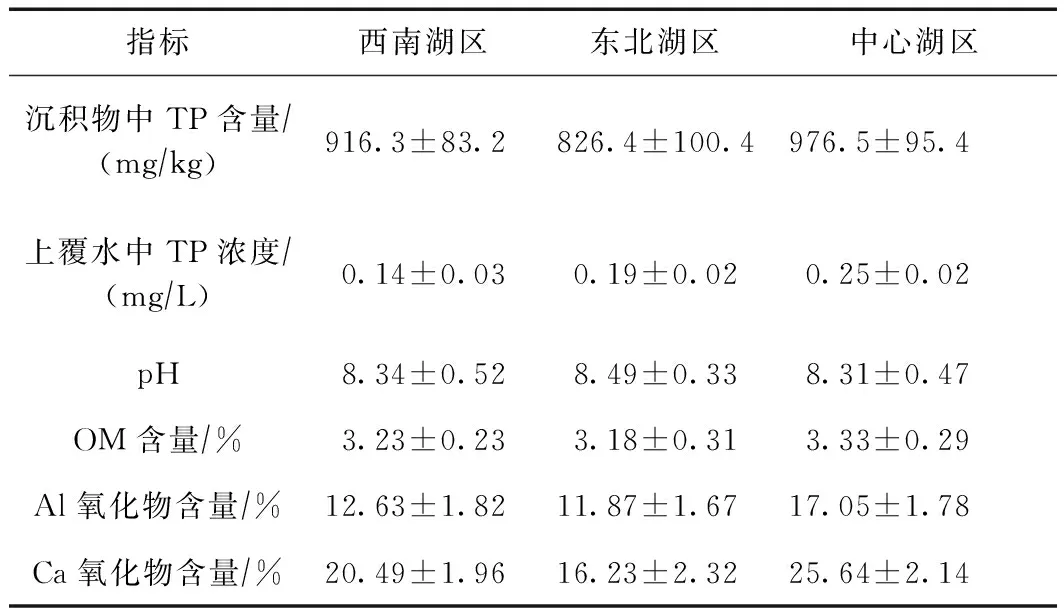
表2 沉积物样品的理化特性
2.2 岱海沉积物对磷等温吸附特征分析
采用修正后的Langmuir等温吸附模型和Freundlich等温吸附模型研究岱海沉积物对磷的吸附等温特征,结果如图3和表3所示. 由图3可见,修正后的Langmuir等温吸附模型(R2为0.907 6~0.974 2)比修正后的Freundlich等温吸附模型(R2为0.877 0~0.953 6)能更好地描述沉积物对磷的吸附等温线. 如表3所示,岱海沉积物样品最大吸附量(Qmax)和亲和力常数(K)的变化范围分别为0.321~0.867 mg/g和0.632~3.849 L/mg. 与我国其他湖泊相比,如滇池(0.85 mg/g)[28]、洞庭湖(0.75 mg/g)[31]、太湖(0.72 mg/g)[32]、黄大湖(0.79 mg/g)[32],岱海沉积物磷的理论最大吸附量相对偏低,这主要是由于岱海沉积物较高的pH削弱了沉积物对磷的吸附,同时也反映出pH对沉积物磷吸附能力的影响较大. 对比岱海3个湖区,中心湖区沉积物具有较高的磷吸附量(0.685 mg/g). 主要原因是:①岱海中心湖区沉积物OM含量较高,导致中心湖区沉积物对磷的理论最大吸附量 (>0.5 mg/g) 较高;②西北湖区和东南湖区沉积物pH较高,高浓度的OH-会通过与含磷阴离子竞争活性吸附点位来削弱沉积物对磷的吸附,同时高浓度的OH-也能够改变沉积物表面的吸附环境[33],进一步削弱中心湖区沉积物对磷的吸附. 综上,岱海沉积物对磷的吸附能力较弱,且pH对岱海沉积物磷吸附能力的影响较大.
2.3 沉积物磷释放风险评估
理论上讲,对于相同的沉积物样品,EPC0和NAP含量是定值. 在研究不同条件对沉积物磷吸附影响时,通常采用沉积物中WA-Pi含量来代替NAP含量. 但也有研究[6-7,34-35]表明,沉积物EPC0和NAP含量可能会随着环境条件(离子强度、pH、温度等)、沉积物自身物理化学性质的改变而不断变化. 因此,该研究均采用修正后的等温吸附模型计算出的参数值进行沉积物内源磷释放风险的评估. 此外,由于磷在液相和固相中最终达到一个动态平衡,沉积物在吸附磷的同时往往伴随着磷的释放,EPC0能够较为直观地反映SRP的迁移[36]. 当沉积物中EPC0大于间隙水中SRP浓度时,沉积物对外释放磷,呈现“源”的角色;反之,沉积物则吸附磷,呈现“汇”的角色[2].
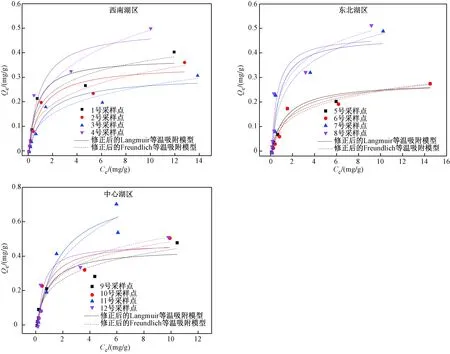
图3 岱海3个湖区沉积物对磷的吸附等温线Fig.3 Sorption isotherms of phosphorus on the sediments from three regions of Daihai Lake
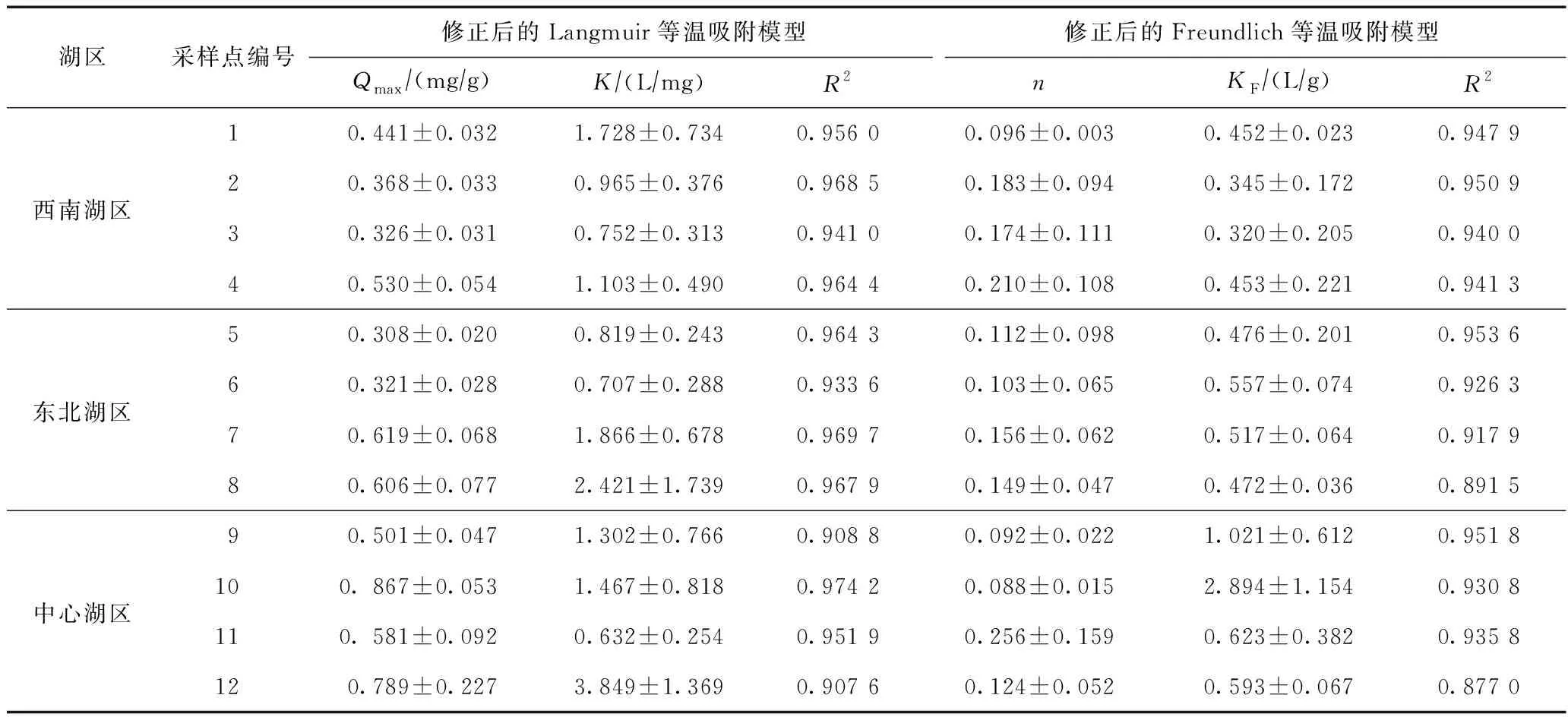
表3 修正后的Langmuir和Freundlich等温吸附模型吸附等温参数
研究[6-7,37]表明,当WA-Pi含量较小时,NAP通常被忽略,且关于沉积物磷吸附特征的研究往往直接采用经典的Langmuir和Freundlich等温吸附模型进行. 该研究通过实验室测试所得WA-Pi含量 (0.043~0.112 mg/g)与等温吸附模型计算所得NAP含量(0.019~0.32 mg/g)(见表4)相近,且岱海各湖区沉积物NAP含量有所差异. 其中,岱海中心湖区NAP含量(平均值为0.133 mg/g)较高,沉积物对磷的吸附能力也受到其NAP含量的影响. 通过修正后的Langmuir等温吸附模型和Freundlich等温吸附模型计算出EPC0. SRPp(interstitial water soluble reactive phosphorus, 间隙水可溶性活性磷)浓度和EPC0之间的关系如图4所示. 当[SRPp]=[EPC0]时,沉积物对磷的吸附量为零,既不是源”的角色,也不是“汇”的角色;当[SRPp]>[EPC0]时,沉积物开始吸收磷,扮演“汇”的角色;当[SRPp]<[EPC0]时,沉积物开始释放磷,扮演“源”的角色. 结果表明,采用修正后的Langmuir和Freundlich等温吸附模型计算出的EPC0均较小,除9号和11号采样点外,其余采样点沉积物[EPC0]均小于[SRPp],表明岱海中心湖区部分沉积物点位扮演磷“源”的角色,存在内源磷释放风险. [NAP]/[EPC0]能够反映沉积物和水溶液对磷的亲和力,亲和力越高,沉积物对磷的吸附能力也越高[38]. 岱海中心湖区沉积物[NAP]和[NAP]/[EPC0]均高于其他两个湖区,这也为中心湖区沉积物内源磷的积累提供了一定条件,潜在地增加了岱海中心湖区沉积物内源磷的释放风险.
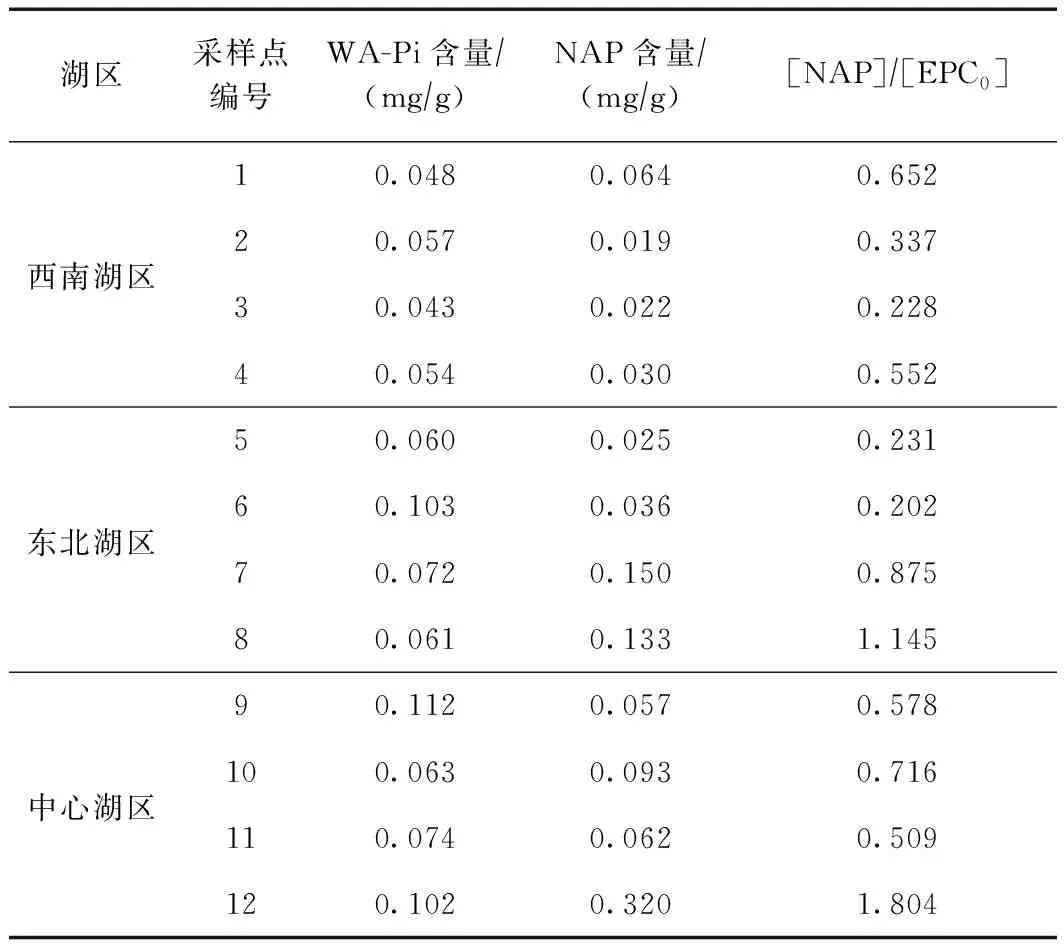
表4 沉积物NAP和WA-Pi参数
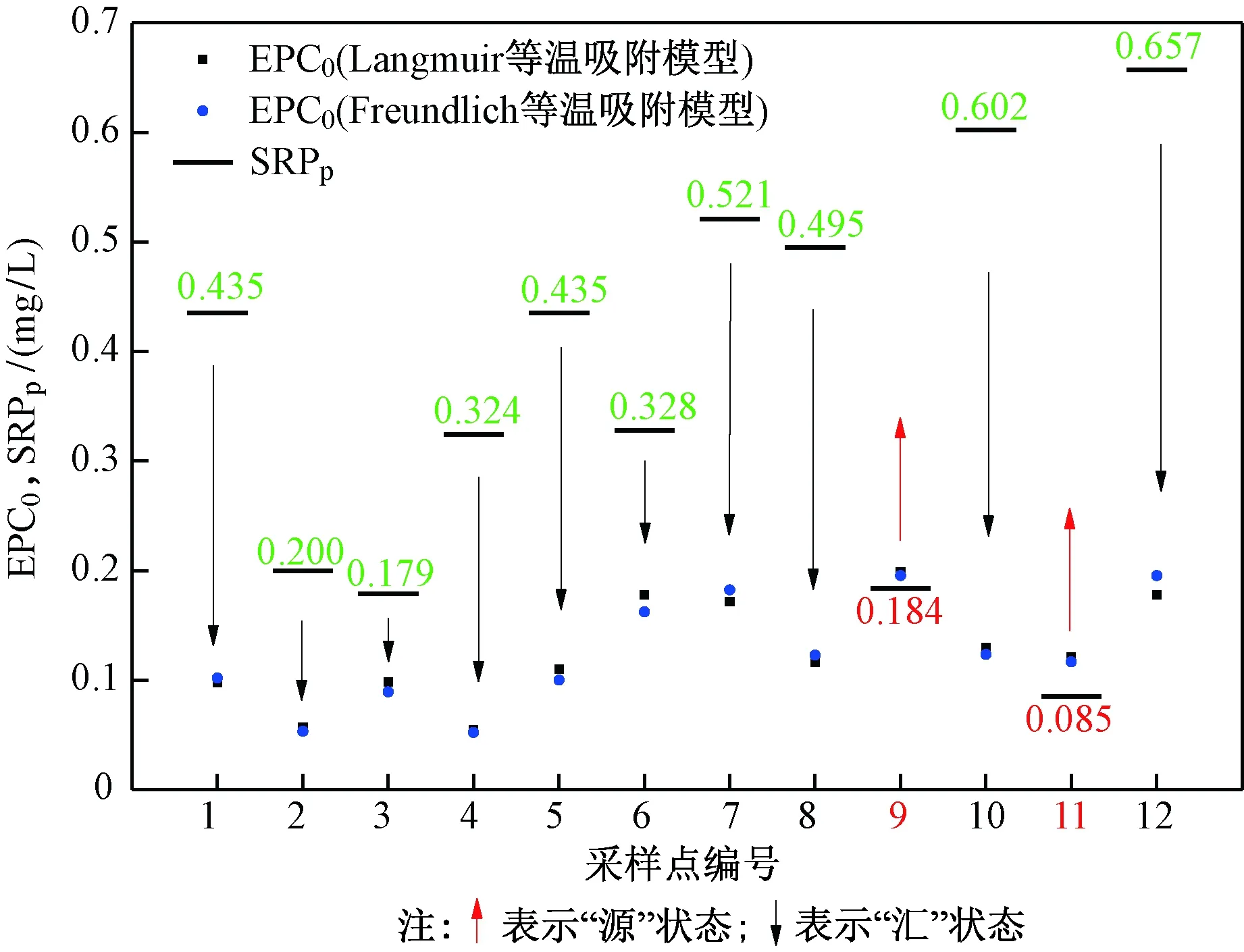
图4 沉积物内源磷释放风险评估结果Fig.4 Risk assessment of endogenous phosphorus release in sediments
岱海中心湖区部分沉积物点位具有内源磷释放风险的主要原因:①中心湖区沉积物自身TP含量较高(976.5 mg/kg,见表1),在一定程度上为沉积物内源磷释放提供了大量的“源”. ②2.1节和2.2节中提到,中心湖区沉积物较高OM含量和较低pH均是沉积物对磷吸附能力较大的主要原因[5,39-40]. 经计算,中心湖区沉积物对的磷吸附能力最大可达0.867 mg/g,这也导致沉积物与间隙水中磷交换频繁,增加了沉积物内源磷的释放风险. ③经过[SRPP]与[EPC0]的对比,中心湖区沉积物9号和11号采样点扮演磷“源”的角色. 综上,中心湖区部分沉积物点位存在内源磷释放风险. 对于西南湖区和东北湖区,一方面,岱海西南湖区和东北湖区位于入湖口附近,存在着较为频繁的水体物质交换,使得该区表层沉积物无法常年累积,导致岱海西南湖区和东北湖区,尤其是部分入湖河流交汇处,沉积物内源磷释放风险较小;另一方面,由于西南湖区和东北湖区沉积物和水体中的pH较中心湖区大,导致水体中磷的沉积及沉积物中磷的固化,由此降低了沉积物磷的释放风险.
3 结论
a) 岱海各湖区沉积物磷释放存在一定的区域性差异. 岱海西南湖区和东北湖区沉积物磷释放风险较小,但中心湖区沉积物磷释放风险较大;岱海中心湖区沉积物磷含量及磷吸附能力均高于西南湖区和东北湖区,一方面可促进沉积物与水体中磷的交换,另一方面也为沉积物内源磷释放提供有利的条件.
b) 岱海水体中营养盐浓度较高,是沉积物内源磷释放的主要原因之一. 一方面,岱海沉积物较高的pH导致其较弱的磷吸附能力,中心湖区沉积物存在内源磷释放风险;另一方面,岱海沉积物与水体中磷交换频繁且交换速率大,吸附解吸过程发生迅速,从而加大了沉积物内源磷的释放风险.
c) 对于岱海沉积物内源磷释放风险的控制,可通过对具有磷释放风险的中心湖区重点防控的方式进行;岱海西南湖区和东北湖区沉积物磷释放风险较小,则可根据实际情况采取相应措施.
