颈椎后路C3~C7椎板切除内固定融合术后中期相邻节段退变的临床研究
2020-09-24曹仰敬申庆丰夏英鹏
曹仰敬,申庆丰,夏英鹏
(1.天津医科大学研究生院,天津300070;2.天津市人民医院脊柱外科,天津300121)
脊髓型颈椎病临床上主要是由多节段椎间盘突出、颈椎后纵韧带骨化、先天性或者退行性颈椎管狭窄等导致多节段脊髓压迫性病变[1]。颈椎后路椎板减压内固定术可以达到重建稳定性、解除脊髓压迫的双重目的[2]。本研究分析患者在行颈椎后路椎板减压内固定术后是否发生相邻节段退变(adjacent segmental degeneration,ASD)。既往认为活动的颈椎内固定融合手术属于刚性固定,无疑会伴发远期固定相邻节段的退变,甚至失稳。但是笔者大量临床病例随访发现,实际上这种并发症的出现并没有想象的多,故而开展此次回顾性研究,尝试明确颈椎后路椎板切除减压内固定融合术后对相邻节段退变的影响。
1 资料与方法
1.1 一般资料 纳入标准:(1)通过相关查体以及影像学检查明确诊断脊髓型颈椎病。(2)大于3个节段受压。(3)X线平片侧位中立位,存在颈椎曲度消失或者反曲。排除标准:(1)有颈椎手术历史。(2)颈椎曲度良好。(3)脊柱手术明确的手术禁忌证。
通过上述标准将2015年5月—2018年5月医院脊柱外科施行颈椎后路椎板减压内固定术的41例患者纳入研究。其中男20例,女21例;年龄24~79岁,平均年龄53岁。减压内固定节段均为C3~C7节段。所有患者术前均行颈椎X线片、CT、MRI检查。
1.2 观察方法
1.2.1 椎间高度 在侧位X线片测量手术节段的椎间高度,以椎间隙上方椎体上终板的中点至下方椎体下终板的中点的距离即为椎间高度。同时计算椎间高度变化=术后椎间高度-术前椎间高度[3]。
1.2.2 X线平片标准 椎间退变标准设定为:X线标准侧位片椎间隙高度丢失与术前相比大于10%;形成肉眼可见的新生骨赘或者原有骨赘增大;或者出现前纵韧带钙化[4-5]。
1.2.3 MRI标准 T2加权像采用Miyazaki等[6]的颈椎间盘退变分级方法观察相邻节段退变情况。Ⅰ级:髓核强度高信号,髓核结构均一白色,髓核、纤维环分界清晰、椎间盘高度正常;Ⅱ级:髓核信号呈高信号,髓核结构白色带有灰带区,髓核、纤维环分界清晰,椎间盘高度正常;Ⅲ级:髓核强度中等信号,髓核结构颜色不均,灰和黑混杂,髓核及纤维环分界不清晰,椎间盘高度正常或降低;Ⅳ级:髓核强度低信号,髓核结构颜色不均,灰和黑混杂,髓核及纤维环分界消失,椎间盘高度正常或降低;V级:髓核强度低信号,髓核结构颜色不均,灰和黑混杂,髓核及纤维环分界消失,椎间盘高度塌陷。具体方法见图1。
1.2.4 固定术后骨性融合标椎 采用Cauthen等[7]的标准:(1)骨小梁桥接融合。(2)融合但植骨边缘有透光影。(3)植骨吸收或者出现透光影而为融合。(4)植骨出现相对活动未融合。(5)不能确定。
1.2.5 颈椎活动度 在过伸及过屈侧位X线片测量C2椎体下缘与C7椎体下缘连线的夹角,夹角之和即为颈椎活动度(range of motion,ROM)。
1.3 手术方法 常规全麻俯卧位,沿C2~T1逐层暴露直至显露C3~C7椎板至小关节外侧。定位满意后,选取合适螺钉,开口锥开口,丝锥套扣,于C3~C7双侧置入侧块螺钉。用尖嘴咬骨钳及磨钻,沿C3~C7椎板双侧小关节突内侧缘小心开槽,右侧保留内侧皮质骨,左侧则小心咬透椎板。将C3~C7椎板由左向右掀去达到脊髓减压。冲洗,减压后脊髓有搏动。取合适长度钛棒弯曲合适弧度后置于螺钉尾端,拧紧尾帽。用磨钻在双侧C3~C7关节突间打磨形成植骨床并植入剪碎的C3~C7棘突骨。C型臂透视内固定位置良好,置伤口引流管2根,逐层缝合伤口(侧块螺钉棒系统固定内植物来自美国强生公司)。
1.4 术后处理 术后3 d拔出引流管后嘱患者佩戴颈托下地活动。
1.5 统计学处理 应用SPSS23.0统计软件进行分析,计量资料以x±s表示,计数资料组间变量采用单因素重复测量方差分析。P<0.05为差异具有统计学意义。
2 结果
2.1 影像学评价结果 所有患者均获得满意的X线片随访及MRI随访,时间为12~26个月,平均18个月。C3~C7减压后共有上下相邻节段两个,即C2/C3和C7/T1,本组符合观察标准的节段共计82个。
2.1.1 术后3 d椎间高度与术前相比差异无统计学意义(P>0.05),末次随访与术后3 d椎间高度对比,差异无统计学意义(P>0.05),见表 1、2。

表1 术前与术后3 d椎间高度变化情况Tab 1 Change of intervertebral height of preoperative and postoperative 3 days
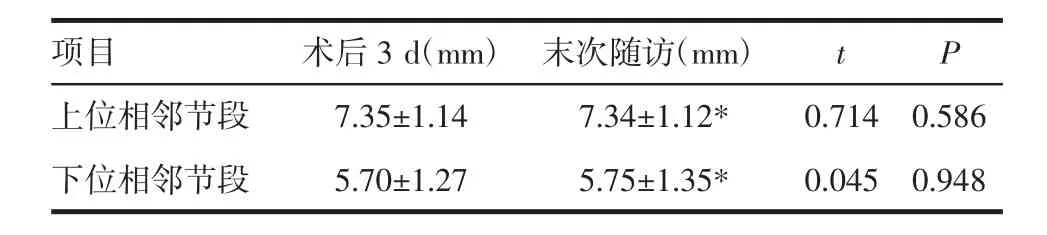
表2 术后3 d与末次随访椎间高度变化情况Tab 2 Change of intervertebral height of postoperative 3 days and the last follow-up
2.1.2 患者在术后3 d与术前X线过伸、过屈位的颈椎活动度相比较,术后3 d X线的颈椎活动度平均值为22.18°±4.09°,术前X线颈椎活动度平均值18.26°±5.68°,颈椎活动度有明显变化,差异有统计学意义(t=5.403,P<0.05);而末次随访时的 X 线颈椎活动度为 16.72°±3.11°,与术后 3 d的 X线颈椎活动度相比较,差异没有统计学意义(t=2.303,P>0.05)。
2.1.3 末次随访时所有患者植骨未达到骨性融合标准,但并未出现内固定松动、脱出、断裂发生。
2.1.4 患者的上位、下位相邻节段未出现新生骨赘或者骨赘增大的节段、前纵韧带钙化,见表3。

表3 术前、术后3 d、末次随访X线相邻节段退变的情况Tab 3 The adjacent segment degeneration observed by X-ray of preoperative,postoperative 3 days and the last follow-up
2.1.5 通过MRI影像学观察,末次随访、术后3 d与术前相比上位、下位相邻节段椎间盘信号无明显变化,见图 1、表 4。

图1 颈椎间盘退变T2像分级Fig 1 Cervical disc degeneration T2 image grade

表4 术前、术后3 d、末次随访MRI显示相邻节段退变的情况Tab 4 The adjacent segment degeneration observed by MRI of preoperative,postoperative 3 days and the last follow-up
3 讨论
回顾近10年的文献,学者们研究了颈椎ASD的影像学资料,发现相邻节段退变大多发生在颈椎前路减压内固定术后。其中Hilibrabd等[8]研究了374例颈椎前路减压融合术后ASD的发生率,随访时间最长为21年,ASD的发生率约为每年2.9%,10年以上的ASD发生率约为25.6%。Babe等[9]对106例颈前路减压融合患者进行8.5年的随访,超过25%的患者出现上相邻节段退变,10%的患者出现下相邻节段退变。Gore和Sepic[10]对146例施行颈椎前路减压融合术的患者术后随访5年,25%的患者在原来的基础上形成新的ASD,25%的患者原来的ASD加重。不仅ASD在前路术后呈高发趋势,而且因为ASD造成的相关症状,而必须采取二次手术的病例也不在少数,Yue等[11]对71例接受颈椎前路减压融合术进行7.2年的随访中发现约有73.2%的患者在此期间出现ASD的情况,12例(16.9%)因ASD而需要再次手术治疗。同样的,Bohlman等[12]报告122例施行颈椎前路减压融合术的患者术后进行6年的随访,9%因为ASD需行手术治疗。Gore和Sepic[10]发现14%的患者因为ASD需要再次行手术治疗。此外Williams等[13]所研究的122例颈椎前路减压融合患者术后6年,9%的患者因ASD需要再次行手术治疗。上述研究表明颈椎前路固定融合术后ASD的概率很高,并且这种ASD发生的症状往往严重,治疗方面再次手术的比例不低。究其原因,学者们普遍认为这种ASD的发生主要是因为颈椎前路固定融合术后,颈椎活动度受限,为了尽可能维持颈椎的正常生理活动,未融合的节段都需要进行代偿,从而受到的应力增加最为显著,关节的退变在超负荷和不平衡的过度运动中明显加速,形成ASD。无论发生机制如何,颈椎术后ASD一旦发生,随之而来的脊髓再次压迫和相关系列神经症状作为手术后继发的医源性中远期并发症不容忽视,甚至付出二次手术的高昂代价。近年学者们也致力于更深层次研究颈椎术后ASD的发生机制,从而探讨避免的方法。
截至目前,多数研究显示融合节段是ASD出现的影响因素之一,Chung等[14]认为前路手术中融合节段越多,越有可能发生ASD。杨晋才等[15]对尸体进行单、双、三节段融合后,发现颈椎整体活动度呈递减趋势,上下位邻近阶段的活动度随着融合节段的延长而呈递增趋势。张睿等[16]分析融合术后其他各节段运动幅度均有不同幅度的增加,尤其邻近节段增加最为显著,主要表现在椎体间角度运动和椎间关节的活动度增大,使得椎间盘压力不均匀增加,从而导致相邻节段退变的发生。而Lee等[17]则认为涉及3个节段或者更多节段的融合时比涉及单、双节段的融合导致ASD的概率低。Hilibrand等[8]则提出多节段融合后术后刚度过高,肌肉的力量无法使颈椎的活动度达到原来的活动范围,也可能是因为融合了容易发生退变的“高危节段”的理论,从而支持多节段融合后不容易发生ASD的观点。而在传统的C3~C7减压融合中,融合的节段均为C3~C7。其中包含了C5/C6和C6/C7这种所谓的“高危节段”,从而提示笔者开展本次回顾性研究,进一步探讨颈椎后路ASD的发生率和相关发生机制。
在传统的颈椎后路C3~C7椎板减压融合术中,下位相邻节段变为C7/T1,上位相邻节段为C2/C3。固定节段囊括了全部下颈椎。而本次研究中,通过侧块螺钉固定于关节突,能够提供强有力的颈椎后路柱固定[18]。并且钉棒系统通过预弯棒、旋棒,以及局部的撑开或者加压,可以通过外力最大程度地恢复颈椎生理曲及椎间高度[19];同时这种力学改变主要发生在颈椎的中后柱结构中,尤其椎板切除减压后,颈椎后柱破坏,后方张力带破坏,以往认为钉棒系统的侧块固定是十分坚强的内固定,伴随融合,一定会造成ASD。但是本研究中期随访发现,尽管没有内固定的松动,但也没有十分明确的融合迹象,不同于常规认知,常规认为平均随访1年以上,如果没能融合,对于颈椎活动度巨大的脊柱结构,后部的侧块单皮质骨螺钉固定无法承受,从而松动。但是无论机制如何,事实是没有发生松动。其次是全段下颈椎固定术后,颈椎活动度应该明显下降,但研究结果显示,尽管存在颈椎ROM的下降,但是下降幅度与手术前相比差异无统计学意义。这一点也违背了常规认知,常规认为长节段全部下颈段后路内固定影响颈椎ROM,而实际随访中尽管没有列入检测标准,但是很多患者反映术后通过一段时间的康复锻炼,颈椎的实际活动度与手术前相比变化并不大,颈椎屈伸旋转活动基本没有受到明显干扰,甚至与同期随访的颈椎单开门椎管成形术患者相比在实际颈椎活动影响方面并不明显。本次研究的这两点发现提示颈椎C3~C7减压内固定术后的颈椎活动度并不是完全丧失,所以颈椎后路钉棒内固定术很可能不是一个绝对“刚性”的内固定,他本身存在一定“弹性”,这一点通过1年以上的随访能得到肯定的融合证据也能侧面得以验证。最后一点,也是最突出的一点,本次研究显示C3~C7内固定术后1年以上,上、下相邻椎间隙没有ASD的发生,椎间高度和活动度得到了保留,这一点显著区别于前路手术后ASD的研究结果。
本次研究结果和发现区别于既往的前路术后ASD的研究结论,可能存在特殊的发生机制。研究发现,在430例施行颈椎后路椎板减压内固定融合术后,仅有0.9%的患者发生ASD[20]。Auadt等[21]研究发现,50例施行颈椎后路椎板减压内固定融合术后在为期3年的随访里,没有患者出现ASD。程真等[3]研究表明,患者施行颈椎后路手术后,椎间高度无明显变化,并且通过维持椎间高度,减小椎间盘椎体的应力,从而减缓骨赘的形成。李亮等[22]研究发现,颈椎后路手术使之椎间高度得以维持,能够增加缓冲、吸收震荡,并防止颈椎相邻节段出现进一步的退变,维持了颈椎稳定性。这些研究的结果和笔者的结果基本吻合,但是他们的研究没有涉及到术后ASD的发生问题。既往Hilibrand等[8]在研究中发现在颈椎前路间盘切除减压术后,C2/C3和C7/T1发生相邻节段退变的可能性远低于其他节段发生,属于低风险发生相邻节段退变的节段。Kotil和Sengoz[23]研究发现仅有24例个案报道出现C2/3的ASD。这和本研究后路内固定术后ASD的结果基本吻合。这一重要发现的机制可能与后路内固定手术的类似半刚性固定有关,其次也与活动钉棒固定可以很好地恢复颈椎生理曲度并能维持这种良好的生理曲度有关。回顾文献这一机制的阐明也与国内外已经发表的研究结论一致。王洪立等[24]和Park等[25]认为手术节段区域颈椎生理曲度恢复不佳可能是引起ASD的原因之一。邓志龙等[26]认为任何颈椎术前、术后生理弧度及手术前后生理弧度的变化都有可能对相邻节段退变的出现产生影响。Lee等[27]认为融合术后生理曲度变直是导致ASD发生的因素。Falsini等[28]认为维持适当的生理前凸矢状位置能够预防术后出现ASD。
本研究对于ASD的评价不仅使用了最传统的X线平片,清晰地显示出骨性结构,早期发现增生的骨赘,并且能更清晰的辨别出上下椎间盘边界,同时增加MRI评估,MRI是观察颈椎间盘退变最敏感的方法,T2像能够清晰地显示出椎间盘的信号强度、髓核结构、椎间盘高度及椎间盘突出程度,两者结合对于ASD的评估达到更加精准的目的,这是既往大多数研究未曾应用过的方法。
总之,本研究结果显示,颈椎曲度欠佳的脊髓型颈椎病患者行颈椎后路C3~C7椎板减压内固定融合术后,中期随访可以有效的保证颈椎生理曲度的存在,同时并不会引发ASD,其机制可能是颈椎后柱的单纯融合不能达到颈椎总体的全刚性固定,同时通过部分减少了颈椎总活动度,加之维持了正常的颈椎生理曲度,使得原本就不容易发生ASD的C2/C3和C7/T1节段,术后生理荷载没有显著增加,从而维持了椎间盘的生理功能,避免了ASD的发生。但是这一结论尚有待大样本病例的远期随访结果进行评估。
