Willis环变异与交通动脉瘤发生的相关性研究
2020-09-18佳木斯大学附属第一医院CT室黑龙江佳木斯154002
佳木斯大学附属第一医院CT室(黑龙江 佳木斯 154002)
刘 健 程纪皓
颅底动脉瘤破裂所导致的自发性蛛网膜下腔出血,是临床较常见的急性出血性疾病[1]。自发性蛛网膜下腔出血在临床上出现的原因中,动脉瘤破裂居主要位置,并且死亡率很高,早期诊断颅内动脉瘤能明显降低死亡率。
1 材料与方法
1.1 临床材料回顾性分析并收集2017年1月至2018年1月在佳木斯大学附属第一医院经CT血管造影检查初步诊断为交通动脉瘤破裂的患者影像学资料共201例。进行之后进一步排除及筛查,排除标准:外伤史及其他脑血管疾病,心、肝、肾功能不全,近期接受过DSA检查;筛选条件:由2名以上经验丰富的主任医师共同诊断,并经DSA或神经外科手术确认。最终确诊为交通动脉瘤的病例169例,其中男61例、女108例,年龄31~82岁,平均年龄(58.3±9.777),经过后处理三维重建技术观察Willis环的解剖变异与交通动脉瘤的关系。
1.2 检查方法使用Philips ICT进行头颈部血管扫描。以5.0~6.0ml/s的流速率经过外周静脉系统注入造影剂优维显(370mgl/ml)70~90ml,并以相同流速追加50ml生理盐水。将触发点设置在主动脉弓或颈总动脉,阈值设置在100HU。扫描参数:准直0.625mm,螺距0.16~0.18,旋转时间0.33s,FOV250mm,管电压110~120KV,管电流360~380mAs。采用矩阵重建1024x1024,扫描层厚1mm,重建层厚1.25mm,将重建的图像传输至EBW后处理工作站进行图像分析,得到血管三维重建图像,直观观察Willis环的形态及变异。
1.3 判断标准本研究参考文献[2-4]依据前、后血流循环将Willis环的变异分为Ⅰ-Ⅳ型。临床上通常将组成Willis环的血管直径小于1mm定义为发育不全,本研究中将两侧同名血管不对称,管径相差1倍以上定义为发育不良;将整条血管结构通过调节宽窗位不能显示定义为血管缺如;并将发育不良与缺如归为一类。
1.4 数据统计169例交通动脉瘤患者中,前交通动脉瘤(见图1-6)68例(40.2%),其中Ⅰ型5例(7.3%)、Ⅱ型11例(16.2%)、Ⅲ型17例(25%)、Ⅳ型35例(51.5%),其中Ⅳ型中,ⅣA型最为多见共16例(23.5%),其次为ⅣD型9例(13.2%);后交通动脉瘤患者101例(59.8%),其中Ⅰ型15例(14.9%)、Ⅱ型29例(28.7%)、Ⅲ型33例(32.7%)、Ⅳ型24例(23.7%),见表1。
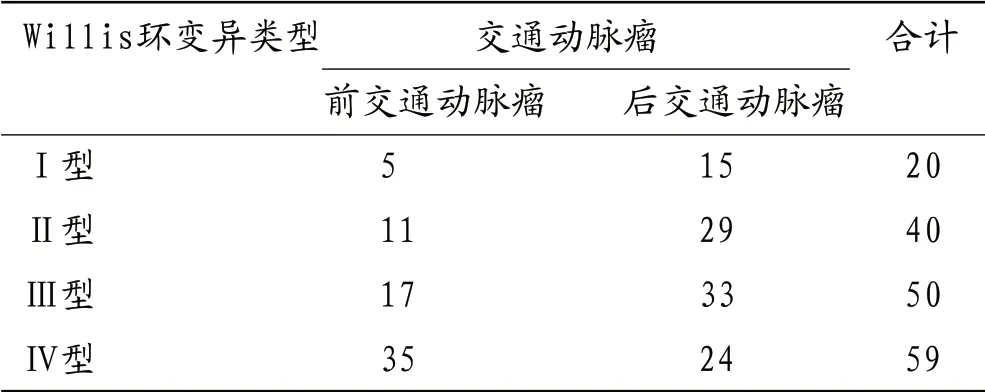
表1 Willis环变异类型与交通动脉瘤的关系
1.5 统计分析数据处理采用SPSS21.0统计学软件,计量资料分析应用χ2检验,年龄用平均值P<0.05具有统计学意义。
2 结 果
2.1 性别因素169例交通动脉瘤患者,其中男61例、女108例,将性别因素与交通动脉瘤病例进行比较,发现前交通动脉瘤组中,男性患者居多,男性患者40例,女性28例;后交通动脉瘤组中,以女性患者居多,女性患者68例,男性33例(χ2=11.326,P=0.001)。
2.2 年龄因素169例交通动脉瘤患者,年龄范围在31-82岁之间,平均年龄(58.3±9.777)。将交通动脉瘤按发生部位分为前后两组,与患者的年龄范围及平均年龄进行比较,前交通动脉瘤组的年龄范围在31-81岁,平均年龄为57.37岁;后交通动脉组的年龄范围在35~82岁,平均年龄为58.93岁。通过以上数据可以发现,后交通动脉瘤组的平均年龄偏大(χ2=6.444,P=0.011)。
2.3 Willis环变异因素68例前交通动脉瘤患者,Ⅳ型最多见,占35例(51.5%),将Willis环前后循环均发生缺如或发育不良的Willis环分型与前后交通动脉瘤的发生进行统计分析,结果具有统计学意义(χ2=14.375,P=0.02)。在Ⅳ型变异中,ⅣA型最多见,占16例(23.5%),其次为ⅣD型9例(13.2%),均存在Willis环前循环的发育不良或缺如,将Ⅳ型中的5个亚型进行统计学分析发现ⅣA型变异与前交通动脉瘤存在相关性,见表2(χ2= 10.973,P=0.027)。101例后交通动脉瘤患者,ⅢA型最多见,其次为ⅢB型,占58.4%,将Willis环后循环缺如或发育不良与其他Willis环变异分型做对比Willis环分型差异(χ2=37.02,P>0.05),Willis环的各变异分型与后交通动脉瘤无统计学意义。
3 讨 论
16世纪中叶国外学者[5]提出Willis环概念,Willis环由前交通动脉、双侧大脑前动脉A1、A2段,双侧颈内动脉、后交通动脉及双侧大脑后动脉P1、P2段组成(见图2),经Kooper等对脑组织标本发现[6]完整的Willis环仅占极少比例,我国居民发生Willis环变异的几率更高[7],超过50%的人,在发生脑动脉闭塞后,此环不能提供良好的侧支血管循环。Willis环的变异和某些脑血管疾病可能有一定关系。Kayembe等人发现,相对于没有动脉瘤的Willis环,有动脉瘤发生的Willis环变异率明显偏高。而大脑前后循环血管的不对称性变异与大脑前交通动脉瘤有显著的相关性[8]。21世纪初期,Schomer、Iqbal等人研究发现当一次颈内动脉发生闭塞时,同侧后交通动脉直径小于1mm对于缺血性脑梗死的发生是一种致命的因素,并且Willis环变异可能改变CVD的发生、严重程度、治疗和康复[9]。Willis环从某种意义上来说是一种循环代偿结构,Willis的交通动脉分别是连通双侧大脑前动脉A1段和双侧大脑后动脉P1段的主要桥梁,Willis环的变异使得远端血管侧壁遭受更大的血流冲击,长时间切应力冲击下可引起血管内壁弹力膜破坏和血管肌层薄弱等退行性改变,从而导致动脉瘤[10]。颅脑动脉瘤本质上是一种颅内动脉壁的异常膨出,好发于颅底动脉分叉处,常伴管壁结构薄弱。按照部位分,约70%发生在Willis环上,本组前交通动脉瘤患者Willis环表现以ⅣA型最多,其次为ⅣD型,均为前后循环均发育不良或缺如型,与其他Willis环变异分型的动脉瘤对照组进行统计学分析,显示存在统计学意义;后交通动脉瘤患者存在后循环发育不良或缺如型最多(超过半数),其与Willis环前循环缺如或发育不良无明显统计学意义,与后循环缺如或发育不良也不存明显的差异关系。这一情况与文献[11]报道基本相符。
颅内动脉瘤发病机制未明,其形成是遗传学、血流动力学以及后天退行性改变等多种因素综合作用的结果,最终导致动脉内腔异常扩张而形成的一种血管瘤样突起[12]。颅内动脉瘤多发生在脑动脉分支、分叉或急剧转弯处区域,尤其是Willis环前交通动脉区域。
胚胎型大脑后动脉也属于Willis环变异的一种,它由颈内动脉供血,在椎-基底动脉供血不足时,胚胎性大脑后动脉作为原发侧枝代偿,对增加后循环血供起到至关重要的作用,胚胎性大脑后动脉也常常提示椎-基底动脉发育不良,往往会引起小脑及脑干梗死[13],本组中脑缺血组脑干梗死及小脑半球梗死病例均有胚胎性大脑后动脉,但可能因样本量不足,无胚胎性大脑后动脉正常组与脑缺血组比较差异无统计学意义,这点有待进一步探讨。
现如今CT血管造影(CTA)在临床上应用越来越广泛,Kazt[14]等用CTA、MRA及DSA对Willis环形态进行对比观察,发现CTA后处理三维重建技术较传统的动脉瘤诊断金标准DSA有更明显的优势,不但节约检查费用,而且患者接受辐射降低。在临床实践中,若CTA检查呈ⅣA型或ⅣD型Willis环,发现前交通动脉瘤则应注意及时处理, 以防短期内破裂或再次破裂。
综上所述,Willis环变异中Ⅳ型变异与前交通动脉瘤的发生存在明显统计学意义,而后交通动脉瘤与Willis环变异未发现明显的统计学意义;通过研究交通动脉瘤与性别和年龄关系后,发现前交通动脉瘤好发于男性,后交通动脉瘤好发于女性,且发病平均年龄偏大。