西格列汀联合胰岛素强化治疗对2型糖尿病早期大血管病变的炎性因子的影响
2020-09-15方晨圆陶少平
方晨圆,杭 宇,陶少平
(皖南医学院第二附属医院内分泌科,芜湖 241000)
2 型糖尿病大血管病变是糖尿病持续发展的产物,也是影响糖尿病患者生活质量和导致其死亡的重要原因。据调查,2型糖尿病患者如果不早期治疗,其发病后第9 年发生大血管病变的机率为20%[1]。导致大血管病变的原因有很多,其中炎性因子如同型半胱氨酸(Hcy)、超敏 C 反应蛋白(CRP)等在其发生发展过程中有重要作用。选择有效的干预措施在降低血糖的同时降低炎性因子对降低大血管并发症的发生风险有重要意义。研究表明,二肽基肽酶-4抑制剂(DPP-4)在降低血糖、调节血脂作用、保护心血管方面有独特的优势[2]。本文对DPP-4西格列汀联合胰岛素对2型糖尿病早期大血管病变的炎性因子的影响进行分析。
1 资料与方法
1.1 资料选择我院从2017年11月~2018年10月收治的101例2 型糖尿病早期大血管病变患者,均符合WHO对糖尿病的相关诊断标准且具有早期大血管病变指标异常(颈动脉内膜中层厚度≥ 1.0mm但尚无颈动脉粥样硬化斑块)。均排除合并恶性肿瘤、冠心病、脑梗塞、严重心、肺、肝、肾功能不全等疾病。随机分为观察组和对照组,分别51、50例。观察组51例中,男性28例,女性23例,年龄29~77岁,平均(55.55±10.70)岁,病程1~8年,平均(4.07±1.13)年,BMI18.7~36.2kg/m2,平均(25.11±3.81)kg/m2;对照组50例中,男性26例,女性24 例,年龄28~79岁,平均(56.90±12.23)岁,病程1~8年,平均(4.14±1.09)年,BMI19.1-34.9kg/m2,平均(24.21±3.18)kg/m2。两组患者性别、年龄等差异无统计学意义(P>0.05)。
1.2 方法
1.2.1 治疗方法两组均在住院期间给予胰岛素泵强化治疗,采用胰岛素泵(美国美敦力公司)将门冬胰岛素(诺和诺德公司)持续皮下输注,根据血糖监测情况调整胰岛素剂量设定,血糖控制达标后摘除胰岛素泵,根据患者情况选择不同品种胰岛素多次皮下注射继续治疗。观察组在此基础上给予磷酸西格列汀片(美国默沙东药业有限公司)口服,100mg/次,1次/d。两组均治疗10周。
1.2.2 检测方法采用7600 Series HITACHI(日本日立公司)自动生化分析仪,胶乳增强免疫比浊法测定CRP;采用7600 Series HITACHI自动生化分析仪,酶循环法检测Hcy、CHOD-PAD底物法测血清总胆固醇(TC)、酶比色法测甘油三酯(TG)、酶直接法测高密度脂蛋白(HDL-C)及低密度脂蛋白(LDL-C)、已糖激酶法测空腹血糖(FBG)及餐后2h血糖(PBG);采用MQ-2000PT(上海惠中医疗科技有限公司)糖化血红蛋白分析(HbA1C)仪,高效液相色谱法检测HbA1C;采用i2000SR Abbott(美国雅培公司)全自动化学发光免疫分析仪,化学发光微粒子免疫检测法测定C肽,包括空腹C肽(FCP)、 餐后2hC肽(PCP)。
1.3 统计学方法所有数据输入SPSS 17.0软件包,计量资料用t检验,计数资料用 χ2检验。
2 结果
2.1 两组治疗前后血糖控制情况两组治疗前FBG、PBG、HbA1C水平均无明显差异,治疗后两组各指标均低于治疗前,治疗后观察组低于对照组(P<0.05),见表1。
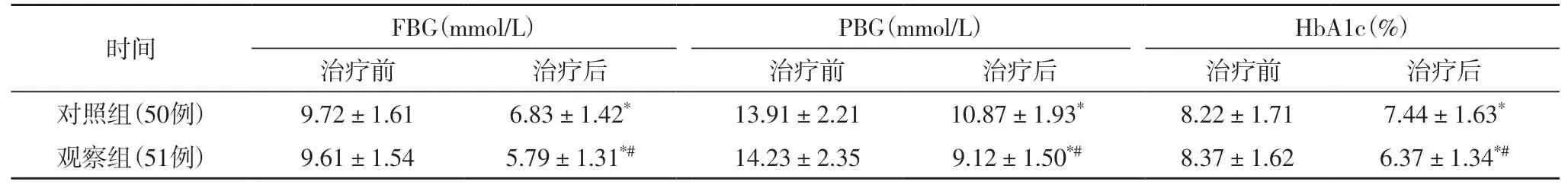
表1 两组治疗前后血糖控制情况
2.2 两组治疗前后血脂水平比较两组治疗前脂类水平无明显差异,治疗后观察组TC、TG、LDL-C、均低于对照组,HDL-C高于对照组,差异均有统计学意义(P<0.05),见表2。
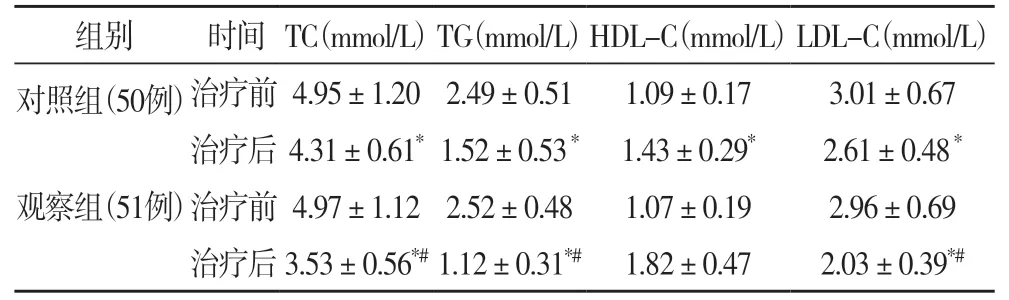
表2 两组脂类水平比较
2.3 两组炎性因子比较两组治疗前CRP、Hcy水平、FCP、PCP水平均无明显差异,治疗后,观察组CRP、Hcy水平均低于对照组,各组治疗后均低于治疗前;观察组FCP、PCP水平均高于对照组,各组治疗后均高于治疗前,差异均有统计学意义(P<0.05),见表3。

表3 两组炎性因子水平比较
2.4 两组不良反应观察组51例中发生不良反应1例,发生率1.96%,患者在治疗4d后出现恶心、中上腹不适,未经特殊处理,后自行缓解;对照组50例中发生不良反应2例,发生率为4.00%,均为低血糖事件,经调整胰岛素用量后未再发生。两组不良反应发生率差异无统计学意义(P<0.05)。
3 讨论
据研究,2型糖尿病在诊断时,其胰岛β细胞已下降为正常人的一半,且以每年5%的速度衰减[3]。导致胰岛β细胞衰减的原因与持续的胰岛素抵抗、炎性因子、氧化应激等对细胞的持续损伤有关。同时上述因素也是内皮细胞损害的原因。有学者认为,内皮功能障碍在2 型糖尿病首次诊断时就已经存在,持续的高血糖、高血脂、炎性因子等的刺激又会使这种损害加重,内皮功能降低,进而导致大血管、微小血管的病变[4]。
胰高血糖素样肽-1(GLP-1)是由胰高血糖素基因表达的一类肠促胰岛素,在机体摄取营养时由肠黏膜内分泌细胞分泌。在未进食时,机体中的GLP-1浓度很低,但在进食后迅速升高,使胰岛素的分泌加快,餐后血糖水平下降。GLP-1可被DPP-4迅速降解,而DPP-4 抑制剂则可抑制其降解,进而提高其有效活性,提高肠促胰岛素释放及水平,起到降糖效果。西格列汀是全球第一个投入使用的DPP-4抑制剂,其结构与DPP-4相似,通过与 DPP-4活性部位的竞争性结合,提高GLP-1及其他生物活性肽的活性,增加胰岛β细胞合成,进而促进胰岛素的分泌。西格列汀还可通过抑制糖尿病患者病理性亢进的食欲,减少其胃排空速度及热量摄入,从而减轻体重。由于GLP-1在体内血糖较低时,其降糖作用较低,其低血糖发生率也较低,因此西格列汀安全性较好。研究表明,西格列汀是一种治疗依从性和耐受性较好的新型降糖药物[5]。
持续皮下胰岛素泵入模拟正常胰岛素生物分泌模式,有利于调控胰岛素剂量,夜晚仅输注微量胰岛素,后半夜自动增加输注胰岛素,既避免了夜间低血糖发生,又预防了凌晨高血糖发生,使全日保持胰岛素正常生理水平。在有效控制高血糖的同时,使血糖水平保持稳定,避免血糖大幅度波动,从而降低糖毒性,保护胰岛β细胞,改善胰岛素抵抗。作为胰岛素类似物的门冬胰岛素,分子间聚合力低,药物起效快,皮下输注后40min达峰时间,作用可持续5h,具有血糖稳定、有较好的模拟生理胰岛素的分泌生物模式等特点,较普通中性可溶性人胰岛素控制高血糖效果明显[6]。本组资料中,观察组治疗10周后血糖水平、HbA1C水平均高于治疗前及对照组,提示西格列汀联合胰岛素可增加降血糖效果。
糖尿病已经被公认为是慢性炎症性疾病,动脉粥样硬化是糖尿病大血管病变的病理基础,而炎性因子如Hcy、CRP在动脉粥样硬化的发生发展中扮演重要角色。作为血管损伤性氨基酸的Hcy 被认为是动脉粥样硬化的独立风险因素[7]。高Hcy可导致血管壁内皮细胞的损伤和弹性改变及血管内血小板的聚集,进而导致粥样斑块的形成。高Hcy还可影响机体内糖类、脂类的代谢,增加糖毒性,增加内皮细胞损伤,及血管壁中脂质及糖蛋白的大量沉积,导致血栓形成,从而促进动脉硬化的发生发展。高Hcy导致内皮细胞损伤的原因与其能降低一氧化氮酶的活性,使一氧化氮合成减少有关,而后者是内皮细胞合成的重要活性物质。
CRP是一种较为敏感的非异性炎症指标,糖尿病患者中CRP增加与胰岛素抵抗有关。胰岛素对CRP的合成有阻断作用,而胰岛素抵抗时,胰岛素生理作用降低,导致肝脏合成CRP增加。大血管病变动脉粥样硬化也是导致CRP增加的因素。同时CRP也可促进动脉硬化的发生发展,其发生机制与氧自由基对血管内皮细胞的损伤、不稳定的斑块脱落有关。另外,CRP可刺激巨噬细胞对LDL的摄取及各种细胞因子的表达,增加其他炎症介质导致动脉粥样硬化的作用。因此对糖尿病患者,CRP可作为大血管病变的动态监测指标。
C肽是胰岛素原的一个多肽链,早期的研究认为C肽不参与生物活动,但近年来的研究认为C肽参与机体物质代谢及糖尿病相关并发症的发生发展,在糖尿病大血管病变中具有重要作用。研究认为,C 肽可促进2 型糖尿病早期大血管粥样硬化病变,其机制与C 肽可促进炎症反应及平滑肌细胞增殖有关。C肽可促进2型糖尿病患者血管内膜、内皮下间隙、部分中膜中斑块的形成和沉积[8],并促进炎性细胞如单核细胞、 CD4+淋巴细胞的趋附诱导炎症反应。C肽还可增强对参与动脉粥样硬化过程的趋化因子、细胞因子、粘附分子的基因具有调节作用的炎症基因核转录因子NF-κB,进而促进疾病进展[9]。此外,C肽通过激活细胞内的SRC激酶 、PI3(磷脂酰肌醇)激酶等诱导平滑肌细胞增殖,进而促进动脉硬化。另有研究发现,随着2型糖尿病的持续发展、胰岛B细胞功能的减退,C 肽会对大血管病变起保护作用,分析原因,可能与其可抑制高糖状态导致的血管平滑肌的增生,减少胰岛素对内皮和平滑肌细胞的负面作用[10]有关。
本组资料中,两组治疗10周后CRP、Hcy水平均较治疗前下降,但观察组下降更为明显。两组FCP、PCP水平较治疗前升高,亦为观察组上升更为明显。提示西格列汀联合胰岛素治疗后可明显降低2型糖尿病患者炎性因子CRP、Hcy水平,改善胰岛素功能,提高C肽水平,从而保护糖尿病大血管,延缓其病变。西格列汀对大血管有保护作用,其机制与增加一氧化氮水平、抑制动脉粥样硬化斑块的形成、抗氧化应激、保护血管内皮等有关。
血脂代谢紊乱是2型糖尿病患者心血管终点事件的危险因素,其发生与胰岛素的分泌减少和胰岛素抵抗关系密切。胰岛素分泌不足和胰岛素抵抗时,机体对非酯化的脂肪酸的释放增加但转化降低,使TC、LDL、TG的合成增加,LDL和HDL的受体活性降低,导致LDL水平升高。在高血糖情况下,LDL易被氧化,引起血管内皮受损,导致动脉内膜内巨噬细胞和平滑肌细胞胆固醇的大量聚集,导致动脉硬化。研究发现,DPP-4 抑制剂可明显降低2型糖尿病患者的血脂谱。其机制可能与该类药物抑制食欲及胃排空,使肠脂蛋白分泌受抑制,进而使血脂降低有关。胰岛素降低血脂的机制与其可上调脂蛋白脂肪酶MRNA的转录和翻译,增加脂蛋白脂肪酶的合成,从而促进脂肪分解有关。本组资料中,观察组治疗10周后其血脂水平均较治疗前及对照组明显降低,提示西格列汀联合胰岛素具有明显的降血脂作用。
总之,西格列汀联合胰岛素治疗可缓解2型糖尿病患者胰岛素抵抗,稳定血糖水平,降低早期大血管病变的炎性因子,延缓2型糖尿病心血管并发症的发生。
