三嗪功能化共价有机框架材料吸附去除水溶液中的抗生素
2020-09-11安书浩潘鹤林彭昌军
田 桢, 安书浩, 潘鹤林, 徐 婷, 彭昌军
(华东理工大学 1.化工学院;2.化学与分子工程学院,上海 200237)
抗生素的广泛使用在保证生命健康的同时也会带来水体污染等问题,高效去除水体中的残留抗生素是保障碧水青山的重要一环。抗生素常用的去除方法有物理法、化学法和生物法[1]。在众多分离方法中,物理吸附法因其效率高、成本低、环境友好等优势已成为人们关注的热点。迄今为止,人们已尝试将各种固体材料作为吸附剂用于水体中抗生素的去除,如活性炭[2]、氧化石墨烯(GO)[3]、黏土矿物[4]、树脂[5]、微孔碳和介孔碳[6]、介孔A-MCM-41[7]、氧化石墨烯聚苯乙烯树脂复合材料(GO/PS)[8]、金属有机框架材料Urea-MIL-101[9]、多孔有机凝胶材料[10]等,它们都对特定的抗生素表现出较好的吸附分离性能。
共价有机框架材料(COFs)[11]具有较大孔隙率和比表面积、灵活可控的孔结构、较高化学及热稳定性等特点,近年来,人们已尝试合成了各种功能性的COFs 材料并将其应用于气体吸附[12-13]、重金属离子[14]和染料[15]的吸附分离中,但是利用COFs 材料去除废水中抗生素方面的应用鲜有报道。本文设计了含三嗪官能团的2,4,6-三(4-氨基联苯)-1,3,5-三嗪(TABT)单体,并将TABT 和均苯四甲酸酐(PMDA)在热溶剂条件下反应,制备了三嗪功能化结晶聚酰亚胺共价有机框架材料(TF-COF),研究了TF-COF对盐酸四环素(TCH)、强力霉素(DOX)、盐酸环丙沙星一水合物(CIPHM)和盐酸莫西沙星(MXFH)等抗生素的吸附效果,获得了吸附等温线和吸附动力学相关数据,并对TF-COF 的循环使用性能进行了探究。
1 实验部分
1.1 原料和试剂
4-氨基-4'-氰基联苯:纯度95%,梯希爱(上海)化成工业发展有限公司;三氟甲烷磺酸:纯度98%,阿拉丁试剂(上海)有限公司;均苯四甲酸酐(PMDA):纯度98%,梯希爱(上海)化成工业发展有限公司;TCH:纯度99%,上海阿达玛斯试剂有限公司;DOX:纯度98%,萨恩化学技术(上海)有限公司;CIPHM:纯度98%,九鼎化学(上海)科技有限公司;MXFH:纯度99%,上海思域化工科技有限公司;阿莫西林三水物(AMXT):纯度98%,上海易恩化学技术有限公司;头孢曲松钠3.5 水合物(CROSH):纯度98%,梯希爱(上海)化成工业发展有限公司;硫酸链霉素(SS):纯度95%,梯希爱(上海)化成工业发展有限公司;磺胺二甲嘧啶钠(SMS):纯度98%,上海麦克林生化科技有限公司。
TCH、DOX、CIPHM、MXFH 的分子结构分别如图1 (a)、(b)、(c)、(d)所示,它们的相对分子质量分别为480.9、444.44、385.82、437.89。

图1 盐酸四环素(a)、强力霉素(b)、盐酸环丙沙星一水合物(c)和盐酸莫西沙星(d)的分子结构Fig.1 Molecular structure of TCH (a), DOX (b), CIPHM (c) and MXFH (d)
1.2 仪器和表征
红外光谱和核磁共振碳谱(13C-NMR)分别采用傅里叶变换红外光谱仪(FT-IR,美国尼高力公司,Nicolet 6700 型)和核磁共振波谱仪(德国布鲁克公司,Bruker AVIII 400MHz 型)表征。材料形貌采用扫描电子显微镜(SEM,日本日立公司,S-3400N 型)和透射电子显微镜(TEM,日本电子株式会社,JEM-2100F型)表征。材料衍射图谱和热重曲线分别采用多晶粉末X 射线衍射仪(PXRD,日本理学电机公司,D/Max 2550 VB/PC 型)和热重分析仪(TGA,德国耐驰公司,STA 499 型)表征。材料孔性质通过采用比表面积与孔隙度分析仪(BET,美国麦克仪器公司,TriStar II 3020 型)测定77 K 下N2的吸附-脱附等温曲线获得。溶液中抗生素浓度采用紫外-可见分光光度计(UV-vis,日本岛津公司,UV-2550 型)测定后获得。
1.3 材料合成
1.3.1 单体TABT 的合成 TABT 的合成步骤参考文献[15],具体为:在50 mL 带搅拌子的圆底烧瓶中加入675 mg 4-氨基-4'-氰基联苯,烧瓶用恒温器冷却至0 °C 后加入5 mL 三氟甲烷磺酸(该酸是超强酸,反应是放热反应,室温下反应会导致烧瓶内温度升高从而有一定危险性)。关闭恒温器,烧瓶温度自然恢复至室温1 h 后,打开磁力搅拌器反应24 h。随后关闭搅拌器,将烧瓶中的混合物转移到装有500 mL 浓度为2 mol/L NaOH 溶液的烧杯中,将烧杯放入超声清洗器中超声,析出黄色固体,抽滤,并用超纯水多次洗涤,直至滤液呈中性。将得到的固体放入烘箱中,在80 °C 下烘干12 h。随后将粗产品放入50 mL圆底烧瓶中,倒入乙醇搅拌3 h 后抽滤,用乙醇清洗固体,将固体放入烘箱中,在80 °C 下烘干12 h,最后得到单体TABT。
1.3.2 TF-COF 材料的合成 称取116.4 mg TABT 和65.4 mg PMDA 放入耐热管中,并加入1 mLN-甲基吡咯烷酮和1 mL 均三甲苯,超声后加入0.1 mL 异喹啉,超声10 min 得到均匀分散的混合物。3 次冷冻-解冻循环脱气后,将耐热管密封放入烘箱中,在180 °C下反应5 d。随后关闭烘箱,烘箱温度降至室温后取出耐热管,抽滤收集管中沉淀物,并用四氢呋喃反复冲洗沉淀物,将沉淀物放入真空烘箱在80 °C 下干燥24 h,获得的固体材料即为TF-COF。图2 示出了TF-COF 的合成示意图。
1.4 吸附实验
1.4.1 吸附等温线 分别配制质量浓度为0.5~1 000 mg/L的TCH、DOX、CIPHM、MXFH 4 种抗生素溶液,分别量取5 mL 并加入2.5 mg的吸附剂TF-COF。放入振荡器,25 °C 下使吸附剂与溶液充分混合。恒温振荡24 h 后过滤,采用紫外-可见分光光度计检测滤液中抗生素质量浓度。采用公式(1)计算材料的平衡吸附量:

其中:qe是平衡吸附量,mg/g;c0和ce分别是抗生素溶液的初始质量浓度和平衡质量浓度,mg/L;V为溶液的体积,mL;m是吸附剂的质量,mg。

图2 TF-COF 合成示意图Fig.2 Synthesis schematic diagram of TF-COF
1.4.2 吸附动力学 分别配制体积为1 000 mL、初始质量浓度为60 mg/L的TCH、DOX、CIPHM、MXFH 4 种抗生素水溶液,分别量取5 mL 并加入2.5 mg 吸附剂TF-COF。放入振荡器,在预定时间t内将混合物过滤,滤液采用紫外-可见分光光度计检测抗生素在t时刻的质量浓度ct,同理按照公式(1)计算t时刻的吸附量qt。
1.4.3 溶液pH 的影响 分别配制体积为1 000 mL、初始质量浓度为60 mg/L 的4 种抗生素水溶液,并倒入不同的烧杯中,调节溶液pH 为2~10,考察pH 对吸附性能的影响。
1.4.4 吸附-脱附循环 分别配制初始质量浓度为60 mg/L 的TCH、DOX、CIPHM、MXFH 4 种抗生素溶液进行吸附实验,再用超纯水和乙醇(体积比为1∶1)混合溶液多次洗涤过滤并收集TF-COF,在80 °C下真空干燥12 h 后用于下一次吸附实验。
2 结果与讨论
2.1 材料表征
图3(a)所示为TF-COF 的傅里叶变换红外光谱,在1 778 cm−1和1 722 cm−1处分别出现了五元酰亚胺环羰基(C=O)的不对称和对称伸缩振动峰,在1 507 cm−1处出现了三嗪环的C=N 面内环振动峰。图3(b)所示为TF-COF 的固体核磁共振碳谱,在化学位移约170 处的峰证实了框架中存在三嗪环[16],化学位移164 处的峰对应于酰亚胺环的羰基碳[17],127~136 处的重叠峰归属于苯中芳香碳。由此可判断TF-COF 是由聚酰亚胺连接而成的三嗪功能化的框架材料。

图3 TF-COF 的傅里叶变换红外光谱(a)和核磁共振碳谱(b)Fig.3 FT-IR spectra (a) and 13C-NMR spectra (b) of TF-COF
通过PXRD 测试表征TF-COF 材料结构的规整性。如图4(a)所示,在2θ为2.16 °处有高强度的衍射峰,说明TF-COF 具有长程有序的晶型结构。结合红外光谱及固体核磁碳谱,可见TF-COF 是三嗪功能化结晶聚酰亚胺共价有机框架材料。图4(b)所示为TF-COF 的热重分析结果,表明材料在600 °C 以下没有明显损失,加热到800 °C 仍有60%剩余材料,说明TF-COF 具有非常好的热稳定性。
通过SEM 和TEM 对材料的微观形貌进行表征,分别如图5(a)和图5(b)所示。表明TF-COF 是由大量球形颗粒聚集而成,且具有片状层层堆叠的形态。
通过测试77 K 下N2吸附-脱附等温线表征TFCOF 的孔性质,如图6(a)所示。标准状态下相对压力(p/p0)较低时吸附量快速增大,说明TF-COF 存在大量的微孔。在相对压力为0.1~0.4 时吸附线出现第2 个坡度,可判断材料中也存在介孔。经非定域密度泛函理论计算得到材料的孔径分布曲线,如图6(b)所示,可见孔径集中分布在1.1 nm 和3.6 nm 处。测量得TF-COF 的BET(Brunauer-Emmett-Teller)比表面积为794 m2/g,孔体积为0.53 cm3/g,表明TF-COF具有较好的孔隙率。

图4 TF-COF 的PXRD 图(a)和热重分析图(b)Fig.4 PXRD (a) and TGA (b) of TF-COF

图5 TF-COF 的SEM (a)和TEM (b)Fig.5 SEM (a) and TEM (b) of TF-COF

图6 TF-COF 的N2 吸附-脱附等温线(a)以及孔径分布(b)Fig.6 N2 adsorption-desorption isotherms (a) and pore size distribution (b) of TF-COF
2.2 吸附选择性
分别配制1 000 mL、质量浓度为100 mg/L 的TCH、DOX、CIPHM、MXFH、AMXT、CROSH、SS和SMS 溶液,各取5 mL,并分别加入2.5 mg 的吸附剂TF-COF,24 h 后过滤,由此获得TF-COF 对不同抗生素的吸附效果,结果见图7。
图7 表 明, TF-COF 对AMXT、 CROSH、 SS、SMS 的吸附量小于30 mg/g,而对CIPHM、TCH、DOX、MXFH 的吸附量分别为110、131、154、157 mg/g,说明TF-COF 具有吸附抗生素的能力,但有一定选择性。材料的选择性和抗生素分子的结构、材料与抗生素分子间的静电相互作用有关。TCH、DOX、CIPHM、MXFH 的分子大小适中,容易吸附在材料上。在后文中,将选择TCH、DOX、CIPHM、MXFH作为研究对象。

图7 TF-COF 对不同抗生素的吸附效果Fig.7 Adsorption effects of TF-COF on different antibiotics
2.3 吸附等温线
图8 所示为TF-COF 质量浓度对抗生素吸附的影响。由图8 可知,在低质量浓度下,材料对抗生素的吸附效果相差不大;在高质量浓度下,材料对TCH和DOX 的吸附效果更好。在实验的质量浓度范围内,TF-COF 对TCH 和DOX 的吸附没有达到饱和,但对CIPHM 和MXFH的吸附已达饱和。
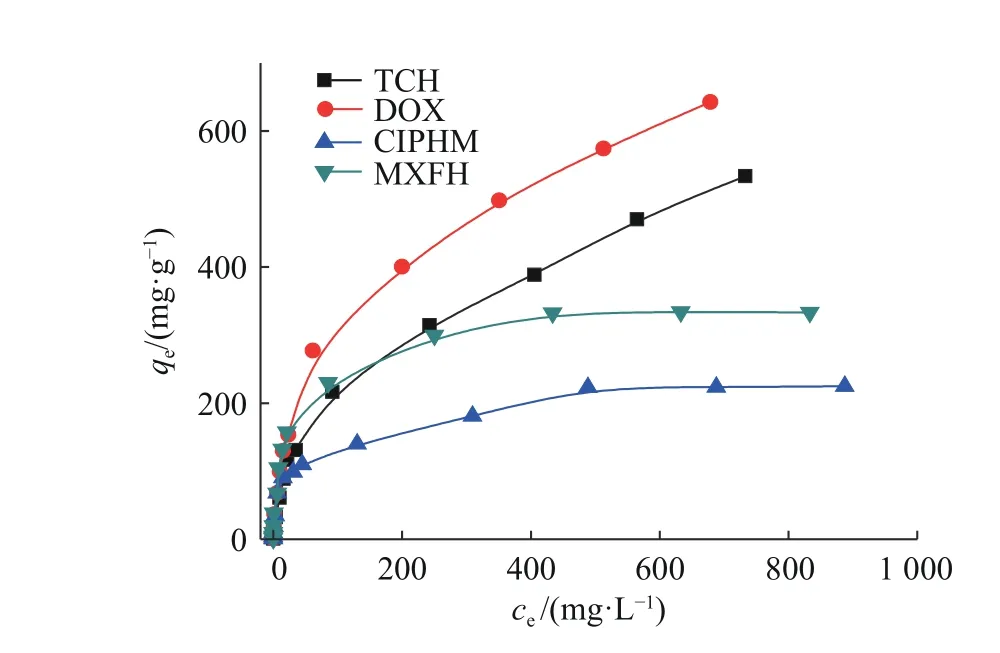
图8 TF-COF 质量浓度对抗生素吸附的影响Fig.8 Effects of the mass concentration of TF-COF on the adsorption of antibiotics
吸附等温线可用来描述吸附平衡时溶液中的吸附质在溶液和吸附剂中的分配情况。为定量研究TF-COF 对TCH、DOX、CIPHM、MXFH 4 种抗生素的吸附行为,评估材料对抗生素的最大吸附量,采用Langmuir 等温模型和Freundlich 等温模型进行了拟合[18]。

其中:qmax为材料的最大吸附量,mg/g;b是Langmuir常数,L/mg;k是Freundlich 常数;n是非均质系数。
图9 示出了TCH、DOX、CIPHM、MXFH 4 种抗生素的Langmuir等温线和Freundlich 等温线,表1给出了相应的拟合结果。由图9 和表1 可知,TFCOF 对TCH 和DOX 的吸附符合Freundlich 模型,对CIPHM 和MXFH 的吸附符合Langmuir 模型。TF-COF 对TCH、DOX、CIPHM 和MXFH 的吸附用Langmuir 模型拟合的最大吸附量分别为518、625、227、337 mg/g。
表2 示出了一些固体吸附剂对4 种抗生素的吸附效果。相较于其他固体吸附剂,TF-COF 有大的比表面积和孔容,孔径分布较为规整,热稳定性好,对4 种抗生素表现出较大的吸附量,表明TF-COF对这4 种抗生素具有良好的吸附效果。
2.4 吸附动力学
图10(a)示出了时间对TF-COF 吸附4 种抗生素的影响。由图可知,在0~60 min 内,吸附量随时间增加而迅速增加,随后趋于平缓,并最终达到平衡。TF-COF 对TCH 和DOX 的吸附平衡时间约为480 min,对CIPHM 和MXFH 的吸附平衡时间约为600 min。
图10(b)示出了准二级动力学模型对吸附过程的拟合结果。准二级动力学模型方程[26]如式(4)所示。由图10(b)可知,准二级动力学模型对4 种抗生素吸附过程的拟合结果很好(相关系数R2> 0.99),说明TF-COF 对TCH、DOX、CIPHM 和MXFH 的吸附符合准二级动力学模型。

式中:k2是准二级吸附速率常数, g/(mg·min)。

图9 TF-COF 对4 种抗生素吸附的Langmuir 等温线(a~b)和Freundlich 等温线(c~d)Fig.9 Langmuir isotherms (a~b) and Freundlich isotherms (c~d) of TF-COF adsorption for four antibiotics
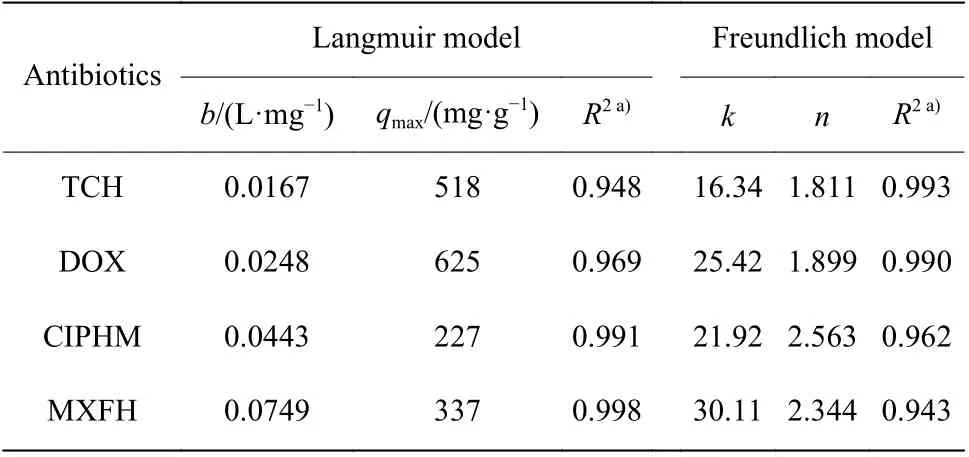
表1 TF-COF 对4 种抗生素吸附的Langmuir 模型和Freundlich模型拟合结果Table 1 Fitting results of Langmuir model and Freundlich model of TF-COF adsorption for four antibiotics
2.5 溶液pH 的影响与循环使用性能
pH 对TF-COF 的吸附影响见图11。实验发现,当pH 为2~7 时,吸附量随pH 的增加逐渐增加;当pH=7 时,TF-COF 对4 种抗生素的吸附量最大;当pH>7 时,吸附量随pH 的增加逐渐减小。TF-COF 在pH=7 时对TCH、DOX、CIPHM 和MXFH 的吸附效果最好,原因可能是在酸性条件下TCH、DOX[27]、CIPHM 和MXFH[25]主要以阳离子的形态存在,TFCOF 的三嗪官能团会质子化而带正电荷,抗生素和材料间会相互排斥,随着酸性减弱,4 种抗生素主要以中性分子的形态存在于溶液中,吸附效果逐渐变好;在碱性条件下,材料的性能不太稳定,碱性越强,吸附效果越差。
TF-COF 吸附-脱附循环5 次后,对TCH、DOX、CIPHM、MXFH 的吸附效果分别如图12 (a)、(b)、(c)、(d)所示。图12 中0 次表示未使用过的TF-COF对4 种抗生素的吸附。由图可知,经过5 次吸附-脱附循环后,TF-COF 对TCH、DOX、CIPHM 和MXFH的吸附量变化很小,说明TF-COF 的再生能力好,可以重复使用。
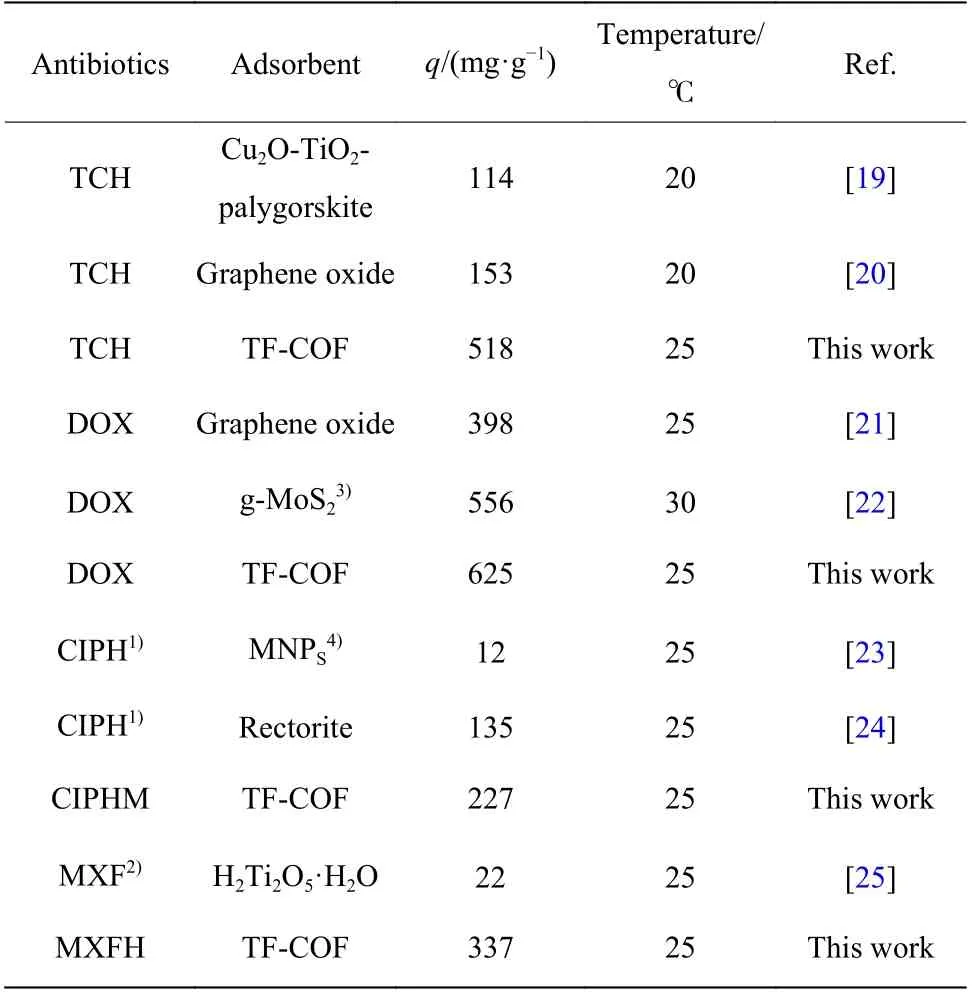
表2 不同材料对4 种抗生素的吸附效果比较Table 2 Comparison of adsorption results of different materials for four antibiotics
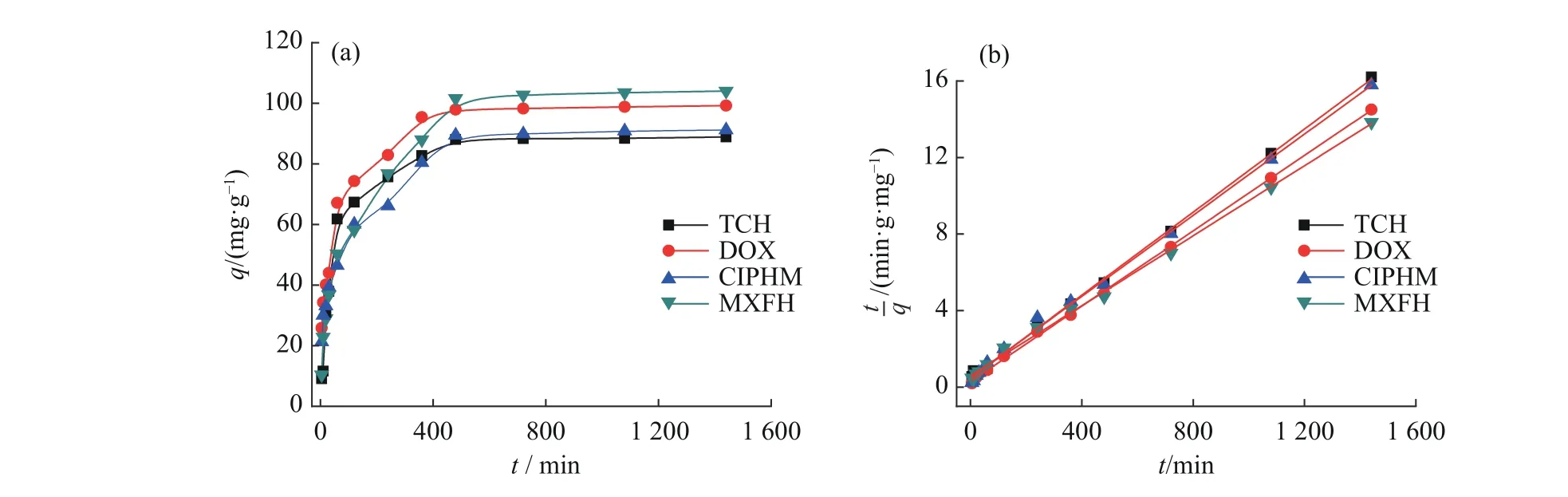
图10 时间对TF-COF 吸附的影响(a)和准二级动力学模型拟合曲线(b)Fig.10 Effect of the time on TF-COF adsorption (a) and pseudo-second-order kinetic model fitting curves (b)

图11 pH 对TF-COF 吸附抗生素的影响Fig.11 Effect of pH on TF-COF adsorption for antibiotics
3 结 论
(1)利用含三嗪官能团的TABT 制备新的具有晶型结构的材料TF-COF,其孔结构比较规整,比表面积较大,且具有非常好的热稳定性。
(2)TF-COF 对抗生素有一定吸附选择性,对TCH、DOX、CIPHM 和MXFH 表现出较高的吸附量。TF-COF 对TCH 和DOX 的吸附符合Freundlich模型,对CIPHM 和MXFH 的吸附符合Langmuir 模型。在25 °C 时,TF-COF 对TCH、DOX、CIPHM 和MXFH的吸附用Langmuir 模型拟合的最大吸附量分别为518、625、227、337 mg/g。

图12 TF-COF 重复使用效果Fig.12 Reuse effects of TF-COF
(3)吸附过程可采用准二级动力学模型描述。TF-COF 在pH=7 时对4 种抗生素的吸附效果最好。5 次循环后,TF-COF 对抗生素的吸附效果基本不变,表现出良好的循环使用性能。
(4)TF-COF 对某些抗生素有较好的吸附效果,为COFs 材料吸附去除水体中抗生素的应用研究提供了参考。
