MICP技术对Mn(Ⅱ)、Cr(Ⅵ)污染土壤的修复效果
2020-09-08许朝阳
许朝阳, 张 贺, 杨 贺, 许 宁
(扬州大学建筑科学与工程学院, 江苏 扬州 225009)
由于工业废水排放和农药、化肥使用量的不断增加,我国的土壤重金属污染问题日趋严重.土壤重金属污染会导致农作物产量和质量下降[1], 影响环境和经济可持续发展, 对生命健康造成严重威胁, 亟须有效治理.
微生物诱导碳酸盐沉淀(microbially induced carbonate precipitation, MICP)是一种通过生物沉淀固定重金属离子的污染场地修复技术[2], 因其环保高效的优点而受到国内外学者的关注.Kumari等[3]认为对污染土壤进行生物修复的主要目标之一是降低重金属离子的生物利用度, 即通过MICP过程使大部分重金属离子由可溶交换态转变为碳酸盐沉淀的形式;DeJong等[4]发现在MICP固定土壤重金属的诸多反应机制中,通过微生物代谢的生物酶水解尿素生成碳酸钙效率最高; Kang等[5]从废弃的金属矿土壤中分离、筛选出SporosarcinasoliB-22菌种, 通过该菌种的生物矿化过程使铜离子去除率达61.8%; 钱春香等[6]利用碳酸盐矿化菌的矿化作用降低溶液中游离的铜离子含量, 有效去除率可达90%以上; Zhao等[7]使用从矿山土壤中分离的GZ-22菌株, 通过MICP技术将可溶性的Cd2+以CdCO3的形式固定于土壤中; 许朝阳等[8]利用芽孢八叠球菌诱导碳酸钙沉积分别修复被铜、铅污染的土壤, 证明了MICP技术用于吸附和固定重金属离子的有效性; Li等[9]使用从土壤中分离出的6种菌株对重金属进行微生物矿化实验, 铅离子去除率接近100%.
重金属污染土壤中往往存在多种金属离子.了解MICP过程中不同重金属离子之间的竞争关系并合理利用,可改善修复效果.另外, 氨作为尿素水解的主要副产物,其挥发和氧化将导致土壤中的pH值下降,易引起碳酸钙溶解[10].MICP方法对重金属污染土在酸性条件下的修复稳定性仍有待深入研究.本文对MICP方法修复Mn(Ⅱ)、Cr(Ⅵ)污染土的效果进行研究, 并在不同酸性条件下测定修复土样中各结合形态的锰、铬离子含量的变化, 分析修复土壤的酸性稳定性;对含Mn(Ⅱ)、Cr(Ⅵ)的溶液进行模拟修复实验, 以研究Mn(Ⅱ)、Cr(Ⅵ)在微生物矿化修复过程中的竞争关系.
1 实验材料
1.1 微生物矿化材料
实验采用能代谢大量脲酶的嗜碱菌巴氏芽孢八叠球菌(ATCC 11859), 培养基成分如表1所示, pH值为8.8~9.0.将接种后的培养基在30 ℃的摇床中恒温培养24 h得到菌液, 其600 nm波长下的吸光度为0.9, 脲酶活性(电导率仪测试3 mL待测菌液与27 mL浓度为1.1 mol·L-1的尿素混合溶液在5 min内的平均电导率变化值)为1.1 mS·cm-1·min-1.MICP反应液为含1.0 mol·L-1氯化钙和1.0 mol·L-1尿素的混合溶液.

表1 培养基成分
1.2 模拟污染土和污染溶液的制备
对扬州市部分主干道附近土壤、垃圾填埋场渗滤液、垃圾焚烧厂底灰和化工厂附近土壤进行采样, 以检测各样本中Mn(Ⅱ)、Cr(Ⅵ)最高含量为准分别配置Mn(Ⅱ)、Cr(Ⅵ)污染土.实验所用原土样为取自长江中下游的粉土, 其物理性质及其Mn(Ⅱ)、Cr(Ⅵ)含量见表2.称取2.740 g MnCl2·4H2O溶于300 mL去离子水中, 倒入1 kg实验粉土中, 充分搅拌均匀后自然风干30 d, 对风干后的污染土壤研磨过筛, 得到Mn(Ⅱ)含量为1.111 g·kg-1的锰污染土样品; 同样地, 称取 2.750 g K2Cr2O7以相同方法制备Cr(Ⅵ)含量为1.062 g·kg-1的铬污染土样品.

表2 粉土的物理性质及其Mn(Ⅱ)、Cr(Ⅵ)含量
分别向1 L的定容瓶中加入5.400 g的MnCl2·4H2O和4.230 g的K2Cr2O7, 分别用去离子水定容制得浓度为1.500 g·L-1的Mn(Ⅱ)污染液和Cr(Ⅵ)污染液, 并用相同方法制备含1.500 g·L-1Mn(Ⅱ)和1.500 g·L-1Cr(Ⅵ)的混合污染溶液, 记为Mn(Ⅱ)+Cr(Ⅵ)污染液.
2 实验部分
2.1 污染土修复实验
将50 mL菌液和50 mL反应液均匀倒入150 g污染土中, 30 ℃下静置10 d为1次修复;再取50 mL菌液和50 mL反应液,以相同条件对同一污染土进行第2次和第3次修复.另将100 mL菌液加入150 g污染土中,在相同条件下修复3次,作为空白对照组.每组修复结束均按照四分法取样2 g, 每组平行取3个试样,采用Tessier五步连续提取法[11], 利用美国Thermo Scientific iCE 3000原子吸收光谱仪对修复前后污染土中各种形态重金属离子的含量进行测定.
2.2 污染溶液修复实验
将各种污染液分别与等体积的菌液和反应液均匀混合(实验测定菌种对Mn(Ⅱ)、Cr(Ⅵ)的耐受浓度分别为1 300, 900 mg·L-1),然后在30 ℃下静置10 d, 备用.取相同体积Mn(Ⅱ)+Cr(Ⅵ)污染液、液体灭菌培养基和反应液混合后进行相同处理作为空白对照组. 等体积菌液和反应液混合后, 在30 ℃下静置10 d生成的沉积物作为基础沉积物.各组污染溶液和空白对照组中的重金属离子含量由原子吸收光谱仪进行测定.各组污染溶液中沉积物和基础沉积物使用日立S-4800场发射扫描电镜(FESEM)、美国Thermo Noran能谱分析仪(EDS)和德国Bruker AXS D8 Advance多晶X射线衍射仪(XRD)进行表征.
2.3 修复土壤的酸性稳定性
3 结果与分析
3.1 污染土修复效果
经原子吸收光谱仪测定, Mn(Ⅱ)、Cr(Ⅵ)污染土中可交换态Mn(Ⅱ)、Cr(Ⅵ)的初始含量分别为570.29, 480.77 mg·kg-1, 经MICP方法修复后土壤中可交换态Mn(Ⅱ)、Cr(Ⅵ)含量如表3所示.由表3可见, 随修复次数增加, Mn(Ⅱ)、Cr(Ⅵ)去除率呈上升趋势,污染土经过3次微生物矿化修复后, 可交换态Mn(Ⅱ)、Cr(Ⅵ)去除率高达85.64%和77.56%,而不含矿化反应液的空白对照组中,修复前后土壤中的可交换态Mn(Ⅱ)、Cr(Ⅵ)含量变化较小.
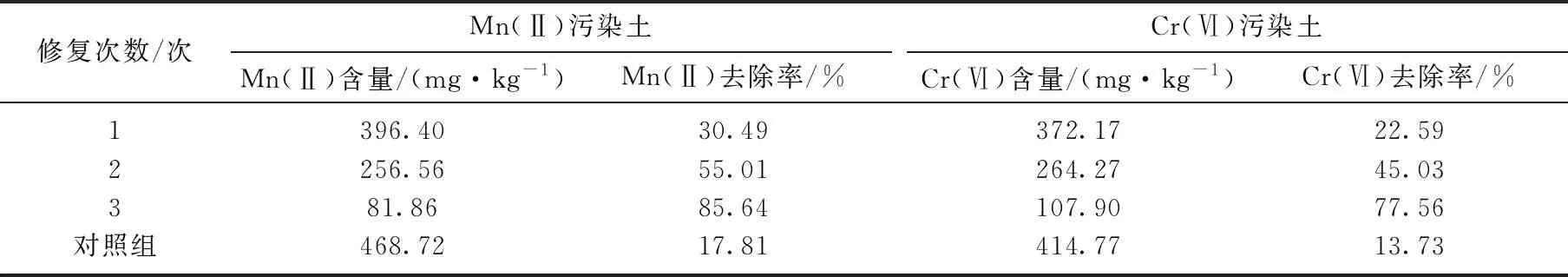
表3 经MICP方法修复的污染土壤中可交换态Mn(Ⅱ)、Cr(Ⅵ)的含量及去除率
图1为修复前后污染土中各结合形态重金属离子的含量.由图1可知,经微生物矿化修复后,污染土中的交换态重金属离子含量明显降低;而其余结合形态的重金属离子含量均有一定程度的增加,其中碳酸盐结合态含量增幅明显.由此可见微生物矿化方法可以将污染土中的可交换态重金属离子有效转化为其他相对稳定的形态.这是由于在微生物矿化反应中,尿素水解菌通过代谢生物酶分解尿素产生的碳酸根与重金属离子结合,使其由可交换态转变为碳酸盐形态, 降低了重金属离子的生物有效性[13], 实现对重金属离子污染土壤的修复.而在空白对照组中缺少底物和钙源,微生物矿化反应无法进行, 因此污染土中可交换态重金属离子含量未发生明显变化.
3.2 污染溶液修复效果
表4为修复后各污染溶液中的重金属离子平均含量.由表4可见, MICP方法修复Mn(Ⅱ)污染液的效果优于Cr(Ⅵ)污染液, 锰离子的平均去除率达65.90%; 在Mn(Ⅱ)+Cr(Ⅵ)污染液中, 锰离子的去除效果依然优于铬离子.而对照组中锰、铬离子的去除率仅为2.85%和2.30%, 这是由于菌种在MICP过程中会释放尿素水解酶,无菌种的对照组中的尿素则无法水解,无法产生与钙离子结合的碳酸根离子,因此MICP过程无法实现.
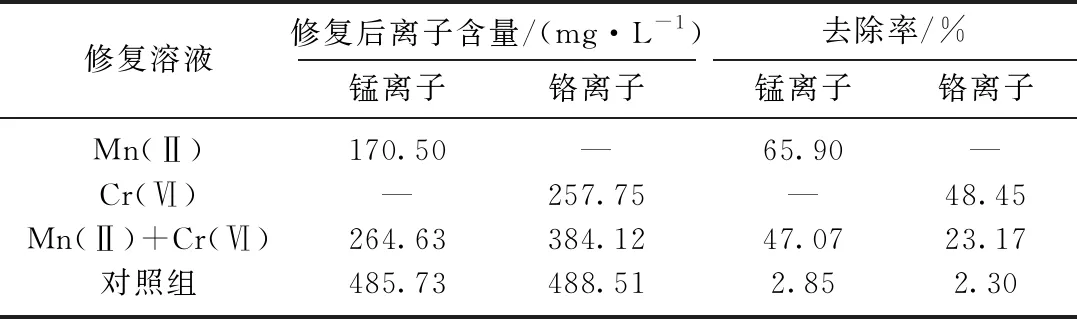
表4 MICP方法对Mn(Ⅱ)、Cr(Ⅵ)污染液的修复效果
从图2所示的溶液沉积物电镜图可见, 基础沉积物晶体大多呈球状, 且相对分散; Mn(Ⅱ)污染液的修复沉积物晶体多以簇状团聚形态存在, 簇状结构的间隙为吸附锰离子提供了空间; Cr(Ⅵ)污染液的修复沉积物以团聚的球状晶体居多,其团聚过程有助于包裹铬离子; 而Mn(Ⅱ)+Cr(Ⅵ)污染液的修复沉积物晶体形貌较分散, 无明显特征.从表5所示的EDS分析结果可见, 沉积物表面有一定量的锰、铬元素,说明在微生物矿化过程中,沉积物可吸附或包裹锰、铬离子,将游离态的重金属离子转变为团聚态矿化产物[6], 达到修复污染液的目的.在Mn(Ⅱ)+Cr(Ⅵ)污染液中的沉积物表面, Mn元素质量百分比大于Cr, 这与表4的结果相符,说明锰、铬离子在转化为碳酸盐结合态过程中存在竞争关系.有研究表明,当有多种重金属离子竞争相同结合位点时, 吸附能力较强的金属离子会从结合位点上取代吸附能力较弱的金属离子[14].在竞争结合位点的过程中,锰离子的吸附能力可能更强,故沉积物中的锰元素的相对含量较高.图3为修复后沉积物的XRD图谱.由图3可见, Mn(Ⅱ)+Cr(Ⅵ)污染液修复沉积物的图谱与Mn(Ⅱ)污染液修复沉积物不同, 但与Cr(Ⅵ)污染液修复沉积物相似,均以亚稳态的球霰石晶型碳酸钙为主.由于球霰石易于溶解,且Cr(Ⅵ)本身对矿物菌的生物活性影响较大, 因此Cr(Ⅵ)污染液的修复效果不如Mn(Ⅱ)污染液, 这与表4中的结果一致.
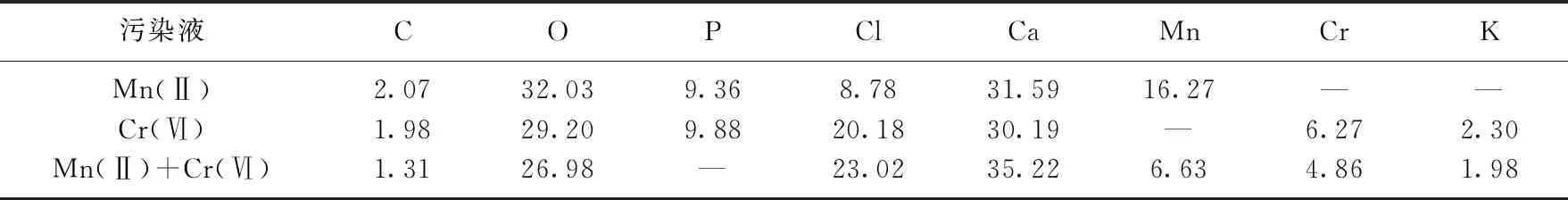
表5 不同溶液修复沉积物表面元素质量百分比
3.3 锰、铬修复土的酸性稳定性试验结果
修复后的Mn(Ⅱ)、Cr(Ⅵ)污染土在不同pH值的酸雨模拟液中浸泡60 d后, 其不同形态的重金属离子含量百分比如图4所示.由图4可见,经酸雨模拟液浸泡后, 可交换态Mn(Ⅱ)和Cr(Ⅵ)含量占比均增加, 且pH值越低, 可交换态离子的增量越大, 如在pH值为2.5的强酸雨中浸泡60 d, 可交换态Mn(Ⅱ)和Cr(Ⅵ)含量平均占比与浸泡前相比分别增加了20.17%和27.28%;而酸雨模拟液浸泡后土壤中碳酸盐结合态的锰和铬离子占比均减少,其他形态的含量占比则无明显变化.其主要是因为微生物矿化反应使锰、铬离子吸附、包裹于碳酸盐沉积物上,而酸雨模拟液使沉积物分解,导致重金属离子释出; 另一方面,酸雨模拟液使土壤酸化,削弱了沉积物对重金属离子的吸附能力[15],导致原先被固定的重金属离子释出,且pH值越低,土壤酸化越明显,可交换态重金属离子的释出量越多.对比图4(a)(b)可见,酸雨浸泡后土中可交换态铬离子的含量百分比增量高于锰离子, 可能是因为同样的土壤酸化程度下,锰离子比铬离子的吸附力较强, 因此Mn(Ⅱ)污染土在酸性环境下的修复稳定性优于Cr(Ⅵ)污染土.
