利用结构控制与物理包覆提高SnO2电化学性能的研究进展*
2020-09-04李玲芳原志朋范长岭
李玲芳,原志朋,胡 壮,范长岭
(1.湖南文理学院 机械工程学院,湖南 常德,415000;2.湖南大学,材料科学与工程学院,长沙,410082)
0 引 言
由于化石燃料的快速消耗以及对电动汽车、电子便携设备和可再生能源需求的不断增长,可充电电池作为电能储存装置备受关注。在多种可充电电池中,锂离子电池(LIBs)因其高能量密度(≈100~265 Wh/kg)、高输出电压(≈3.6~3.8 V)和长循环寿命(≈500~1 000次)而备受关注。2019年,诺贝尔化学奖被授予约翰G·B.Goodenough、M.S.Whittingham和A.Yoshino,以表彰他们在LIBs的发明和发展方面所做的努力,进一步证明了锂离子电池的重要性。目前,锂离子电池在电动汽车与混合动力汽车上的应用是研究者们关注的重点,要实现锂离子电池在电动汽车上的应用,则需提高锂离子电池的能量密度,研发比容量超过目前商用电极材料2~3倍的新型电极材料。
负极材料作为锂离子电池的重要组成部分,一直是研究的重点。金属氧化物作为负极材料的具有很高的理论容量,如钛基氧化物(TiO2和Li4Ti5O12)、锰基氧化物(MnO、Mn3O4、Mn2O3和MnO2),铁基氧化物(Fe3O4和Fe2O3)、Co3O4、NiO和SnO2等。二氧化锡(SnO2)以其高的理论比容量(1494 mAh/g)、安全的工作电压(0.3-0.5V vs Li/Li+)、天然的丰度、低成本和环境友好性而被认为是最重要的下一代锂离子电池负极材料料之一。对于SnO2电极,电化学过程包括以下两个反应(分别为转化反应与合金化反应)[1]:SnO2+4Li++4e-↔Sn+2Li2O,Sn+xLi++xe-↔LixSn(0≤x≤4.4)。即在放电过程中,锂首先与氧结合形成无定形的Li2O,同时金属锡被还原出来,分散在无定型的网格中,无定型的网格起到了缓冲介质的作用,因此改善了材料的循环性能;随后锂与锡发生合金化反应形成LixSn。在放电过程中,第二个反应是完全可逆的,但第一步的可逆性尚有争议[2]。有研究表明[3-5],对于微米级SnO2材料,第一反应被认为是不可逆的,因此理论容量约为780 mAh/g。而纳米级SnO2的第一反应可逆/部分可逆,理论容量最高可达1 494 mAh/g。
目前已有一些综述性文献从不同角度讨论了SnO2作为锂离子电池负极材料的研究进展。马昊[6]等在综述锡基负极材料的论文中谈及了锡基氧化物的特殊结构制备手段,Chen[]等详细讨论了各种纳米结构的SnO2,并简要介绍了SnO2石墨烯复合材料;Wu等[]在关于石墨烯/金属氧化物复合电极的材料的综述中列举了2009—2011年报道的SnO2/石墨烯纳米复合材料作为锂离子电池负极材料的典型实例;Deng[9]则综述了SnO2/石墨烯纳米复合材料的合成方法与结构优化问题。但这些综述文献中都只强调了SnO2与石墨烯的协同效应,没有对SnO2近年来的发展进行全面论述。
本文首先分析了SnO2负极材料在储锂过程中的电化学性能特点,然后结合本实验室的工作,综述了目前通过微观结构控制与构建物理包覆层来缓解其储锂过程中膨胀、粉化与团聚问题的国内外研究工作。虽然本文只关注SnO2基复合材料,但其概念和策略对其他金属氧化物复合材料有借鉴意义。
1 SnO2的储锂特点
1997年,日本富士公司首先发现SnO2作为锂离子电池负极材料具有很高的质量比容量和体积比容量。从图1可知,目前SnO2基复合材料的容量集中在500~1 000 mAh/g之间,只有极少工作能够达到SnO2理论容量;循环周期约为100~500周,也低于商用锂电的寿命要求,因此,SnO2负极材料要走上实用之路还需要研究者们进一步努力。SnO2作为锂离子电池负极材料主要存在以下问题[34]:(1)在Li+嵌入/脱嵌过程中,SnO2的体积变化很大(≈300%),巨大的体积膨胀造成其颗粒破裂和固态电解质膜不断生成,最终导致活性物质与集流体失去电接触,从而失去活性造成容量的快速衰减[35-36];(2)SnO2的本征导电性很差,室温下的电阻率为10-2~10-3Ωcm,导致电子传递速率低,反应动力学缓慢[37-38];(3)由于Sn+Li2O→SnO2反应的高能垒,使得SnO2+4Li++4e-→Sn+2Li2O转化反应的可逆性差,由于这个反应导致Li+的不可逆消耗,因而SnO2的初始库仑效率低(≈50%),并且循环过程中容量会逐渐降低[39-41];(4)在循环过程中,由于再结晶和表面能最小化,Sn颗粒逐渐变成更大的颗粒或团簇,这些较大的颗粒/团簇活性较低,甚至部分Sn彻底失活,导致合金化反应的可逆性降低[42-43]。
2 SnO2的结构控制
针对以上这些电化学性能缺陷,研究者们做出了很多努力。其中,构建SnO2纳米颗粒是较常用的方法,纳米结构的主要优点是具有更高的比表面积,可以增加锂离子进入电极材料的途径,缩短锂离子的传输路径,提高快速充放电的能力,缓冲充放电过程引起的体积的变化。最近研究表明纳米颗粒的Sn+Li2O→SnO2转化反应可以完全或部分可逆,这可能是由于锂离子和电子转移距离较短而导致Sn/Li2O界面间的扩散动力增加[44-45]。Hu等认为如果Sn纳米粒子的直径<11 nm,则转化反应是完全可逆的[45]。
构建中空、多孔或层级结构也是研究者们的重要关注点[46-49]。这些结构的比表面积一般较高,孔洞的边界可以阻止循环过程中Sn粒子单元的团簇,改善循环性能。此外,丰富的孔洞可以使电解质更好渗透,增强Li+的传输,并缓冲锂嵌入与脱嵌导致的SnO2体积膨胀效应。图2为3种不同微观结构的SnO2颗粒:(a)为多孔双壳空心球,这种结构不仅可以促进液体电解质快速扩散到双层球体中,而且可以缓冲锂离子插入/脱出过程中的大体积变化,100次循环后容量保持为911 mAh/g[50];(b)为三维锯齿状碳涂层多孔SnO2准纳米立方体,独特的结构提供了SnO2更好的电化学动力学和优异的结构稳定性[51];(c)为一种碗状SnO2@C空心粒子,在保留空心结构优点的同时,减少了过多的空心内部空间,表现出高容量、稳定的循环性能和优异的倍率性能[52]。

图2 3种不同微观结构的SnO2粒子及其形成原理Fig 2 Three kinds of SnO2 particles with different microstructures and their formation
3 构建物理包覆层
虽然纳米结构可以有效提高反应可逆性,改善能量密度,但是纳米颗粒的高表面能却会促进电池循环过程中的电极材料聚集与Sn颗粒增大,而且SnO2颗粒与电解液直接接触会带来许多副反应。因此,许多研究者提出可通过在纳米SnO2表面构建稳定的物理包覆层来改善上述缺陷,包覆层覆盖在SnO2表面,隔绝SnO2与电解液的直接接触,减少SEI膜的形成,提高库伦效率。而当包覆材料具有高导电性时,还能提高SnO2的倍率性能。碳材料是研究者最主要的选择,由于具有优异的化学稳定性、力学性能和高电导率,无定形碳、碳纳米管(CNTs)和还原氧化石墨烯(Gr)被广泛地用于与SnO2纳米材料形成复合材料以提高其电化学性能。除此之外,也有研究者探讨了导电聚合物和金属(或金属氧化物)涂覆SnO2颗粒表面对于电化学性能的改性效果。这些研究均证明了构建物理包覆层是一种简单有效的提高SnO2循环寿命的方法。
3.1 与碳材料复合
本课题组研究了将SnO2与纤维素热解硬碳复合(图3a),再用PVDF热解碳包覆后形成的复合物(图3b),以及SnO2与葡萄糖热解碳的复合物(图3c)。纤维素热解过程中不会形成胶体,直接形成硬碳颗粒,在没有PVDF热解碳包覆时,部分SnO2颗粒形成了四方单晶颗粒;加入PVDF包覆层后,SnO2为嵌在硬碳表面的类球状纳米颗粒(形成示意图见图3d)。葡萄糖热解过程中会完全胶化,从而将SnO2颗粒包裹在无定形碳内部,制备过程更加简单。图3e为加入不同PVDF包覆量的SnO2/硬碳复合物的循环性能,最高循环保持率为87.1%。

图3 SnO2与无定形碳的复合物(a,b,c),形成机理(d)与循环性能(e)Fig 3 The composite of SnO2 and amorphous carbon (a,b,c),it’s formation mechanism (d) and electrochemical performance (e)
目前,葡萄糖[53]或蔗糖[54]、有机金属框架[55]、乙二醇(EG)[56]、聚苯乙烯(PS)球[35]、多巴胺(DA)[57]、和生物材料[58-59]等各种有机化合物经碳化处理得到的,已被广泛用于形成SnO2/C复合材料。Wang[]等利用有机金属框架HKUST-1作模板,引入锡源后炭化,再用浓硝酸处理,在三维多孔碳骨架中制备单分散的SnO2颗粒,该复合材料在50次循环后表现出900 mAh/g的高可逆容量(100 mA/g),即使在200次循环后仍保持880 mAh/g的稳定容量(100 mA/g)。Hu等[61]在三维多孔碳化滤纸上沉积SnO2纳米晶,在500 mA/g电流密度下可逆容量为526 mAh/g。
但不可否定的是,制备SnO2与无定形碳复合物通常需要采用传统煅烧的方法,难以控制颗粒尺寸,使得转化反应的可逆性较低,而且有机化合物热解形成的无定形碳的导电性和柔韧性相对较低。因此SnO2与CNTs或Gr的复合也是近年来的研究重点。
一维空心碳纳米管具有较高的机械强度和柔韧性、良好的导电性和电解质传输性能、较大的比表面积和易于与Li+相互作用的结构,非常适合用作原位锚定SnO2纳米颗粒的模板并改善SnO2纳米颗粒的电化学性能[65-66]。图4为不同文献中SnO2/CNTs复合物的形貌[15][65-66],可以看出形貌基本类似,均为许多SnO2颗粒固定在复合材料的原始碳纳米管的侧壁上,SnO2的尺寸仅为几纳米。这些研究均证明:CNTs模板促进了SnO2纳米颗粒的均匀分散,抑制了电池循环过程中的的颗粒团聚;交叉堆叠的超定向碳纳米管薄膜提供了坚固的分层结构,缓冲了体积膨胀效应,并促进了电子传输;CNTs基纳米复合材料的多孔结构还有利于电解质渗透到材料中,从而提供更短的Li+转移路径[14][67]。

图4 SnO2/CNTs复合物的形貌Fig 4 .orphology of the SnO2/CNTs composite
为了探索SnO2与CNTs之间产生的不同化学键对电化学性能的影响,Cheng[15]采用水热法制备了SnO2@CNTs复合材料:将多壁碳纳米管与SnCl2·2H2O水热处理后得到SnO2@CNTs复合材料(标记为SC),然后将所制备的SnO2@CNTs复合材料在Ar中于管式炉中500 ℃退火2 h(标记为SC-H),两种复合物的合成与成键过程示意图如图5a所示。图5d、e为SC-H的HETEM照片,显示出比SC更高的结晶度,图5b、c、f、g中可看出SC-H的电化学性能优于SC,两者的化学键组成如图5h所示。因此研究者认为含Sn-O-C键较多的SnO2@CNTs的转化反应动力学较差,导致可逆容量较低。相反,含较多Sn-C键的SnO2@CNTs在充电过程中可以将Sn和Li2O转化为SnO2,表现出可逆稳定的转化反应,同时Sn-C键可以为SnO2材料提供超快的电子转移路径。该途径可以大大提高SnO2@CNTs复合材料的转化反应动力学。
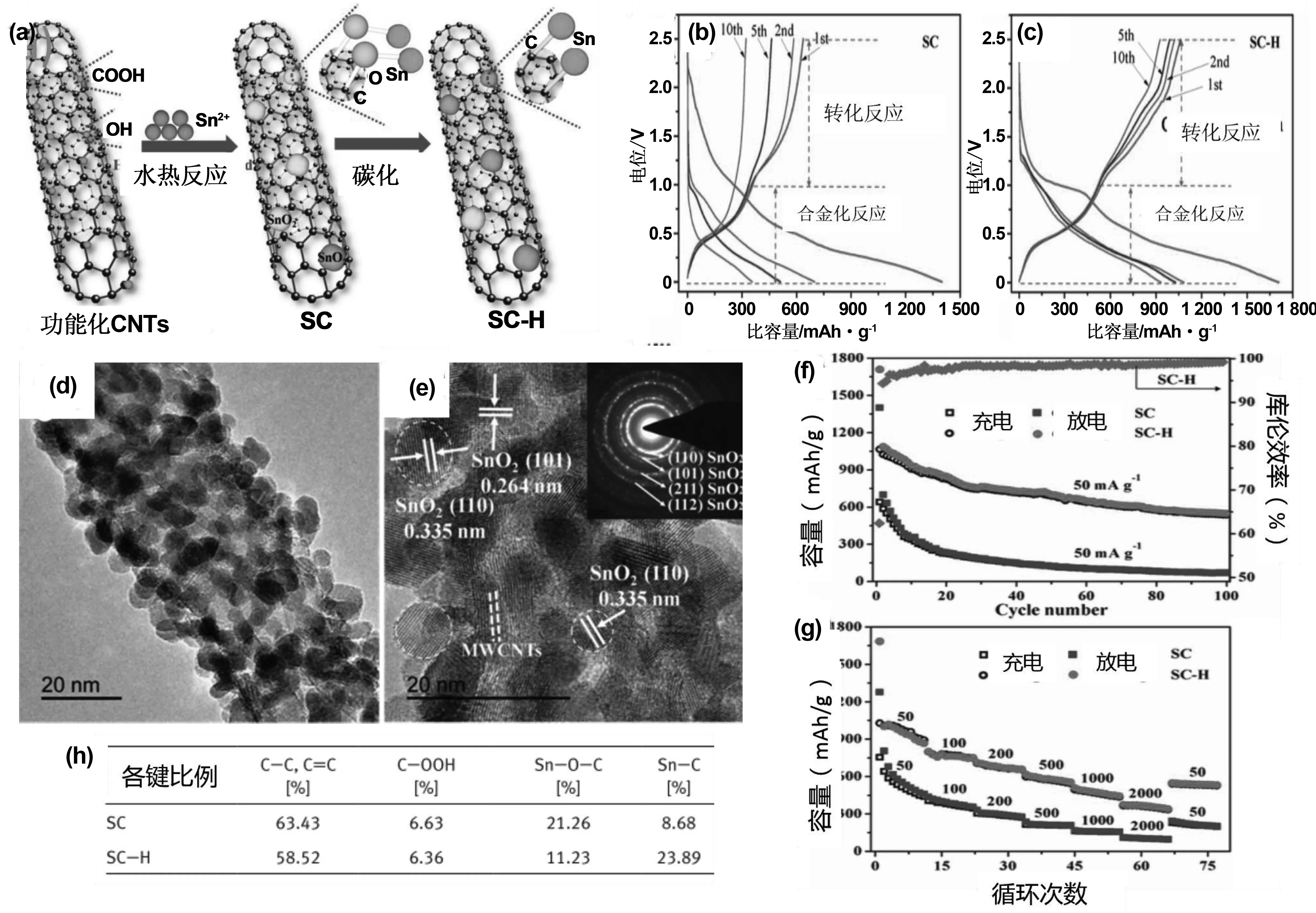
图5 调整SnO2@CNTs复合材料的化学键以增强电化学反应动力的图示Fig 5 Adjust the chemical bond of SnO2@CNTs composites to enhance the dynamics of electrochemical reaction
除无定形碳与CNTs之外,还原性氧化石墨烯(Gr)由于具有比表面积大、机械柔韧性强、化学稳定性好、导电性好等优点,被认为是与SnO2纳米颗粒形成均质复合材料的理想包覆剂[68-69]。而且作为负极材料,它还具有744 mAh/g的高理论容量[70]。此外,石墨烯表面的羧基和羟基等官能团可以作为客体材料的成核中心,用于各种原位和自组装合成。因此制备SnO2/Gr纳米复合材料的一般方法是利用Sn2+/Sn4+离子与氧化石墨烯(GO)表面含氧基团(-OH、-C-O-C-和-COOH)之间的相互作用,在GO表面原位生成SnO2纳米颗粒[71],原理图见图6a[4]。与CNTs不同的是,石墨烯的化学官能化还可能产生局部的高活性区域,可以在此区域通过用杂原子(例如N、P等)掺杂GO来增强负载能力和结合力,从而为SnO2纳米晶的成核引入额外的活性中心[23][72-73]。
制备SnO2/Gr纳米复合材料的目的是最大限度地利用组合优势来提高电化学性能,减少甚至解决石墨烯或SnO2单独作为活性材料的电极问题。在SnO2/Gr纳米复合材料中,由于尺寸效应和界面相互作用,复合材料将具有明显的协同效应。一方面,SnO2锚定或分散在Gr上,降低或抑制了Gr的团聚和再堆积,增加了纳米复合材料的活性中心;另一方面,Gr作为SnO2的载体,可以诱导超细SnO2在石墨烯表面成核与生长,形成分散均匀、形貌可控的超细纳米结构,复合材料的典型结构见图6b[43]。此外,SnO2/Gr三维多层结构将形成有效的电子导电网络,缩短锂离子的迁移路径,提高材料的倍率性能,如图6c所示,复合材料在2A/g的大倍率下依然可以放出≈200 mAh/g的比容量,且可逆性良好[88]。

图6 SnO2/Gr复合材料的形成机理(a),典型微观形貌(b)与电化学性能(c)Fig 6 Formation Mechanism(a) ,typical morphology (b) and electrochemical performance (c) of SnO2/Gr composites
由于目前已有一些关于SnO2/Gr复合材料的综述论文[9][74-75],因此而本文不再详述。
3.2 其他包覆材料
研究者发现,与碳质材料相比,导电聚合物—如聚吡咯(PPy)[76-77]、聚多巴胺(PDA)[78-79]、聚苯胺(PANI)[25][27]、聚3,4-乙烯二氧噻吩/聚苯乙烯磺酸盐(PEDOT/PSS)[48]、聚丙烯酰胺(PAAM)[26]等等—能在SnO2纳米颗粒表面形成更致密、更柔韧的涂层,增强了对Sn纳米颗粒团聚的抑制作用。
Yuan[76]采用液相沉积法与原位化学聚合制备了粒径610~730 nm的SnO2/PPy空心球,在100 mA/g电流密度下循环600次后,复合材料容量为899 mAh/g。优异的电化学性能归功于PPy包覆层与SnO2空心球之间的协同效应,保证了良好的电子导电性、快速的锂离子扩散以及足够的空隙空间来缓冲体积膨胀。Li[48]合成了具有核壳结构的SnO2@C/PEDOT/PSS微球,非晶态碳包裹的超细SnO2纳米粒子聚集成规则的微球,再被PEDOT/PSS层包裹,形成了具有双重保护层的核壳结构,这种分层结构提供了充足的离子/电子传输通道,抑制了电解液的不良反应,提高了导电性,缓冲了整个电极的内部应力,从而实现了稳定的循环性能。其初始可逆容量为1 170 mAh/g,在0.1 C下保持了441 mAh/g的高容量,并在2 C的高倍率下进行了1 200次稳定循环。
除碳质材料和导电聚合物外,在SnO2颗粒上均匀涂覆一层无机材料(如金属或金属化合物)也能有效地减缓SnO2的体积变化,如TiO2[80],Fe2O3[81-82],NiCo2O4[83],HfO2[84],MoO3[85],Si[86],Cu[87]等。其中TiO2是最常用的无机包覆材料,在SnO2@TiO2核壳结构中,TiO2壳层起到了物理屏障的作用,缓冲了SnO2纳米颗粒内部的体积变化,防止了其粉化,同时通过保持电极的结构完整性,提高了循环稳定性。Zhou[]等通过微波辅助盐酸刻蚀反应和随后的煅烧制备了分级空心的SnO2@TiO2纳米胶囊,纳米胶囊在780 mA/g下循环200次后容量稳定在770 mAh/g。
4 结 语
SnO2具有较高的理论容量,工作电位安全,对环境友好,是最有希望替代商用石墨的负极材料。然而其缺点也是显而易见的,在电化学储能过程中,其转化反应的可逆性远低于合金化反应,因而不能完全获得其理论容量。此外,较大的体积膨胀引起活性物质的粉化和剥离,本征电导率差,以及充放电过程中Sn颗粒的长大与团簇,都是SnO2实用化过程中的阻碍。本文从微观结构控制与构建物理包覆层两方面入手,结合本课题组的工作,综述了近年来国内外研究者对于提高SnO2负极材料的储锂性能所作出的努力。研究者通过各种制备手段形成层状/多孔/空心结构,利用其中的大量孔洞缓冲SnO2电极的体积变化,促进电解质渗透。但结构修饰不能显著提高SnO2的电导率,因此需要在这些结构的空隙边界上建立致密的导电层。炭质材料和导电聚合物所构建的导电物理层不仅可以有效地抑制SnO2的粉化与团聚,还可以增强电极的结构稳定性和电子导电性,因此这被认为是最有效的改善SnO2电化学性能的措施。两种策略协同使用,可以使得SnO2既具有良好的循环稳定性,又具有较高的体积比能量密度。
然而,要实现SnO2及其复合材料的商业化,还有很多问题需要解决。SnO2负极材料由于形成固体电解质界面(SEI)层,在初始循环中存在较大的不可逆容量损失,这对锂离子电池的循环性能、库仑效率和安全性有着重要影响。此外,目前鲜有以SnO2纳米复合材料为负极制备全电池的研究,而这是其商业化进程中必不可少的一步,因此研究者需要进一步优化SnO2基全电池的各种制备参数,研究全锂离子电池中SnO2阳极的性能增强策略和失效机理。
