微波消解-原子荧光光谱法测定小麦粉中汞含量的不确定度评定
2020-09-02王婧,刘旭,刘萍,吴静
王 婧,刘 旭,刘 萍,吴 静
(陕西省粮油产品质量监督检验中心,陕西 西安 710016)
汞作为一种具有污染持久性、生物富集性及剧毒性等特点的环境污染物[1],在全球范围内备受关注。汞以不同的化学形态排入环境,污染空气、水和土壤,从而进一步污染食品[2],人们食用被污染的食品后可以引发一系列疾病,如神经系统,消化系统及心血管等方面的疾病[3]。测量不确定度是新兴的一种评定测量可靠度的方法,能合理表征赋予被测量值的分散性,是与测量结果相关联的一个参数[4]。测量不确定度对测量结果质量的优劣、检测方法的确认和实验室专业技术水平的评价具有十分重要的意义。目前,针对汞的检测方法主要有原子荧光光谱法[5-6]、冷原子法[7-8]和电感耦合等离子体质谱法[9-12]等,对于汞测定不确定度评定方面的相关报导多集中在水、水产品和土壤中,在粮食方面的少之又少。我们采用GB 5009.17—2014《食品安全国家标准食品中总汞及有机汞的测定》对小麦粉中总汞含量进行测定,并从样品制备、标准曲线浓度及样品测量等方面评定了不确定度,为评估检测结果的科学性和检测结果的准确性提供可靠的理论依据。
1 材料与方法
1.1 仪器与试剂
AFS 9700双道原子荧光光度计,北京海光仪器有限公司;AF-2汞空心阴极灯,北京有色金属研究总院;PL203电子天平,梅特勒-托利多仪器上海有限公司;Multiwave PRO微波消解仪,奥地利安东帕有限公司;BHW-09A45赶酸仪,上海博通化学科技有限公司;Direct 8超纯水仪,美国Millipore公司。
汞标准溶液(100 μg/ml),购于中国计量科学研究院;硝酸和过氧化氢为优级纯;氢氧化钠和硼氢化钾均为分析纯;实验用水为超纯水。
1.2 仪器工作条件
光电倍增管负高压240 V,灯电流30 mA,载气(Ar)流量400 ml/min,屏蔽气流量900 ml/min,原子化器高度8 mm,读数时间16 s,延迟时间4 s,载流为硝酸溶液(1∶9)。在此条件下测定标准系列溶液和样品供试液,扣除空白的荧光强度值,标准曲线法定量。
1.3 样品前处理
准确称取小麦粉样品0.400 g(精确至0.001 g),置于消解管内,加入2.0 ml过氧化氢和4.0 ml硝酸,设置微波消解仪的最大功率为800 W,爬升时间10 min,保持时间20 min,待消解结束冷却后取出,缓慢打开罐盖排气,用少量水冲洗内盖,将消解管放在控温电热套内于80℃加热,赶去棕色气体,冷却后将消化液转移至25 ml容量瓶中,用少许水分3次洗涤消解管内壁,洗涤液合并于转入容量瓶中并定容至刻度,混匀备用;同时作空白试验。
1.4 标准工作曲线配制
100 μg/ml汞标准溶液逐级稀释得到10 ng/ml的标准工作液,分别移取标准工作液0.50、1.00、2.00、4.00和5.00 ml定容至50 ml,制得质量浓度为0.1、0.2、0.4、0.8和1.0 ng/ml的标准系列溶液。
1.5 样品测定
按1.2仪器条件,预热30 min,对汞标准系列溶液进行测试,以质量浓度为横坐标,荧光强度响应值为纵坐标,利用线性最小二乘法对测定值进行拟合,得到相应的标准曲线,然后测定样品。
2 结果与分析
2.1 数学模型
式中,X为试样中汞的含量,mg/kg;C0为空白溶液中汞浓度,ng/ml;C1为测定溶液中汞浓度,ng/ml;V为试样消化液定容总体积,ml;m为试样质量,g;1 000为换算系数。
2.2 不确定度来源分析
不确定度分量来源于样品制备不确定度、标准溶液配制不确定度及样品测量不确定度。
样品制备的不确定度与样品称量及消化液定容引入的不确定度有关。标准溶液配制的不确定度与标准储备液自身、标准曲线绘制及标准曲线拟合引入的不确定度有关。样品测量的不确定度与样品测量的重复性及回收实验引入的不确定度有关。
2.3 不确定度分量的分析与计算
2.3.1样品制备引入的不确定度
2.3.1.1样品称量
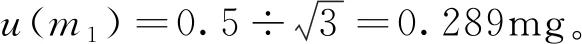
样品称量的相对标准不确定度为:
2.3.1.2消解液定容
微波消解后的样品溶液使用25 ml的A级容量瓶定容,容量瓶引入的不确定度包括由校准引入的不确定度u(V25 ml)和由温度效应(环境温度24℃)引入的不确定度u(T25 ml)。
根据JJG 196—2006《常用玻璃量器检定规程》[13],其最大允许误差为±0.03 ml,按均匀分布,则25 ml容量瓶引入的相对不确定度为:
urel(V25 ml)=0.017 3÷25=6.92×10-4
通过温度变化范围和体积膨胀系数可以估算出温度效应引入的不确定度,玻璃的膨胀系数(9.8×10-6/℃)远小于水的膨胀系数(2.1×10-4/℃),因此可以忽略不计[3]。容量瓶的校准温度为20℃,样品测定时环境温度为24℃,取均匀分布,则温度效应引入的相对不确定度为:
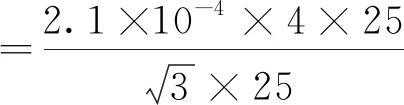
=4.85×10-4
消解液定容过程引入的相对不确定度为:
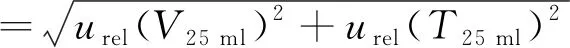
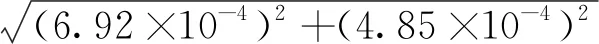
=8.45×10-4
计算得出样品制备的相对标准不确定度为:
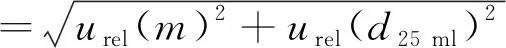
=1.11×10-3
2.3.2标准曲线浓度引入的不确定度
2.3.2.1标准储备液
本实验采用的汞标准溶液浓度为100 μg/ml,已知标准物质证书给出的扩展不确定度为0.8%,k=2,则汞标准溶液的相对标准不确定度为:
2.3.2.2标准曲线配制
标准系列溶液由100 μg/ml(即1.0×105ng/ml)汞标准溶液经2级逐级稀释配制而成,配制步骤见表1。
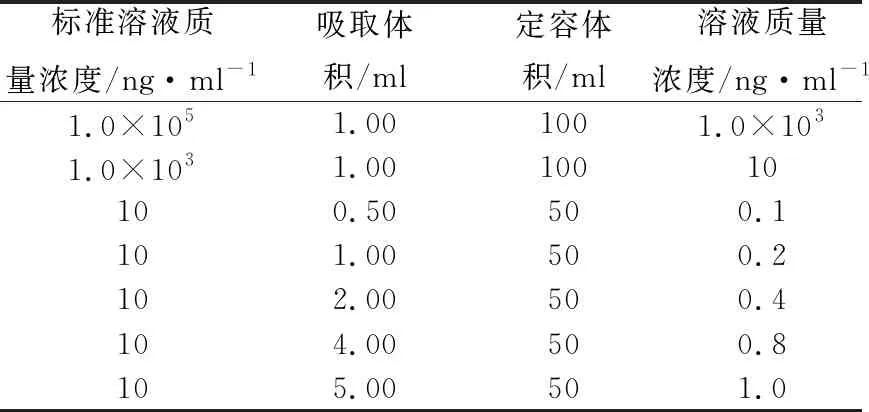
表1 标准系列溶液的配制

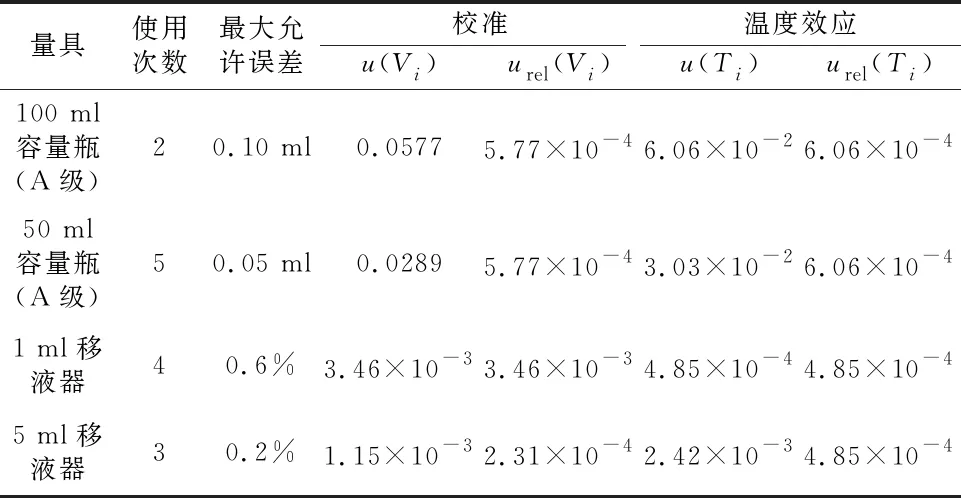
表2 标准溶液配制过程中量器引入的不确定度
=0.007 1
样品测定时环境温度为24℃,取均匀分布,则合成由温度效应引入的相对不确定度为:
标准曲线配制过程引入的相对不确定度为:
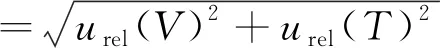
=0.007 4
2.3.2.3标准曲线拟合
对5个浓度水平的标准溶液分别重复测定3次,测得其荧光强度响应值,结果见表3。

表3 标准系列溶液测定结果
利用线性最小二乘法对标准曲线进行拟合,得到回归方程为:y=134.856x-0.472,相关系数:R=0.999 6。则由标准曲线拟合引入的标准不确定度为:
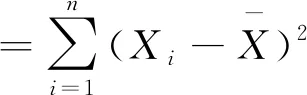
=1.8

=2.71
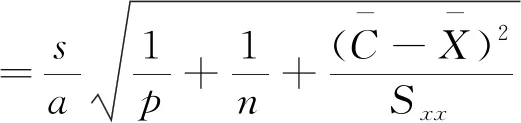
=0.009 8
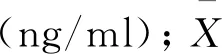
标准曲线拟合引入的相对标准不确定度为:
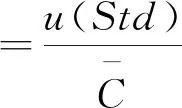
=0.036 2
计算得出标准曲线浓度的相对标准不确定度为:
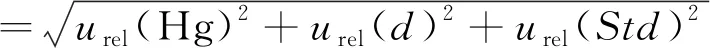
=0.037 2
2.3.3样品测量引入的不确定度
3.3.3.1样品测量重复性
选取1份市售小麦粉样品,按照1.3节方法前处理后,在1.2节仪器条件下平行测定7次,结果见表4。

表4 样品测定结果 mg/kg
由表4可知,由样品测量重复性引入的相对不确定度为:
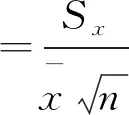
=4.47×10-3
2.3.3.2回收实验准确度
测定样品加标回收率结果见表5。则由样品回收实验引入的相对不确定度为:

表5 样品中的加标回收率
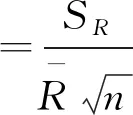
=0.014 8
计算得出样品测量的相对标准不确定度为:
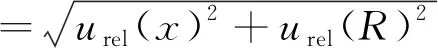
=0.015 5
2.4 相对不确定度的合成与扩展
2.4.1合成标准不确定度
根据以上计算得出各不确定度分量,见表6。
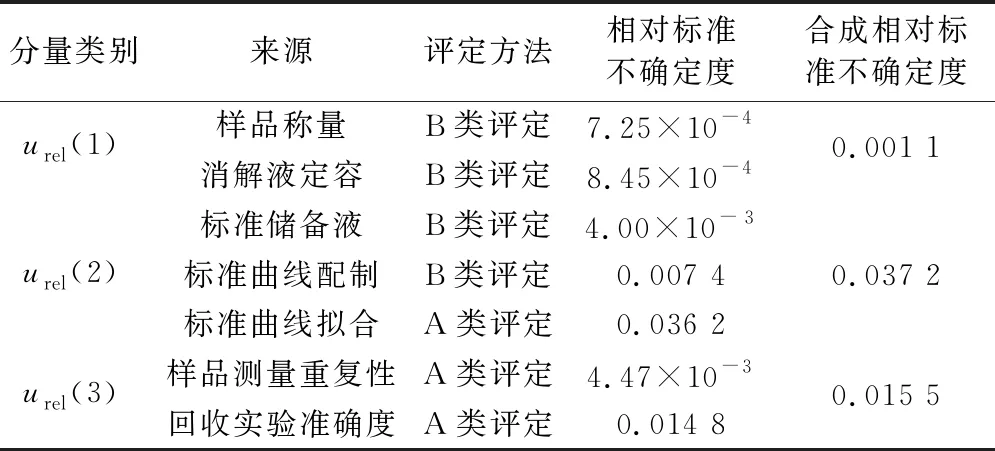
表6 不确定度分量表
根据不确定度来源分析,可知表6中各不确定度分量互不相关,合成为:
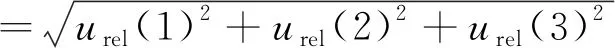
=0.040 3
2.4.2扩展不确定度评定
样品中汞含量为0.016 9 mg/kg,取包含因子k=2,置信水平P=95%,则扩展不确定度为:
U=2u(X)=0.001 4mg/kg。
2.5 结果表示
小麦粉中汞含量为:
X=(0.016 9±0.001 4)mg/kg,k=2,P=95%。
3 结论
以微波消解-原子荧光光谱法测定小麦粉中的汞含量,结果表示为汞含量为0.016 9±0.001 4 mg/kg,k=2,P=95%。从影响测定结果的不确定度分量得出,标准曲线拟合引入的不确定度最大,其次是回收实验引入的不确定度,由其他因素引入的不确定度贡献都很小,可忽略不计。因此,在试验过程中调整标准曲线的浓度梯度,使标准曲线的中点与样品的质量浓度接近,必要时使用回收率校正因子对测量数据结果进行修正[15],用以降低测定结果的不确定度,从而提高实验结果的准确性。
