一种基于先验图像的锥束CT金属伪影校正算法
2020-09-01刘仰川朱叶晨
刘仰川,高 鹏,2,朱叶晨,高 欣
一种基于先验图像的锥束CT金属伪影校正算法
刘仰川1,高 鹏1,2,朱叶晨1,高 欣1
(1. 中国科学院苏州生物医学工程技术研究所医学影像技术研究室,江苏 苏州 215163;2. 南京理工大学电子工程与光电技术学院,江苏 南京 210094)
为了有效抑制锥束CT(CBCT)重建中金属植入物引入的伪影,提出一种基于先验图像的金属伪影校正算法。首先对含金属伪影的重建图像进行双边滤波、金属阈值分割、组织聚类等预处理,获得金属图像和不含金属信息的先验图像;再对二者正向投影,获得金属投影区域和先验投影数据;而后利用先验投影数据及金属边界邻域的投影数据对金属投影区域插值,获得修复的投影数据;最后利用FDK算法对修复的投影数据重建,并将其与金属图像融合,获得最终的校正图像。为了验证该算法的性能,利用三维Shepp-Logan头部模型数据和临床头部CT数据开展金属伪影校正实验,结果表明:与常用的线性插值算法和图像修补算法相比,该算法的校正图像均方根误差最小、峰值信噪比最大。这说明该算法在有效保留图像边缘信息的同时,可有效地抑制金属伪影。
锥束CT;金属伪影校正;双边滤波;先验图像;插值
近年来,锥束CT(cone beam computed tomography,CBCT)因体积小、辐射剂量低、各向同性空间分辨率高等优点[1],在口腔科、骨科的应用越来越广泛,是目前最有前途和实用性的成像方式之一[2-3]。然而,病人体内携带的金属植入物[3](如金属义齿、骨钉等)会给重建图像带来严重的条状伪影(金属伪影),极大影响诊断准确性。金属伪影校正[4](metal artifact reduction,MAR)算法可以在图像重建过程中,减少甚至消除条状伪影,改善重建图像质量。
目前,锥束CT的MAR算法主要分为3类[5]:①插值法:从原重建图像或投影数据中分割出金属区域,并对金属区域插值,再将重建图像与金属图像融合,实现金属伪影校正;②迭代法:借助迭代重建算法的平滑和去伪影特性,采用不同参数对金属投影区域和非金属投影区域分别重建,再进行图像融合,实现金属伪影校正;③混合法:将2种或多种MAR方法结合(通常是将插值法、迭代法结合),以提升校正性能。迭代法和混合法复杂度高、耗时严重[6-7],临床应用局限性大,而插值法复杂度低、计算效率高,是当前MAR主流算法。因此,本文围绕插值法开展研究。MEILINGER等[8]提出了一种基于互信息和边缘滤波的MAR算法,利用阈值法从原重建图像中分割出金属图像,并将金属邻域像素点插值到金属区域,再通过正向投影及边缘滤波,获得修复的投影数据。ZHANG等[9]利用锥束CT的成像几何关系定位金属投影区域,再利用拉普拉斯扩散法将金属边缘投影数据插值到金属区域,获得修复的投影数据。BEISTER等[10]提出了一种基于前投影数据的简约MAR算法,利用阈值法从原重建图像中分割出金属图像,并对金属图像正向投影确定其投影位置,再利用三维线性插值法将金属边缘投影数据插值到金属投影区域,获得修复的投影数据。以上算法简单、快速,但校正图像中容易出现严重的次级伪影(因校正不当而产生的新伪影)。为此,PRELL等[11]提出了一种可降低次级伪影的MAR算法,先对原重建图像高斯滤波和金属阈值分割,再对分割出的金属图像正向投影,后使用三维线性插值算法对金属投影区域插值,并进行归一化处理,获得修复的投影数据。该算法能较好地消除金属伪影并产生较少的次级伪影,但校正图像中的组织边缘容易被模糊,导致边缘信息缺失。
针对现有插值类MAR算法校正后的图像存在次级伪影及边缘模糊的问题,本文提出一种基于先验图像的CBCT金属伪影校正算法(prior-image- based MAR,PIB-MAR)。该算法在2个方面做出改进:①采用双边滤波对原重建图像进行预处理,去除噪声并保留边缘信息;②采用先验投影数据及金属邻域投影数据对金属投影区域插值,抑制次级伪影产生。为了验证算法的性能,利用三维Shepp-Logan头部模型数据和临床头部CT数据进行金属伪影校正实验,并与常规的线性插值算法(linear-interpolation-based MAR,LIB-MAR)[11]、图像修复算法(image-inpainting-based MAR,IIB- MAR)[12-13]进行比较。
1 锥束CT金属伪影校正算法
本文提出的锥束CT金属伪影校正算法流程如图1所示。
第1步:预处理。对含金属伪影的重建图像进行双边滤波、金属阈值分割、组织聚类等预处理,获得金属图像和先验图像。
第2歩:金属伪影校正。对金属图像和先验图像进行正向投影,获得金属投影区域和先验投影数据,再对金属投影区域进行修复,获得修复的投影数据。

图1 锥束CT金属伪影校正流程图
第3步:CT图像重建。利用FDK算法对修复的投影数据进行重建,得到中间重建图像,与第1步分割出的金属图像进行融合,获得最终的校正图像。
1.1 双边滤波
针对含金属伪影的CT图像,采用双边滤波器(bilateral filter,BF)[14-15]进行滤波,去除部分伪影和噪声。BF是一种非线性滤波器,基于像素间的欧式距离及灰度差异,在有效去除图像噪声的同时,保留图像边缘信息。针对CT图像,BF采用高斯分布的加权平均函数对图像进行平滑,权重系数由2部分组成:①像素间的灰度差值范围,即像素范围域滤波核函数;②像素间的欧式距离,即空间域滤波核函数。
设()为含金属伪影的重建图像,将灰度值进行归一化,经双边滤波,得到输出图像,即


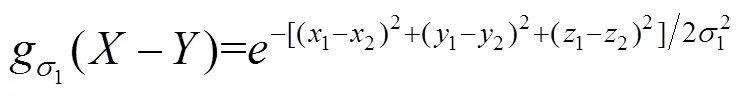


1.2 金属阈值分割
针对双边滤波后的CT图像,采用阈值法进行金属分割,获得金属图像。阈值分割是一种传统且最常用的图像分割算法[17-18],具有简单、计算量小、性能稳定等优点。在MAR算法中,金属分割的准确性至关重要,可直接影响其效果。
CT图像中,不同组织的CT值差异较大,如空气的CT值为–1 000 HU、脂肪为–120~–90 HU、骨为300~2 000 HU,而各类金属的CT值远大于2 000 HU,甚至上万。因此,可采用阈值法将金属从CT图像中分割出来,即

其中,为阈值,可通过直方图法确定取值,一般设为最大像素值的30%。从上式可以看出,像素值大于和等于的区域为金属图像,在二值图像中设为1,其他区域的像素值设为0。
1.3 先验图像生成
利用软组织CT值对CT图像中分割出的金属区域进行填充;借助“类组织模型”的思想[19],采用三维K-means算法[20]将填充后的CT图像聚类为空气、脂肪、软组织和骨;给不同聚类的组织赋值,获得不含金属信息的先验图像prior,即

1.4 投影修复
根据锥束CT成像几何关系,分别对分割出的金属图像、生成的先验图像进行正向投影,获得金属投影区域和先验投影数据。如果直接利用先验投影数据替换原投影数据中的金属区域,修复后的边缘连续性差,容易导致重建图像中出现次级伪影。为此,采用改进的修复方法,即利用先验投影数据、金属边界邻域的投影数据对金属投影区域进行插值。


1.5 FDK重建与融合
采用FDK算法[21]对修复后的投影数据重建,获得中间重建图像,并与分割出的金属图像融合,获得最终的校正图像。FDK是在二维滤波反投影(filtered back-projection,FBP)算法基础上发展出的一种三维重建算法。FDK属于近似重建算法,其原理是将锥形束射线视为具有不同倾斜角度的扇形束射线面的集合,中心扇形束射线面(垂直于平板探测器)对应的投影数据采用FBP算法重建,而非中心扇形束射线面对应的投影数据采用修正的FBP算法重建,从而将锥形束重建问题转化为扇形束重建问题。
FDK算法先对投影数据进行预加权,适当修正体素到坐标系原点的距离和角度差;再对不同角度的投影数据进行水平方向的一维滤波;最后沿射线方向进行三维反投影。该过程可表示为


中间重建图像与金属图像的融合过程为

其中,metal()为金属图像;metal为金属区域;cor()为最终的校正图像。
2 实验与结果
2.1 图像质量评价指标
采用均方根误差(root mean squared error,RMSE)、峰值信噪比(peak signal to noise ratio,PSNR)对校正后的重建图像质量进行定量评价[22]。
RMSE定义为


PSNR定义为

PSNR可用来判断图像噪声抑制能力,值越大表示抑制效果越好。PSNR是一种普遍采用的评估图像质量的客观度量,有时无法与人的主观感受完全匹配。
2.2 Shepp-Logan头部模型数据校正实验
为了验证本文算法的有效性,在原三维Shepp-Logan头部模型[23]中加入2个金属球,进行金属伪影校正实验,模型参数见表1。

表1 三维Shepp-Logan头部模型参数[23]
表1中,为椭球的附加强度值,为椭球的中心坐标,,,分别为椭球在,,轴方向上的半轴长系数(长度为130 mm),,,分别表示椭球绕,,轴旋转的角度;序号1~10为原Shepp-Logan模型参数,序号11~12为金属球参数。Shepp-Logan头部模型中的多个椭球组成不同类型的组织,包括空气、脂肪、骨、软组织和水。三维Shepp-Logan头部模型尺寸为256×256×256、体素尺寸为0.5859×0.5859×0.5859 mm3(各向同性),图2给出模型的向第128层切片、向第115层切片和向第185层切片。
采用CBCT扫描方式,对三维Shepp-Logan头部模型进行正向投影。射线源到平板探测器中心距离为1 000 mm,到旋转中心的距离为550 mm;射线源的管电压为140 kV,射线能谱采用BOONE和SEIBERT[24]提出的TASMIP算法得到;平板探测器的像素矩阵为560×560,平板探测器的像元尺寸为0.5×0.5 mm2;扫描范围为0~360°,角度步长为1°,投影角共360个。
在40~140 kV的射线能谱上,取能量步长为10 kV,在美国标准与技术研究院(National Institute of Standards and Technology,NIST)官网上[5],分别查找空气、脂肪、骨、软组织和水、钛合金对应不同射线能量的吸收系数。利用射线驱动模型对各能量段的吸收系数进行正向投影[25],获得单能投影数据,再经加权融合,获得最终的投影数据[26],即

其中,w为第个能量段的权重系数;为第个角度上第个能量段的投影数据;为能量段总数,值为10;p为第个角度的投影数据,图3给出第90个角度(90°角)对应的投影数据。
采用FDK算法对采集的投影数据进行CT图像重建(图4)。从图4可以看出,重建图像中可见明显的呈明亮条形和暗带的金属伪影,图像质量较差。
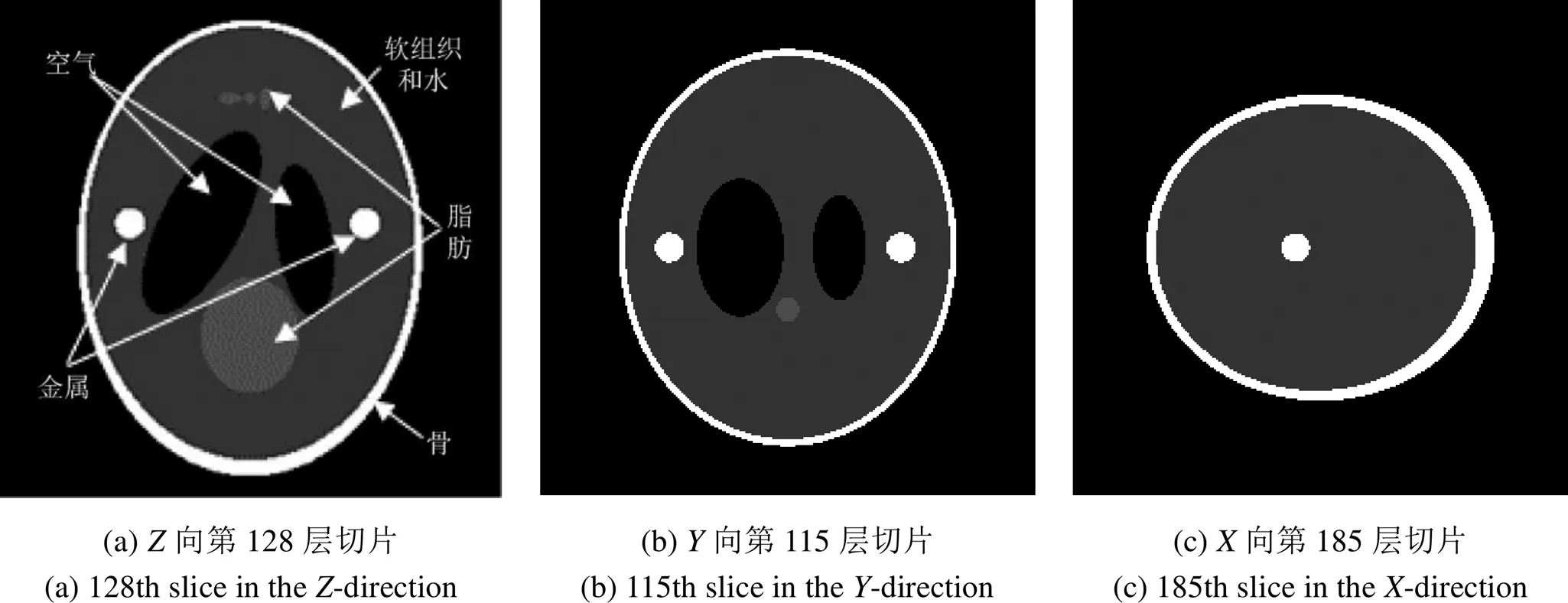
图2 三维Shepp-Logan头部模型。图像尺寸为256×256,灰度窗口为[0, 1]

图3 Shepp-Logan模型的90°角投影数据。图像尺寸为560×560,灰度窗口为[0.0001, 3.3128]
采用本文PIB-MAR算法进行校正,图5为该算法的各阶段结果。图5(a)为BF处理后的图像,原图像中的噪声和轻微伪影得到平滑,边缘信息得到保留;图5(b)为金属阈值分割图像,金属得到准确分割,边缘清晰;图5(c)为先验图像,各组织得到准确聚类;图5(d)为投影修复图像,金属投影区域连续性较好(对比图3);图5(e)为中间重建图像,原金属区域连续性较好;图5(f)为最终的校正图像,金属伪影得到有效校正(对比图4(a))。
分别采用常规的LIB-MAR和IIB-MAR算法对原重建图像进行校正,并与本文的PIB-MAR算法进行对比,结果如图6所示。

图5 基于先验图像的Shepp-Logan模型的金属伪影校正各阶段结果

图6 Shepp-Logan模型的金属伪影校正结果对比。第1~3列分别为Z向第128层切片、Y向第115层切片和X向第185层切片;第1~3行分别为LIB-MAR,IIB-MAR和PIB-MAR算法校正结果。图像尺寸为256×256,灰度窗口为[0, 0.07]
从图6中可以看出,相比原重建图像(图4),LIB-MAR算法对应的校正图像伪影有所减少,两金属间的暗带也被消除,但引起了次级伪影,部分组织结构被破坏;与LIB-MAR算法相比,IIB-MAR算法在组织结构保护上有更好的效果,但引起了更严重的次级伪影;与前2种MAR算法相比,PIB-MAR算法对应的校正图像伪影较少且组织结构较完整,与原始图像(图2)最接近,获得了最优的校正效果。
为了直观地对比3种算法的校正效果,绘制向第128层切片第116行的灰度曲线,如图7所示。其中,参考灰度曲线来自原Shepp-Logan图像 (图2)。
从图7(b)~(d)可以看出,PIB-MAR算法对应的红色虚线与参考图像对应的绿线最贴近,这表明该算法对应的校正图像质量最优。
为了定量地比较3种MAR算法的优劣,在伪影较为严重的向第128层切片上选取3个尺寸为25×30的感兴趣区域(region of interest,RoI),如图6所示。分别在单个及所有RoI上计算不同算法对应的RMSE值和PSNR值,结果见表2。其中,参考图像为原Shepp-Logan图像(图2)。

图7 Shepp-Logan模型的金属伪影校正结果的Z向第128层切片第116行的灰度曲线 ((a)为完整的灰度曲线; (b)~(d)分别是(a)中黑色虚框1~3的放大图)

表2 单个及所有RoI区域上,不同MAR算法对应的RMSE值和PSNR值
表2中,在同一RoI上,PIB-MAR算法对应的RMSE值最小;在所有RoI上,PIB-MAR算法对应的RMSE为0.002 1,比LIB-MAR和IIB-MAR算法分别减少了12.50%和41.67%。表明PIB-MAR算法对应的校正图像与原始图像的偏差最小。在同一RoI中,PIB-MAR算法对应的PSNR值最大;在所有RoI上,PIB-MAR算法对应的PSNR为53.439 1,比LIB-MAR和IIB-MAR算法分别提高了1.65%和7.93%。表明该算法对校正图像中的噪声具有最强的抑制能力。
2.3 临床头部数据校正实验
为了进一步验证PIB-MAR算法的性能,采用临床头部数据进行MAR实验。临床数据经降采样、归一化、金属植入处理,图像尺寸为256×256×138 mm3,体素尺寸为0.5 mm,层厚为1 mm,中心切片如图8(a)所示。采用上述CBCT扫描方式,对临床数据进行正向投影、FDK重建,得到原重建图像,如图8(b)所示,其中可见明显的金属伪影。分别采用LIB-MAR,IIB-MAR和PIB-MAR算法对原重建图像进行MAR,结果如图8(d)~(f)所示。
由图8可知,LIB-MAR算法去除了金属周围的大部分伪影,也基本去除了右下角的条纹状伪影,但校正图像中仍存在较多的次级伪影;IIB-MAR算法虽然去除了暗带状金属伪影,但图像中金属邻域连续性差且存在严重的次级伪影。与2种MAR算法相比,PIB-MAR算法去除了绝大部分金属伪影,校正图像中次级伪影轻微,取得了最佳的金属伪影校正效果。
为了定量比较3种算法的优劣,选取3个尺寸为30×30的RoI进行RMSE值、PSNR值计算,结果见表3。
表3中,在同一RoI上,PIB-MAR算法对应的RMSE值最小;在所有RoI上,其对应的RMSE为0.002 4,与LIB-MAR和IIB-MAR算法相比,分别减少了31.42%和69.23%。这表明PIB-MAR 算法对应的校正图像与原始图像的偏差最小。在同一RoI上,PIB-MAR算法对应的PSNR值最大;在所有RoI上,其对应的PSNR为57.122 4,与LIB-MAR和IIB-MAR算法相比,分别提高了18.15%和42.44%。这表明PIB-MAR算法具有最强的金属伪影抑制能力。
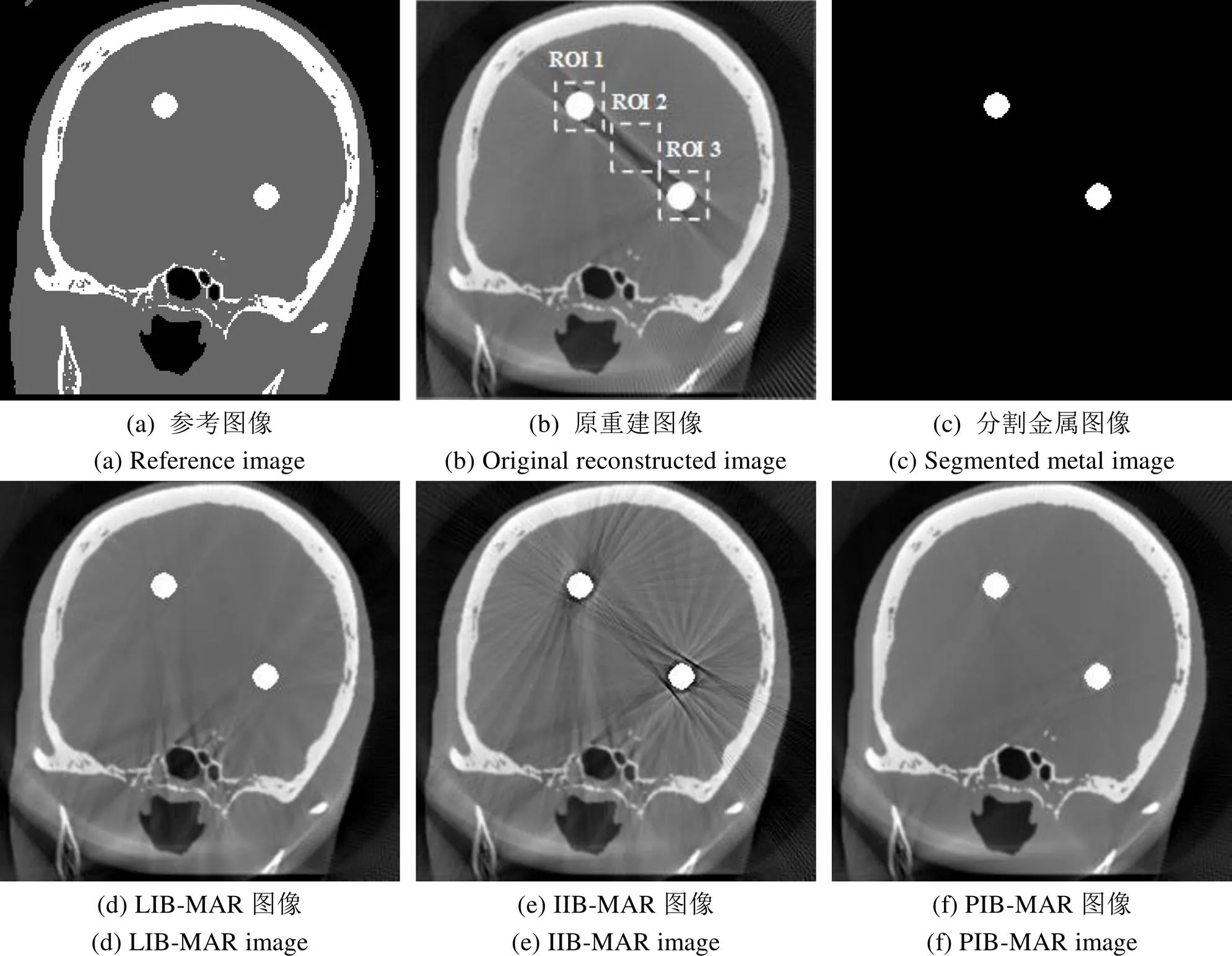
图8 临床数据的金属伪影校正结果。图像尺寸为256×256,灰度窗口为[0, 0.05]

表3 Shepp-Logan体模的单个及所有RoI上,不同MAR算法对应的RMSE和PSNR值
3 结 论
本文提出了一种基于先验图像的CBCT金属伪影校正算法,该算法首先对含金属伪影的重建图像双边滤波、金属阈值分割、组织聚类等预处理,可较好地去除重建图像中的噪声并保留边缘信息,从而获得金属图像和不含金属信息的先验图像;再对二者正向投影,获得金属投影区域和先验投影数据;而后利用先验投影数据及金属边界邻域的投影数据对金属投影区域插值,获得修复的投影数据,目的是抑制次级伪影产生;最后利用FDK算法对修复的投影数据重建,并与金属图像融合,获得最终的校正图像。利用三维Shepp-Logan头部模型数据和临床头部CT数据进行金属伪影校正实验,结果表明,该算法在RMSE,PSNR 2项指标上,均优于常用的LIB-MAR和IIB-MAR算法,获得较好的金属伪影校正效果。
[1] GOVILA S, GUNDAPPA M. Cone beam computed tomography - an overview[J]. Journal of Conservative Dentistry, 2007, 10(2): 53-58.
[2] VENKATESH E, ELLURU S V. Cone beam computed tomography: basics and applications in dentistry[J]. Journal of Istanbul University Faculty of Dentistry, 2017, 51(3): 102-121.
[3] BORNSTEIN M, SCARFE W, VAUGHN V, et al. Cone beam computed tomography in implant dentistry: a systematic review focusing on guidelines, indications, and radiation dose risks[J]. The International Journal of Oral & Maxillofacial Implants, 2014, 29(Supplement): 55-77.
[4] 肖文, 曾理. CT图像的金属伪影校正方法综述[J]. 中国体视学与图像分析, 2019, 24(1): 29-36. XIAO W, ZENG L. The review of metal artifact reduction for CT images[J]. Chinese Journal of Stereology and Image Analysis, 2019, 24(1): 29-36 (in Chinese).
[5] 李铭. CT金属伪影校正研究[D]. 北京: 中国科学院大学, 2015. LI M. The research on metal artifacts reduction in computed tomography[D]. Beijing: University of Chinese Academy of Sciences, 2015 (in Chinese).
[6] WANG G, FREI T, VANNIER M W. Fast iterative algorithm for metal artifact reduction in X-ray CT[J]. Academic Radiology, 2000, 7(8): 607-614.
[7] ZHU Y C, LIU Y C, ZHANG Q, et al. A fast iteration approach to undersampled cone-beam CT reconstruction[J]. Journal of X-Ray Science and Technology, 2019, 27(1): 111-129.
[8] MEILINGER M, SCHUTZ O, SCHMIDGUNST C, et al. Alignment correction during metal artifact reduction for CBCT using mutual information and edge filtering[C]//2009 Proceedings of 6th International Symposium on Image and Signal Processing and Analysis. New York: IEEE Press, 2009: 135-140.
[9] ZHANG Y B, ZHANG L F, ZHU X R, et al. Reducing metal artifacts in cone-beam CT images by preprocessing projection data[J]. International Journal of Radiation Oncology·Biology·Physics, 2007, 67(3): 924-932.
[10] BEISTER M, PRELL D, KYRIAKOU Y, et al. GPU-accelerated metal artifact reduction (MAR) in FD-CT[C]//Medical Imaging 2010: Physics of Medical Imaging. San Diego: SPIE Press, 2010: 76223D.
[11] PRELL D, KYRIAKOU Y, STRUFFERT T, et al. Metal artifact reduction for clipping and coiling in interventional C-arm CT[J]. American Journal of Neuroradiology, 2010, 31(4): 634-639.
[12] BORNEMANN F, MÄRZ T. Fast image inpainting based on coherence transport[J]. Journal of Mathematical Imaging and Vision, 2007, 28(3): 259-278.
[13] 张意, 蒲亦非, 张卫华, 等. 基于一致性扩散的非迭代快速CT金属伪影去除算法[J]. 四川大学学报: 工程科学版, 2013, 45(2): 81-87, 93. ZHANG Y, PU Y F, ZHANG W H, et al. A novel non-iterative metal artifact reduction algorithm using coherence transport in computed tomography[J]. Journal of Sichuan University: Engineering Science Edition, 2013, 45(2): 81-87, 93 (in Chinese).
[14] GUNTURK B. Fast bilateral filter with arbitrary range and domain kernels[C]//2010 IEEE International Conference on Image Processing. New York: IEEE Press, 2010: 3289-3292.
[15] OZA S, JOSHI K R. CUDA based fast bilateral filter for medical imaging[C]//2018 5th International Conference on Signal Processing and Integrated Networks (SPIN). New York: IEEE Press, 2018: 930-935.
[16] PAPARI G, IDOWU N, VARSLOT T. Fast bilateral filtering for denoising large 3D images[J]. IEEE Transactions on Image Processing, 2017, 26(1): 251-261.
[17] 陈金位, 吴冰. 二维直方图重建和降维的Otsu阈值分割算法[J]. 图学学报, 2015, 36(4): 570-575. CHEN J W, WU B. A otsu threshold segmentation method based on rebuilding and dimension reduction of the two-dimensional histogram[J]. Journal of Graphics, 2015, 36(4): 570-575 (in Chinese).
[18] 陈培兴, 王明泉, 李世虎, 等. 基于形态学和Otsu的固体火箭发动机CT缺陷三维分割[J]. 图学学报, 2015, 36(4): 581-586. CHEN P X, WANG M Q, LI S H, et al. 3D CT defects segmentation of solid rocket motor based on the morphology and otsu[J]. Journal of Graphics, 2015, 36(4): 581-586 (in Chinese).
[19] BAL M, SPIES L. Metal artifact reduction in CT using tissue-class modeling and adaptive prefiltering[J]. Medical Physics, 2006, 33(8): 2852-2859.
[20] SHI B Q, LIANG J, LIU Q. Adaptive simplification of point cloud using k-means clustering[J]. Computer-Aided Design, 2011, 43(8): 910-922.
[21] RODET T, NOO F, DEFRISE M. The cone-beam algorithm of Feldkamp, Davis, and Kress preserves oblique line integrals[J]. Medical Physics, 2004, 31(7): 1972-1975.
[22] LIU Y C, ZHANG C S, LI W R, et al. An adaptive multiscale anisotropic diffusion regularized image reconstruction method for digital breast tomosynthesis[J]. Australasian Physical & Engineering Sciences in Medicine, 2018, 41(4): 993-1008.
[23] 刘泽, 孙丰荣, 李艳玲, 等. 基于3D Shepp-Logan头部模型的三维医学图像重建仿真[J]. 生物医学工程学杂志, 2006(5): 938-943. LIU Z, SUN F R, LI Y L, et al. The three-dimension medical image reconstruction simulation on 3D Shepp-Logan head phantom[J]. Journal of Biomedical Engineering, 2006, 23(5): 938-943 (in Chinese).
[24] BOONE J M, SEIBERT J A. An accurate method for computer-generating tungsten anode X-ray spectra from 30 to 140 kV[J]. Medical Physics, 1997, 24(11): 1661-1670.
[25] SIDDON R L. Fast calculation of the exact radiological path for a three-dimensional CT array[J]. Medical Physics, 1985, 12(2): 252-255.
[26] 陈平, 潘晋孝, 刘宾. 连续能谱X-CT投影仿真算法[J]. 无损检测, 2009, 31(2): 102-104. CHEN P, PAN J X, LIU B. Simulation arithmetic of X-CT projection based on consecutive spectrum[J]. Nondestructive Testing, 2009, 31(2): 102-104 (in Chinese).
A prior-image-based metal artifact reduction method for cone beam CT
LIU Yang-chuan1, GAO Peng1,2, ZHU Ye-chen1, GAO Xin1
(1. Medical Imaging Department, Suzhou Institute of Biomedical Engineering and Technology, Chinese Academy of Sciences, Suzhou Jiangsu 215163, China; 2. School of Electronic and Optical Engineering, Nanjing University of Science and Technology, Nanjing Jiangsu 210094, China)
To effectively suppress the artifacts caused by metal implants in the reconstruction process of cone beam CT (CBCT) image, a prior-image-based metal artifact reduction method was proposed. Firstly, the reconstructed image with metal artifacts was preprocessed by bilateral filtering, metal threshold segmentation and tissue clustering to produce the metal image and the prior image without metal information. Secondly, the metal image and prior image were respectively forward-projected to produce the metal projection region and prior projection data. Then, the metal projection region was interpolated by the prior projection data and the metal neighborhood projection data to produce the restored projection data. Finally, the CT image was reconstructed by the FDK algorithm and was fused with the metal image to produce the final corrected image. To verify the performance of the proposed algorithm, the metal artifact reduction experiments were carried out on the 3D Shepp-Logan head phantom and clinical head CT data. The experimental results show that compared with the commonly used linear-interpolation-based method and image-inpainting-based method, the corrected image of the proposed method can keep the root-mean-square error to the minimum and the peak signal-to-noise ratio to the maximum. This indicates that the proposed method can effectively suppress metal artifacts while preserving image edge information.
cone beam CT; metal artifact reduction; bilateral filtering; prior image; interpolation
TP 751.1
10.11996/JG.j.2095-302X.2020040529
A
2095-302X(2020)04-0529-10
2020-02-11;
2020-04-22
22 April,2020
11 February,2020;
国家自然科学基金项目(61801475);中国博士后科学基金项目(2018M642320);江苏省博士后科研资助项目(2018K180C);中科院苏州医工所自主部署项目(Y95K091K05);天津市科技计划项目(19YDYGHZ00030)
National Natural Science Foundation of China (61801475); China Postdoctoral Science Foundation (2018M642320); Jiangsu Planned Projects for Postdoctoral Research Funds (2018K180C); Suzhou Institute of Biomedical Engineering and Technology (CAS) Planned Projects (Y95K091K05); Science and Technology Plan Projects of Tianjing (19YDYGHZ00030)
刘仰川(1987-),男,山东济宁人,副研究员,博士。主要研究方向为X射线断层成像技术。E-mail:liuyangchuan2006@163.com
LIU Yang-chuan (1987-), male, associate professor, Ph.D. His main research interests cover X-ray tomography. E-mail:liuyangchuan2006@163.com
高 欣(1975-),男,吉林吉林人,研究员,博士。主要研究方向为介入诊疗。E-mail:xingaosam@yahoo.com
GAO Xin (1975-), male, professor, Ph.D. His main research interests cover interventional diagnosis and treatment. E-mail:xingaosam@yahoo.com
