上颌窦黏膜病变对上颌窦底提升术的影响及治疗对策
2020-08-29容明灯周腾飞
容明灯, 周腾飞
南方医科大学口腔医院牙周种植科,广东 广州(510280)
上颌窦底提升术(maxillary sinus floor elevation,MSFE),以下简称窦底提升术,包括侧壁开窗入路的外提升和经牙槽嵴顶入路的内提升,自Tatum 教授开创以来获得了极大的发展,已被公认为一种有效的上颌后牙区的骨增量手段[1]。然而,上颌窦黏膜病变(sinus membrane lesions)如病理性增厚及囊肿等,种类繁多,临床表现及预后不一,给这一治疗方式的疗效带来了不确定性。因此,口腔种植治疗中加强对这些疾病的认识及处理显得格外重要,笔者对上颌窦黏膜病变对上颌窦底提升术的影响及治疗对策作一专题述评。
1 健康上颌窦黏膜的解剖生理学
上颌窦是人体最大的一对气化鼻旁窦,上颌窦黏膜(sinus membrane,SM),以下简称黏膜,又叫施耐德膜(Schneiderian membrane,SM),内衬于窦腔骨壁上并通过上颌窦口与鼻腔黏膜相续。黏膜为一薄层纤毛柱状呼吸上皮,具体由假复层纤毛柱状上皮、固有层及基底骨膜三层构成[2]。纤毛柱状上皮主要由带纤毛的柱状细胞及分泌黏液的杯状细胞构成;固有层结缔组织含有胶原、血管(不及鼻腔黏膜丰富)、神经及腺体;而基底骨膜层则紧贴窦腔的皮质骨壁,包含具有再生分化潜能的间充质干细胞。黏液-纤毛清除系统(muscus-cilia clearance system,MCS)及窦口-鼻道功能复合体(ostio-meatal complex,OMC)共同组成了黏膜的防御屏障,也是窦腔通气引流的解剖组织学基础[3]。通过纤毛的定向协同摆动,黏膜可将分泌的黏液及其中的脱落坏死组织、致病菌、异物等逆重力从窦口转运出去。除机械防御外,黏膜还具有保温加湿、血供营养、成骨潜能等诸多功能[4]。黏膜由上颌动脉的分支上牙槽后动脉、眶下动脉及其交通支牙槽上颌窦动脉等营养,由上颌神经的分支眶下神经、上牙槽前、中、后神经等支配[5]。其中牙槽上颌窦动脉可有黏膜下、切迹和骨壁骨管内三种行走形式,窦提升术中需注意避免损伤它们而出血,尤其是骨管内形式出血风险高。
健康的上颌窦黏膜呈淡蓝色,吸烟者的黏膜将变黄且薄[2]。研究发现,当窦黏膜厚度低于2 mm时,即难以在CBCT 上显示[6](图1)。
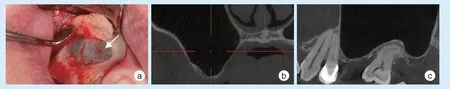
Figure 1 The healthy sinus membrane图1 健康的上颌窦黏膜
研究报道黏膜厚度在新鲜尸体上检测为0.3~0.8 mm[7],在CT 影像上为0.80~1.99 mm[8-10]。性别、年龄、种族、测量方法及部位等因素都会使结果产生较大的变异性。
健康的黏膜具有弹性,窦提升术中剥离时不容易撕裂穿孔。研究表明健康黏膜可被一维方向拉伸132.6%,二维方向上拉伸124.7%,而大于7.3 N/mm3的张力可导致黏膜穿孔[7]。健康黏膜可以抵御窦提升剥离过程产生的适当张力而不破裂[9]。此外,黏膜对窦提升手术操作也有充分的适应性,表现为术后轻度可逆的炎性水肿,通常在术后1 周达到顶峰,再于6~12 个月后逐渐恢复正常[11]。健康黏膜良好的顺应性使得窦提升术对上颌窦的通气引流影响较小。
2 上颌窦黏膜病变
上颌窦黏膜病变的病因多样:①窦外因素,如邻近根尖周炎、牙周炎、残根及种植体脱入上颌窦、季节环境、过敏性鼻炎、吸烟等;②窦内因素,包括主窦口堵塞、副窦口异常黏液回流及窦内原发疾病等。事实上,任何损害上颌窦的黏液转运及通气引流的因素,都可能诱发内衬黏膜的病变。黏膜病变类型不同,临床表现也不一,具有特定的人口学特点。通常,炎性病变的黏膜组织学上表现为纤毛细胞的脱落减少、杯状细胞的增多、固有层纤维化及炎症细胞浸润;宏观上则表现为黏膜增厚、息肉或囊性化、黏液蓄积及感染[12]。
针对这些病变,口腔临床上主要使用全景片和CBCT 来检测。相比于全景片,CBCT 影像重叠、扭曲少,信息量和分辨率更高,被广泛应用于窦提升术前后对上颌窦的评估中[13]。除关注传统参数如缺牙区剩余牙槽嵴高度、宽度等外,对黏膜健康状态的评估同样不可忽视。有研究报道黏膜病变在口腔种植患者中的检出率高达45.1%,并可能对手术效果产生影响[14]。
黏膜病变种类繁多,表现不一。本述评中,根据黏膜病变的CBCT 影像学特点,主要讨论其中三大类:①黏膜病理性增厚;②息肉/囊性病变;③气-液平面。其中息肉和囊肿有时具有相似的影像学表现,将其归类一起讨论。而气-液平面的病因又与窦黏膜相关,因此也被纳入分析。而其他影像学上可见的类型如突入窦腔的根尖周囊肿、角化囊肿、真菌性的上颌窦结石、良/恶性肿瘤病变等,在此述评中不做赘述。
2.1 黏膜病理性增厚
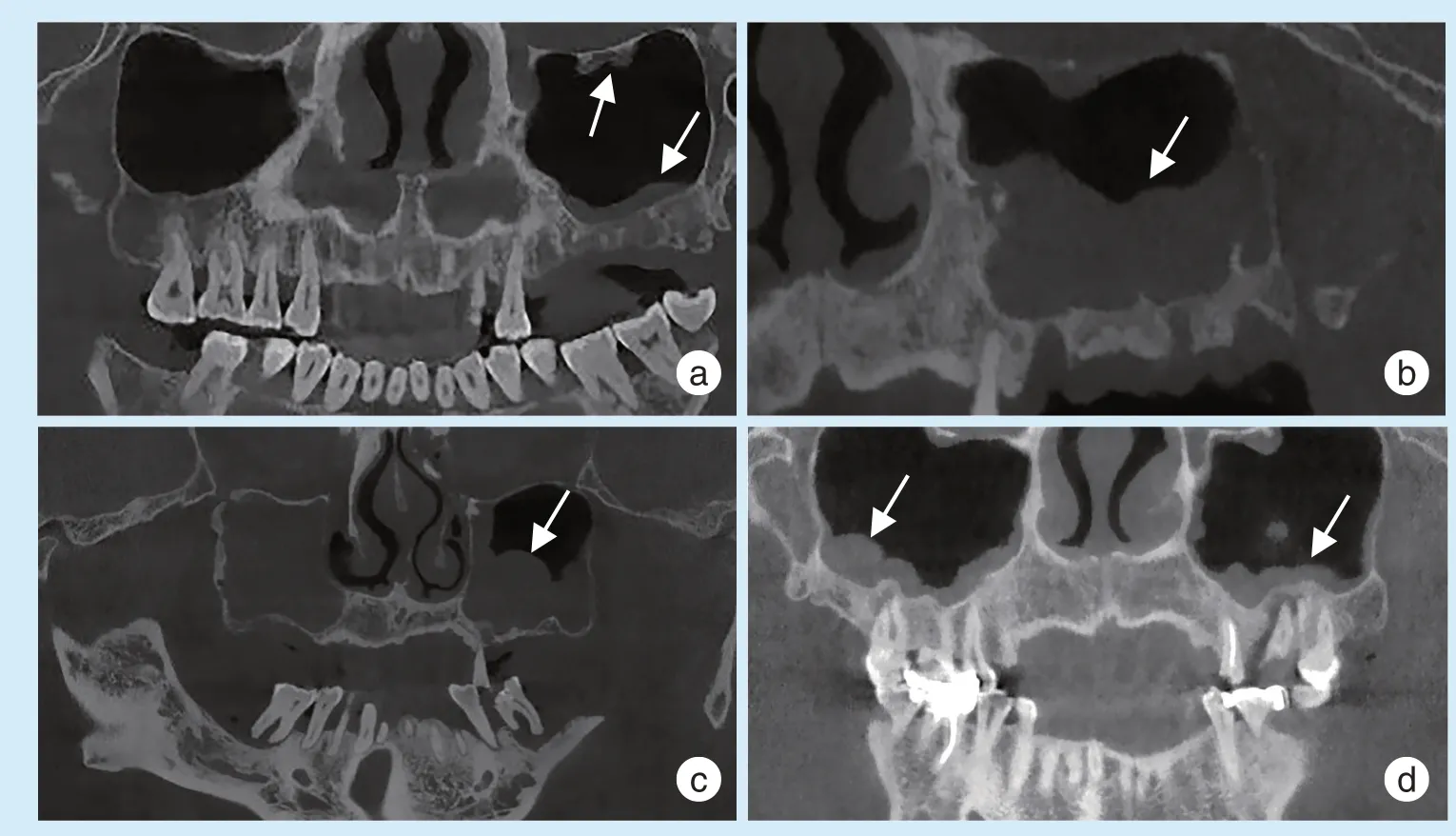
Figure 2 Pathological membrane thickening of maxillary sinus图2 上颌窦黏膜的病理性增厚
黏膜增厚是影像学上最常见的病变类型,一项系统评价研究指出其发病率在40%~60%[17],具体因样本选择、检测工具、部位、增厚的阈值设定等因素而存在较大变异。增厚的黏膜影像上常为均匀平坦样、息肉样、不规则样等多种形式,其中又以均匀平坦样增厚最为多见[16](图2)。黏膜增厚可单独或伴随其它病变一起出现。当前学术界对黏膜病理性增厚(pathological membrane thickening,PMT)的阈值仍未达成共识,出现了1、2、3、4、5 mm 等多种阈值标准[17]。尽管如此,2 mm 仍被广泛采纳作为黏膜病理性增厚的阈值[18],主要考虑到:厚于2 mm 的黏膜在大多数上颌窦炎的患者中能被检出;而薄于2 mm 者在CBCT 上难以显影。同样,黏膜病理性增厚的病因也未有定论。炎症、过敏和鼻腔及窦口-鼻道复合体的解剖变异(如鼻中隔偏曲、窦腔分隔、泡状鼻甲、哈勒腔等)被认为与之相关[17]。
2.2 息肉/囊性病变
上颌窦息肉/囊性病变(polyp/cystic lesion)也是一种常见的良性黏膜病变,CBCT 检出率约7%[19]。多数不伴明显的临床症状,当息肉/囊肿较大时也可有头痛,面颊部窦区的压迫感、鼻塞、鼻后溢液等症状。根据其组织学及影像学特点,我们常将其简单分为五类:息肉、黏液囊肿、潴留囊肿、假性囊肿、血肿及脓肿(图3)。需指出的是,假性囊肿、血肿及脓肿非真性囊肿,但因其具有相似的囊肿样影像学特点,因此也一并在此分类中对其讨论。
2.2.1 上颌窦息肉(polyps) 主要有两类:一是普通息肉,临床检出率18.2%,影像上呈圆形,带蒂,体积较小,常附着起源于窦腔的外侧和上壁。通常无临床症状,也无需特殊处理[15]。另一类是上颌窦鼻后孔息肉(antrochoanal polyps,ACP),即Killian 息肉[20]。它是少见的良性病变,单侧好发,多见于儿童及青少年中。病因多为慢性上颌窦炎及过敏反应的激惹。影像上表现为窦腔内的囊性部分以及穿过窦口、中鼻道,延伸至后鼻孔的实体部分,呈哑铃状。它可有伴阻塞与鼻液溢漏等症状,一般需手术摘除,预后良好,但可有复发。

Figure 3 Maxillary sinus polyp/cystic lesions图3 上颌窦黏膜息肉或囊肿样病变
2.2.2 黏液囊肿(mucocele) 多因过敏反应、手术粘连、外伤等导致上颌窦口狭窄、堵塞,黏液、脱落上皮等蓄积形成,具有大量杯状细胞化生的衬里上皮;也有研究认为它是窦黏膜的上皮包含性囊肿中央液化坏死而来[19,21]。囊腔增大的静水压可刺激前列腺素、甲状旁腺素释放,从而激活破骨细胞,导致周围骨质侵蚀。囊肿多见于额窦及筛窦,在上颌窦则较为少见。影像学上可见窦腔大范围的软组织影像,或充满整个窦腔,可伴有邻近骨壁的压迫性吸收或硬化,但又不同于恶性肿瘤导致的虫蚀样、溶骨样破坏。黏液囊肿伴感染时则为黏液化脓性囊肿(脓液囊肿)。黏液囊肿有时需要与慢性炎症下的全窦腔浑浊区分,后者不伴有邻
近骨壁的侵蚀且通常有邻近的病灶牙。由于其较大的体积和骨侵蚀性,黏液囊肿通常是窦提升术的禁忌证,需要在术前摘除。
2.2.3 潴留囊肿(mucous retention cysts,MRC) 又称黏膜囊肿,因黏膜内的浆液性腺体导管阻塞,黏蛋白和干酪样物蓄积形成,具有衬里上皮[19]。它通常较小,圆球形或半球形,一个或多个,分布于单侧或双侧上颌窦。窦口附近腺体较多,是其好发区域。潴留囊肿在影像上常难以检出,且多无临床症状,也无需特殊处理。
2.2.4 假性囊肿(antral pseudocysts) 或称非分泌型囊肿,最为常见。囊肿无衬里上皮,非真性囊肿,多由牙源性感染或过敏反应导致血管通透性增大,血浆成分外渗至软组织间隙内形成[19]。影像学上为孤立的圆顶状或类圆形低密度软组织影,邻近区域常能发现牙周、根尖周病灶,且其所在部位的牙槽突常较薄。体积较小的假性囊肿通常也不伴临床症状,无需特殊处理。
2.2.5 术后黏膜下血肿及脓肿(post-operative maxillary hematoma/abscess) 血肿常因窦底血管、窦黏膜损伤导致黏膜下出血,抬升黏膜后形成,而术前窦腔正常。它又被称为术后上颌窦囊肿,非真性囊肿[22]。术后黏膜下血肿不同于窦腔积血,后者多由于黏膜穿孔出血形成,二者皆可逐渐自行机化消散。血肿的机化过程可伴内衬上皮的长入,此时则会形成真性囊肿。上颌窦黏膜下脓肿多由局部牙源性病灶的化脓性感染扩散导致。术后黏膜下血肿及脓肿影像上同囊肿形状相似,呈圆顶样或类圆形膨隆,邻近可发现病灶牙的存在,皆非真性囊肿。通常在完善病灶牙的治疗或拔除病灶牙后,“囊肿”消失,或转归为略增厚的黏膜影像。
囊肿的病理检查是其确诊分型的金标准。在缺乏病理诊断的情况下,考虑到潴留囊肿和假性囊肿二者具有相似的影像表现和临床行为,临床上有时并未加以区分而统称为潴留(或假性)囊肿,其处理方式也相似。
2.3 气-液平面
气-液平面(air-liquid level)是上颌窦内的空气与液体的交界面,因二者对射线的透射性差异而形成。液平面通常是上颌窦急性炎症的强烈指示信号,可由急性上颌窦炎或慢性上颌窦炎急性发作导致[23]。此外,上颌窦的骨瘤、外伤骨折、窦腔内囊肿破裂囊液外溢等也会出现液平面。上颌窦的积液可为“水”性(炎性渗出液)、血性(黏膜穿孔出血)和脓性(化脓性感染),具有不同于黏膜的影像学灰度值。积液中有时可见气泡,积液充满窦腔时液平面消失。黏膜穿孔后骨移植材料流失至窦腔可引发术后急性上颌窦炎,影像上可见夹杂了阻射性骨颗粒的液平面(图4)。
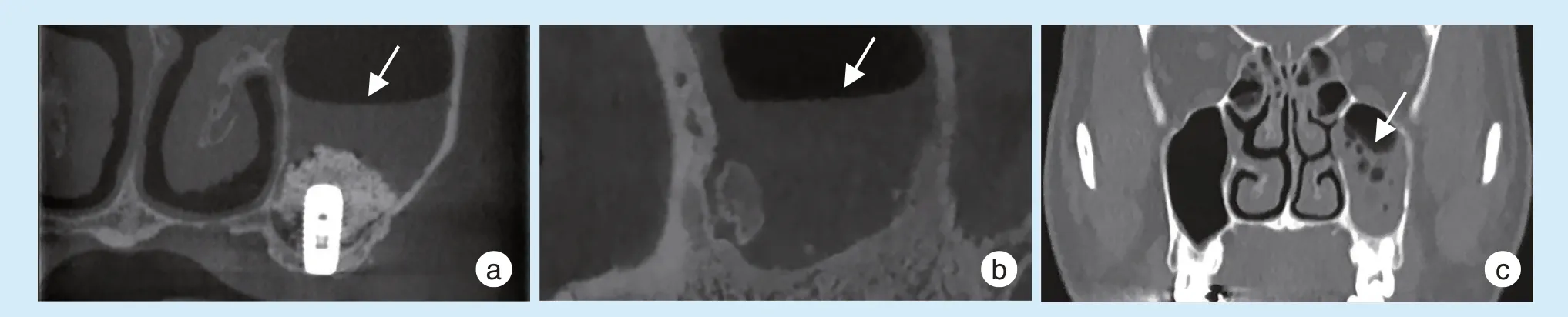
Figure 4 Air-liquid level of maxillary sinus图4 上颌窦窦腔的气-液平面
牙源性上颌窦炎占上颌窦炎10%~12%,而任何损害窦黏膜完整性的解剖及医源性因素都能导致,如牙根突入窦腔、牙周/根尖周病变、上颌后牙区的牙拔除、口腔-上颌窦穿通/瘘管、口腔种植治疗导致的黏膜穿孔等[24]。急性上颌窦炎是指具有显著的鼻窦炎症状且病程不超过4 周,通常继发于病毒性的上呼吸道感染,典型症状如头痛、鼻塞、脓涕、面部疼痛、嗅觉减退等;慢性上颌窦炎通常无疼痛,在急性加重时也可伴有疼痛;而牙源性上颌窦炎除鼻窦炎的症状外,一般同时具有邻近口腔及牙的病灶表现[23]。
3 黏膜病变对上颌窦底提升术的影响及治疗对策
3.1 黏膜增厚
黏膜撕裂穿孔是窦提升术的一个常见并发症,可能导致移植物感染及上颌窦炎[25]。以往认为过薄的黏膜拉伸强度下降,在剥离时更容易发生穿孔[26]。近期研究发现增厚的黏膜同样也会诱发穿孔:1.5~2 mm 厚的黏膜在经牙槽嵴顶入路提升时穿孔最少[27],1~1.5 mm 厚的黏膜在经外侧壁入路提升时穿孔最少[4]。过薄的黏膜抗性降低;过厚的黏膜可能改变其原有的组织学结构,黏膜脆性增大且易粘连;而厚度适中的黏膜因兼具较好的力学抗性和合理的组织学结构而不易穿孔。此外,显著抬升的黏膜还可能阻塞窦口,研究表明厚度大于5 mm且伴有息肉的黏膜与窦口堵塞相关[28]。
尽管病理性增厚的黏膜可能与黏膜穿孔和窦口阻塞相关,当前研究仍然认为2~5 mm 且无症状的黏膜增厚可以进行窦提升术[29];甚至黏膜增厚大于5 mm 者,在确保其窦口通畅开放的情况下也不容易导致骨移植的失败[30]。因此,无症状的黏膜增厚不是窦提升术的禁忌证。然而,笔者依然建议:对于黏膜增厚大于5 mm 者,需仔细评估其窦口的开放性;而对伴有窦口阻塞且黏膜显著增厚的患者,窦提升术应慎重。应当积极查找及清除致病因素,待3~6个月再评估后再行治疗(图5)。
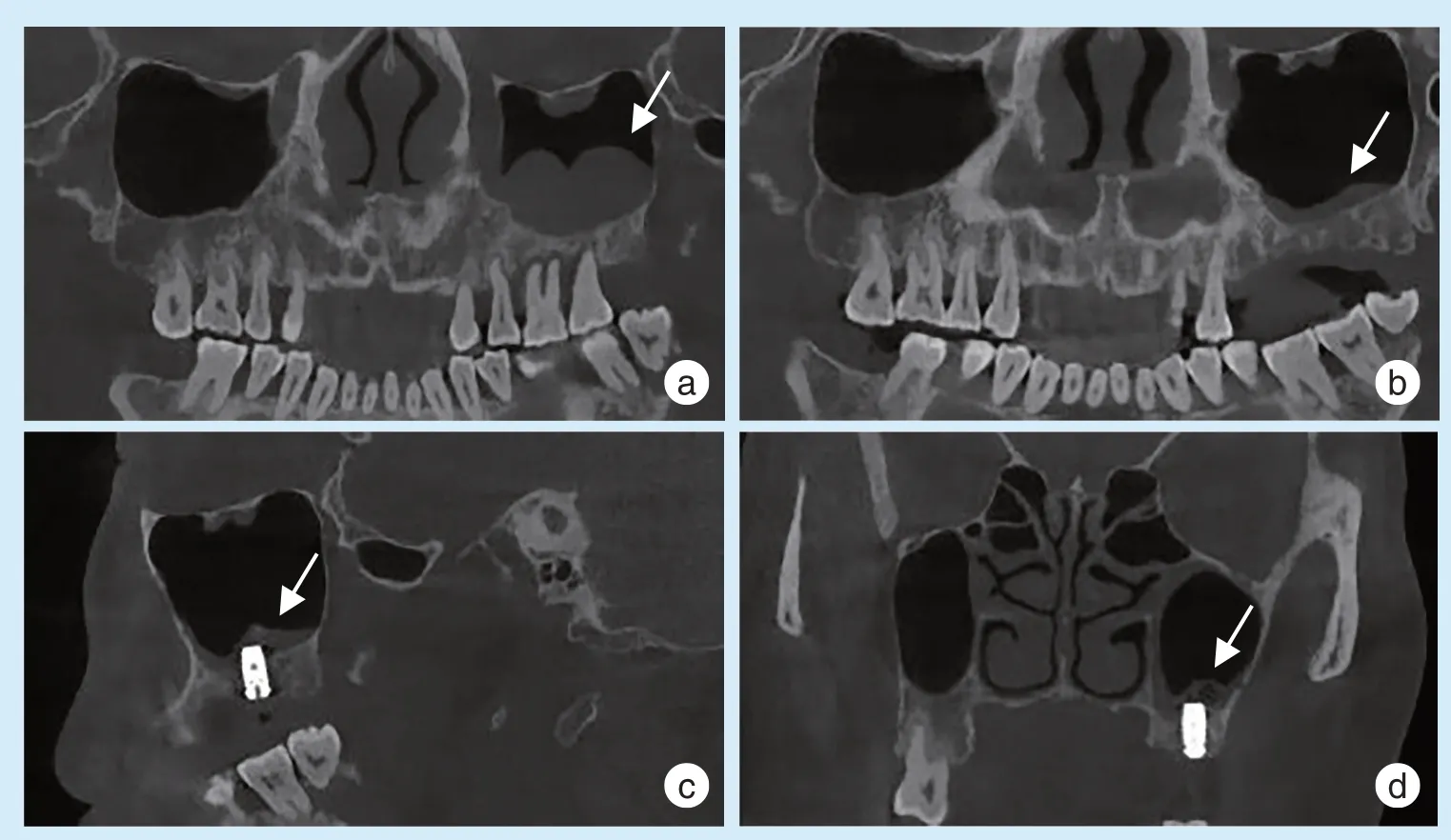
Figure 5 Maxillary sinus membrane thickening and sinus floor elevation图5 上颌窦黏膜增厚与窦提升术
3.2 息肉/囊性病变
小的普通息肉常无需处理[18];上颌窦后鼻孔息肉则需术前摘除[20],为减少复发,通常采用功能性内窥镜上颌窦手术(functional endoscopic sinus surgery,FESS)摘除其窦腔部分及基底附着[31];黏液囊肿也需术前摘除[21]。潴留囊肿和假性囊肿生物学行为温和,通常无需处理。以往认为上颌窦囊肿是窦提升术的绝对禁忌证,应当在窦提升术前将囊肿摘除[32]。近年来,研究表明假性囊肿不再是窦提升术的禁忌证,其存在也不会对新骨形成、术后并发症和种植成功率产生明显影响[33]。
然而,术区的过大的囊肿也存在风险:①囊肿膨胀及囊壁菲薄化使得黏膜张力及脆性增大;若伴有感染,黏膜易与骨壁粘连。这些都容易导致黏膜的撕裂穿孔;②术中囊肿破裂囊液外溢,可能诱发骨移植物的感染;③囊肿改变了上颌窦的局部解剖形态,盲视下的内提升手术风险增加;④抬升的囊肿可能会阻塞窦口,干扰窦腔的生理性通气引流,从而诱发感染;⑤保留囊肿的方案理论上存在误诊漏诊的可能性。目前,临床上关于较大的假性(潴留)囊肿对窦提升术的影响仍存在争议,主要存在以下三种处理方式:①保留囊肿同期行窦提升术;②术前摘除囊肿,二期行窦提升术;③术中同期行囊肿摘除和窦提升术。笔者提出这些风险并非更鼓励术前摘除囊肿的方案,而是为了说明在处理囊肿时应有更全面考虑。
在进行临床方案抉择时,囊肿的大小可作为一个定量指标辅助参考。研究表明上颌窦窦口高度一般为18~35 mm,平均为25.6 mm[34]。当囊肿较大时(高度大于18 mm 者),保留的囊肿合并术后的炎性水肿很可能会堵塞窦口;若术中或术后囊肿破裂,囊液的引流不畅,从而诱发感染和窦底提升手术失败;而对于小于18 mm 的较小囊肿,即便存在囊肿破溃的意外,由于窦腔正常的通畅引流,再辅之以耳鼻喉科的窦口引流等处理后,感染可被有效控制。也有研究报道这一参考高度是窦腔高度的一半,认为窦腔平均高度为25 mm,而一半的窦腔高度再加上10 mm(通常足够用于窦提升)也不会阻塞窦口[35]。
笔者认为,在考虑囊肿的大小对窦提升术的影响时,需综合考虑囊肿高度、窦口高度、提升高度、预估炎性水肿高度及窦内炎症等多个因素。理论上可以简单认为,当囊肿高度及上窦提升高度之和不超过窦口高度时,可以保留囊肿进行窦提升术(窦腔无炎症情况下)。考虑到人群的窦口高度存在较大的变异性,因此笔者更建议采用“窦口高度的一半”这一比例性指标。
基于上述分析,笔者谨慎建议如下:以窦口一半高度作为界,低于一半高度的小囊肿可以保留并行窦提升术(保留囊肿存在误诊漏诊可能性,需加强术前影像分析,精细术中操作,同时严格术后随访)(图6)。而对于大于一半高度的大囊肿,主要有两种处理方式:①术前摘除囊肿,延期行窦提升术;②术中摘除囊肿,同期行窦提升术。
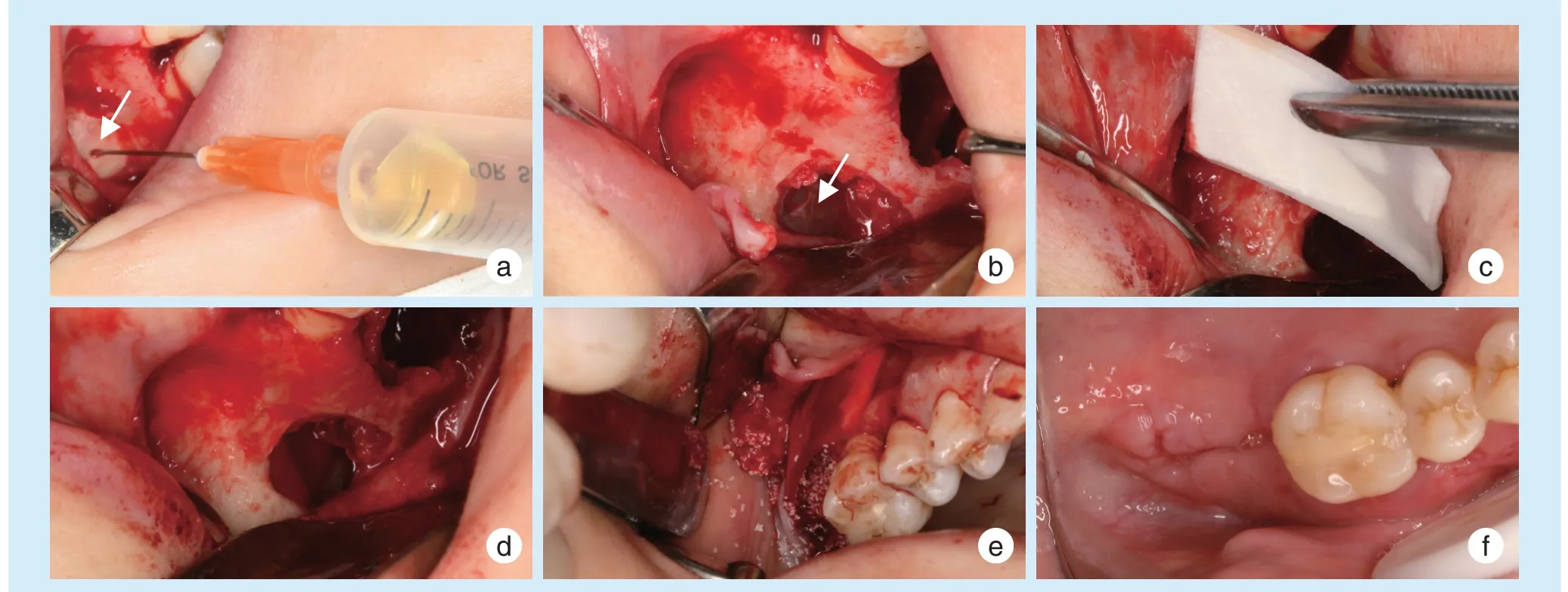
Figure 6 Sinus floor elevation with the cyst retained图6 保留囊肿行窦提升术
3.2.1 术前摘除囊肿,延期行窦提升术 对于黏液囊肿、上颌窦后鼻孔息肉、诊断不明且特别大的囊肿等,建议转诊至耳鼻喉专科进一步确诊并手术摘除后再行窦提升术。Caldwell-Luc 术式创伤大,愈合期长(6~12 个月),并发症也更多。FESS 或侧壁开窗入路等方式已成为主流手术用于术前摘除窦内囊肿[36]。这种“两步法”的保守处理,可以减少窦提升术时的风险和并发症。然而,它也显著延长了治疗周期,且二次手术也增加了患者的花费和身心痛苦。
3.2.2 术中摘除囊肿,同期行窦提升术 对于诊断明确且体积不大的囊肿,可同期行囊肿摘除和窦提升术,囊肿的摘除由口腔医生完成(图7)。多采用共用一个侧壁开窗口摘除囊肿合并外提升,或采用一个侧壁开窗口摘除囊肿合并经牙槽嵴顶的内提升进行处理[33]。笔者常用注射器抽吸囊液缩小囊肿的体积,再配合血管钳抓取其蒂部来摘除。囊肿的摘除很难避免黏膜的穿孔,可以轻柔地剥离穿孔周围的黏膜来缩小穿孔范围。对穿孔的关闭常采用直接缝合、生物膜、块状骨、颊脂垫等修复方式。Bio-guide 等可吸收性生物膜被常用来关闭穿孔,穿孔较大时还需使用膜钉固定以防止膜的继发性移动。同期种植需要良好的骨质条件、种植体的初期稳定性、窦内无感染等,对医生的术前评估及术中操作要求更高,同时也需结合患者自身对治疗周期及费用等方面的诉求。
结合当前口腔医学临床、基础研究及笔者科室团队的临床经验,认为对窦内息肉囊肿的处理需综合考虑多方因素,成功的治疗计划需涵盖以下要素:①全面的术前影像学分析;②完善的术前设计;③合理的外科工具选择;④精细的术中操作;⑤严格的术后随访等。术前CBCT 影像学分析时,除传统窦提升术需考虑的因素(如窦底形态、剩余牙槽嵴高度、宽度、上颌窦侧壁厚度、血管分布、窦内分隔等)之外,需额外关注息肉/囊肿的位置、囊肿大小高度、窦口高度、窦口的开放性、窦内炎症等信息。术中应遵循合理的外科程序,确保入路正确,术野清晰,操作轻柔,切忌盲目和蛮力操作导致囊肿破裂。超声骨刀等工具可以显著减少软组织的损伤,降低穿孔破裂的风险。若保留囊肿同期进行窦提升术,在骨粉充填或种植体植入时医生的操作更需谨慎。术后影像学分析需仔细评估是否存在黏膜(囊肿)的破裂和骨移植物的流失,同时做好积极的抗感染应对,并定期随访观察囊肿的转归。
3.3 气-液平面
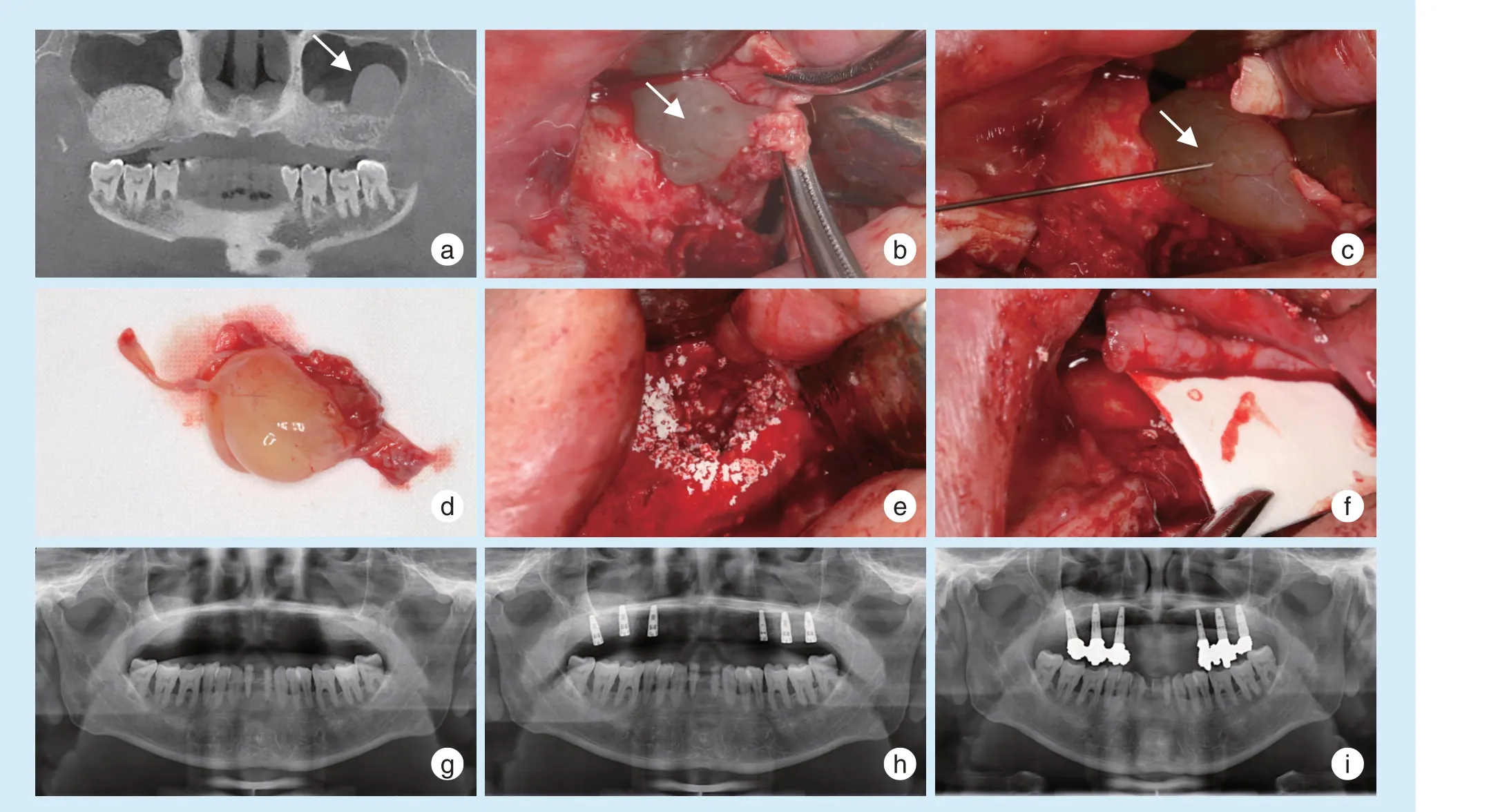
Figure 7 Simultaneous sinus floor elevation with the cyst excised图7 摘除囊肿同期行窦提升术
液平面指示上颌窦急性炎症,也是窦提升术的禁忌证,需要在术前积极处理[23]。否则即便窦黏膜完整,也很容易导致炎症的激惹扩散。建议耳鼻喉专科会诊来协助诊治。通常,对急性上颌窦炎的处理主要包括对症支持治疗(鼻减充血剂等),冲洗引流和抗炎治疗。麻黄碱等药物可以收缩黏膜血管,开大窦口,通畅其自然引流。采用生理盐水等冲洗引流(图8)可以促进感染炎性渗出物的快速排出。如果炎症扩散到上颌窦以外或患者同时存在发热、脓涕等症状时,还可考虑加用一线抗生素治疗(如阿莫西林及头孢类等;过敏者采用左氧氟沙星、克拉霉素或多西霉素)。慢性上颌窦炎的急性发作者,处理基本同急性者,但在伴有息肉的患者中需辅以类固醇药物。对炎症顽固反复及药物治疗无效者,可考虑FESS 等手术治疗[37]。
4 术后上颌窦炎
术后上颌窦炎(post-operative sinusitis)是一类感染性的并发症,与传统的上颌窦炎相比,它在病因、临床症状、微生物组成及处理上均有所差异。术后上颌窦炎的病因多是牙源性感染或骨移植材料经黏膜穿孔扩散入窦腔导致[38]。值得注意的是,临床上一些小的或发生在种植体植入阶段的黏膜穿孔,术中视诊和Valsava 动作(捏紧患者鼻孔,嘱患者屏气并用力做呼气动作,若有漏气感及血/气泡冒出则有黏膜穿孔出现)往往难以发觉,而这些遗漏诊治的穿孔可导致术后上颌窦炎。条件允许时,手术放大镜或内窥镜及术后影像学评估可以帮助进行辨别。遗憾的是,仍然有一些小穿孔在术后即刻的影像上难以发现。术后上颌窦炎症状出现于窦提升术后,此外还可有特殊的口腔学表现(局部的肿痛、口腔-上颌窦穿通/瘘管、骨粉经瘘管溢出形成“爆米花”征等);影像学上表现为患侧囊肿破裂后变小,窦腔内液平面或浑浊,骨粉流失于窦腔中等;由于口腔环境的多菌群环境且牙周、根尖周病变多为厌氧菌感染,术后上颌窦炎常为厌氧菌为主的混合性感染(革兰阴性的消化链球菌、普氏菌、梭杆菌等),而传统上颌窦炎多为需氧菌感染(卡他莫拉菌、嗜血杆菌、肺炎链球菌等)[39]。
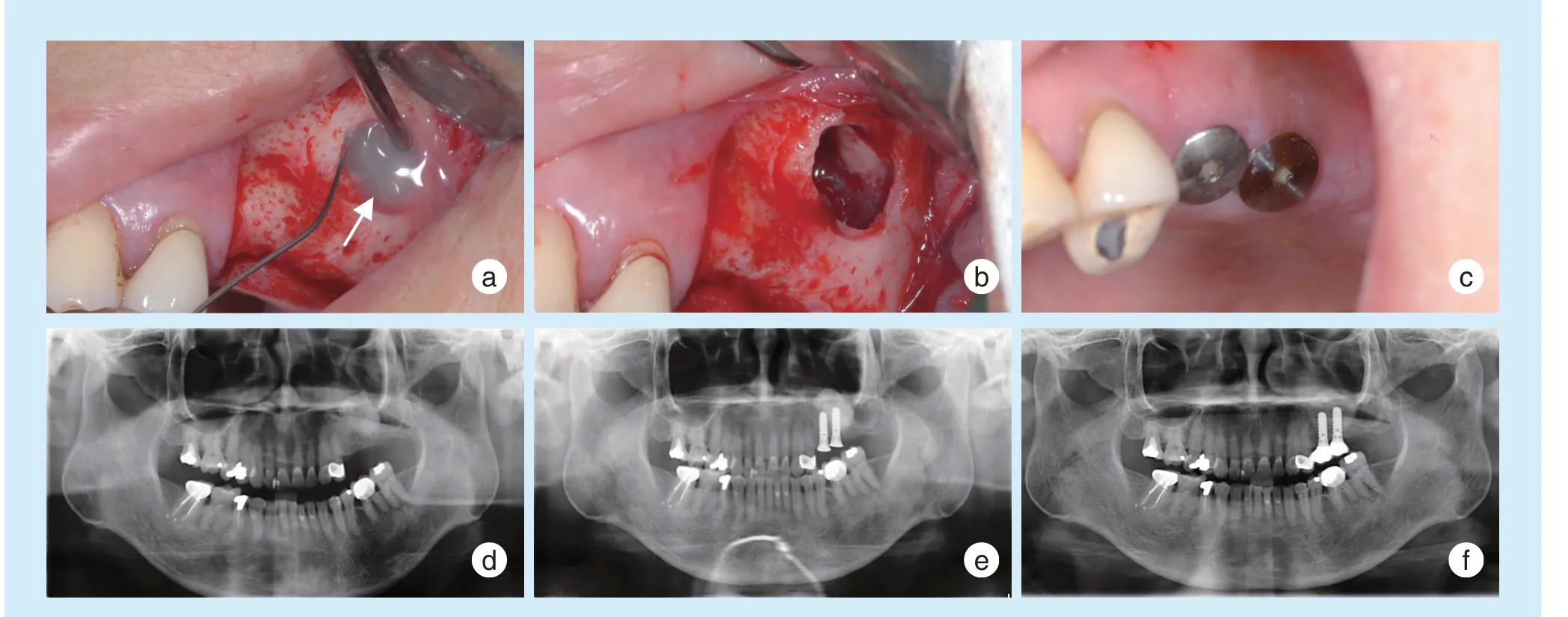
Figure 8 Presurgical maxillary sinusitis(air-liquid level)and sinus floor elevation图8 术前上颌窦炎(气-液平面)与窦提升术
笔者对术后上颌窦炎的治疗原则是:根除病因,通畅引流,控制感染,循序渐进,预防并发症以及口腔-耳鼻喉科协作治疗。在没有任何急性感染症状如发热、出血、溢脓等时,首选抗生素治疗,也可配合对症治疗(减鼻充血剂)和冲洗引流等处理。同时,消除口腔局部的病灶格外重要。此外,根据其微生物学特点还需同时加入针对这些厌氧菌的抗生素,如在阿莫西林的基础上联合甲硝唑类等药物。最后,对于术后上颌窦炎顽固反复、迁延不愈,或经口腔治疗、药物治疗等基础治疗无效者,外科清创手术(FESS 或侧壁开窗入路)也被推荐。术中需仔细清理窦内的坏死组织及感染的骨粉,必要时拔除种植体,并彻底冲洗引流。二期的骨增量手术需待上颌窦炎完全愈合后再开展。应当警惕严重的二级并发症如眶区蜂窝织炎、脑脓肿等的发生。对无法处理的术后上颌窦炎患者,建议将其转诊或在耳鼻喉医生会诊协助下治疗。事实上,耳鼻喉医生在上颌窦黏膜病变的治疗中扮演了重要角色,其工作应当贯穿术前诊断、预防性治疗、最终治疗等完整环节。无论如何,预防永远是最好的治疗方案。
5 总 结
上颌窦黏膜病变给上颌窦底提升术这一成熟的治疗方式带来了不确定性。基于当前的口腔医学临床及基础研究,并结合笔者科室团队的临床经验,对伴上颌窦黏膜病变的窦提升术这一专题进行归纳,并给出笔者团队的临床抉择流程以供参考(图9)。
①上颌窦黏膜病变病因复杂,常见类型有黏膜病理性增厚,黏膜息肉/囊性病变,窦腔气-液平面等;②2~5 mm 的黏膜病理性增厚影响较小,可同期行窦提升术;大于5 mm 且伴有窦口阻塞者需慎重;③黏膜的息肉/囊性病变对窦提升的影响需考虑息肉/囊肿的位置、类型、大小、窦内炎症、窦口开放性等因素。小的普通息肉、囊肿无需处理,可以考虑窦提升术;上颌窦-后鼻孔息肉、黏液囊肿需要术前手术摘除;小于一半窦口高度的囊肿可保留囊肿同期行窦提升术;大于一半高度者需考虑术前摘除囊肿延期行窦提升术或术中摘除囊肿并同期行窦提升术;对于较大的且分类不明的囊肿,优先考虑转诊或请耳鼻喉专科会诊协助治疗;④气-液平面是急性上颌窦炎的指征,治疗上需联合抗炎、对症支持及引流治疗;⑤术后上颌窦炎同样以抗炎、对症支持、引流治疗为主,必要时行外科清创术;⑥术前口腔颌面部病灶的清除、术前全面的CBCT 影像学分析、完善的术前设计、合理的外科工具的选择、精细的术中操作、严格的术后随访和口腔-耳鼻喉科协作管理等共同构成了伴上颌窦黏膜病变的患者行窦提升术的保护基石。
受限于笔者的临床经验及临床认识的深度,本述评的观点也将带有一定的局限性。因此,鼓励口腔医生结合自己的临床经验,根据患者的实际情况作出最佳的个性化诊疗方案,以最大程度降低其手术风险和减少并发症,达到最佳的治疗效果。未来仍需大量基础研究来进一步揭示上颌窦黏膜病变的分子学机制,以及大量大样本、前瞻性、长期随访的临床研究来深入验证分析其对窦提升术及种植的影响。
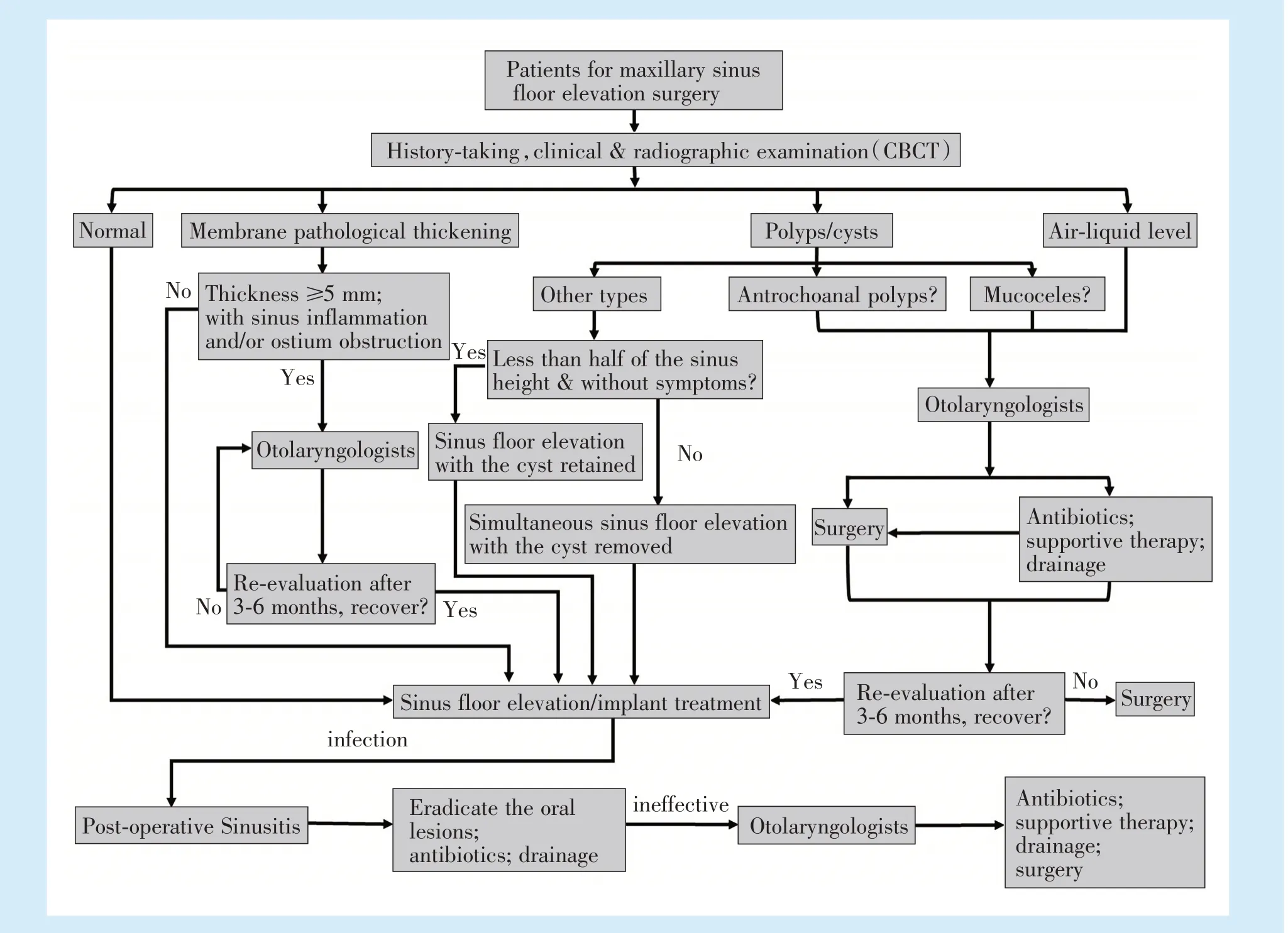
Figure 9 A decision-making workflow for patients with sinus membrane lesions who undergo the maxillary sinus floor elevation surgery图9 伴上颌窦黏膜病变的患者窦提升治疗的临床抉择流程图
致谢:感谢张雪洋主任和刘卫平主任对牙周种植科团队在上颌窦底提升术方面的理论指导和技术支持。
