邻苯三酚自氧化法对茶叶中茶多酚的抗氧化性能应用研究
2020-08-28陈仕学姚元勇卢忠英汪兰秦馨
陈仕学,姚元勇,卢忠英,汪兰,秦馨
(铜仁学院材料与化学工程学院,贵州铜仁554300)
茶作为当今世界上最为普及的功能性饮料,具有各种保健功效,从而引起人们的广泛关注。茶叶含有多种人体必须的有效成分,主要为咖啡碱、茶多酚(tea polyphones,TP)、氨基酸等,其中茶多酚约占茶叶干重15%~30%。茶多酚是茶叶中最重要的保健成分之一。茶多酚作为一种新型的天然抗氧化剂,具有消除体内产生的自由基、抗癌、抗氧化等功效。2015年,高媛圆等[1-3]研究证明:茶多酚对老年痴呆、糖尿病和乳腺癌具有防治和抑制作用;2019年,张劲等[4]对茶叶中的茶多酚功能进行研究,表明茶多酚具有抗氧化、降血脂、降血糖、清除人体自由基等功能,发现其对人的身体无毒副作用,且茶叶中的茶多酚含量是其他植物所无法相比的[5],因此在化工、食品、医药、护肤品等行业具有广阔的应用前景和开发价值[6-8]。
目前,国内外许多研究者对茶叶中茶多酚的抗氧化作用都作了一定的文献报道,认为茶多酚之所以具有抗氧化能力,是因为茶多酚中的主要成分儿茶素具有供氢功能的酚羟基[9],如王媛等报道:茶多酚具备优良的氢供体,因而能与体内过量的自由基作用,形成比较稳定的酚氧自由基,从而避免生物体遭受过量自由基造成的氧化损伤[10-11];程德竹等[12]运用紫外可见光分光光度法定量测定茶叶中茶多酚,通过加入茶多酚对邻苯三酚自氧化产生的超氧自由基的清除作用来评价茶叶中茶多酚抗氧化能力。但是由于不同测试体系的测试方法与其条件相差比较大,将对试验结果产生较大影响。
为了使试验更加准确可靠,本文首先要确定邻苯三酚自氧化反应条件,即邻苯三酚在碱性环境中自氧化的测定波长、反应时间、反应速率。在此条件下,测定不同类型茶叶中茶多酚对邻苯三酚自氧化反应产生超氧自由基的清除能力,从而评价不同类型茶叶抗氧化能力的强弱。目前,关于铜仁地区不同类型茶叶中茶多酚的提取有相关报道[13-14],但对其本地的茶叶中茶多酚抗氧化能力研究未见报道。因此,本文梵净山绿茶、梵净山小酱白茶、铜仁苦丁茶、石阡苔茶(红茶)为原料,采用邻苯三酚自氧化体系来评价不同类型茶叶的抗氧化能力,以期对开展茶叶的综合利用提供一定的参考依据。
1 材料、试剂与仪器
1.1 试验材料
梵净山绿茶、梵净山小酱白茶、铜仁苦丁茶、石阡苔茶(红茶):贵州芳瑞堂生物科技有限公司。
1.2 试验试剂
邻苯三酚:阿拉丁化学试剂网;磷酸盐(phosphate beffered soiution,PBS)缓冲液:博士德生物工程有限公司;盐酸:成都金山化学试剂有限公司;氢氧化钠:天津市恒兴化学试剂有限公司。以上试剂均为分析纯。
1.3 试验仪器
HHS数显式电热恒温水浴锅:上海博迅实业有限公司;100 μL~1 000 μL 移液枪:上海汉林有限公司;MP电子分析天平:上海恒平科学仪器有限公司;C-30玻璃仪器气流烘干器:郑州长城科贸有限公司;759S紫外可见分光光度计:上海棱光技术有限公司。
2 试验方法
2.1 邻苯三酚自氧化反应条件确定
2.1.1 检测波长的确定
精密量取5mL(pH=8.0)PBS缓冲溶液与0.1 mL(0.4 mg/mL)邻苯三酚溶液于10mL容量瓶中,用蒸馏水定容至10 mL。反应5 min后,以(pH=8.0)PBS缓冲液做空白对照,进行紫外光谱扫描,确定吸收峰波长。
2.1.2 反应时间与反应速率的确定
在检测波长确定下,每隔5 min进行1次紫外光谱扫描,共扫描50 min,然后以吸光值A对反应时间作线性关系图。挑选出线性关系最好的一段,其所经历的时间即为反应时间t,其方程的斜率为邻苯三酚自氧化速率V0,从而确定邻苯三酚自氧化反应时间与反应速率。
2.2 茶多酚的抗氧化试验研究
2.2.1 不同类型不同质量浓度茶叶中茶多酚对超氧自由基的清除
精密量取0.1 mL(0.4 mg/mL)邻苯三酚溶液和5 mL(pH=8.0)PBS缓冲液、分别加入不同浓度(0.04、0.06、0.08、0.12、0.14 mg/mL)的梵净山绿茶溶液 1 mL,置于10 mL容量瓶中,用蒸馏水定容至10 mL,反应5 min后,以(pH=8.0)PBS缓冲溶液做空白对照,在320 nm波长处,每隔5 min测定1次吸光值[15],共反应25 min;同法分别加入不同浓度(0.06、0.08、0.1、0.14、0.16 mg/mL)梵净山小酱白茶茶多酚溶液、不同浓度(0.1、0.12、0.14、0.16、0.18 mg/mL)石阡苔茶红茶茶多酚溶液、不同浓度(0.08、0.1、0.12、0.14、0.16 mg/mL)铜仁苦丁茶茶多酚溶液,从而比较不同类型不同浓度茶多酚的超氧自由基清除作用,以吸光值A对反应时间t作线性关系图,斜率记作V1,代入式(1),计算出不同质量浓度下的茶多酚对超氧自由基的清除率Y。

式中:Y为清除率;V1为邻苯三酚自氧化后加入样品检测吸收值;V0为邻苯三酚自氧化后检测吸收值。
2.2.2 不同类型茶叶中茶多酚对自由基的清除率与质量浓度线性关系
根据上述2.2.1的计算结果,以不同类型茶叶中茶多酚的质量浓度为横坐标,超氧自由基的清除率为纵坐标作图,得出茶叶中茶多酚对自由基的清除率与质量浓度的线性方程,根据方程可算出当清除率为50%时的茶多酚质量浓度(IC50)值,IC50值可以作为衡量抗氧化物清除超氧自由基能力的一个指标,其值越小,说明清除自由基能力越强[16]。通过比较不同类型茶叶中茶多酚的IC50大小,从而评价不同类型茶叶的抗氧化能力。
3 结果与分析
3.1 邻苯三酚自氧化反应测定波长
根据2.1.1的操作,其结果见图1。
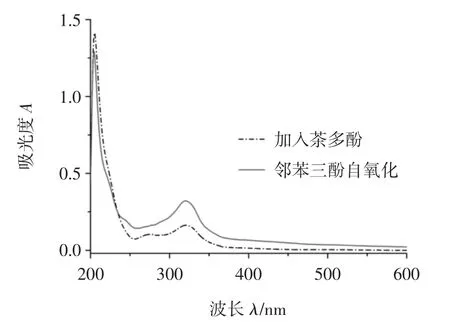
图1 邻苯三酚自氧化吸收波长扫描图Fig.1 Scanning image of catechol self-oxidation absorption wavelength
由图1可得,邻苯三酚法的原理为,邻苯三酚在碱性环境下会发生自氧化,产生超氧自由基,加入抗氧化剂后超氧自由基与其反应,超氧自由基的量减少,吸收峰降低。由此可知,邻苯三酚在碱性环境下发生自氧化时,在320 nm处出现最大吸收峰,故选择320 nm作为邻苯三酚自氧化的测定波长。
3.2 邻苯三酚自氧化反应时间确定
根据2.1.2的操作,结果见图2。
从图2可以看出:随着时间推进,反应体系在320 nm下吸光值逐渐增加,从35 min开始,其每分种的吸光度值的增量开始逐渐减小,到达50 min时,吸光度值趋于平衡,因而整个反应过程的吸光度值A和反应t的线性关系较差。而在前25 min的反应时间内,数据点均匀分布在趋势线两边,其线性关系较好,故邻苯三酚自氧化反应时间为25 min。
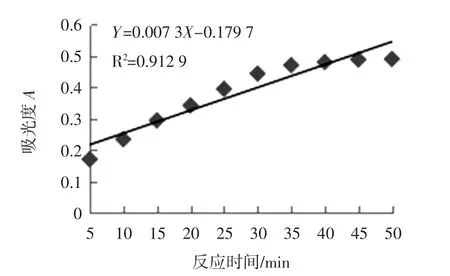
图2 邻苯三酚体系自氧化反应时间Fig.2 Autooxidation time of pyrogallol system
3.3 邻苯三酚自氧化反应体系速率的确定
根据2.1.2的操作,其结果见图3。
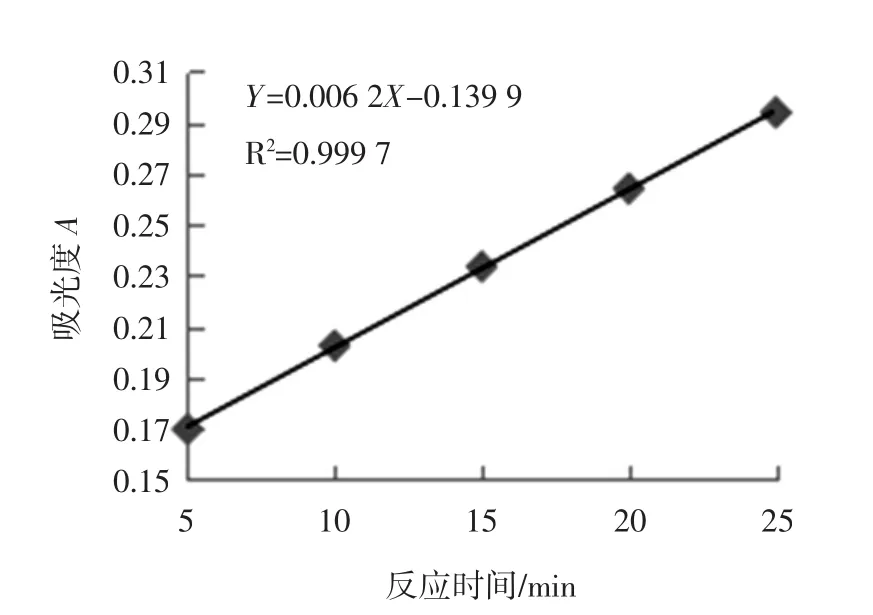
图3 邻苯三酚自氧化反应体系速率Fig.3 Rate of pyrogallol autooxidation reactionsystem
根据图3,在25 min内,吸光值A对反应时间的线性关系良好,其方程斜率为邻苯三酚自氧化速率V0(0.006 2),相关系数可以达到0.999 7,而且每一段时间间隔内,有色中间产物(半醌)都以稳定的增量增加,且反应速率趋于稳定,故确定该反应速率V0为0.006 2。
3.4 茶叶中不同类型不同质量浓度的茶多酚对超氧自由基的清除
3.4.1 绿茶中不同质量浓度的茶多酚对超氧自由基的清除作用
根据2.2.1的操作,结果见图4。
根据图4中的线性方程斜率代入(1)式,可计算出不同质量浓度的梵净山绿茶茶多酚对超氧自由基的清除率,分别为:Y0.04=29.03%、Y0.06=41.94%、Y0.08=50%和Y0.12=70.96%、Y0.14=92.00%。由此可知,随着绿茶茶多酚质量浓度的增加,其所含的茶多酚含量也增加,对超氧自由基的清除能力也越来越强。
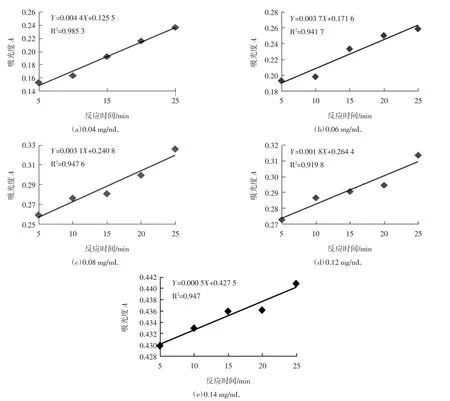
图4 绿茶中不同质量浓度的茶多酚的反应体系吸光值与时间线性关系Fig.4 Linear relation diagram of absorbance value and time in reaction system of green tea polyphenols with different mass concentrations
3.4.2 绿茶茶多酚对超氧自由基的清除率与质量浓度线性关系
别呦呦别过头,朝司大愣子抿嘴一笑。司大愣子心里直痒痒,但媳妇的话是圣旨,他不敢违抗,只好恋恋不舍地走了。
根据2.2.2的操作,结果见图5。
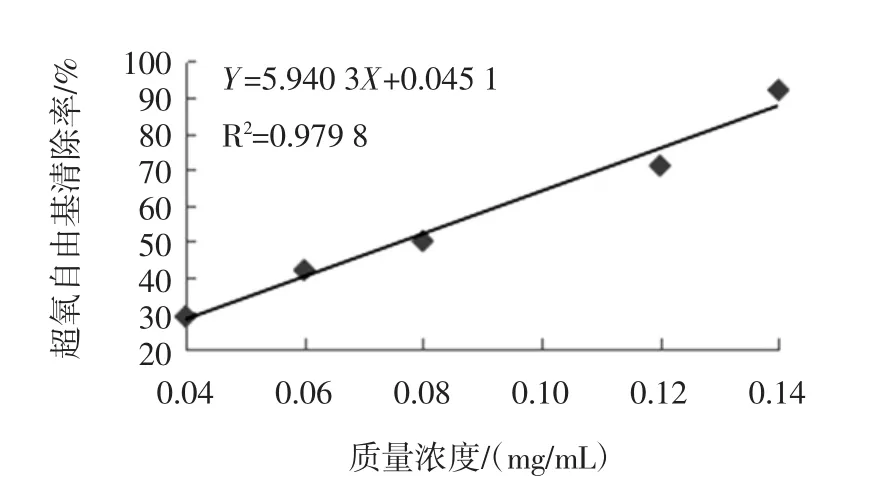
图5 超氧自由基清除率与绿茶茶多酚质量浓度线性关系Fig.5 Linear relationship between the scavenging rate of superoxide anion free radicals and the mass concentration of green tea polyphenols
由图5线性方程可知,相关系数R2=0.979 8,数据点分布在趋势线两边,线性关系良好,根据该图线性拟合所得曲线的线性关系式Y=5.940 3X+0.045 1,当清除率为50%时(将Y=50%代入线性方程)计算绿茶茶多酚质量浓度(X值),即为IC50值为0.080 mg/mL。且绿茶茶多酚质量浓度与超氧自由基清除率呈正相关,随着绿茶茶多酚质量浓度的增加,对超氧自由基的清除能力也越来越强。
3.4.3 白茶茶多酚对超氧自由基的清除作用
根据2.2.1的操作,结果见图6。
根据图6中的线性方程斜率代入(1)式,计算不同质量浓度的梵净山小酱白茶茶多酚对超氧自由基的清除率为分别为:Y0.06=27.42%、Y0.08=38.71%、Y0.1=51.61%和Y0.14=69.35%、Y0.16=93.55%。由此可知,随着白茶茶多酚浓度的增加,其所含的茶多酚含量也增加,对超氧自由基的清除能力也越来越强。
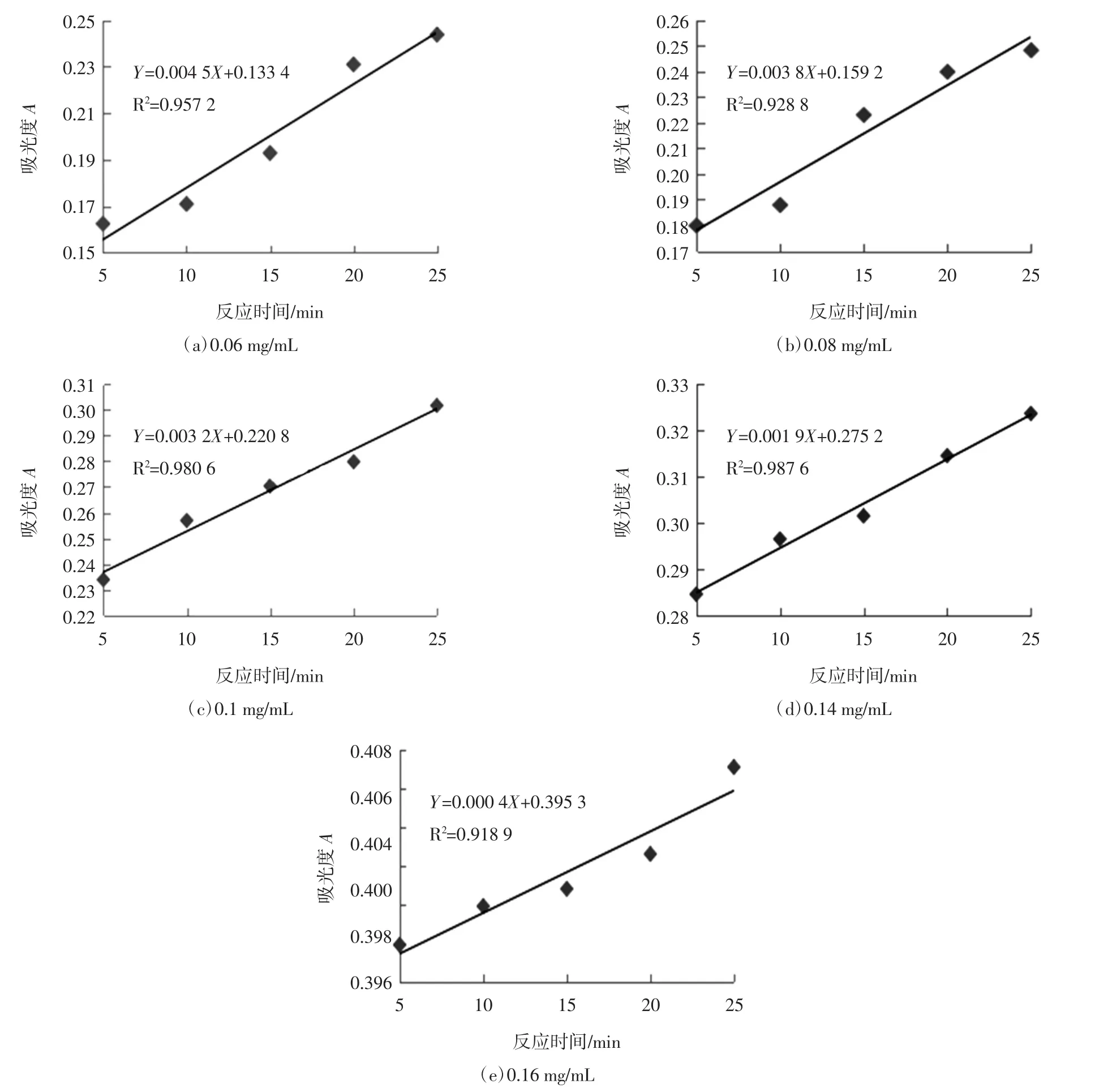
图6 不同质量浓度的白茶茶多酚中反应体系吸光值与时间线性关系Fig.6 Linear relation diagram of absorbance value and time in reaction system of white tea polyphenols with different mass concentrations
3.4.4 白茶茶多酚对超氧自由基的清除率与质量浓度线性关系
根据2.2.2的操作,结果见图7。
由图7的线性方程可知,相关系数R2=0.973 6,数据点分布在趋势线两边,线性关系良好,根据该图线性拟合所得曲线的线性关系式Y=6.207 7X-0.109 1,当清除率为50%时(将Y=50%代入线性方程),得梵净山小酱白茶茶多酚的IC50为0.098 mg/mL。其值大于3.4.2梵净山绿茶中茶多酚的IC50=0.080 mg/mL,从而得出绿茶的抗氧化能力大于白茶。然而,茶叶中具有抗氧化能力的物质主要是茶多酚,其茶多酚含量的多少可直接影响茶叶抗氧化能力的强弱,由制作工艺可知,绿茶属于未发酵茶,白茶经过轻微的发酵处理,其茶多酚含量会有一定程度的损失。从而导致抗氧能力小于绿茶。
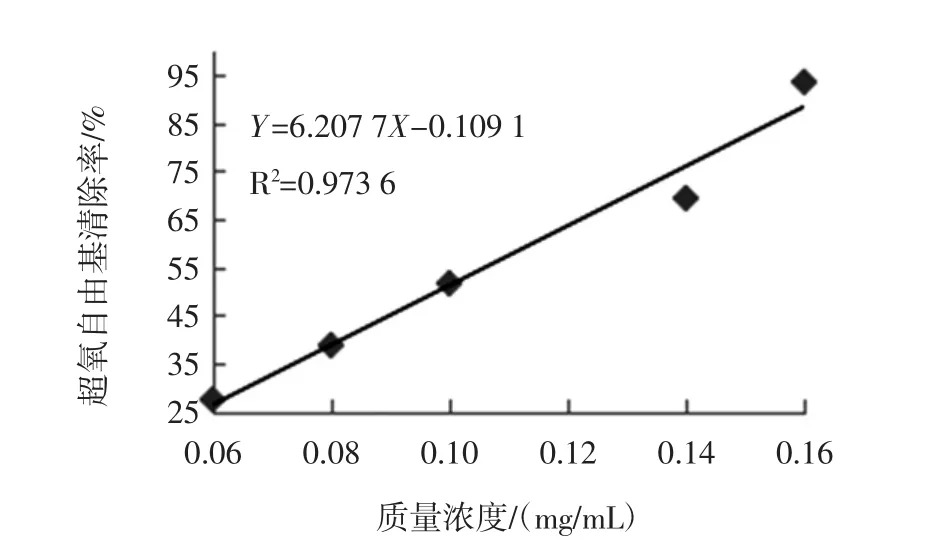
图7 超氧自由基清除率与白茶茶多酚质量浓度线性关系Fig.7 Linear relationship between superoxide free radical scavenging rate and white tea polyphenol mass concentration
3.4.5 红茶茶多酚对超氧自由基的清除作用
根据2.2.1的操作,结果见图8。
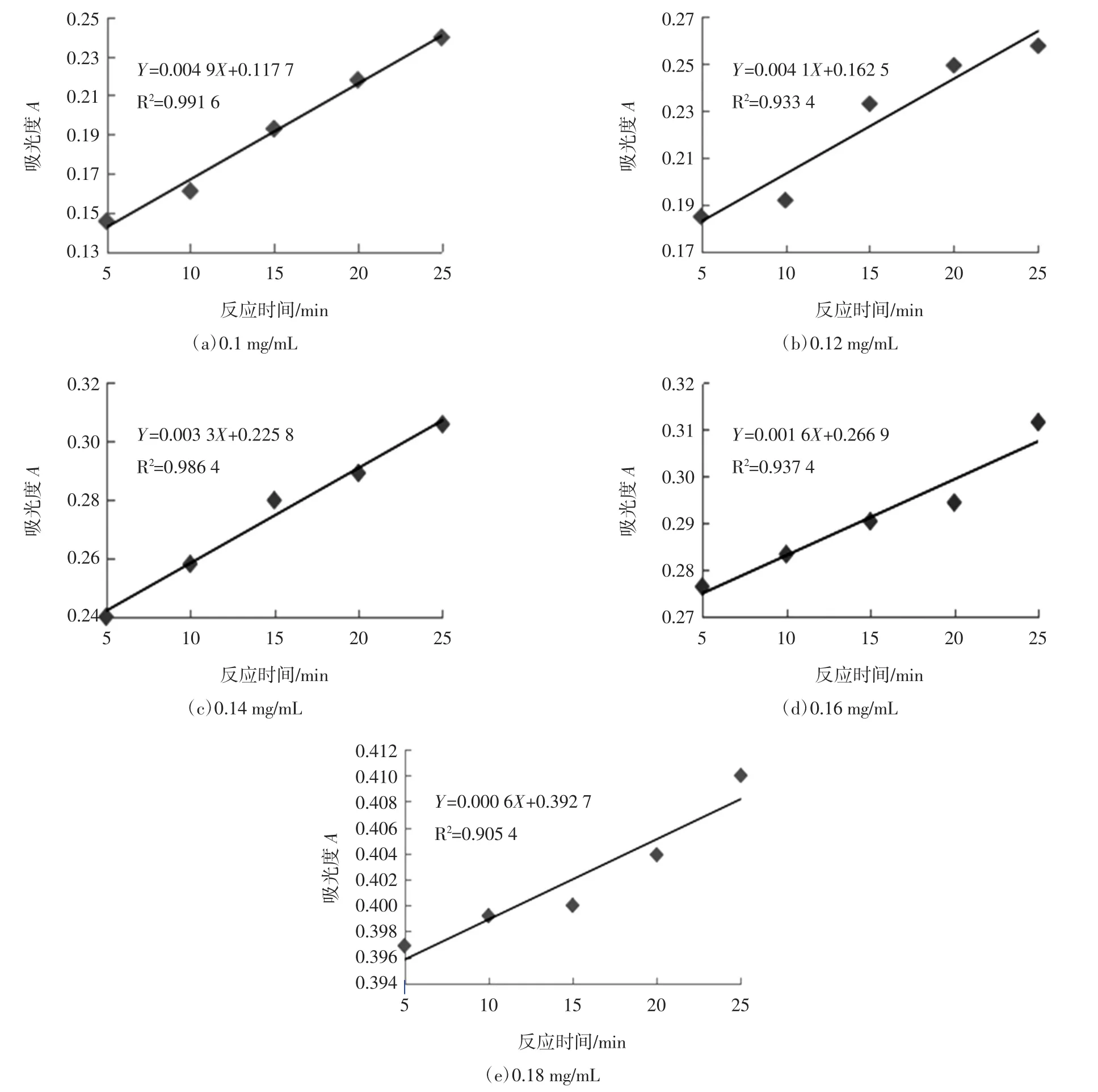
图8 不同质量浓度的红茶茶多酚中反应体系吸光值与时间线性关系Fig.8 Linear relation diagram of absorbance value and time in reaction system of black tea polyphenols with different mass concentrations
根据图8中的线性方程斜率代入(1)式,计算不同质量浓度的石阡苔茶(红茶)茶多酚对超氧自由基的清除率为分别为:Y0.1=20.97%、Y0.12=33.87%、Y0.14=46.76%和Y0.16=74.19%、Y0.18=90.32%,由此可知,随着红茶茶多酚浓度的增加,其所含的茶多酚含量也增加,对超氧自由基的清除能力也越来越强。
3.4.6 红茶茶多酚对超氧自由基的清除率与质量浓度线性关系
根据2.2.2的操作,结果见图9。
由图9的线性方程可知,相关系数R2=0.979 4,数据点分布在趋势线两边,线性关系良好,根据该图线性拟合所得曲线的线性关系式Y=8.951X-0.720 9,当清除率为50%时(将Y=50%代入线性方程),得石阡苔茶(红茶)茶多酚的IC50为0.136 mg/mL。其值大于3.4.2梵净山绿茶中茶多酚的IC50=0.080 mg/mL,从而得出绿茶的抗氧化能力远大于红茶,这是因为茶叶中抗氧化能力主要成分是茶多酚,其茶多酚含量多少可直接影响茶叶抗氧化能力的强弱,由制作工艺可知,红茶属于全发酵茶,红茶在制作过程中经过深度发酵处理,其茶叶中茶多酚含量损失比较大,从而导致红茶抗氧能力远小于绿茶。
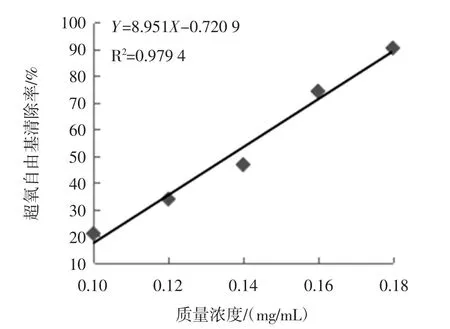
图9 超氧自由基清除率与红茶茶多酚质量浓度线性关系Fig.9 Linear superoxide free rate and mass of black tea polyphenols
3.4.7 苦丁茶茶多酚对超氧自由基的清除作用
根据2.2.1的操作,结果见图10。
根据图10中的线性方程斜率代入(1)式,计算不同质量浓度的铜仁苦丁茶茶多酚对超氧自由基的清除率为分别为:Y0.08=20.97%、Y0.1=33.87%、Y0.12=48.39%和Y0.14=66.13%、Y0.16=85.48%。由此可知,随着苦丁茶茶多酚浓度的增加,其所含的茶多酚含量也增加,对超氧自由基的清除能力也越来越强。
3.4.8 苦丁茶茶多酚对超氧自由基的清除率与质量浓度线性关系
根据2.2.2的操作,结果见图11。
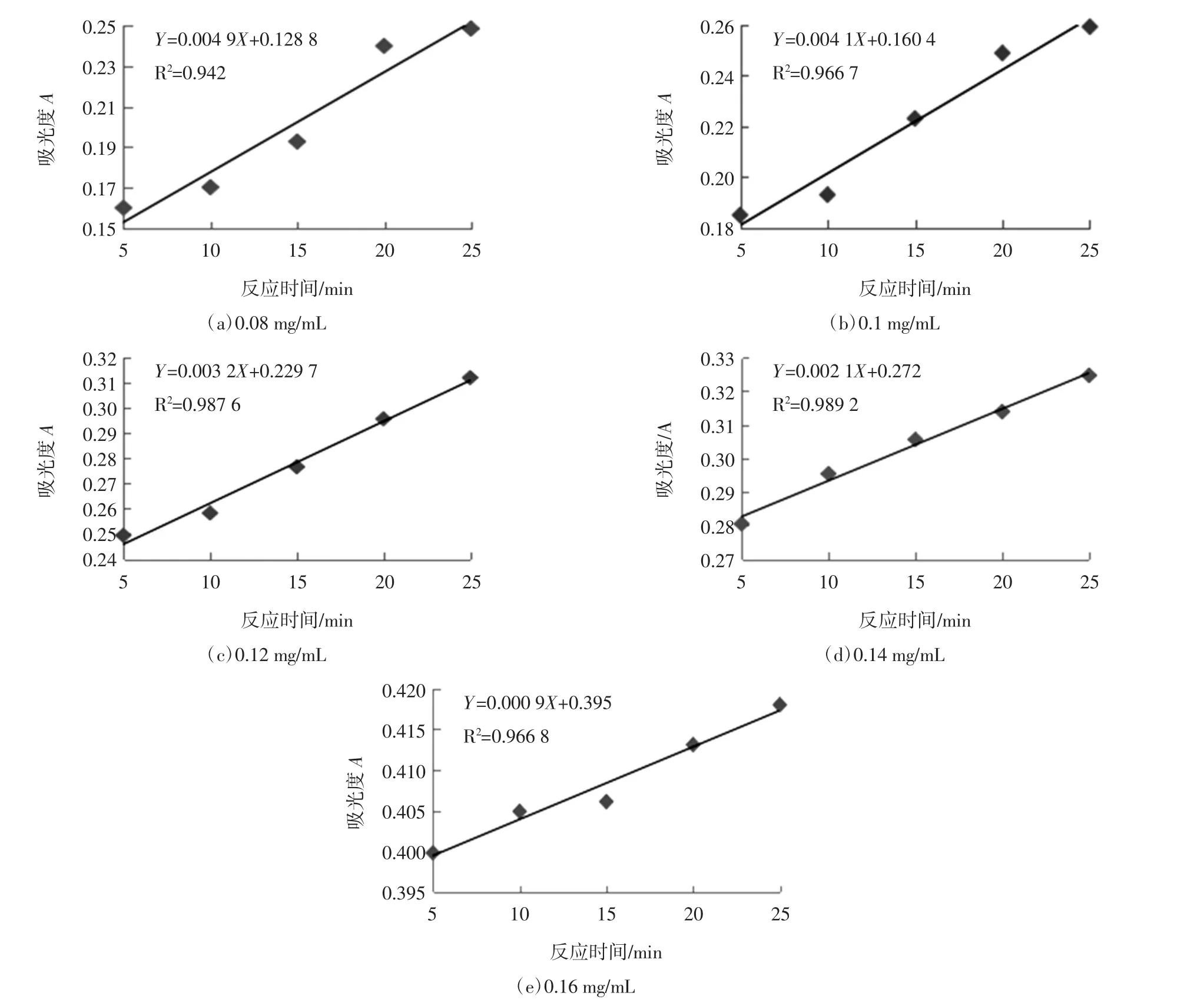
图10 不同质量浓度的苦丁茶茶多酚中反应体系吸光值与时间线性关系Fig.10 Linear relation diagram of absorbance value and time in reaction system of broadleaf holly leaf polyphenols with different mass concentrations
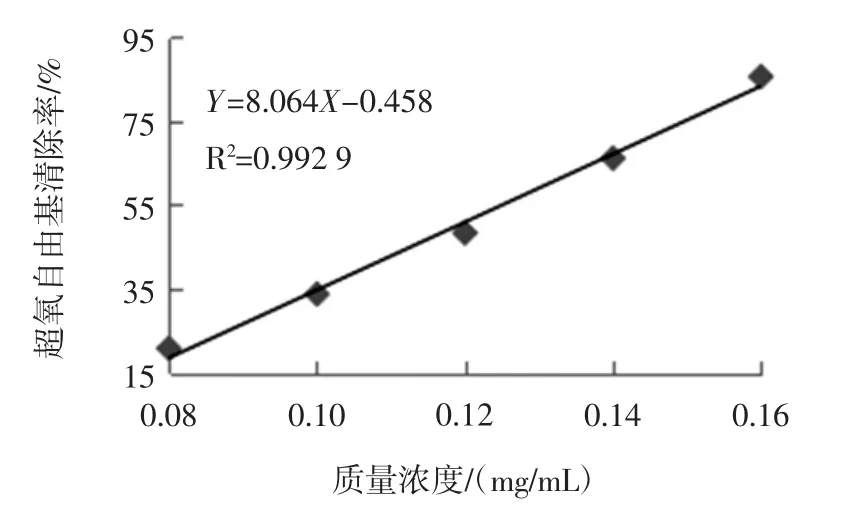
图11 超氧自由基清除率与苦丁茶茶多酚质量浓度线性关系Fig.11 Linear relationship between superoxide anion radical scavenging rate and the mass concentration of broadleaf holly leaf polyphenols
由图11的线性方程可知,相关系数R2=0.992 9,数据点分布在趋势线两边,线性关系良好,根据该图线性拟合所得曲线的线性关系式Y=8.064ⅹ-0.458,当清除率为50%时(将Y=50%代入线性方程),得到铜仁苦丁茶茶多酚的IC50为0.119 mg/mL。其值大于3.4.2梵净山绿茶中茶多酚的IC50=0.080 mg/mL,从而得出绿茶的抗氧化能力大于苦丁茶,茶叶中抗氧化能力主要成分是茶多酚,苦丁茶的制作工艺与绿茶相似,都是未经过发酵处理,属于未发酵茶,但由于苦丁茶含有大量的多糖、黄酮、皂苷、熊果酸、咖啡碱、氨基酸、维生素、挥发油等200多种成分[17],提取过程产生的杂质较多,对其中的茶多酚含量有一定程度影响。所以,苦丁茶的抗氧化能力小于绿茶。
4 结论
根据试验建立邻苯三酚自氧化模型,其条件为:邻苯三酚自氧化的检测波长为320nm、浓度为0.4mg/mL、PBS缓冲液pH=8.0、V(邻苯三酚溶液):V(PBS缓冲液)=0.1∶5、反应时间25 min,测得4种不同类型茶叶中[梵净山绿茶、梵净山小酱白茶、铜仁苦丁茶、石阡苔茶(红茶))茶多酚清除超氧自由基能力的IC50分别为:0.08、0.098、0.119、0.136 mg/mL,即 4 种类型茶叶抗氧化能力依次为:梵净山绿茶>梵净山小酱白茶>铜仁苦丁茶>石阡苔茶(红茶)。由于茶叶中主要的抗氧化活性物质是茶多酚,茶叶的发酵程度不同,抗氧化活性物质茶多酚含量也存在较大差异[18]。即茶叶中的茶多酚含量的大小直接影响茶叶的抗氧化能力,梵净山绿茶为不发酵茶,保留了茶叶中原有的天然物质,其所含的茶多酚含量会比其他类型茶叶茶多酚含量高很多。因此,绿茶的抗氧化能力最强;梵净山小酱白茶为微发酵茶,经过轻微的发酵工艺处理,所含的茶多酚会有一定程度的损失,使抗氧化能力降低;红茶为全发酵茶,在发酵过程中发生了化学反应,产生新的化学物质,茶多酚含量会有很大程度的损失,其抗氧化能力有很大程度减弱;苦丁茶制作工艺和绿茶相似,但由于含有大量的多酚,多糖、黄酮、皂苷、熊果酸、咖啡碱、氨基酸、维生素、挥发油等200多种成分,对其中的茶多酚含量有一定程度影响。从而影响苦丁茶中茶多酚的抗氧化能力,由此可知,茶叶的制作工艺不同,其主要成分茶多酚的抗氧化能力不同,这为后续的应用研究提供一定的参考依据。
