三维分层脑组织的建立及DBS刺激电极下移仿真研究
2020-08-26陈义保柴永生刘希宽刘宇航
王 琦,陈义保,柴永生,李 岩,刘希宽,李 林,刘宇航
(烟台大学机电汽车工程学院,山东 烟台 264005)
受环境、社会压力、老龄化等因素的影响,人脑内部某些核团会出现工作异常的现象,导致越来越多的人患上了神经系统疾病[1],此类疾病主要有帕金森病、癫痫等.帕金森病患者主要表现为身体运动迟缓,动作僵硬,手脚等部位震颤,晚期还伴随有严重的并发症[2],严重影响了患者的生活质量,目前,医师们多采用深部脑刺激术(Deep brain stimulation,DBS)来治疗帕金森病.DBS是通过手术的方式在脑内特定位置放置刺激电极,通过电刺激的方式来抑制细胞核团的异常放电状况[3].目前,深部脑刺激手术尤其对丘脑底核(Sub-thaiamic nucleus,STN)的刺激术为帕金森病的重要治疗方法.
对STN定位的精确与否直接影响到手术的成功,术中开颅过程脑脊液的流失和空气进入颅内可能会导致脑组织的漂移,进而影响靶点的准确定位,电极往往过深,固定电极时,固定帽的下压也可能造成电极的移位[4],术后患者剧烈的牵拉运动也可能导致电极的移位,电极的移位、折断,植入设备故障等状况在术后任何时候都有可能发生,有时需要再次手术,给病人带来不必要的痛苦和麻烦[5].
为了研究电极的移位给脑组织带来的影响,本文基于真实人脑的解剖学结构构建分层脑组织模型,并对电极下移2、3、4、5 mm过程进行仿真,为了模拟真实的手术环境,本文对脑膜结构进行了重建并施加固定约束,刺激电极模型基于DBS手术常用的型号为3389神经刺激电极进行建立,基于DBS医师手部动作估计控制刺激电极下移速度为5 mm/s,通过三维有限元仿真方法得到脑组织内部可视化位移结果和靶点下移数据,并在不同的电极-脑组织摩擦系数情况下进行了结果的对比,以期为临床医学提供一定的数据参考.
1 方 法
1.1 三维脑组织模型的建立
为了体现脑组织各向异性的材料属性,本文中分别构建丘脑底核(脑深部刺激靶点)、灰质、白质、刺激电极四部分结构并分层定义材料属性,其中,采用黏弹性属性定义脑组织材料.通过创建脑膜结构固定脑组织,向电极施加位移加载并控制电极下移速度来模拟真实手术条件.本文基于手术穿刺路径建立各部分组织,穿刺进针的基本原则是避开脑沟、脑室和其他重要核团,穿刺路径上的主要脑组织依次为灰质、白质、丘脑底核,所以主要针对这三部分脑组织进行建模,具体建模流程如下:
(1)利用Mimics软件提取灰度值不同的脑组织,得到面网格模型并控制网格质量.
(2)在Mimics将面网格导出为STL格式并导入Hypermesh软件中进行体网格的生成.
(3)在Hypermesh中将体网格导出为inp格式并导入ANSYSWorkbench的FE(finite element)模块中生成对应的模型.
1.1.1 Mimics建立脑组织面网格模型 利用医学建模软件Mimics建立各部分脑组织,该软件的阈值分割功能可以基于人脑的断层扫描图谱建立人体组织,其中成年男性的头颈部断层扫描图谱等资料来源于山东省医学影像学研究所.建立的模型包括STN、灰质、白质和电极等结构,参照脑立体定向图谱找到丘脑底核并构建,如图1(a)所示为丘脑底核分别在水平面,冠状面,矢状面的位置[6],构建的丘脑底核在三维脑组织中的位置如图1(b)所示.
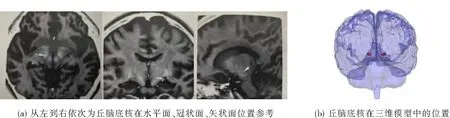
图1 丘脑底核在颅内的位置
在Mimics中利用阈值分割功能先提取全脑模型,再建立脑灰质模型,对各部分脑组织面网格质量进行控制后,利用Mimics中的布尔操作功能执行布尔减操作得到白质模型.在Mimics中由质量参数Q(Quality parameter)来衡量三角网格质量:
其中,H表示三角形的高,B表示三角形的底边长,Q越接近1表示三角网格质量越高,在有限元分析中,通常取Q为0.3~0.4之间[7],以灰质为例,将形状参数控制为0.35进行网格优化操作,图2(a)、(b)所示为相应网格质量对应的网格数量(横坐标为质量,纵坐标为数量).未经过网格优化的面网格数量庞大,且低于网格质量系数0.35的网格数为整体的5%,经过网格优化和缩减处理后的面网格全部达到了质量要求,并且数量仅为处理之前的十分之一.建立好的脑组织壳体模型如图3所示.
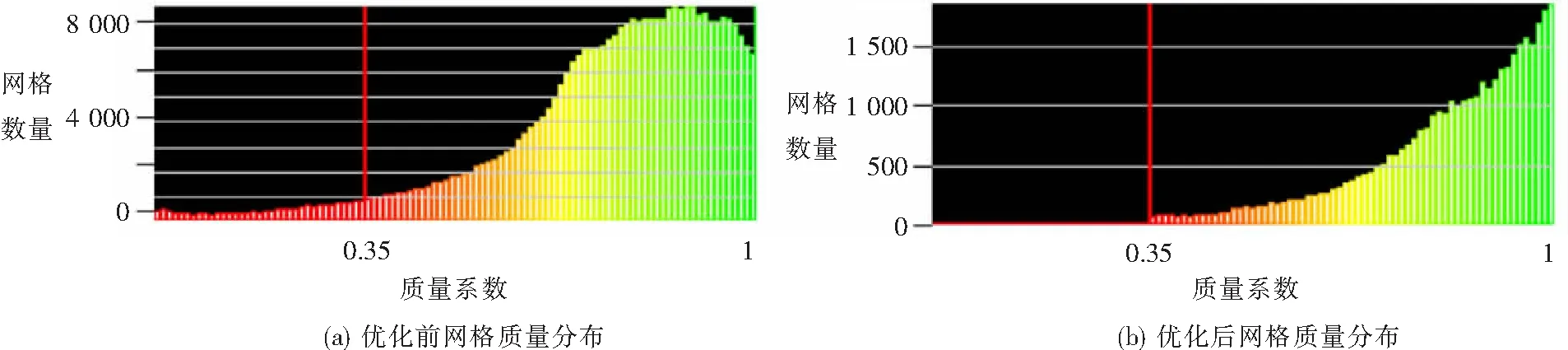
图2 面网格优化
在植入刺激电极之前要先植入微记录电极,微记录电极会探测到异常放电的神经核团从而确定刺激电极的最佳植入位置,微电极植入方法是通过一根由额中回穿刺至STN附近的导管植入,确定STN最终位置后,植入刺激电极[8].选择额中回为穿刺起点可以避免破坏血管或其他重要核团,防止脑脊液的流失,在Mimics软件中,只需要在额中回和STN上确定两点即可确定穿刺路径,在颅骨上创建一点,使三点在一条直线上,导出穿刺路径为txt格式,坐标系默认,穿刺路径上点坐标如表1所示,点1为额中回穿刺点,点2为STN上的点,点3为颅骨上的点.
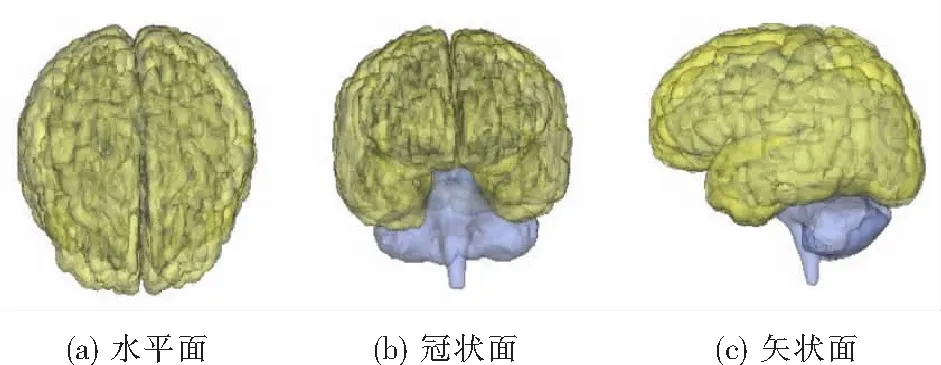
图3 脑组织壳体模型
在DBS手术中,细胞异常放电的记录过程多采用FHC公司生产的微电极和电生理记录系统,其中微电极材料为金属钨.深部脑刺激手术使用的刺激电极为Medtronic公司生产,由刺激触点的长度和间距不同分为3387、3389、3391等不同型号,其中3389型号的刺激电极多用于STN的刺激,电极的导线及刺激触点部分材料为铂铱合金,电极的直径为1.27 mm[9-10],基于表1的数据创建电极,Point3设置为电极的起点,Point2设置为电极的终点,电极的直径为1.27 mm创建电极并和各部分脑组织进行布尔操作,电极和脑组织接触的部分区域网格得到加密以控制模拟计算结果更加准确,得到的脑组织-电极模型如图4所示.

表1 穿刺路径空间坐标
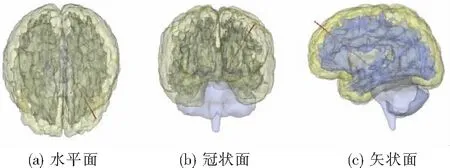
图4 脑组织-电极模型
1.1.2 Hypermesh生成体网格 在Mimics中将模型导出为STL格式的文件,STL文件是三角网格文件,将STL文件导入Hypermesh中,用Tetra功能由面网格生成体网格,由于脑组织模型极度不规则,在生成体网格的过程中会出现重叠和交叉单元,可以用网格删除和replace功能对重叠和交叉单元进行删除和节点移动的处理,处理好生成的体网格如图5所示.
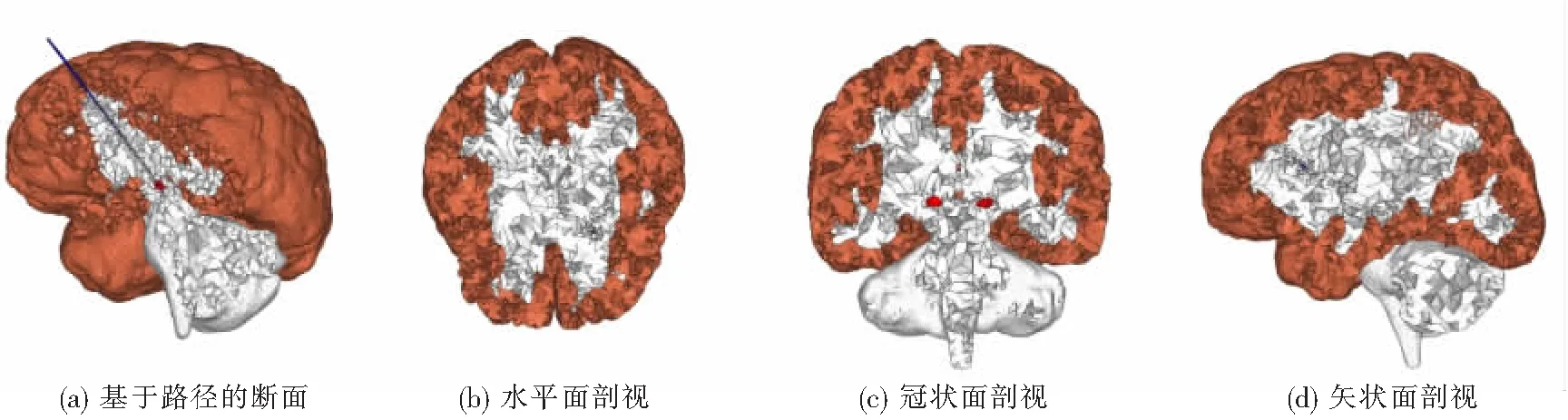
图5 脑组织体网格模型
1.1.3 导入FE模块生成几何体 在Hypermesh中将网格导出为inp文件,在workbench中的FE有限元模块可以导入inp文件,联合分析模块可以自动由网格生成几何体.具体的单元信息如表2.图6分别为各个部分的侧视和俯视图.
电极型号为3389的刺激电极前段7.5 mm为刺激区域,成功的脑深部刺激手术电极的植入部位应该使得刺激区域准确地插入丘脑底核,如图7所示.
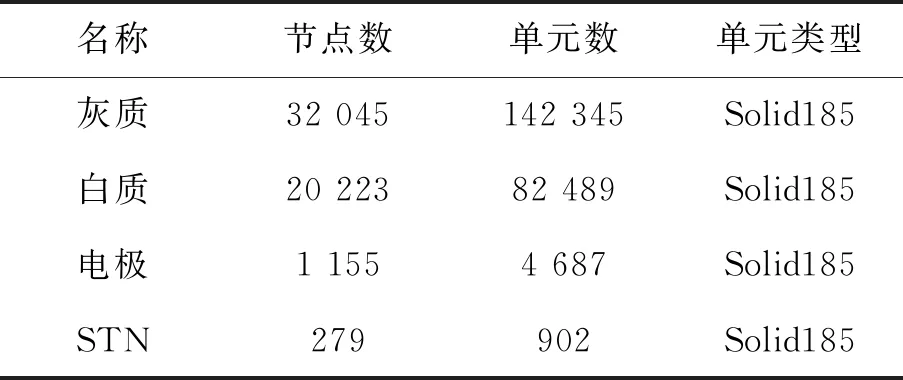
表2 各部分模型网格信息表
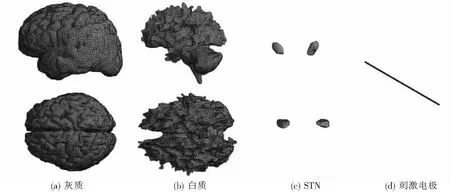
图6 Workbench脑组织网格模型
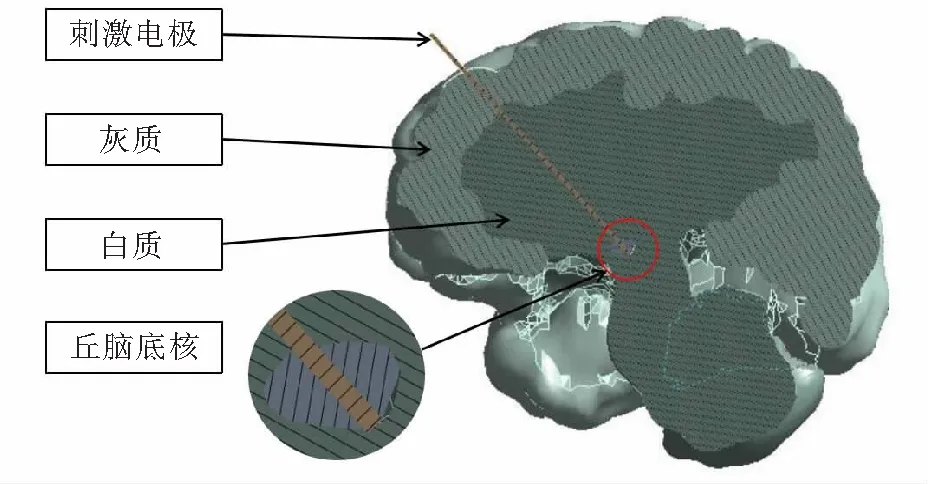
图7 Workbench中生成的脑组织几何模型
1.2 脑组织材料的定义及边界条件
1.2.1 脑组织材料的定义 脑组织外形极度不规则,其内部存在多种功能性核团,许多核团以不同的排列方式存在,所以表现出非均质和各向异性的特性,许多学者已经对脑组织进行了大量的材料属性研究,脑组织表现出非常复杂的材料特性,具有明显的非线性、黏弹性等材料力学属性,目前,常用的脑组织材料力学测试方法为剪切、压缩及拉伸试验等[11-12],荷兰的Dommelon及美国的Prevost利用压痕试验探究了脑组织的属性,证明了脑组织的黏弹性特征[13-14].李岩研究了脑组织刺破后穿刺路径上的脑组织区域性差异,分为3类:浅层脑组织、脑室旁组织、丘脑脑组织,通过实验数据啮合出三阶Prony级数中各项参数的数值[15],如表3所示.
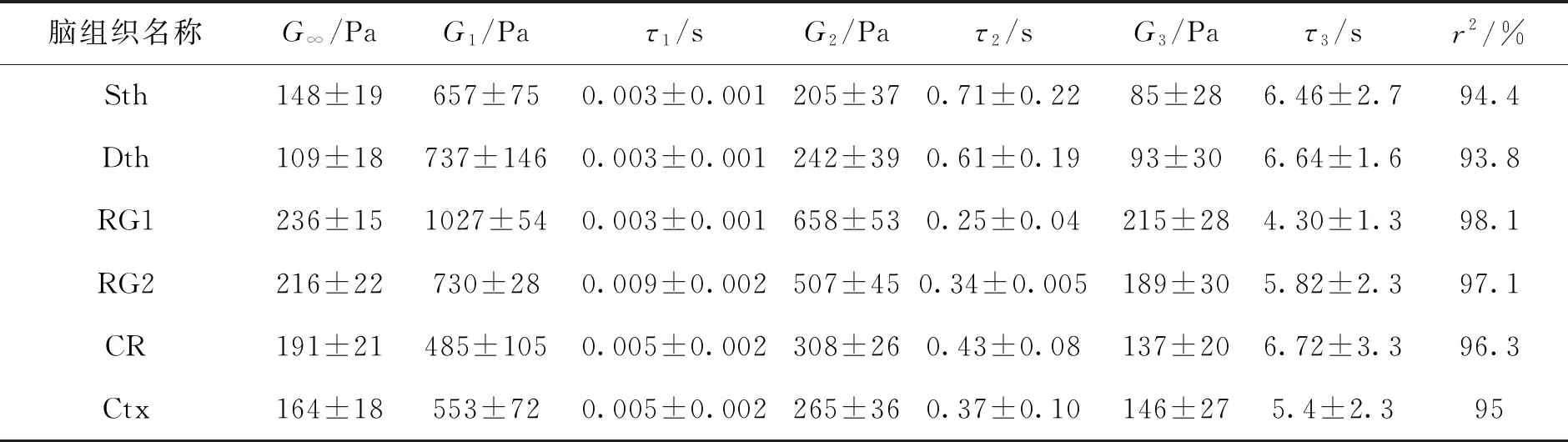
表3 三阶Prony级数参数值[15]
用Prony级数表达黏弹性属性的基本形式为
(1)
(2)
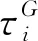
(3)
(4)
式(3)(4)中G0和K0分别为黏弹性材质的瞬态模量,定义式如下:
(5)
(6)
在Workbench中定义模型的黏弹性需要定义剪切模量、松弛时间和相对模量,表3中Ctx和CR是浅层脑组织,RG1和RG2为脑室旁组织,Sth和Dth为丘脑组织,本文利用CR的数据定义脑灰质,用RG1的数据定义脑白质,Sth数据定义丘脑底核组织.由式(3)、(4)计算得到的数据如表4、5、6所示.灰质、白质、丘脑底核剪切模量依次是191 Pa,236 Pa,148 Pa.
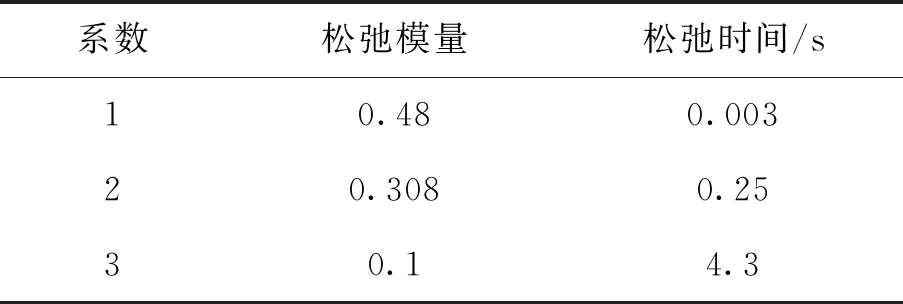
表4 灰质材料属性
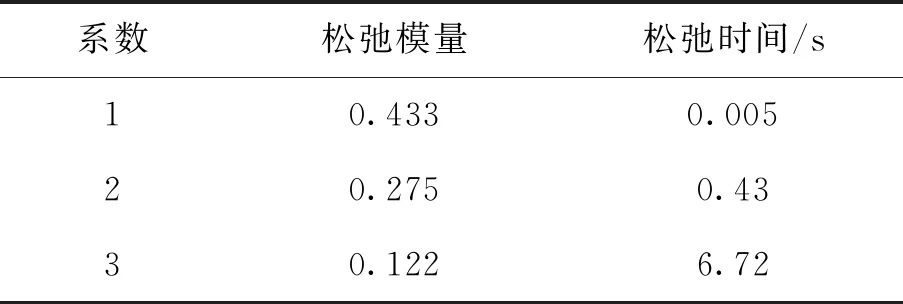
表5 白质材料属性
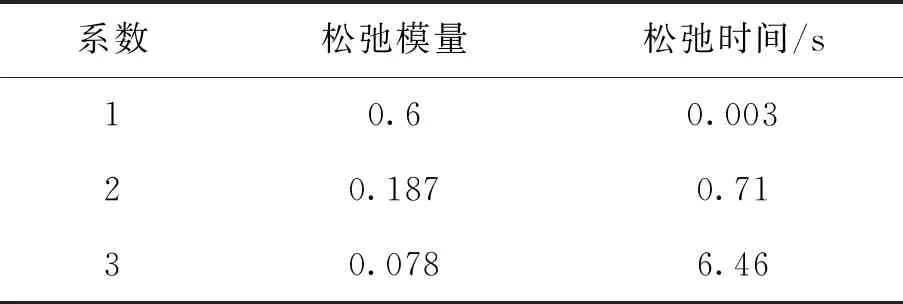
表6 丘脑底核材料属性
1.2.2 脑组织边界条件 人的头部由外到内依次为头皮、颅骨、硬脑膜、蛛网膜和软脑膜,脑的被膜对脑有支撑,保护和营养功能,为了模拟脑膜对大脑的支持作用,在Workbench中FE有限元模块中由网格创建面结构对脑膜结构进行了模拟如图8所示.

图8 脑膜结构
为了模拟手术过程中脑组织在颅内的状态,创建脑膜结构包括大脑左、右,小脑左、右,延髓和中脑部分,在Workbench中分别给这五部分添加固定约束.丘脑底核、白质、灰质之间采用Bonded接触方式,刺激电极和各脑组织之间采用Frictional接触方式.在DBS手术中,由于脑膜结构比脑组织坚硬,在进行脑组织穿刺之前要先将硬脑膜和蛛网膜切开再进行穿刺,如图8(c)所示,穿刺区域周围不添加脑膜结构,来模拟手术中切开的部分脑膜.
2 结 果
经查阅相关资料得,电极植入位置往往过深,这可能是由于开颅后脑脊液的泄漏和空气进入颅内造成的,电极的下移数据大体在4~6 mm区间内,且安装电极固定帽的过程中也可能造成电极下移,临床上在固定电极时往往将电极向外拔出1~2 mm,本文将脑组织和电极的相对位移加载在了电极上,对电极下移2、3、4、5 mm分别在摩擦系数μ=0.05和μ=0.1情况下进行了仿真分析,控制电极的位移速度为5 mm/s,如图9,10所示.图9所示为脑组织在摩擦系数为0.1情况下电极下移给脑组织带来的影响,图10为丘脑底核参考点位移.当电极下移2 mm时,丘脑底核参考点下移1.028 5 mm,电极下移3 mm时,丘脑底核参考点下移1.572 3 mm,电极下移4 mm时,丘脑底核参考点下移2.134 2 mm,电极下移5 mm时,丘脑底核参考点下移2.706 9 mm.
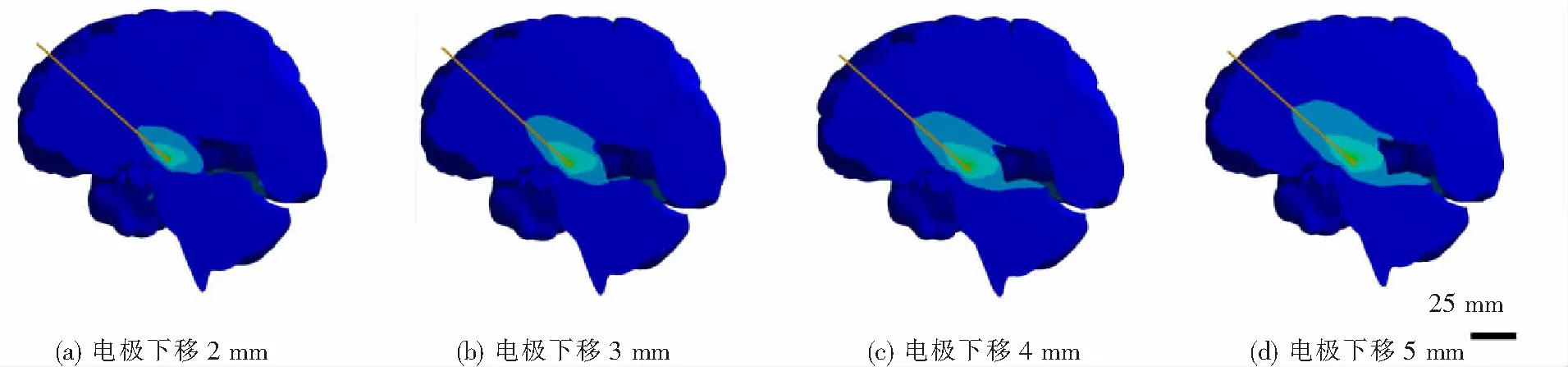
图9 脑组织位移云图(μ=0.1)

图10 丘脑底核参考点位移(μ=0.1)
图11为在摩擦系数为0.05情况下电极下移脑组织位移云图,图12为丘脑底核参考点下移距离.当电极下移2 mm时,丘脑底核参考点下移1.005 2 mm.电极下移3 mm时,丘脑底核参考点下移1.521 5 mm.电极下移4 mm时,丘脑底核参考点下移2.053 5 mm,当电极下移5 mm时,丘脑底核参考点下移2.596 4 mm.
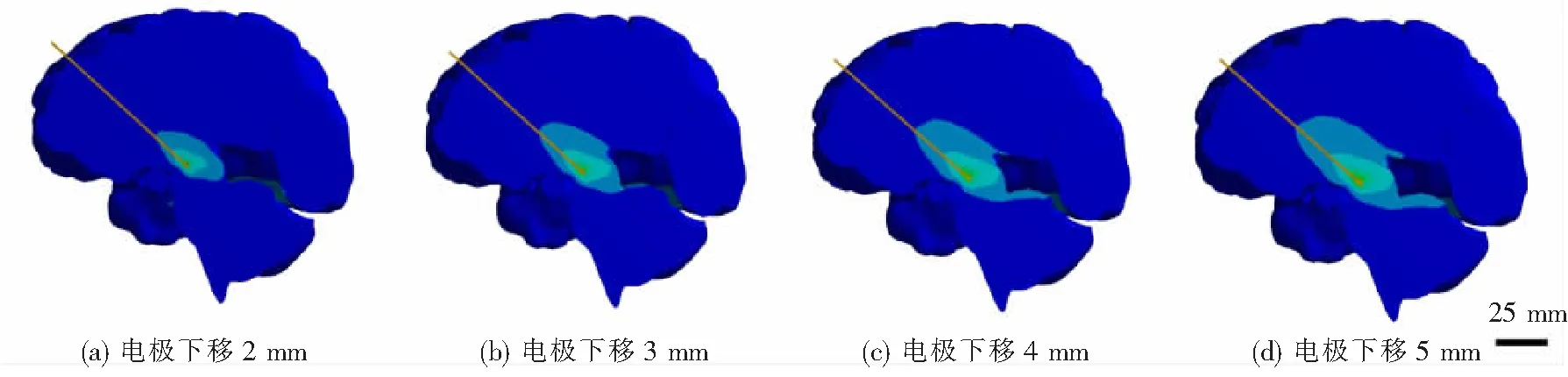
图11 脑组织位移云图(μ=0.05)

图12 丘脑底核参考点位移(μ=0.05)
3 讨 论
本文基于穿刺路径上的脑组织进行了三维重建,并用线弹性、黏弹性描述了脑组织的材料属性,针对手术过程中电极下移的过程进行了仿真研究,电极下移可能由于术中脑脊液的泄露和空气的进入颅内导致脑组织形状改变有关,在电极固定帽的安装过程中也可能导致电极下移,本文旨在研究电极下移对靶点位置的影响,将脑组织固定,电极和脑组织之间的相对位移被等效地添加到电极上.分别对电极下移2、3、4、5 mm在摩擦系数为0.05和0.1的情况下进行了仿真,通过对脑组织内部位移分布结果的观察得到,随着刺激电极的下移,和电极接触部分的脑组织会产生位移,灰质和白质部分的位移显然是由于电极对脑组织的摩擦作用造成的,脑组织最大位移点存在于和刺激电极尖端接触的部分脑组织中,显然这是由于刺激电极尖端对脑组织的挤压作用造成的,由于丘脑底核的位置在刺激电极尖端附近,且核团内部和电极存在接触,所以丘脑底核的下移应为电极对脑组织的摩擦作用和挤压作用共同造成的结果.以摩擦系数为变量,当电极分别下移2、3、4、5 mm时,将摩擦系数从0.1降低为0.05可以分别使靶点位移降低2.3%、3.2%、3.7%、4%,说明摩擦作用对丘脑底核造成的位移是非常小的,造成丘脑底核下移的主要原因是电极尖端对丘脑底核下层脑组织挤压作用产生的.综上所述,电极的下移会造成靶点的漂移,下移的数值近似为电极下移数值的一半,减小电极和脑组织之间的摩擦系数可以减少靶点漂移现象,但影响较小,在脑组织整体位置不改变仅考虑电极位置下移情况下,靶点移位主要是由于刺激电极对丘脑底核下层脑组织的挤压而产生的.
脑组织被硬脑膜、蛛网膜、软脑膜等背膜包裹,其内部还存在复杂的血管网络系统,血管可以对脑组织起到一定的固定作用,在以后的工作中,可以考虑将血管等结构添加到模型当中,使模型更加贴近真实的脑组织,仿真结果更加有说服力.
