铜合金成分分析与检测方法研究
2020-08-26屠晓栋
屠晓栋
(宁波中普检测技术服务有限公司,浙江宁波 315100)
1 电解重量法
此方式能够用于各种类型的铜合金的检测,精确度和准确性都较高,在国际和我国国家标准中都有相关的规定,此途径检测的铜的主要机理是基于处于酸性环境之中,通以一定的电流进行电解,此时铜于铂电极中将会析出,之后再测定电解之前的阴极电极+试样和电解之后的阴极电极+出铜的质量,最后分析两者之间的质量差就可以测定出铜含量。
1.1 阴极主要的电极反应过程
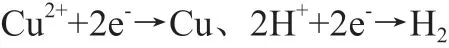
1.2 阳极主要的电极反应过程

而对于含铜量超过99.90%的样品,进行检测前需要考虑样品是否有被氧化的情况出现,所以在这之前需要利用CH3COOH(1+4)溶液进行浸泡处理一段时间,之后利用纯水和酒精进行洗涤和烘干以备检测。
对于含铜量较大的材料通常利用硝酸/硫酸液体将样品完全溶解,如果仅仅利用硫酸进行溶解时,在后续的电解过程中其阴极就会出现较多的氢气,此时电解而出的铜具有较大的空隙非常易于被氧化,但是仅仅通过硝酸进行溶解时,因为反应过程产生的大量的NO2-将会使得铜会再次溶解,容易使得电解过程中铜的析出不完全。所以通常来说其电解液中通常在每150mL的电解液里有2~5mL的硝酸溶液(ρ为1.4g/mL)、5mL的硫酸(ρ为1.84g/mL)。
铜的其他合金材料因为其可能含有各种元素,在进行溶解时使用的酸也各异。通常来说通过硝酸来进行样品的溶解,之后加入H2SO4,然后稀释后进行电解操作。如果样品中有较多的Sn时,利用硝酸溶解样品时将会出现较多的偏锡酸不溶物,此时必须要加入一定量的HClO7以及H2SO4进行进一步的溶解完全发烟,然后利用稀硝酸溶解,添入到电解液中进行电解。而如果样品中Pb含量大于1%时,利用硝酸把样品完全溶解后则不需要加入H2SO4,可加入少量HCl溶液(0.1g/mL),因为较少的氯离子并不对电极产生腐蚀。样品中的Si成分较多时,可利用HF/HNO3对于样品进行溶解,然后利用聚四氟乙烯的容器来替换玻璃材质的杯子,可加入一定量的Pb(NO3)2溶液来保护铂阳极,然后加入约0.002%的NH4Cl缓冲溶液来进行电解过程。
样品的溶解温度关于检测的精度有较大影响,所以检测过程中需要进行低温溶解,在微沸状态下去除氮氧化物。过度的沸腾将会使得元素的分析造成损失,使得检测的结果较低。而氮氧化物也必须去除干净,其将会对于后续的电解过程造成阻碍,通常在微沸状态下反应下1.5~3h后反应基本完全。如果利用聚四氟乙烯容器进行电解反应时,可以加入一些双氧水溶液来对于原溶液进行还原去除氮氧化物。
电解时的电流密度较小,铜处于阴极聚集将会增多,金属之间的相互干扰较小。铜合金里的Au、Ag、Se、Te浓度较小,Sn浓度较高时需要提前去除;Sn、As、Sb、Bi含量较低时,通过利用低的电流、静止进行电解,则能够避免这类物质的析出。因此如果是纯铜材料通常利用小电流、静止电解法进行电解检测,而含铜量小于99.9%的合金,在进行样品的检测、分析时,也需要通过小电流进行电解。企业在进行质量管控的检测中通常利用的是大电流密度、通过搅拌进行电解,通常其可以达到4~6A,等到电解液的蓝色变清澈之后电流降至2A~5A,这样的电解过程中使得Bi元素基本都处在阴极。而无论电流的大小,Ag元素都会在阴极析出。而精确检测时也必须要对电解后残余液体的铜含量进行检测。
通常来说,电解液蓝色褪去之后再通以2A的电流,反应30min后,其残余铜含量小于0.05mg时,其铜和铜合金含量小于万分之一天平的感量,则认定铜已经析出完全。
2 碘量法
和电解法相比较,碘量法的分析精度较电解法差,通常企业中把其作为质量管控的分析途径。因为此途径分析更加快速,其通常用于检测黄铜与锌白铜合金的铜量的检测。碘量法的原理通常在微酸性环境中使得Cu与I-产生碘化亚铜(Cu2I2),析出I2,然后用硫代硫酸钠的标准溶液检测I2,进而折算出铜的质量。
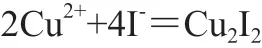
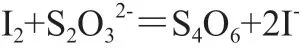
而滴定检测趋于结束时,需要加入SCN-,使得其和Cu2I2产生Cu2(CNS)2,这样,整个滴定过程则更加完全,进而使得Cu2I2所黏有微量I2得以释放,然后用淀粉和I2构成蓝色络合物消失则指示为滴定完成。通常取样品0.3~0.5g,利用HNO3溶液完全溶解;同时也能够通过盐酸与双氧水溶液进行,此方式适用于含Sn量较大的合金;而如果合金中Si含量较大时,则需要加入一定量的HF促进溶解。硫代硫酸钠进行滴定I2的要求的溶液环境为pH=3。而如果pH<3时,处于高价的As、Sb也被I-还原进而产上I2导致其最终的检测结果较高,如果pH>4,此时的Cu2+被还原同时整个反应较慢同时并不彻底,导致检测结果较低。样品全部溶解后利用氨水中和有,然后利用CH3COOH溶液把沉淀溶解,此时的溶液pH=3左右。
利用碘量法分析其干扰因子较多,NO2-、As5-、Sb6-、Fe3+等都可能为I-还原,进而使得分析的结果较大。溶液的pH为3时能够有效去除As5-、Sb6-的影响,加入氟化物后能够络合Fe,溶液煮沸、蒸发能够去除NO2-。KSCN溶液中有部分的还原物物质。在利用时能够加入部分的碘溶液进而使得氧化。假如碘化钾溶液中的I-在空气中被氧化产生了一部分的I2,也可以提前通过硫代硫酸钠将其滴定至无色。
碘化钾的使用量通常为理论使用量的2~3倍。硫代硫酸钠标准溶液通常利用纯铜(光谱纯)液体或者黄铜标样来滴定其溶液的浓度,也能够利用磺酸钾基准试剂来滴定其含量。
相关文献还显示出了一种能够迅速利用碘量法检测黄铜中铜含量的方式,也就是利用硝酸将溶液完全溶解,护体的液体加入顺序为Pb(NO3)2一CO(NH2)2一HNO3溶液,经过冷却后加硫氰酸钾溶液,然后利用硫代硫酸钠标准溶液滴定至乳白色,然后再次加入碘化钾淀粉溶液,使得蓝色消失。此途径利用尿素来还原氮氧化物氧,此方式不用进行蒸发,溶液的pH可以不做考虑,而且此分析方式更加迅速。利用此方式对于样品进行分析,经过检测样品中,Cu=61.00%、S=0.14%、Sr=0.23%(而样品的标准值为61.04%),和通常的碘量法进行对比,此方法的检测精密度不足,不过更加迅速便捷。
3 火焰原子吸收光谱法
依据成分的不同,铜合金中铜检测的方式又多种。如果Cu含量为0.000 5%~0.060%时,GB/T 11067.2—2006中规定了一种火焰原子吸收光谱分析Cu含量的方式,此方式的主要检测机理为把铜合金完全用酸溶解后,微沸蒸干,用水稀释一定的量后制成待检测的溶液。然后通过原子吸收光谱仪处在一定的波长下检测铜的吸光度,确定铜的浓度。
各种元素的原子在通过一定的能量照射后,将会在原子的最外层出现一定的电子跃迁过程。也就是说,各种元素的原子将会有特定的吸收波长。原子吸收光谱正是依据这种机理,依据何种吸收波长来确定元素的种类,然后依据吸收波长的强度用于检测各种元素的浓度。
刘守琼等利用电感耦合等离子体原子发射光谱法(Inductively Coupled Plasma Atomic Emission Spectrometer,ICPAES)检测了Ag-Cu的金属元素的含量,其检测的含量在0.5%~12.0%。样品检测前先利用HNO3进行溶解,之后定容利用PE7300型电感耦合等离子体发射光谱仪开展检测。通过分析,样品检测的相对标准偏差(RSD%)均小于1%,其样品的加标回收率在97%~103%。
4 X射线荧光光谱法(XRF)
因为XRF光谱仪的价格较为昂贵,利用此仪器进行检测的企业并不多。
铜合金和铝合金、钢铁有所不同,它通常要对含量达到80%~90%的材质进行检测。XRF光谱仪是作为检测高成分材质的最好的方式。
在进行检测分析样品时,一般利用外标法进行检测,通常把样品中铜的检测分析荧光强度和特定的铜浓度的样品中的相同的分析线荧光强度作为对比,进而分析出样品的含铜量。
铜合金样品通常只能进行车削,不可以磨光,通过车削导致的条纹将会对于光有一定的屏蔽效果进而导致出现一定的检测误差,而在检测高浓度的样品来讲,这样的偏差其绝对值较大是不被允许的,需要利用一定的数学方式加以校对来进行抵消。通过校对后其检测的精度大大强于碘量法。
5 其他元素的检测
除铜元素外,铜合金中某些微量的杂质元素也会影响合金的使用性能,因此科研工作者们也对该领域进行了广泛的研究。
荣百炼等[8]采用辉光放电质谱法(Glow Discharge Mass Spectrometry,GDMS)分析了铜合金,不仅分别测定出了铜和其他金属杂质的含量,还根据GDMS的工作原理和测试结果对未知元素进行了判定,最终确定了合金中1.273%的Li的存在。辉光放电质谱法(GDMS)作为一种固体直接分析技术,已广泛应用于各种金属、半导体材料的痕量和超痕量杂质分析。检测时离子源将惰性气体(通常为氩气)在高压下电离,采用所形成的离子撞击固体试样表面,使试样表面原子发生溅射,并扩散到等离子体中转化为离子,最后在电磁场的作用下,通过使样品的离子分类,测量和记录不同类离子的强度得到质谱图。
除了测量铜合金中铜的含量,ICP-AES还广泛应用于合金中杂质元素的测量。
刘伟等采用ICP-AES法对铜合金中的Pb、Zn、Cd、P、Sb、Fe等杂质的含量进行了测定。刘吉玲等将铜合金溶解后,将溶液中Ag、Cu以及干扰元素Fe去除后,使用试剂比色测试了合金中的铝含量。此外,光谱分析法在分析合金杂质元素方面也取得了一定的成果,刘继升等采用光谱法分析了Ag-Cu合金中的微量杂质元素的含量。
6 结束语
合金新材料化学成分的定量分析,以上几种方法中兼顾到金属的各自化学特性,充分发挥被分析元素的特性,将铜和合金元素进行了检测测定,既简化了分析程序,同时排除了元素间的相互干扰,给予铜合金检测的适用性以更好的选择。
