奥西替尼对非小细胞肺癌伴脑部转移患者的疗效观察
2020-08-26侯志华薛娜娜魏晗魏红艳薛瑾瑜张莹
侯志华 薛娜娜 魏晗 魏红艳 薛瑾瑜 张莹
肺癌是目前世界上发病率、患病率及死亡率都很高的恶性肿瘤之一,其中又以非小细胞肺癌为主,临床资料显示,超过八成以上的肺癌均属于非小细胞肺癌[1,2]。美国癌症研究所制定的肺癌诊疗指南中建议[3],对于已经失去手术指征的肺癌晚期患者采用吉非替尼联合放疗治疗方案是目前临床上相对成熟的治疗方案之一,该方案能够有效促进肿瘤细胞凋亡,但是该方案有可能对机体的免疫功能发生抑制作用,不利于患者康复及后续的生存质量。随着临床上对非小细胞肺癌的研究深入,发现我国非小细胞肺癌患者约有半数以上存在表皮生长因子受体EGFR基因突变现象,相应的1,2代络氨酸激酶抑制剂存在不同程度的耐药性。奥西替尼则属于第三代络氨酸激酶抑制剂药物,是当前唯一治疗EGFR T790M突变阳性并且耐药性相对较少的小分子药物。有相关动物实验表明,奥西替尼能够抑制非小细胞肺癌小鼠肿瘤生长,提高其生存时间。目前国内关于奥西替尼靶向治疗非小细胞肺癌患者尤其是发生脑部转移的患者研究相对很少,本研究将对奥西替尼的临床效果做一阐述,报告如下。
1 资料与方法
1.1 一般资料 搜集我院2018年1月至2019年7月我院接收治疗的晚期非小细胞肺癌伴脑转移的38例患者作为研究对象。研究对象按照入院先后顺序分为对照组和试验组,每组19例。对照组男12例,女7例;平均年龄(63.47±6.63)岁;病例分型为腺癌的患者为18例,鳞腺癌患者1例。试验组男13例,女6例;平均年龄(61.89±7.26)岁;病例分型为腺癌的患者为17例,鳞腺癌患者2例。2组患者在年龄、性别比以及疾病分型分期等基础资料比较差异均无统计学意义(P>0.05),具有可比性。见表1。
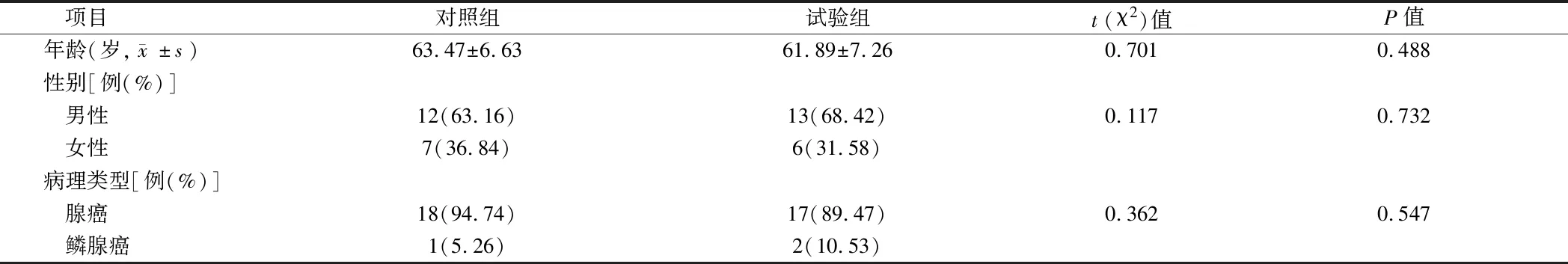
表1 2组患者基本情况对比分析 n=19
1.2 纳入标准 (1)所有患者经过MRI影像学和病理切片确诊,并且都符合《非小细胞肺癌临床实践指南》中的诊断标准[4];(2)患者均具有脑转移发生,并且均肺癌为原发灶转移至脑部;(3)所有患者经过基因检测发生T90M突变;(4)所有患者预计生存期>3个月,无全身衰竭或恶病质状况发生。
1.3 排除标准 (1)合并严重肝肾衰竭、自身免疫性疾病或伴有严重心脑系统功能衰竭的患者;(2)肺癌已经发生广泛全身转移、恶病质状态患者;(3)合并严重精神障碍或者拒不配合研究治疗的患者;(4)无法耐受奥西替尼或者中途退出试验研究的患者;(5)在奥西替尼治疗前应用过其他EGFR抑制剂治疗的患者。
1.4 治疗方法 对照组患者给予传统治疗方案,采用吉非替尼(阿斯利康制药有限公司,250 mg/片)+放疗方法进行治疗;试验组采用奥西替尼(阿斯利康制药有限公司,80 mg/片)+放疗方法进行治疗;除靶向治疗药物有所不同以外,其余放疗剂量和对症治疗都保持一致,21 d为1个治疗周期,本次试验研究共进行2个周期。
1.5 评价指标 (1)血清指标:治疗前后分别抽取2组患者空腹静脉血5 ml,采取酶联免疫吸附法检测癌胚抗原(CEA)以及血管内皮生长因子(VEGF)的含量变化。(2)脑部肿瘤长径:治疗前后分别用MRI方法检测肺癌脑转移患者脑部肿瘤长径变化情况,观测治疗效果。(3)不良事件发生率:搜集2组患者治疗过程中相关不良反应发生率的情况,主要包括肝功能损伤、白细胞下降、瘙痒、皮疹、腹泻、口腔溃疡等。
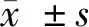
2 结果
2.1 2组患者CEA含量变化比较 治疗前2组患者CEA的含量比较,差异无统计学意义(P>0.05)。对照组和试验组患者治疗前后对比分析,CEA的含量均有明显下降(P<0.05);但试验组患者治疗后CEA的含量下降程度更加明显,差异有统计学意义(P<0.05)。见表2。
2.2 2组患者VEGF含量变化比较 治疗前2组患者VEGF的含量比较,差异无统计学意义(P>0.05)。对照组和试验组患者治疗前后比较,VEGF的含量均有明显下降(P<0.05);但试验组患者治疗后VEGF的含量下降程度更加明显,差异有统计学意义(P<0.05)。见表2。
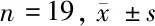
表2 2组患者CEA及VEGF含量变化比较
2.3 2组患者脑部肿瘤长径变化比较 对照组患者治疗前后脑部肿瘤长径比较,虽然治疗后脑部肿瘤的长径有下降趋势,但差异无统计学意义(P>0.05)。试验组患者治疗后脑部肿瘤的长径有明显下降(P<0.05),并且治疗后试验组患者脑部肿瘤长径明显短于对照组(P<0.05)。见表3。
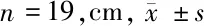
表3 2组患者脑部肿瘤长径变化分析
2.4 2组患者不良事件发生率比较 2组患者不良反应事件发生率差异均无统计学意义(P>0.05)。见表4。
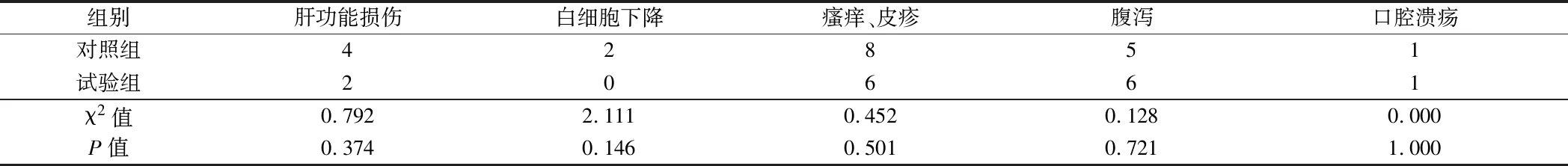
表4 2组患者不良事件发生率比较 n=19,例
3 讨论
近年来非小细胞肺癌患者的患病人数有显著上升趋势,并且以高年龄患者为主,相关研究表明,>50%的非小细胞肺癌患者的年龄都>65岁,患者年龄大,相应的脏器功能活性有所下降,并且基础疾病种类较多,一般预后情况不容乐观[5-8]。非小细胞肺癌早期患者一般临床症状不明显,到晚期时随着癌细胞扩散、转移等,手术意义已经不大。一般临床上依靠药物、放疗等内科治疗途径来缓解症状,延长患者生存期等。
相关研究表明,在确诊为晚期非小细胞肺癌的同时,约有10%的患者同时会被检查出已经发生了中枢神经系统转移[2],并且在接受规范化治疗的同时约有半数的患者会发生中枢神经系统转移。肺癌患者中有85%以上的都属于非小细胞肺癌,其中肺腺癌患者又存在更大的比重,基因检测结果表示部分肺腺癌患者中会发生EGFR基因突变,于是抑制EGFR基因突变的药物是抑制疾病进展、延长病患生存期和保障患者生存质量的重要突破口。
EGFR基因突变会导致癌细胞增殖异常活跃,病灶扩散、转移能力大大加强,因此遏制EGFR基因突变进一步发展、切断肿瘤细胞进展的信号通路,就能阻止肿瘤细胞生长甚至可以缩小肿瘤体积以达到治疗疾病的目的。奥西替尼是一种既能抑制EGFR基因又能控制其发生T790M基因突变的药物[9,10]。近年来,奥西替尼在治疗非小细胞肺癌患者的过程中发挥的重要作用,1次/d,每次80 mg,采用空腹或者随餐共同服用的模式进行治疗。同第一代靶向治疗非小细胞肺癌患者的药物相比,奥西替尼有其明显的优点,首先奥西替尼起效迅速,服药10 d内就能起到一定临床治疗效果,而且不容易发生耐药性。奥西替尼是一种小分子药物,能通过血脑屏障,更加适合肺癌发生脑转移患者的临床治疗。
放射治疗是肺癌发生脑转移后的重要治疗方法之一,近年来,放疗技术和放疗设备都有不小的提升,但是临床上出现的放疗抵抗现象是制约肺癌脑转移患者疗效的重要因素。研究表明,EGFR信号传导通路在放疗作用下可能被进一步激活,导致EGFR发生自身磷酸化,使得疾病加重。所以单纯放疗不是目前临床上的最佳治疗方案,需要配合药物进行控制,进一步遏制EGFR信号传导通路的进一步激活,这也是本次试验研究选择放疗联合化疗药物综合治疗的原因之一。
有相关研究表明,非小细胞肺癌患者尤其是肺腺癌患者的血清肿瘤标记物癌胚抗原CEA的含量普遍高于正常值[11-13],通过分析治疗前后CEA的含量能够直观展现肿瘤细胞在患者体内的活性和增殖能力。VEGF是血管内皮细胞特异性肝素结合生长因子,能够发挥促进血管新生的效能。肿瘤组织作为患者体内异常增生的实体,它的生长、转移同样需要依赖新生血管生成来维持营养物质及氧气的输送、使用。通过检测VEGF的含量同样能够反应肿瘤组织的活性和发生进展速度。本次研究结果表明,无论是传统的治疗方案或是使用奥西替尼的化疗方案均能够使血清CEA的含量、VEGF的含量降低,并且奥西替尼的化疗方案血清CEA、VEGF的含量降低趋势更加明显,差异有统计学意义(P<0.05)。研究结果提示,奥西替尼能够通过下调CEA、VEGF的含量来发挥抑制肿瘤增殖、分化的目的,进而特异性地杀灭肿瘤细胞,发挥作用机制尚不明确,但可能与抑制EGFR T790M突变阳性或降低突变表达效应有关联。还有研究表明,奥西替尼对于治疗肺癌患者的长期疗效效果尤其明显,能够显著提升患者的五年生存率[14]。研究结果显示,应用奥西替尼的试验组患者脑部肿瘤长径在阶段性实验结束后已经出现明显缩小,说明奥西替尼这一小分子药物相
较于传统药物更能够有效地通过血脑屏障,发挥抑制局部肿瘤增长的效果。并且奥西替尼的试验组不良事件发生率与对照组无明显差异,说明在治疗安全性及患者耐受性方面可以与传统药物基本保持一致。
综上所述,奥西替尼靶向治疗非小细胞肺癌发生脑部患者的疗效明显,能够更加有效抑制血清CEA及VEGF的含量,缩小转移病灶的肿瘤体积,并且毒副反应与传统药物基本保持一致,为临床上治疗晚期非小细胞肺癌患者提供了一条新的解决方案,但是由于癌症发病机制多样,受多旁路途径激活以及上皮细胞—间质细胞转化等可能发生耐药性机制的影响,这一治疗方案的临床应用广度仍然需要今后大量的临床、基础实验来证实。
