基于活血功效的云南鼠尾草最佳提取工艺研究
2020-08-26张彦如林雅雯张海珠
张彦如,白 雪,曹 波,林雅雯,张海珠*
(1.大理大学药学与化学学院,云南大理 671000;2.成都中医药大学药学院,成都 611137)
云南鼠尾草(Salvia yunnanensisC.H.Wright)是唇形科鼠尾草属多年生草本植物,又名小丹参、紫丹参、小红草乌、小红党参,主要分布于我国西南地区,其根入药,有活血祛瘀、通经止痛、清心除烦、凉血消痈等功效〔1〕。云南鼠尾草有着悠久的药用历史,明代《滇南本草》曾记载:“一味可抵四物汤补血之功”,民间主要将其用于治疗妇科和骨伤疾病等〔2〕。现代药理实验研究表明,云南鼠尾草具有广泛的生物活性,能抑制和解除血小板聚集,改善微动脉、微静脉痉挛和血液流态,防止血栓形成,改善微循环障碍,对血管重塑具有调节作用,增加心肌供氧量的同时还可以降低需氧量〔3〕;具有抗肝炎、抗病毒和抗肿瘤等活性〔4〕。随着现代药理作用的深入研究,云南鼠尾草日益受到重视,市场需求日益增大。
目前鼠尾草属药用植物的提取方法主要是以某一有效成分为指标,如丹参酮ⅡA、丹酚酸B〔5-7〕,通过多次加热回流获得提取物〔8〕。该方法评价指标单一,仅从化学角度确定中药的提取工艺或进行质量评价,无法密切关联临床功效和活性〔9-10〕。有研究表明云南鼠尾草活血功效优于丹参,体内、体外均能显著抑制血小板聚集〔2〕,因此本研究针对其活血的功效指标来评价云南鼠尾草的最佳提取工艺,弥补了仅仅采用化学成分检测的不足,以期为鼠尾草属药用植物的深度开发应用提供基础实验室数据。
1 材料
1.1药材与试剂云南鼠尾草经大理大学段宝忠教授鉴定为唇形科植物云南鼠尾草(Salvia yunnanensisC.H.Wright)(产自云南大理,粉粹过20目筛);甲醇(分析纯,四川西陇科学有限公司);水合氯醛(分析纯,国药集团化学试剂有限公司,批号:20180305);二磷酸腺苷(ADP,分析纯,北京索莱宝科技有限公司,批号:716E021);二甲基亚砜(DMSO,分析纯,富宇精细化工有限公司,批号:821D0311);0.9%氯化钠溶液(石家庄四药有限公司,批号:2001173203)。
1.2实验动物SPF级健康雄性SD大鼠,体质量200~220 g,购买自长沙市天勤生物技术有限公司,动物许可证号:SCXK(湘)2014-0011。正式实验前,动物适应性饲养1周,饲养环境为常规日夜周期,温度(21±2)℃,湿度40%~45%,自由进食饮水。
1.3仪器AggRAM血小板凝集仪(美国海伦娜公司);SK5210HP型超声波清洗器(上海科导超声仪器有限公司);TGL-18C飞鸽台式离心机(上海安亭飞鸽仪器有限公司);RQ∕ZC真空采血管(成都瑞琦科技实业股份有限公司);LGJ-50F冷冻干燥机(广州市星烁仪器有限公司)。
2 方法
2.1样品制备云南鼠尾草药材在60℃烘箱中干燥6 h至恒重,粉粹后过20目筛。准确称量3.000 g药材细粉按L9(34)正交试验设计方案进行超声提取,提取液经真空冷冻干燥为粉末,依次命名为E1~E9。准确称量不同冻干粉0.100 g,用含5%DMSO的0.9%氯化钠溶液500 μL超声溶解,配制成浓度为200 mg∕mL的生药原液。每种生药原液按照1:0.7剂距稀释分别得6个梯度浓度用于后续检测体外抗血小板聚集能力。测定前用0.45 μm滤膜过滤,续滤液即为待测样品溶液。正交试验因素水平表见表1。
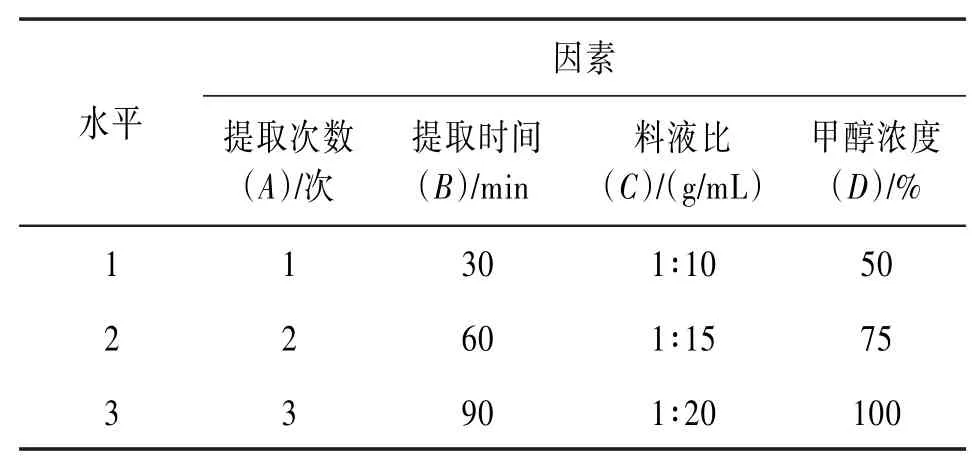
表1 正交试验因素水平表
2.2富血小板血浆(PRP)和贫血小板血浆(PPP)的制备健康雄性SD大鼠,腹腔注射10%水合氯醛(0.3 mL∕100 g)进行麻醉,腹主动脉取血,以0.13 mol∕L枸橼酸钠1:9抗凝。800 r∕min离心10 min,取上清液后,沉淀部分以相同条件再次离心,合并2次上清液得到 PRP;剩余部分以 3 500 r∕min 离心 15 min,吸取上清液即为PPP。PRP和PPP需要保持在18~25℃条件下,以PPP调节PRP的血小板浓度至4×108个∕mL〔11-13〕。
2.3体外抗血小板聚集试验取用PPP 300 μL进行透光度调零,精密量取PRP 250 μL于测试杯中,然后分别精密加入25 μL待测样品溶液,放入磁珠搅拌均匀,预热通道内37℃温育3 min,之后再将测
试杯放入调零后的检测通道,准确加入25 μL ADP(0.256 mg∕mL),记录最大血小板聚集率和血小板聚集曲线,每组平行测定2次,应在血液采集后2 h内完成检测,以含5%DMSO的0.9%氯化钠溶液作为对照溶液测定空白血浆的最大聚集率。
2.4数据处理血小板聚集抑制率计算公式〔14〕如下:
正交试验数据采用SPSS 20.0统计软件进行方差分析,P<0.05为差异有统计学意义,实验数据取2次独立实验数据的平均值。使用GraphPad Prism 6.01软件处理抗血小板聚集实验数据,并绘制浓度-抑制率曲线。
3 结果
3.1方法学考察结果
3.1.1 稳定性考察 取同一待测样品溶液,分别于0、2、4、6、12、24 h按“2.3”项测定其最大血小板聚集率,计算RSD。最大血小板聚集率RSD为2.50%,表明待测样品溶液在24 h内稳定性良好。
3.1.2 重复性考察 取同一待测样品溶液6份,在“2.3”项条件下分别测定,平行测定2次,记录样品溶液的最大血小板聚集率,计算得RSD为2.36%,说明该试验方法具有良好的重复性。
3.1.3 精密度考察 取同一待测样品溶液,在“2.3”项条件下连续测定6次,记录最大血小板聚集率,计算RSD,RSD值为1.64%,表明仪器的精密度良好。
3.2云南鼠尾草体外抗血小板聚集作用由图1可明显看出,9种不同提取工艺所得云南鼠尾草提取物对体外ADP诱导的血小板聚集均有抑制作用,且抑制率与提取物浓度呈正相关;E4对血小板聚集作用的抑制率最高,其余依次为E3、E8、E7、E6、E2、E9、E5,抑制血小板聚集作用最弱的是E1。不同工艺提取物浓度与抑制率的二次曲线回归方程见表2。最佳半数有效浓度(EC50)值越小,提取物抗血小板聚集作用对应的药液浓度越低,抗血小板聚集效率越高。因此,可以根据抑制曲线的线性关系和EC50值来评价不同提取物抗血小板聚集作用的效果。

表2 血小板抑制率曲线二次回归拟合
3.3正交试验结果根据前期试验资料,选取料液比、甲醇浓度、提取时间及提取次数4个因素进行L9(34)正交试验,确定从云南鼠尾草中提取发挥活血功效化学成分的最佳超声提取条件,结果见表3,方差分析见表4。
由表3分析可知,甲醇浓度的极差最大(19.006),说明甲醇浓度对云南鼠尾草中发挥活血功效化学成分的提取影响最大,其次是提取次数、料液比,最后是提取时间。试验结果表明,各因素影响程度大小为甲醇浓度(D)>提取次数(A)>料液比(C)>提取时间(B)。由表4中P值可知,因素D对提取效果具有显著影响(P<0.05),而因素A、B、C无显著影响(P>0.05)。结合云南鼠尾草体外抗血小板聚集作用结果,E4的血小板聚集作用抑制率最高,故云南鼠尾草中活血功效化学成分的最佳提取条件是A2B1C2D3,即料液比1:15、甲醇浓度100%、提取时间30 min、提取次数2次。在此条件下,测得体外ADP诱导抗血小板聚集的EC50为4.141 mg∕mL。

表3 L9(34)正交试验设计方案及结果
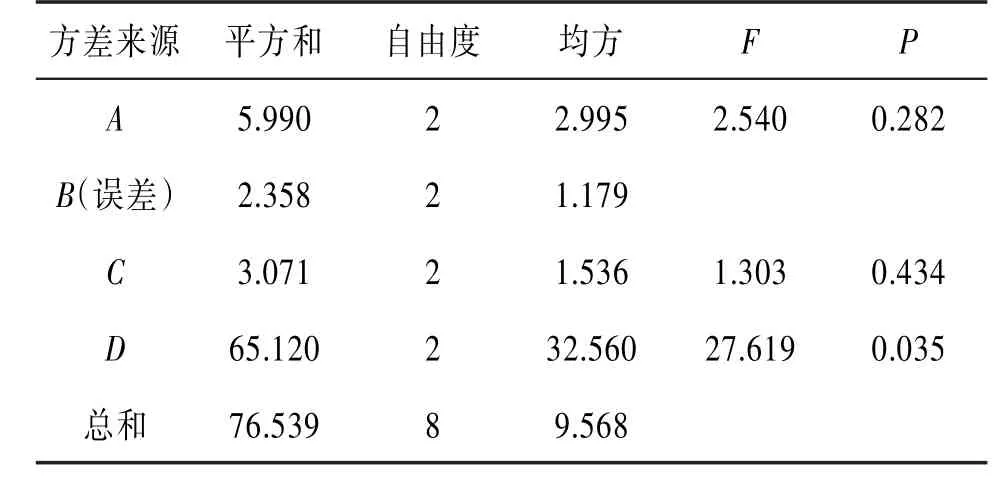
表4 正交试验方差分析
4 讨论
云南鼠尾草主要分布于云南、贵州、四川等地,在西南地区有近600年的药用历史,其味苦、微寒,《红河中草药》中记载:“活血行瘀,调经止痛”,是彝族、苗族、白族等少数民族常用药材〔15〕。虽然云南鼠尾草未被《中国药典》收载,但已被云南、贵州等省中药材部颁标准所收载,目前市场上以云南鼠尾草为原料的药品主要有丹莪妇康煎膏、紫灯胶囊、紫丹活血片、银丹心泰滴丸、龙金通淋胶囊等。其相关的单方和成方制剂在妇科、心系、骨伤和血瘀肿痛等领域广泛应用〔2〕,具有良好的民间临床应用经验和基础,鉴于此应进一步加强其物质基础与药效间的相关研究,促进云南鼠尾草的资源利用和产品开发,使其更好地服务于人类。
中药化学成分复杂,作用机制不明确,具有多成分、多途径、多靶点协同作用的特点。现有的提取工艺方法多数以指标性成分的含量测定为主,根据某一个或几个化学成分含量的多少来评判提取方法的优劣。例如,大黄药材的提取工艺研究中以总游离蒽醌〔16〕、大黄酸〔17〕、番泻苷 A〔18〕等含量来确定最佳提取工艺,其中总游离蒽醌与大黄泻下通便的功效几无关联,且与大黄利湿退黄、清热泻火的功效关系也不明确,因此单一指标性成分的定量分析难以实现对中药材提取工艺全面客观的评价。
目前从云南鼠尾草中共分离鉴定了85种化合物,主要化学成分为脂溶性菲醌化合物和水溶性酚酸类化合物〔19〕。云南鼠尾草中发挥活血功效的成分有丹酚酸A、丹酚酸B、丹酚酸C、丹参素、迷迭香酸、迷迭香酸甲酯、异阿魏酸等〔20〕,显然仅以单一成分为指标研究云南鼠尾草的提取工艺存在明显不足。因此本研究以活血功效为指征,紧密结合临床疗效,从整体活血成分群考察云南鼠尾草的最佳提取工艺。
由于实验条件有限,未开展云南鼠尾草中发挥活血功效的活性成分及其抗血小板聚集作用强弱研究。因此,课题延续工作将围绕建立系统方法考察云南鼠尾草中活性成分的抗血小板作用机制,为进一步筛选出高疗效、低副作用、高生物利用度的活血化瘀药物奠定基础。
