花生壳生物炭中溶解性碳黑对菲的环境行为研究*
2020-08-24马雍基
马雍基 陈 全,2 陈 懿 王 琳 吴 敏,2#
(1.昆明理工大学环境科学与工程学院,云南 昆明 650500;2.云南省土壤固碳与污染控制重点实验室,云南 昆明 650500)
生物炭是一种由生物质热解产生的富碳材料,在土壤固碳[1]、保水[2]、改善肥力[3-4]和污染治理[5]等方面都存在巨大的应用潜力,因此在农业和污染土壤修复方面引起了广泛关注。由于生物炭的芳香性、疏水性和多孔性,生物炭可作为土壤中疏水性有机污染物的有效吸附剂[6]。然而,近年来有研究发现,生物炭中的溶解性碳黑(DBC)很可能具有与生物炭不同的吸附特性[7-9]。有研究表明,DBC极易溶于水,且具备强迁移性[10-11],其理化性质会随着原生质和热解条件的变化而改变[12]1249,[13]。生物炭中DBC主要由小的芳香簇组成,含有羧基和少量的酚基[14]764,且具有高光敏组分,阳光照射下可生成单线态氧和超氧化物[15]。因此,DBC对环境中污染物的迁移能起到不可忽视的作用。
作为一种多环芳烃类疏水性有机污染物,菲具有强生态毒性及致癌特性,并广泛存在于环境中[16-18]。本研究从不同热解温度的花生壳生物炭中提取DBC,采用多种方法多角度研究其理化性质及对菲吸附能力的差异,并探索其根本原因,为进一步了解生物炭中溶解性物质与生物炭颗粒物的理化性质差异和为生物炭在环境中的实际应用提供参考。
1 材料与方法
1.1 生物炭和DBC的制备
采用高速粉碎机(800A)将干燥的花生壳粉碎,在氮气条件下慢速热解3 h制备生物炭。热解温度设置为200、400、500 ℃。花生壳原生质和不同热解温度下的生物炭过60目筛后用密封袋封存,分别标记为P和P200、P400、P500。将P、P200、P400或P500分别与去离子水1∶200(质量比)混合,采用超声仪(KH-800TBD)超声0.5 h后用0.45 μm微孔滤膜过滤得到DBC。DBC一部分冷冻保存;另一部分冷冻干燥,得到固体的DBC,分别标记为PD、PD200、PD400、PD500。
1.2 生物炭和DBC的表征
(1) 用比表面积分析仪(JW-BK132F)测定原生质和生物炭的比表面积。
(2) 将冷冻保存的DBC恢复至室温,用去离子水稀释后采用总有机碳(TOC)分析仪(德国元素vario TOC select)分析TOC含量。
(3) 分别称取2 mg花生壳原生质、生物炭和固体的DBC,利用元素分析仪(德国元素vario MICRO cube)测定C、H、O和N元素含量,每个样品平行测定3次。
(4) 将固体的DBC与溴化钾1∶200(质量比)混合并研磨压片,利用傅立叶变换红外光谱(FTIR)仪(Varian 640-IR)在400~4 000 cm-1内以8 cm-1的分辨率扫描32次。
(5) 将固体的DBC以1∶1(质量比)溶于重水后测核磁共振氢谱。
(6) 将冷冻保存的DBC稀释至TOC为20 mg/L,利用紫外分光光度计(岛津UV-2600)测量紫外光谱,范围设置为200~800 nm,采样间隔为1 nm。
1.3 荧光猝灭和荧光内过滤效应(IFE)校正
以三维荧光扫描菲,得到250 nm激发光下的3个峰。选取DBC荧光响应值最小的峰(激发波长250 nm、发射波长350 nm)对菲进行定量分析。菲在0~200 μg/L内的荧光响应值具有非常好的线性关系,因此在这个浓度范围内选取8个点进行实验。使用氮气将背景溶液吹扫30 min,避免由氧气引起的静态猝灭。将4种DBC以去离子水分别稀释至初始TOC为20、30 mg/L。分次向装有2 mL DBC的比色皿中加入50 μL菲,并置于磁力搅拌器(JB-10)上搅拌2 min,并测量溶液在250、350 nm处的紫外吸光度以进行IFE校正[19]。菲荧光强度的明显降低可能是由于DBC引起的IFE影响,因此应对其进行校正,IFE校正公式见文献[20]。
2 结果与讨论
2.1 生物炭和DBC的理化性质分析
花生壳生物炭和DBC的基本理化性质见表1。随着热解温度的升高,生物炭的比表面积增加;除PD外,DBC的C、O、H、N元素含量下降;TOC含量减少,其中PD200的TOC比PD400、PD500高出1个数量级,这是因为生物炭中的水溶性挥发性物质含量逐渐减少[12]1251;生物炭的H/C、O/C和(N+O)/C减小,说明热解温度越高,生物炭的芳香性越高,亲水性和极性越低。PD200的H/C明显低于其他3种DBC,表明PD200具有更高的芳香性。除PD外,随着热解温度的升高,DBC的O/C和(N+O)/C增加,反映出DBC的亲水性和极性随着热解温度的升高而增强[21]。
为获取DBC的官能团结构信息,采用FTIR对DBC进行了表征,结果见图1。1 605 cm-1处的特征峰代表芳香性C=C[22],4种DBC表现出不同丰度,PD200的芳香性最强,PD400、PD500、PD的芳香性依次减弱。1 385 cm-1处的特征峰代表酚羟基[14]763,PD500有最突出的丰度,说明其酚羟基含量最高。1 110 cm-1处的特征峰归属于C—O—C,除PD外,PD200、PD400、PD500都有明显的特征峰吸收带,并且随着热解温度的增加,C—O—C丰度有增高的趋势。1 070 cm-1处的特征峰代表脂肪族碳链,只有PD有明显的特征峰,可能是原生质中的脂肪族碳链在热解过程中发生了断裂。
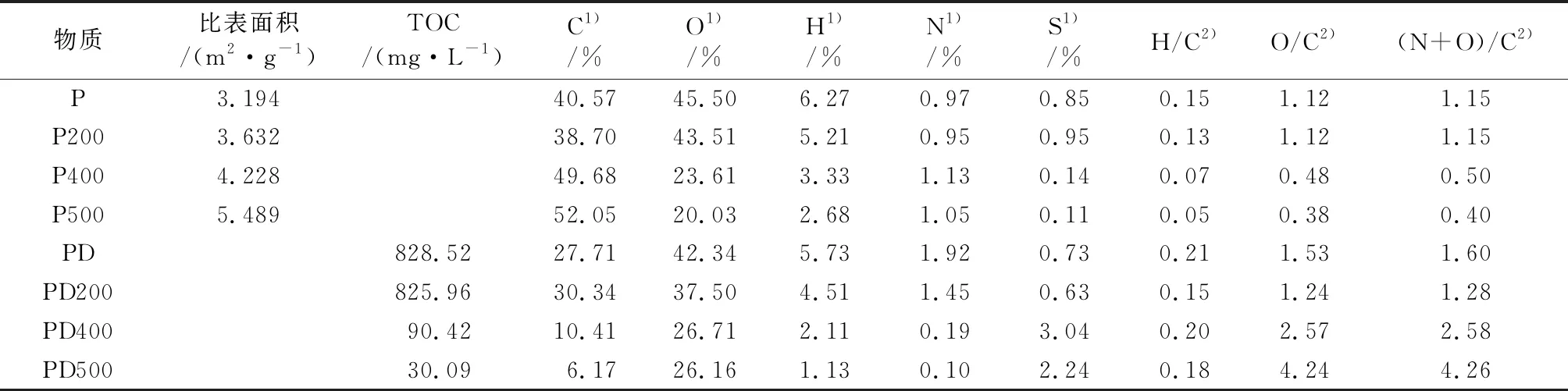
表1 花生壳生物炭和DBC的基本理化性质
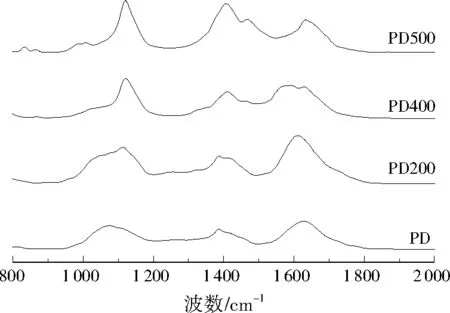
图1 DBC的FTIRFig.1 FTIR of DBC
核磁共振氢谱可提供化合物分子中所有H原子的信息,进一步确定DBC的结构特征,结果见图2。6.5×10-6~8.2×10-6共振峰代表芳香性H,相较其他DBC,PD200有明显的共振峰,因此PD200具有最高的芳香性,与FTIR表征一致。3.2×10-6~4.4×10-6共振峰代表醇、醚或酯碳键上的H,4种DBC在此处的共振峰随着热解温度增高而明显降低。1.8×10-6~3.2×10-6共振峰代表不饱和碳上的α -H,随着热解温度的增高,α -H含量先增加后降低,其中PD400最高。1.2×10-6~1.8×10-6共振峰为脂肪族H[23],随着热解温度的增加,DBC脂肪族H的共振峰逐渐减小,这一现象与FTIR数据也十分吻合。总的来说,随着热解温度的升高,DBC中会形成更多的酚羟基和醚键,而脂肪族碳链、醇或酯会逐渐断裂。
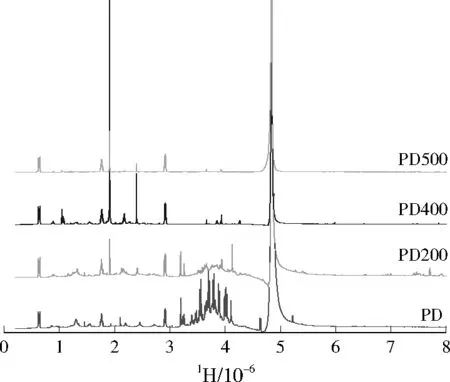
图2 DBC的核磁共振氢谱Fig.2 NMR 1H spectra of DBC
由于DBC中含有芳香烃和其他官能团,在紫外可见光区会显示强吸光度。在260 nm处会出现取代苯和酚的π-π电子迁跃,故经常用260 nm处的吸光度来代表天然有机质中芳香烃C=C的相对含量[24]。如图3所示,4种DBC在260 nm处的吸光度为PD200>PD400>PD500>PD。这也代表了其芳香性的排序。

图3 DBC的紫外光谱Fig.3 UV spectrogram of DBC
2.2 DBC对菲的吸附行为
由图4可以看出,4种DBC与菲都有较强的结合能力,但随着菲浓度的增加,结合率均有轻微的下降。该结果和文献[25]一致。与低TOC质量浓度(20 mg/L)相比,高TOC质量浓度(30 mg/L)DBC具有更强结合菲的能力,而DBC与菲的表观结合能力在不同TOC浓度时均表现为PD200>PD400>PD500>PD。这与DBC的芳香性一致,因为随着热解温度增高,生物炭的内部碳组分不断聚合[26],高芳香性的DBC不易被洗出,因此高温热解(≥400 ℃)得到的生物炭中溶出的DBC中芳香性物质较少,不易与菲发生荧光猝灭作用。而PD由于没有经过热解反应,其溶出的DBC中脂肪族碳含量较高,而芳香性较低,因而较难与菲发生荧光猝灭作用。
研究表明,以猝灭后与猝灭前荧光响应值的比值(F0/F)为纵坐标,TOC浓度为横坐标作出的图呈严格线性相关时,只存在动态猝灭或静态猝灭;如果不呈线性,是向上弯曲的曲线,则表示在这一过程中两种猝灭类型同时存在。动态猝灭是由于分子之间的碰撞而引发的猝灭现象,静态猝灭由于荧光物质和猝灭剂之间的相互结合而导致的猝灭现象[27]。根据图5可认为,DBC与菲之间同时存在动态和静态猝灭。相比较低TOC浓度DBC,高TOC浓度DBC与菲的猝灭曲线向上弯曲的程度更强。根据文献[28]可知,在DBC与菲之间的荧光猝灭过程中,静态猝灭为主要猝灭类型。

图4 DBC与菲的结合率Fig.4 Binding rate of DBC and phenanthrene

图5 DBC对菲的荧光猝灭Fig.5 Fluorescence quenching of phenanthrene by DBC
3 结 论
(1) 随着热解温度的升高,花生壳生物炭中DBC的TOC含量减少,其中PD200的TOC比PD400、PD500高出1个数量级。
(2) 随着热解温度的升高,DBC中会形成更多的酚羟基和醚键,而脂肪族碳链、醇或酯会逐渐断裂。
(3) 4种DBC中,PD200的芳香性最强。DBC的芳香性越强,对菲的吸附能力越强。
