大剂量免疫球蛋白联合美罗培南治疗新生儿败血症临床评价*
2020-08-24余金蓉
袁 立,余金蓉,赵 明
(1. 湖北省应城市人民医院新生儿科,湖北 孝感 432400; 2. 湖北省武汉市第一医院新生儿科,湖北 武汉 430022)
新生儿败血症(NS)是指出生28 d 内出现的新生儿感染性疾病,在活产儿中发生率为1‰~8‰,全世界每年约100 万新生儿因败血症死亡,占新生儿死亡总数的1/4[1]。早产儿由于免疫系统尚未发育完善,免疫功能低下,增加了感染风险。临床多用抗生素治疗NS,但随着细菌耐药性的加重,常规抗生素疗效欠佳。美罗培南为新一代碳青霉烯类抗生素,可通过抑制细菌细胞壁的合成而发挥抗菌作用,抗菌活性强且抗菌谱广[2]。免疫功能低下与新生儿感染的发生密切相关,近年来,免疫疗法在NS 治疗中逐渐受到重视。静脉注射免疫球蛋白(IVIG)能补充机体内源性球蛋白,提高免疫功能,增强其抗感染能力[3-4]。本研究中探讨了大剂量免疫球蛋白联合美罗培南治疗NS 的临床疗效及对患儿血清胆红素和血小板水平的影响。现报道如下。
1 资料与方法
1.1 一般资料
选取应城市人民医院新生儿科2017 年1 月至2018 年12 月收治的NS 患儿160 例,均符合NS 诊断标准[5],其家属签署知情同意书。排除伴先天性重要脏器畸形、自身免疫性疾病、血液系统疾病及已使用其他免疫制剂者。按随机数字表法分为对照组和观察组,各80 例。两组患儿一般资料比较,差异无统计学意义(P >0.05),具有可比性。详见表1。
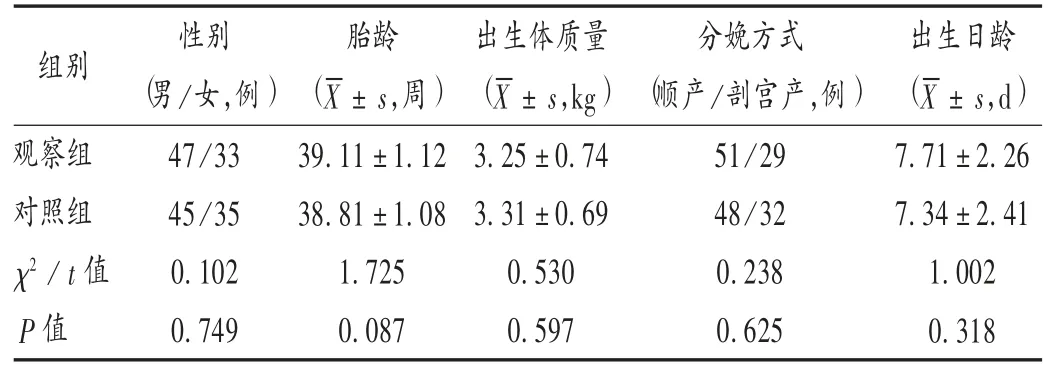
表1 两组患儿一般资料比较(n =80)
1.2 方法
两组患儿均予维持水电解质平衡、改善微循环及其他对症支持治疗,并予静脉滴注注射用美罗培南(珠海联邦制药股份有限公司,国药准字H20113179,规格为每支按C17H25N3O5S 计0.5 g)20 mg/kg,每8 h 1 次,治疗7 d。观察组患儿加用大剂量(400 mg/kg)静注人免疫球蛋白(pH4)(国药集团上海血液制品有限公司,国药准字S20023011,规格为每瓶2.5 g ∶50 mL)静脉滴注,初始滴速为4~6 滴/分,若能耐受则逐渐加快滴注速率,于2 h 内滴完,连用3 d。
1.3 观察指标及疗效判定标准
观察指标:1)症状改善时间,记录患儿拒奶改善时间、体温稳定时间及神经症状改善时间。2)血清学指标,采集患儿空腹静脉血,应用IMMAGE 型全自动特种蛋白分析仪(美国Beckman Coulter 公司)测定血清免疫球蛋白(Ig)G,IgM,IgA 水平;应用酶联免疫吸附(ELISA)法检测白细胞介素8(IL-8)、降钙素原(PCT)水平,应用免疫散射比浊法检测C 反应蛋白(CRP)水平;应用全自动生化分析仪检测丙氨酸氨基转移酶(ALT)、总胆红素(TBil)水平,应用XT-1800i 型全自动血细胞分析仪测定血小板计数(PLT)、平均血小板体积(MPV)。
疗效判定[6]:治愈,病情好转,症状基本消失,实验室检查结果无异常;显效,病情好转,大部分症状消失,实验室检查中仅1 项未恢复;进步,病情控制,但症状依然存在;无效,病情无明显好转,甚至有加重。总有效=显效+有效。
1.4 统计学处理
采用SPSS 20.0 统计学软件分析。计量资料以表示,行t检验;计数资料以率(% )表示,行χ2检验。P <0.05 为差异有统计学意义。
2 结果
结果见表2 至表7。

表2 两组患儿临床疗效比较[例(%),n =80]
表3 两组患儿症状改善时间比较 ± s,d,n =80)
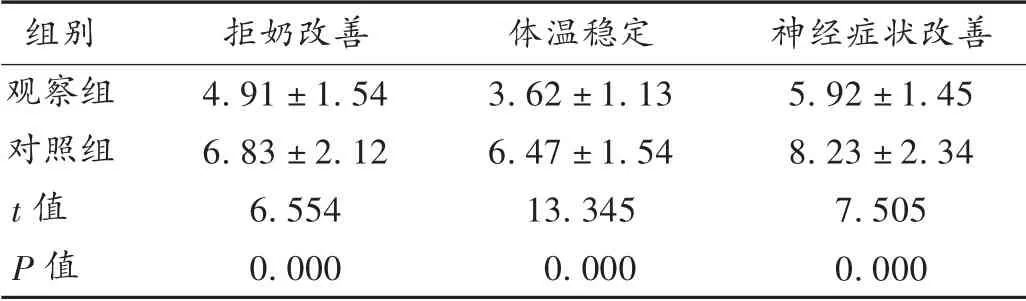
表3 两组患儿症状改善时间比较 ± s,d,n =80)
5.92 ±1.45 8.23 ±2.34组别观察组对照组t 值P 值拒奶改善4.91 ±1.54 6.83 ±2.12 6.554 0.000体温稳定3.62 ±1.13 6.47 ±1.54 13.345 0.000神经症状改善7.505 0.000
表4 两组患儿血清免疫球蛋白水平比较 ± s,g/L,n =80)
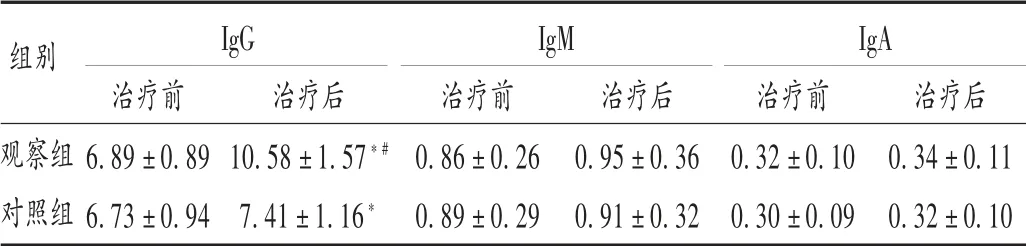
表4 两组患儿血清免疫球蛋白水平比较 ± s,g/L,n =80)
注:与本组治疗前比较,*P <0.05;与对照组治疗后比较,#P <0.05。表5 和表7 同。
治疗前6.89±0.89 6.73±0.94组别IgG IgM IgA观察组对照组治疗后10.58±1.57*#7.41±1.16*治疗前0.86±0.26 0.89±0.29治疗后0.95±0.36 0.91±0.32治疗前0.32±0.10 0.30±0.09治疗后0.34±0.11 0.32±0.10
表5 两组患儿血清炎性因子水平比较 ± s,g/L,n =80)
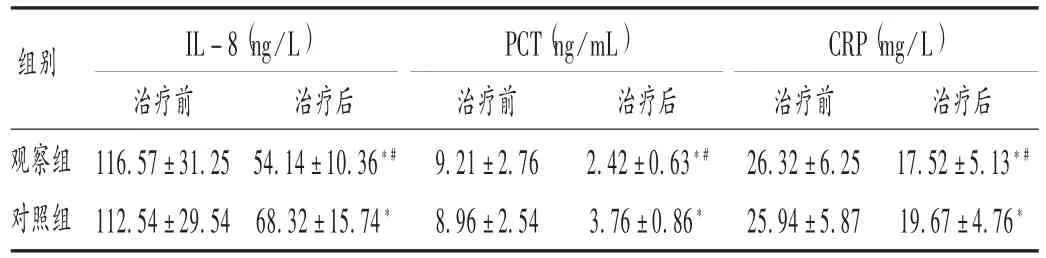
表5 两组患儿血清炎性因子水平比较 ± s,g/L,n =80)
治疗后54.14±10.36*#68.32±15.74*组别IL-8(ng/L) PCT(ng/mL) CRP(mg/L)观察组对照组治疗前116.57±31.25 112.54±29.54治疗前9.21±2.76 8.96±2.54治疗后2.42±0.63*#3.76±0.86*治疗前26.32±6.25 25.94±5.87治疗后17.52±5.13*#19.67±4.76*

表6 两组患儿不良反应发生情况比较[例(%),n =80]
表7 两组患儿血清ALT,TBil,PLT,MPV 水平比较 ± s,n =80)

表7 两组患儿血清ALT,TBil,PLT,MPV 水平比较 ± s,n =80)
治疗后25.91±8.21 26.12±4.65 ALT(U/L) TBil(μmol/L) PLT(×109/L) MPV(fL)组别观察组对照组治疗前28.12±6.25 27.68±5.46治疗前71.54±19.54 68.74±9.12治疗后34.12±10.21*#41.45±7.68*治疗前103.56±28.25 101.45±26.74治疗后167.24±36.41*#145.32±30.66*治疗前11.72±3.15 11.66±2.76治疗后9.51±2.41*#10.35±2.38*
3 讨论
NS 是新生儿常见危重感染性疾病,是导致新生儿死亡的重要原因。美罗培南对NS 病原菌有较高的抗菌活性,作用优于第3 代头孢类抗生素。美罗培南不仅化学稳定性高,抗菌作用强,且肾毒性及神经毒性较小,安全性更高[7]。近年的研究认为,对于NS 患儿,除予以抗生素治疗外,免疫治疗也尤为重要。IVIG 能提高患儿机体被动免疫力,增强抗感染能力[8]。本研究结果显示,大剂量IVIG 联合美罗培南治疗NS 能促进患儿临床症状改善。
IVIG 是提取自人胎盘血或健康人静脉血的生物制品,主要活性成分为具有抗广谱病毒及细菌作用的IgG,静脉输注后不仅能杀灭病原体,还具有免疫调节作用,广泛应用于原发性或继发性免疫球蛋白缺陷症的治疗[9]。新生儿感染治疗时联合IVIG 与基础治疗,能有效提高疗效[10]。本研究结果显示,IVIG 能有效提高患儿血清IgG水平,从而增强机体免疫功能及对病原体的清除能力。
NS 发病机制为致病菌侵入新生儿体内,在血液循环中生长繁殖,产生毒素,从而引起全身炎性反应。IL-8属中性粒细胞的关键趋化因子,能促进炎性因子的表达及释放。PCT 和CRP 均是感染性疾病的重要诊断指标[11]。本研究结果显示,治疗后,观察组患儿血清IL-8,PCT,CRP 水平均明显低于对照组,表明大剂量IVIG 联合美罗培南治疗NS 能有效减轻炎性反应。
NS 发生后机体过度的炎性反应可导致全身脏器损伤。肝脏是败血症常累及的靶器官,肝脏组织出现损伤时,肝细胞转氨酶会释放入血,并会对胆汁代谢产生影响,导致外周血胆汁酸水平升高[12-13]。血小板是成熟骨髓巨核细胞脱落下来的胞质小块,在败血症发生时,细菌及其代谢物质会损伤血管内皮细胞,细胞毒素会抑制骨髓造血功能,导致血小板产生减少;此外,血小板数量的减少会引起血小板代偿性体积增大,表现为MPV 增高[14-15]。血小板指标对NS 的诊断有重要价值[16],其水平与NS 预后密切相关[17]。本研究结果显示,治疗后,观察组患者TBil 及MPV 均明显低于对照组,PLT 明显高于对照组,表明大剂量IVIG 联合美罗培南治疗NS,能改善胆红素和血小板水平。两组不良反应发生率无显著差异,表明联合治疗方案不会明显增加不良反应。
综上所述,大剂量IVIG 联合美罗培南治疗NS,能有效改善患儿症状,增强机体免疫功能,减轻炎性反应,并改善胆红素和血小板水平。
