铁质文物常用除锈试剂的除锈效率及其腐蚀性的比较研究
2020-08-24成小林李延祥
张 然,成小林,潘 路,李延祥
(1.中国国家博物馆,北京 100079;2.金属文物保护国家文物局重点科研基地(中国国家博物馆),北京 100079;3.北京科技大学,北京 100083)
0 引 言
铁的化学性质比较活泼。在自然环境中,铁质文物极易和水、空气、土壤等因素发生作用,导致迅速、严重的腐蚀。无论是出土的,还是室外空气中的铁质文物,其表面往往都有不同程度的锈蚀。
按对铁质文物的影响,锈蚀产物可以分为无害锈和有害锈两类。无害锈是指结构相对紧密、坚硬、稳定的锈蚀成分,不参与进一步的腐蚀过程,对腐蚀具有一定的抵抗作用。有害锈结构疏松,具有一定的蓄水功能,可以使水分子进入内部,发生化学和电化学腐蚀,此外有害锈可能本身也会参与腐蚀过程,导致铁器进一步损坏。因此在铁质文物保护过程中,除锈是重要的步骤,应该除去有害锈,保留无害锈。在实际工作中,通常要除去铁器上的疏松锈层,保留致密的锈层。除锈工作是后续脱盐、缓蚀、封护等工作的基础。除锈处理不好,会影响脱盐、缓蚀、封护等工作的效果。
常用的除锈方法可分为物理方法和化学方法两大类。物理方法包括手工法、小型机械法、超声波清洗法、喷砂法、激光清洗法等;化学方法包括化学试剂法、电化学法、氢气还原法、等离子体还原法等[1]。两类方法各有利弊。一般认为,物理方法的可控性较化学方法强,化学方法可控性相对差些,一旦控制不好,会对铁器造成不可逆的损害;除锈试剂往往对铁基体也有腐蚀性,除锈后如果不清理干净,可能会对铁器造成损害;有些除锈试剂有毒性,对人员、环境也有损害[2]。
但化学方法也有其优势,能够有效地溶解或软化锈蚀产物,作为物理方法的辅助方法可以减轻除锈工作强度。尤其对于鎏金、错金银的铁器,化学方法可以选择性地去除金银纹饰上的铁锈,而不与金银发生反应。在辽代嵌金银饰铁器[3]、张家川回族博物馆藏方型错金铁牌饰[4]、战国错银铁镜[5]等的保护过程中,都使用了化学试剂帖敷的方法。
目前铁质文物保护中,常用的除锈试剂包括磷酸、乙二胺四乙酸二钠Na2EDTA、柠檬酸、醋酸、酒石酸、草酸、甲酸、六偏磷酸钠等[3-16]。其原理主要是利用试剂的酸性以及与铁离子的络合能力,将锈蚀产物溶解或软化。为了抑制除锈过程中试剂对铁基体的腐蚀,可以加入少量的缓蚀剂[17]。目前国内文物保护领域对于不同试剂除锈效果、除锈试剂对铁基体的腐蚀性等方面的研究特别是定量研究还比较缺乏。本研究以磷酸、柠檬酸、酒石酸、Na2EDTA 4种常用除锈试剂为研究对象,研究试剂与铁锈粉末、锈块、铸铁片、带锈铸铁片等多种样品的相互作用。其中铁锈粉末为文物上脱落的铁锈研磨而成,成分较为均匀,便于比较试剂的除锈能力;锈块为文物脱落的锈蚀产物块,更接近实际文物情况;铸铁片与试剂的作用可以测试试剂对铁基体的腐蚀性;而带锈铸铁片与试剂的作用可研究铁基体对除锈过程的影响。通过试剂与不同样品的作用,综合评估试剂的除锈效果以及对铁基体的腐蚀,为铁质文物保护中除锈试剂的选择提供一些建议。
1 实验内容
1.1 实验试剂
研究4种常用铁器除锈试剂,分别为:磷酸、柠檬酸、酒石酸、Na2EDTA,均为分析纯,配成质量分数5%的水溶液。在部分实验中添加质量分数0.3%的六亚甲基四胺作为缓蚀剂。
1.2 实验样品
选用四种样品进行实验:
1)Z30铸铁片。高邮市秦邮仪器化工有限公司生产。矩形,尺寸为50 mm×25 mm×2 mm,表面积为28 cm2。使用前,先后用乙醇、丙酮棉球擦拭干净,快速吹干后放入干燥器中备用。
2)铁锈粉末。来自山东青州香山汉墓出土大批铁剑上自然脱落的铁锈粉末,呈褐色。将铁锈粉末研磨至120目过筛,并混合均匀,在烘箱中于110℃下烘干2 h,放入干燥器中备用。
3)铁锈块。来自山东青州香山汉墓出土大批铁矛头上自然脱落的铁锈块,选择其中质量为0.5~2 g,长度不超过1.5 cm,表面为红褐色或黑色,没有白色沉积物的锈块。锈块通体矿化,基本没有铁芯。用超声波清洗器将锈块在纯净水中清洗3次,每次10 min,除去浮锈,在烘箱中于110℃下烘干2 h,放入干燥器中备用。
4)带锈Z30铸铁片。将3.5%NaCl溶液(质量比)滴加在Z30铸铁片表面,每天滴加一次,每次铁片两面各滴加1~2 mL,持续90 d,使铁片表面腐蚀。用机械法将表面浮锈除去,再使用超声波清洗器将铁片在纯净水中清洗5 min,取出后用乙醇脱水,快速吹干后放入干燥器中备用。
1.3 实验仪器
X射线荧光能谱仪(EDXRF)。仪器型号:HORIBA XGT-5000 X射线显微分析仪;电压50 kV;探头光斑100μm;电流自动;扫描时间100 s;工作曲线P3。测量时每个样品取三个点,结果取平均值。
X射线衍射仪(XRD)。仪器型号D/max 12 kW粉末衍射仪;仪器所属北京北达燕园微构分析测试中心;X射线 CuKα(0.154 18 nm);管电压40 kV;管电流100 mA;单色器石墨弯晶单色器;扫描方式θ/2θ扫描;扫描速度 8°(2θ)/分;采数步:0.02°(2θ);环境温度(25.0 ±1)℃;湿度(30.0 ±5)%。
电感耦合高频等离子体原子发射光谱(ICPAES)。仪器型号Leeman Prodigy型全谱直读发射光谱。
视频显微镜。仪器型号Hirox KH3000型;仪器所属中国国家博物馆。
电子天平。仪器型号Precisa XT 220A型。最大称量220 g,解析度0.000 1 g。
1.4 实验方法
1.4.1 Z30铸铁片均匀腐蚀全浸实验 依据参考文献[18]进行均匀腐蚀全浸实验。具体操作方法为:将干燥后的Z30铁片称重,3片铁片为一组悬挂于试剂溶液中,溶液体积为1 500 mL。浸泡过程中容器用封口膜封口。分别使用不加缓蚀剂和添加缓蚀剂的溶液进行实验。
铁片于24 h后取出,迅速用水将表面冲洗干净,再用乙醇棉球反复擦拭,直至没有铁屑粘在棉球上为止,再用丙酮棉球擦拭,快速吹干后放入干燥器中,质量稳定后称重。
实验过程中需观察铁片在不同试剂中的腐蚀现象,再根据参考文献[18]计算腐蚀速率R(mm/a)。
使用以下公式计算缓蚀效率:
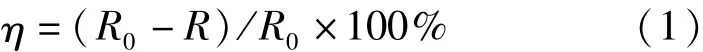
式中,η为缓蚀效率;R0为不添加缓蚀剂的溶液腐蚀速率,mm/a;R为添加缓蚀剂的溶液腐蚀速率,mm/a。
1.4.2 铁锈粉末溶解实验 内容如下:
1)锈粉的成分测量。用EDXRF进行成分分析。用XRD进行物相分析。
2)溶解实验。按照参考文献[19]用浓盐酸将锈粉溶解,测定其酸不溶物含量。用Na2EDTA络合滴定法测定铁含量,用ICP-AES测定硅、钙、铝等元素含量。
称取0.5 g锈粉,加入25 mL除锈试剂。每种试剂要做6 份,分别于1 d、3 d、7 d、14 d、28 d、63 d 后进行取样测量。取样时用干燥的玻璃坩埚过滤器过滤除锈液,用去离子水充分洗涤,洗涤液并入滤液。
3)滤渣的分析。将盛有滤渣的玻璃坩埚放入烘箱,在110℃下烘干2 h,取出后放入干燥器,1 d后进行称量。用显微镜观察滤渣的颜色、形态并与未浸泡的锈粉进行对比,计算锈粉质量减少率,计算公式如下:
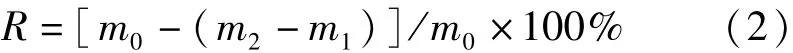
式中,R为质量减少率;m0为锈粉初始质量,单位为g;m1为空坩埚质量,单位为g;m2为盛有滤渣的坩埚质量,单位为g。
滤渣用EDXRF进行成分分析,用XRD进行物相分析。
4)滤液的分析。将滤液用去离子水定容至100.0 mL或250.0 mL,其中一部分用Na2EDTA络合滴定法测定铁含量,剩余溶液用ICP-AES测定硅、钙、铝、磷含量。
5)Na2EDTA络合滴定法测定铁含量。盐酸、磷酸、柠檬酸、酒石酸浸泡锈粉的滤液可以直接滴定,即取25.00 mL溶液,调节pH值至2~3,加入磺基水杨酸作为指示剂,加热到50~60℃,用事先标定的Na2EDTA(0.01 mol/L)溶液滴定至由紫红色变为亮黄色为终点。平行滴定三次。
Na2EDTA浸泡锈粉的滤液需沉淀处理后才能滴定。即取25.00 mL溶液,加15 mL NaOH(10%),加热至沸腾后,逐滴加入2 mL H2O2,稍冷后用定量滤纸倾泻过滤,并用少量去离子水淋洗烧杯也并入滤纸中,过滤后再用少量去离子水淋洗沉淀2~3次。用热的HCl(1∶1)溶解沉淀,用去离子水和盐酸交替淋洗至滤纸完全无黄色,溶解液用1∶1盐酸和10%氢氧化钠调节pH值为2~3,加入磺基水杨酸作为指示剂,加热到50~60℃,用事先标定的Na2EDTA(0.01 mol/L)溶液滴定至由紫红色变为亮黄色为终点。平行滴定3次。
计算溶解铁量占锈粉总质量的百分数,计算公式如下:
R=V1×c/25.00×V0/1 000×88.86/m0×100%(3)式中,R为溶解铁量(以FeOOH计)占锈粉总质量的百分数;V1为滴定消耗的Na2EDTA体积,单位为mL;c为滴定用的Na2EDTA浓度,单位为mol/L;V0为滤液定容体积,单位为mL;m0为锈粉初始质量,单位为g。
1.4.3 铁锈块溶解实验 将事先称重的铁锈块浸泡在250 mL试剂中,每种试剂浸泡3个锈块。28 d后取出,在纯净水中超声清洗3次,每次10 min,在烘箱中于110℃下烘干2 h,放入干燥器中,1 d后进行称量。观察颜色与形态变化,计算质量减少率。计算公式如下:
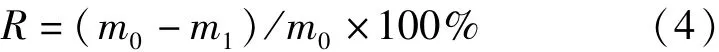
式中,R为质量减少率;m0为锈块原始质量,单位为g;m1为浸泡后的锈块质量,单位为g。
1.4.4 带锈Z30铸铁片浸泡实验 将干燥后的带锈Z30铁片称重,3片铁片为一组悬挂于试剂溶液中,溶液体积为1 500 mL。浸泡过程中容器用封口膜封口。
铁片于2 h后取出,用纯净水冲洗表面,然后迅速用纸吸干表面的水,再用乙醇、丙酮棉球擦拭,快速吹干后放入干燥器中,质量稳定后称重。
观察浸泡后铁片表面状况,比较不同试剂浸泡的铁片表面露出的铁基体的面积,计算质量变化。
2 结果与讨论
2.1 Z30铸铁片均匀腐蚀全浸实验
2.1.1 实验现象 Z30铸铁片在除锈试剂浸泡过程的实验现象见表1。

表1 除锈试剂浸泡Z30铸铁片的实验现象Table 1 Experimental phenomena of Z30 cast iron sheets soaked in the rust removal reagents
2.1.2 实验结果 Z30铸铁试片在不同试剂中的腐蚀速率、缓蚀效率计算结果见表2。
2.1.3 讨论 本实验所用几种试剂均为弱酸性试剂。试剂的酸性可以用电离常数p Ka来判断,p Ka越小,酸性越强。表3列出了各种除锈试剂的电离常数。
Z30铸铁在几种试剂中的腐蚀速率顺序为磷酸>酒石酸>柠檬酸>Na2EDTA,这与几种试剂的酸性顺序是一致的。
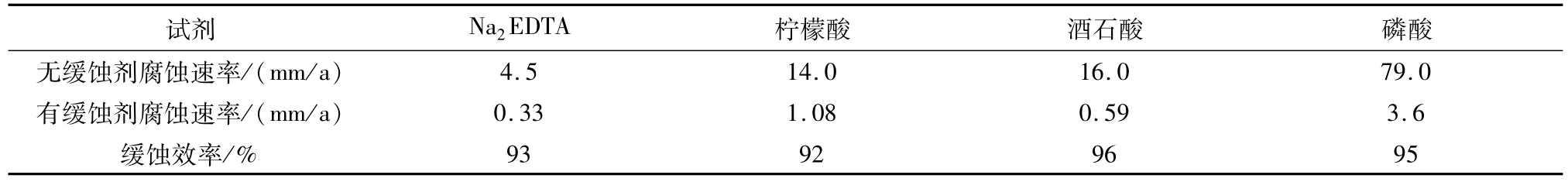
表2 Z30铸铁试片在试剂中的腐蚀速率与缓蚀效率Table 2 Corrosion rates and inhibition efficiencies of Z30 cast iron sheets in the reagents
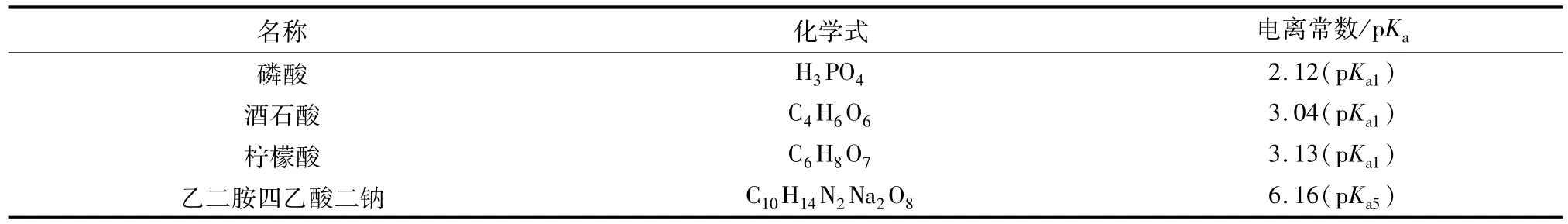
表3 除锈试剂的电离常数[20]Table 3 Ionization constants of the rust removal reagents
虽然几种试剂均为弱酸,但Z30铸铁在其中的腐蚀速率都很高,尤其过量磷酸对铁的腐蚀速率更是高达79 mm/a(作为对比,Z30铸铁在3.5%NaCl溶液中腐蚀速率为0.076 mm/a[21])。因此,除锈过程中试剂对铁基体的腐蚀是非常严重的。在铁器文物特别是有铁基体的文物上一定要慎用这类试剂。在使用时应避免长时间大面积浸泡,可使用局部帖敷的办法,并随时观察,及时停止帖敷。另外可以在酸性除锈试剂中加入合适的酸洗缓蚀剂来降低铁基体的腐蚀。在本实验中,添加0.3%的六亚甲基四胺作为缓蚀剂后,试剂对铁片的腐蚀速率显著降低,缓蚀效率达到90%以上,但仍有明显的腐蚀性。在用试剂处理后应使用碱性溶液进行清洗,避免试剂残留。
2.2 铁锈粉末溶解实验
2.2.1 颜色与形态变化 铁锈粉末经试剂浸泡前后的颜色与形态变化见表4和图1~8。

表4 铁锈粉末浸泡前后颜色形态Table 4 Colors and conditions of rust powder before and after soaking

图1 原始锈粉的显微照片Fig.1 Micrograph of original rust powder

图3 Na2EDTA浸泡63 d的锈粉显微照片Fig.3 Micrograph of rust powder after soaking in Na2 EDTA for 63 days

图5 酒石酸浸泡63 d的锈粉显微照片Fig.5 Micrograph of rust powder after soaking in tartaric acid for 63 days

图7 磷酸浸泡14 d的锈粉显微照片Fig.7 Micrograph of rust powder after soaking in phosphoric acid for 14 days
2.2.2 质量变化 锈粉经不同试剂浸泡后质量变化见表5。
盐酸能够溶解锈粉总质量的80.05%。几种弱酸性试剂溶解锈粉的能力均低于盐酸。

图4 柠檬酸浸泡63 d的锈粉显微照片Fig.4 Micrograph of rust powder after soaking in citric acid for 63 days

图6 磷酸浸泡7 d的锈粉显微照片Fig.6 Micrograph of rust powder after soaking in phosphoric acid for 7 days

图8 磷酸浸泡63 d的锈粉显微照片Fig.8 Micrograph of rust powder after soaking in phosphoric acid for 63 days
磷酸在7 d内溶解锈粉的速率高于柠檬酸、酒石酸、Na2EDTA。而在14 d时溶解的质量分数与7 d相比有明显的下降,到28 d质量减少率为负数,即残余的固体质量已经超过了原始固体质量。到63 d固体质量继续上升。
柠檬酸、酒石酸和Na2EDTA对锈粉的溶解速率相差不大,且都比较缓慢。浸泡63 d也只能溶解总质量的30%左右。
除磷酸外,其余试剂对锈粉的溶解速率都是初期较快,随后逐渐变慢。
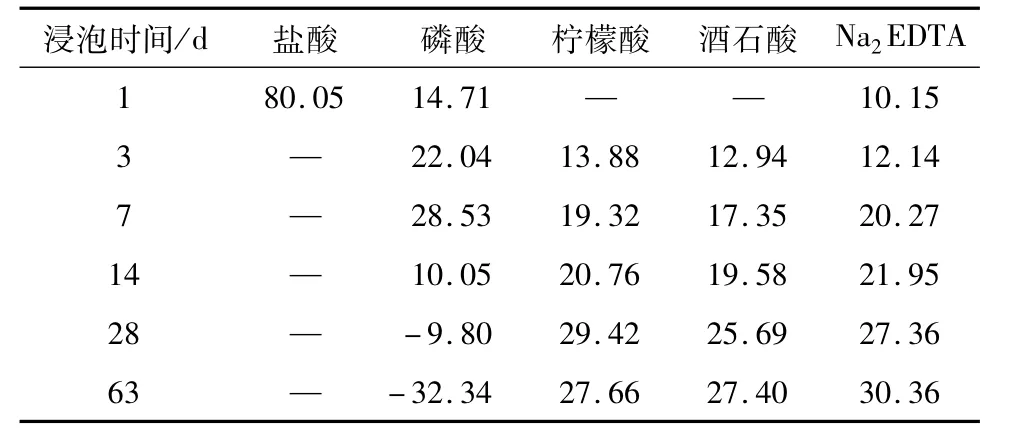
表5 锈粉经试剂浸泡后的质量减少率Table 5 Mass loss rates of rust powder after soaking in the reagents (%)
2.2.3 滤渣成分分析 用EDXRF对原始锈粉、盐酸加热溶解后的锈粉、柠檬酸、酒石酸、Na2EDTA浸泡63 d的锈粉进行分析。结果见表6。

表6 经试剂浸泡后的锈粉EDXRF分析结果Table 6 EDXRF results of rust powder after soaking in the reagents (%)
原始锈粉主要含铁、硅、钙三种元素,其中以铁为主,含量高达86.5%。
锈粉经过盐酸浸泡后,铁含量下降到3.2%。由于锈粉的总质量下降到了19.95%,可以认为锈粉中大部分铁已经溶解。锈粉经柠檬酸、酒石酸、Na2EDTA浸泡后,铁含量稍微降低,由于锈粉总质量是下降的,因此锈粉中的铁溶解了一部分。
锈粉经几种试剂浸泡后,硅含量都有明显上升。说明几种试剂对含硅化合物的溶解能力都比较弱。
原始锈粉中钙含量较少,因此本实验难以准确说明各试剂对含钙化合物的溶解能力。
由于锈粉经磷酸浸泡的质量变化较为特殊(先下降后上升),因此对磷酸浸泡不同时间的锈粉都进行EDXRF分析,结果见表7。
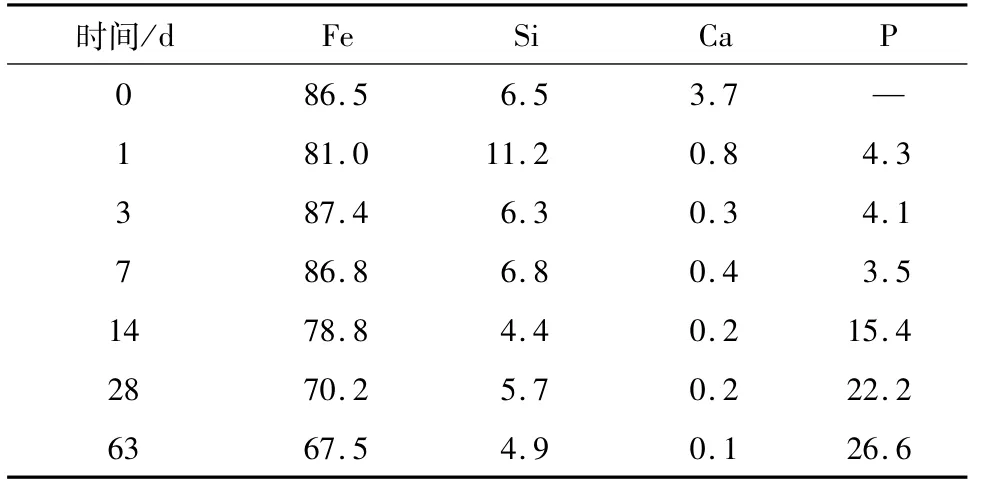
表7 经磷酸浸泡不同时间后的锈粉EDXRF分析结果Table 7 EDXRF results of rust powder after soaking in phosphoric acid for different time (%)
在前7 d内,锈粉中磷含量不高,到14 d时明显上升,28 d、63 d磷含量继续上升。结合锈粉质量变化,推测前7 d内磷酸对锈粉的作用以溶解为主,而之后则生成了不溶于水的磷酸盐,并且这种产物越来越多。
对原始锈粉和磷酸浸泡63 d后的锈粉进行了XRD分析。结果表明,原始锈粉中主要成分为针铁矿(α-FeOOH)和纤铁矿(γ-FeOOH);经磷酸浸泡63 d后,针铁矿和纤铁矿消失,取而代之的是斜红磷铁矿和红磷铁矿(化学式均为FePO4·2H2O)。说明经过长时间的浸泡,原始锈粉中的α-FeOOH和γ-FeOOH与磷酸反应转化成了不溶于水的FePO4·2H2O。
2.2.4 滤液成分分析 使用Na2EDTA络合滴定法测定滤液中的铁含量。锈粉经不同试剂浸泡,溶解铁量占总质量的百分数见表8。
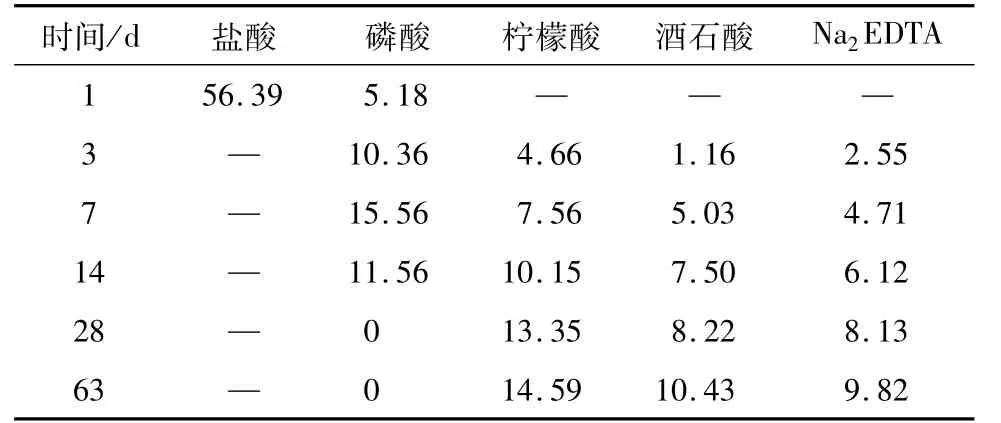
表8 试剂浸泡锈粉后溶解铁量占总质量的百分数Table 8 Ratios of dissolved iron of rust powder after soaking in the reagents to total mass (%)
锈粉经盐酸溶解,溶解铁量占总质量的56.39%。
磷酸在7 d内溶解铁的速率高于柠檬酸、酒石酸、Na2EDTA,而在14 d时溶液中的铁含量下降,到28 d已经难以测出。结合滤渣的分析结果得知此时溶液中的铁转移到了沉淀中。用ICP-AES对磷酸溶解7 d、14 d、63 d的滤液进行分析。结果表明从7 d到63 d,溶液中的铁含量在减少,这与滴定分析的结果一致,溶液中磷含量也减少,与滤渣中的磷含量变化相反,进一步说明了溶液中的铁转移到了沉淀中,生成了不溶性的磷酸铁。
柠檬酸、酒石酸、Na2EDTA溶解铁的速率都比较缓慢,63 d浸泡溶解铁量分别占总质量的14.59%、10.43%、9.82%。
2.2.5 讨论 讨论了二个议题。
1)常用除锈试剂对铁锈粉末溶解速率的比较。综合以上实验结果,可以得出结论:
在磷酸、柠檬酸、酒石酸、Na2EDTA 4种试剂中,常温下磷酸对锈粉溶解速率最快,柠檬酸、酒石酸、Na2EDTA溶解速率较为接近。磷酸与铁锈的作用比较特殊,既有溶解的过程,又有生成不溶性磷酸铁的过程。
铁锈与除锈试剂主要有两方面的作用。
一方面是除锈试剂具有酸性。铁的氧化物与酸反应而溶解:
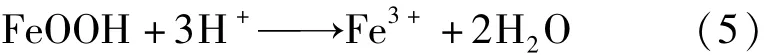
几种试剂溶解锈粉速率的顺序为磷酸>酒石酸、柠檬酸、Na2EDTA,这与试剂酸性强弱顺序基本一致(表3)。
另一方面是除锈试剂具有络合性,与铁离子反应生成络合物:
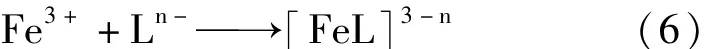
式中,Ln-为络合剂阴离子。
总体而言,上述几种试剂都能与铁离子形成稳定的溶解度高的络合物。除磷酸外,其余几种试剂浸泡锈粉在63 d内没有不溶于水的产物产生。在实际的文物除锈中,可选择用贴敷法进行操作。除锈之后用水反复洗涤即可以将残余的试剂及生成的络合物基本清洗干净。也可用少量弱碱性溶液(如碳酸钠或碳酸氢钠)中和残余的酸性试剂。
2)磷酸与铁锈作用的推测。磷酸与铁离子在较强的酸性条件下会生成无色可溶的络合物H[Fe(HPO4)2]或 H3[Fe(PO4)2],而在碱性条件下则可以形成磷酸铁(FePO4)沉淀。
浸泡在磷酸中,铁锈按(5)式溶解,反应初期溶液酸性较强,生成的是无色可溶的络合物。但溶解过程消耗H+,随着溶解的不断进行溶液pH上升,到一定程度时则会产生FePO4沉淀。
用磷酸进行除锈,如需要更多的溶解铁锈,则磷酸应过量,这样溶解过程中pH上升缓慢,不会有磷酸铁产生。以下实验结果可以证明:
实验方法同1.4.2,但试剂的用量变为250 mL,磷酸浸泡锈粉28 d后锈粉的质量减少率为45.63%,锈粉颜色变化不大,也没有结块现象。说明没有磷酸铁产生。
有时需要促进磷酸铁的产生以形成具有保护、钝化作用的磷化膜,即对铁器进行磷化处理,这时就需要在磷酸中加入碱性物质如氧化锌等,或用磷酸盐代替磷酸,调节溶液pH使磷化膜产生。相关配方已有很多研究[22]。
2.3 铁锈块溶解实验
2.3.1 颜色与形态变化 磷酸、柠檬酸、酒石酸、Na2EDTA浸泡的锈块体积、表面颜色与浸泡前相比均相差不大。
2.3.2 质量变化 锈块经不同试剂浸泡28 d后的质量变化见表9。
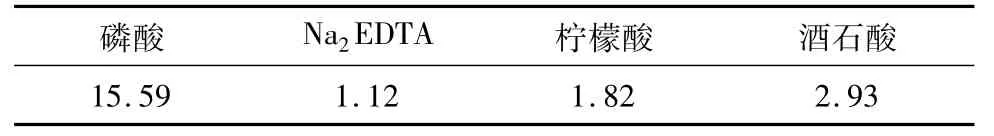
表9 锈块经不同试剂浸泡28 d后的质量减少率Table 9 Mass loss rates of rust fragments after soaking in the reagents for 28 days (%)
这里的锈块减少的质量分为两部分,一部分是溶解的铁锈质量,另一部分是虽然未溶解,但是变得疏松或变为细小的颗粒,从而可以比较容易去除(例如通过超声)的铁锈质量。
2.3.3 讨论 讨论了对锈块的除锈速率和锈块溶解的比较。
1)常用除锈试剂对锈块的除锈速率的比较。由质量变化的结果可知,磷酸对锈块的除锈速率最快。锈块经过28 d浸泡,平均质量减少率为15.59%。
柠檬酸、酒石酸、Na2EDTA对锈块的除锈速率都很低。锈块经过28 d浸泡,平均质量减少率也仅为1%~3%。
总体而言,试剂的酸性越强,除锈速率越高。与铁锈粉末溶解实验的结果一致。
2)铁锈粉末溶解与锈块溶解的比较。表10列出了不同样品经不同试剂浸泡28 d的质量减少率。
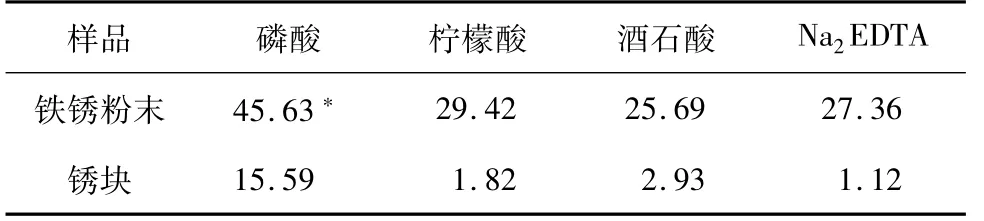
表10 不同样品经试剂浸泡28 d的质量减少率Table 10 Rates of mass reduction of different samples after soaking in the reagents (%)
相同的试剂对锈块的溶解速率要小于对锈粉的溶解速率,且溶解速率越慢的试剂这种差异越明显。这是因为实验所用锈粉为铁器外层质地松软、容易脱落的铁锈;而锈块经过超声清除浮锈,剩余的锈块比较坚硬。两者成分可能不尽相同。且锈粉经过研磨过筛,比表面积很大,与试剂可以充分接触。而锈块比表面积小,难以与试剂充分接触。
2.4 带锈Z30铸铁片浸泡实验
2.4.1 实验现象 带锈Z30铸铁试片在试剂中浸泡,铁片表面均产生大量气体,铁锈逐渐脱落并沉降到容器底部,逐渐有灰黑色的铁基体露出。试片从溶液中取出后接触空气,有返锈现象,灰黑色的铁基体稍变黄。
图9为带锈Z30铸铁试片经不同试剂浸泡后的照片。由浸泡后露出的铁基体面积可以比较不同试剂的除锈效果。除锈效果从强到弱的顺序为磷酸>柠檬酸>酒石酸>Na2EDTA。

图9 试剂浸泡前后的带锈Z30铸铁试片照片Fig.9 Photographs of rusted Z30 cast iron sheets before and after soaking in the reagents
2.4.2 实验结果 带锈Z30铸铁试片在不同试剂中浸泡的失重数据见表11。

表11 带锈Z30铸铁试片在试剂浸泡后的失重Table 11 Mass loss of rusted Z30 cast iron sheets after soaking in the reagents (g)
质量减少的顺序为磷酸>柠檬酸>酒石酸>Na2EDTA。这与观察到的除锈效果顺序一致。
2.4.3 讨论
1)带锈铁片在酸性试剂中的除锈机理。带锈铁片在酸性试剂中浸泡,会发生三种作用[23]:
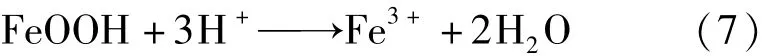
溶解作用:铁锈与酸作用发生化学溶解,反应式为:机械剥离作用:由于铁锈比较疏松,溶液会透过锈层接触铁基体,对铁进行腐蚀:
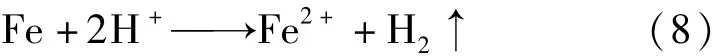
反应生成的氢气具有一定压力,会促使锈层变得松动,并从铁片表面脱落。
还原作用:铁与酸发生反应,首先生成氢原子。氢原子非常活泼,部分转化为氢气逸出,另一部分则与氧化铁反应,将高价铁氧化物还原成易溶于酸溶液的低价铁氧化物:
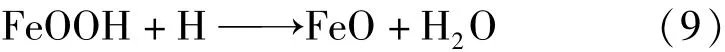
2)铁基体对除锈过程的影响。通过观察以及对比不同样品实验结果发现,试剂腐蚀铁基体的速率远高于溶解铁锈的速率,由此产生的机械剥离作用和还原作用使带锈铁片在酸性试剂中浸泡时,有大量铁锈从试片上脱落,但尚未溶解而沉降到容器底部。在工业清洗中,这一过程对除锈具有促进作用;但在铁器文物保护中,宁可降低除锈效率也应尽量避免基体的腐蚀,因此应添加适当的缓蚀剂以减缓腐蚀,并且避免长时间浸泡。
3 结 论
通过以上实验研究,可以得出以下结论:
1)总体而言,酸性试剂对铁基体的腐蚀都很强烈。几种试剂对Z30铸铁试片的腐蚀速率顺序为磷酸>酒石酸>柠檬酸>Na2EDTA。腐蚀速率顺序与试剂的酸性顺序一致。加入六亚甲基四胺作为缓蚀剂可有效减缓腐蚀。
2)几种试剂对铁氧化物为主的铁锈的除锈速率顺序为:磷酸>柠檬酸、酒石酸、Na2EDTA。除锈速率主要取决于试剂的酸性。试剂对于不含铁基体的锈块溶解效果低于对粉末的溶解效果,其中过量磷酸对锈块仍有较好的溶解效果,而柠檬酸、酒石酸、Na2EDTA对锈块的溶解则极为缓慢。
3)磷酸与铁锈作用比较特殊。在磷酸过量或溶液酸度较高时以溶解作用为主。当磷酸量少或溶液酸度较低时,则会生成磷酸铁固体。
4)几种试剂对带锈Z30铸铁试片的除锈效果为磷酸>柠檬酸>酒石酸>Na2EDTA。除锈过程包括溶解作用、机械剥离作用和还原作用,其中后两者是试剂与铁基体反应而产生的。
5)铁质文物化学除锈操作方法和对试剂的选择。在铁器除锈操作中,应根据除锈目的和锈蚀种类选择合适的试剂。应先对铁器进行尽量详细的分析检测,探查铁器中是否存在铁基体,确定铁锈成分。如果条件允许,可选择待除锈铁器的小块、残块或器物上的一小部分进行实验,以选择合适的试剂种类、试剂浓度、温度及操作方法。
酸性试剂对铁基体都有很强的腐蚀,因此在铁质文物保护中应尽量避免使用酸性试剂除锈。如不得不使用,应避免长时间浸泡,可使用宣纸或棉花帖敷的方式。且应随时观察,及时停止,并应当添加合适的酸洗缓蚀剂来降低试剂对铁基体的腐蚀,以免对文物造成不可逆的破坏。
磷酸既具有除锈,又具有钝化的作用,并且除锈效率较高。用较多的磷酸与铁器作用可以除锈,当除到合适的程度时,可通过调节磷酸溶液pH、添加促进剂等方式使除锈液变为钝化液,完成钝化。
致 谢:本研究中EDXRF测量由中国国家博物馆马燕如、王永生老师完成,ICP-AES测量由北京大学考古文博学院崔剑锋老师完成,XRD测量由北京北达燕园微构分析测试中心完成。中国国家博物馆丁莉老师对本文的修改提出了宝贵的建议,在此一并表示衷心的感谢!
