ICG磁性PLGA纳米粒的制备及其在小鼠体内的脑靶向作用*
2020-08-22杨畅马广龙张俊朗WafaAljamal李勇军
杨畅,马广龙,张俊朗,Wafa Al-jamal,李勇军
(1.贵州医科大学 省部共建药用植物功效与利用国家重点实验室 & 贵州省药物制剂重点实验室, 贵州 贵阳 550004; 2.贝尔法斯特女王大学 药学院, 北爱尔兰 贝尔法斯特 BT9 7BL;3.贵州医科大学 民族药与中药开发应用教育部工程研究中心, 贵州 贵阳 550004)
研究发现,脑肿瘤[1]、脑血管疾病[2]、中枢神经系统感染[3]、精神疾病[4]等脑部疾病对人类的身体健康影响日益增大,因此构建一种新型的脑靶向药物传递系统,使药物浓集于脑部达到增加疗效、降低药物毒副作用的目的,已经成为全球脑部疾病药物研发的热点。吲哚菁绿(indocyanine green,ICG)是被美国食品药品监督管理局(food & drug administration,FDA)批准用于临床的近红外荧光染料[5-7],因其具有优异的光学特性、良好的组织渗透力、低生物体干扰性及低毒性等优点,被广泛作为造影剂应用于荧光成像,但ICG在水中稳定性差、体内消除较快(血液半衰期2~4 min)及细胞摄取率低等缺陷又限制了其在诊疗方面的应用[5-8]。聚乳酸-羟基乙酸共聚物[poly(lactide-co-glycolic acid),PLGA]是由乳酸(lactic acid,LA)和羟基乙酸(glycolic acid, GA)这两种单体按照不同比例缩聚而成,且经美国FDA批准用于组织工程、医用材料、药物载体的生物降解高分子聚合物[9-10]。PLGA具有良好的生物相容性、生物可降解性、合成简单、稳定性高、降解速度可调节以及可塑性良好等特点[9-11],将ICG载入PLGA,可提高ICG的稳定性,调节其在体内的循环和分布,放大ICG的荧光成像效应[7,12]。本研究将ICG和四氧化三铁纳米颗粒共载于PLGA纳米粒中,追踪四氧化三铁纳米颗粒在磁场中的运行轨迹,以观察磁性纳米粒在小鼠体内的脑靶向情况,现将结果报告如下。
1 材料与方法
1.1材料
1.1.1实验动物 NOD/SCID gamma(NSG)小鼠,系非肥胖糖尿病(non obese diabetic, NOD)和重症联合免疫缺陷(severe combined immunodeficient,SCID)基础上敲除白细胞介素2受体γ链(interleukin 2 receptor gamma chain,IL-2Rγ)的小鼠,雄性、4只、体质量20~25 g,英国Envigo公司提供,为清洁级动物。本实验获得英国贝尔法斯特女王大学批准(NO.2841)。
1.1.2试剂 PLGA(瑞士Corbion Purac)、ICG(美国Adooq)、聚(乙二醇)甲醚-嵌段-聚(丙交酯-共-乙交酯)[poly(ethylene glycol) methyl ether-block-poly(lactide-co-glycolide),PEG-PLGA]、聚乙烯醇[poly(vinyl alcohol),PVA]、甲醇(色谱级)、乙腈(色谱级)、二甲基亚砜(dimethyl sulfoxide,DMSO)及12~14 kDa的透析管(英国Sigma-Aldrich)、69%浓硝酸(英国VWR公司)、10 kDa超滤管(爱尔兰Merck Millipore),四氧化三铁纳米颗粒(20 g/L,甲苯)由Wafa J. Al-Jamal实验室提供,实验用水为超纯水。
1.1.3仪器 ENTRIS 224i-1S分析天平(德国赛多利斯)、MERAFUGE 8R冷冻离心机(美国Thermo Scientific)、FLUOstar® Omega 酶标仪(英国BMG Labtech)、Zetasizer Nano ZS90激光粒度分析仪(英国Malvern Panalytical)、55AA原子吸收分光光度计(美国安捷伦)、JEM-1400Plus透射电镜(日本JEOL)、直径8 mm的F645-N52-10磁铁(英国Magnet Expert)以及Bruker In Vivo Xtreme小动物活体荧光成像仪(美国布鲁克)。
1.2方法
1.2.1纳米沉淀法制备ICG磁性PLGA纳米粒 称取PLGA 6 mg和PEG-PLGA 4 mg溶于乙腈3 mL中,超声混合溶解,备用;ICG 1 mg溶于甲醇溶液1.5 mL,与20 g/L四氧化三铁纳米颗粒溶液50 μL混合,加PLGA混合溶液中混合均匀,磁力搅拌下逐滴滴入到5%(W/V)PVA水溶液6 mL中,磁力搅拌4 h,4 ℃、6 000 r/min超滤离心15 min,超纯水重悬洗涤沉淀10次,得浓缩液1.2 mL,4 ℃保存,备用。
1.2.2激光粒度分析仪测定ICG磁性PLGA纳米粒的粒径、聚合物分散性指数(polymer dispersity index,PDI)及Zeta电位 取ICG磁性PLGA纳米粒溶液10 μL与10 mmol/L NaCl溶液990 μL混合,置于样品池中,Zetasizer Nano ZS90激光粒度分析仪上测定其粒径、PDI及Zeta电位分布。
1.2.3透射电镜检测ICG磁性PLGA纳米粒形貌及粒径 取ICG磁性PLGA纳米粒溶液200 μL滴于铜网上,滤纸吸去多余的液体,晾干,置于JEM-1400 Plus透射电镜中观察其形貌和粒径大小。
1.2.4ICG紫外可见吸收光谱测定及标准曲线绘制 取2 g/L ICG标准品溶液5 μL置于96孔板中,与DMSO溶液95 μL混合,2倍稀释,得100.000 0、50.000 0、25.000 0、12.500 0、6.250 0、3.125 0及1.562 5 mg/L一系列浓度的ICG标准品溶液,置于FLUOstar® Omega 酶标仪中检测其紫外可见吸收光谱,并绘制标准曲线。
1.2.5紫外可见吸收光谱法测定ICG的包封率和载药量 取ICG磁性PLGA纳米粒溶液5 μL置于96孔板,加DMSO 95 μL溶液混匀,采用FLUOstar® Omega 酶标仪检测793 nm处吸光度;采用紫外可见吸收光谱法计算ICG的包封率(包封率=纯化后的药物量×100%/纯化前的药物量)和载药量(载药量=纳米粒内包封的药物量×100%/载药纳米粒的总重量)[12-13]。
1.2.6原子吸收分光光度法测定四氧化三铁纳米粒的包封率和载药量 取ICG磁性PLGA纳米粒溶液200 μL于100 ℃金属浴蒸干,加69%浓硝酸200 μL,80 ℃消化4 h,冷却至室温,加超纯水稀释至4 mL,于原子吸收分光光度计上检测四氧化三铁纳米粒的包封率和载药量[12],计算方法同ICG。
1.2.7小动物活体荧光成像 随机取健康且生长状态相似的NSG小鼠2只,1只小鼠头部放置磁铁,1只小鼠头部未放置磁铁;同时经尾静脉注射ICG磁性PLGA纳米粒溶液(ICG为1 μg/g),1 h和24 h后分别于小动物活体成像仪下(激发波长为760 nm、发射波长为830 nm、曝光10 s)拍摄其活体荧光成像照片。另取2只健康且生长状态相似的小鼠,同前述样操作,经尾静脉注射ICG磁性PLGA纳米粒溶液(ICG为1 μg/g)1 h后取出脑部,并分别于取脑前后将整体动物和离体脑部置于小动物活体成像仪下(激发波长为760 nm、发射波长为830 nm、曝光10 s)拍摄其荧光成像照片,并利用系统自带的分子成像软件对离体脑部的近红外荧光强度进行定量分析。
1.3统计学分析
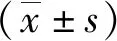
2 结果
2.1ICG磁性PLGA纳米粒的性质表征
激光粒度分析仪检测结果显示,ICG磁性PLGA纳米粒的粒径为(172.77±2.14)nm,PDI为(0.225±0.015),Zeta为(-4.18±0.67)mV(图1);透射电镜观察结果显示,四氧化三铁纳米颗粒表现为黑色小点,均匀分布于PLGA纳米粒中,且ICG磁性PLGA纳米粒呈球形(粒径约为200 nm),与激光粒度分析仪结果一致(图2);紫外可见吸收光谱法检测结果显示,ICG标准品在DMSO溶液中于793 nm有最大吸收,线性范围为1.562 5~50.000 0 mg/L(图3);ICG磁性PLGA纳米粒中ICG包封率和载药量分别为61.8%和0.165%。四氧化三铁纳米颗粒消解后的包封率和载药量分别为40.1%和0.042%。
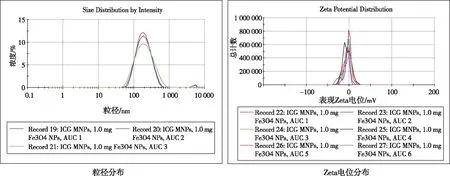
图1 ICG磁性PLGA纳米粒的粒径和Zeta电位分布Fig.1 Size and Zeta potential measurements of ICG magnetic PLGA nanoparticles
15 000× 60 000×图2 ICG磁性PLGA纳米粒的透射电镜结果Fig.2 TEM images of ICG magnetic PLGA nanoparticles

图3 ICG标准品在DMSO中的紫外可见吸收光谱和标准曲线Fig.3 UV-Vis spectra and the standard curves of ICG in DMSO
2.2小动物活体荧光成像
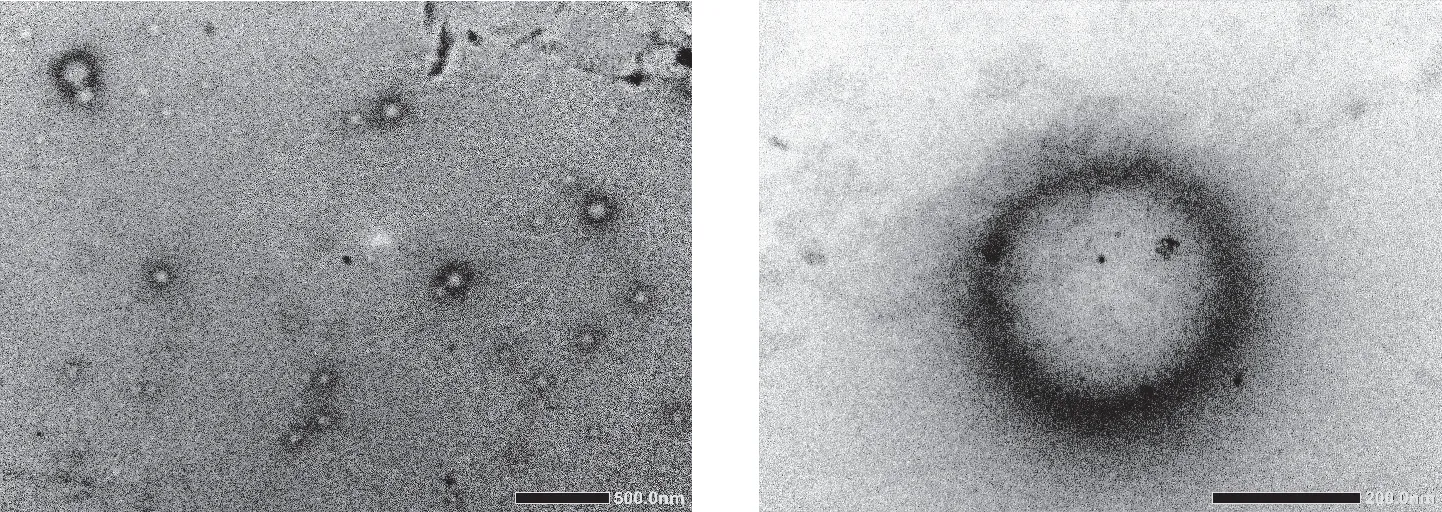
小动物活体荧光成像仪下可见,ICG磁性PLGA纳米粒在磁场作用1 h后向放置磁铁的NSG小鼠头部聚集,未放置磁铁的NSG小鼠体内见ICG磁性PLGA纳米粒主要集中于腹部,ICG磁性PLGA纳米粒在磁场作用24 h后2只小鼠体内均未见明显的荧光(图4);取脑前后,将2只尾静脉注射ICG磁性PLGA纳米粒的NSG小鼠放置于小动物活体荧光成像仪下观察,无论是活体动物还是离体组织均显示放置磁铁1 h后的NSG小鼠头部的荧光强度高于未放置磁铁的NSG小鼠(图5),定量分析结果显示放置磁铁的NSG小鼠头部的累积荧光强度约为未放置磁铁的NSG小鼠的1.2倍(图6)。
图4 NSG小鼠静脉注射ICG磁性PLGA纳米粒后1 h和24 h的活体荧光成像结果Fig.4 In vivo imaging of NSG mice at 1 h and 24 h after intravenous injection ICG magnetic PLGA nanoparticles
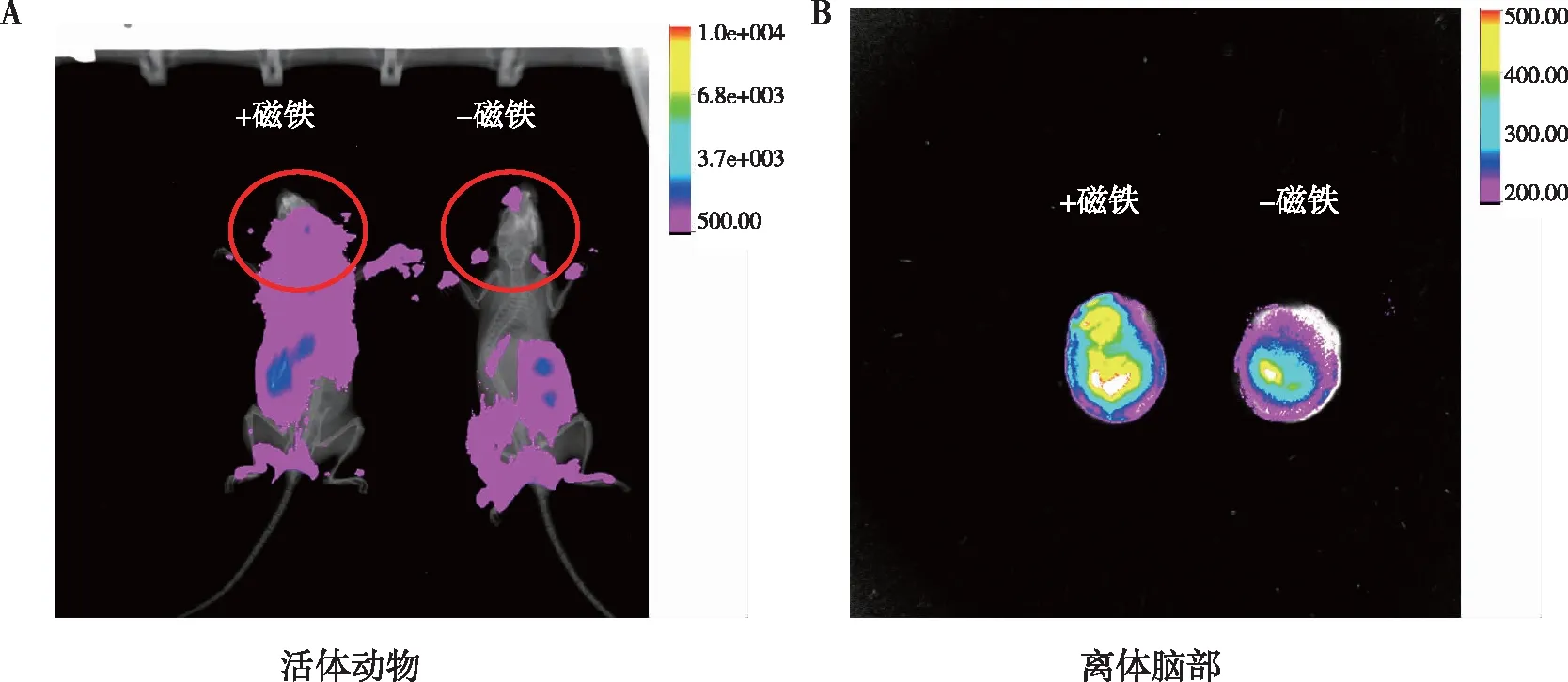
图5 NSG小鼠静脉注射ICG磁性PLGA纳米粒1 h后整体动物和离体脑部的荧光成像结果Fig.5 Fluorescence imaging of the whole animal and isolated brain at 1 h after intravenous injection of ICG magnetic PLGA nanoparticles in NSG mice

图6 NSG小鼠静脉注射ICG磁性PLGA纳米粒1 h后离体脑部内的累积荧光强度Fig.6 Sum fluorescence intensity in isolated brain of NSG mice at 1 h after intravenous injection ICG magnetic PLGA nanoparticles
3 讨论
实验结果显示制备得到的ICG磁性PLGA纳米粒的粒径约为173 nm,PDI约为0.225,Zeta电位约为-4.18 mV,粒径较小,尺寸均一,分散度较好。Zeta电位为负值,其负电荷可能来源于PLGA表面末端离子化的羧基,但由于PVA在聚合物表面形成了稳定的网络结构,屏蔽了聚合物表面电荷,因此其Zeta电位值较低[14]。透射电镜下四氧化三铁纳米颗粒呈黑色小点,均匀分布于PLGA纳米粒中,与原子吸收分光光度法分别从定性和定量两方面表征了磁性PLGA纳米粒,证实PLGA成功将四氧化三铁纳米颗粒载入其中。借鉴Wafa课题组建立的ICG药物传递系统策略[13],结合ICG磁性PLGA纳米粒包封率和载药量的常见测定方法[12],通过DMSO破坏ICG磁性PLGA纳米粒的结构,将ICG游离出来,通过紫外可见吸收光谱法进行测定,其包封率和载药量,较其他文献报道略高[12,15],这可能与选用的PLGA类型有关。在磁场的作用下,经小动物活体成像仪可观察到ICG磁性PLGA纳米粒在1 h内朝NSG小鼠脑部聚集,证实了ICG磁性PLGA纳米粒的确具有一定的脑靶向作用,可用作脑部药物传递系统。但其脑靶向的作用力较弱,仅比无磁场作用的磁性PLGA纳米粒高1.2倍。这可能与磁性纳米粒在药物载体中的装载量较小有关。尽可能的保证在较小的粒径范围内提高载磁量,将有助于磁靶向力的进一步提高,从而将更多的药物运输到脑部。经24 h动物体内代谢后,未见小鼠体内呈现出ICG的荧光,提示ICG磁性PLGA纳米粒可能已经被肝脏代谢或者经肾脏排出体外[16-18],安全性较好。
目前,用于脑靶向的纳米递药载体有脂质体、固体脂质纳米粒、聚合物胶束、树枝状聚合物、碳纳米管、聚合物纳米粒、磁性纳米粒等[19-20]。其中磁性纳米粒由于受到机体内部环境(如复杂的血管网络)、精确磁场的施加方式、磁场强度等问题的影响[21-22],以及可能出现的微血管聚集栓塞现象[23-25],导致磁驱动的脑靶向策略的可行性一直不明确。虽然已有科学家通过各种方法成功制备了磁性PLGA纳米粒[26-29],但其主要用于肿瘤[12,26-28]和类风湿性关节炎[29]的治疗;只有美国圣约翰大学Sadoqi课题组将其用于脑部药物传递系统[15]。通过荧光检测ICG磁性纳米粒在SD大鼠的组织分布情况,发现游离的ICG不能进入脑部,且游离的ICG和ICG磁性纳米粒主要分布于肝、肾、脾和肺部组织。本研究结果显示经包裹后的ICG磁性纳米粒可以进入脑部,且在磁场的作用下进入脑部的ICG较无磁场作用的ICG磁性纳米粒多。因此证实ICG磁性PLGA纳米粒具有一定的脑靶向作用。通过小动物活体成像仪直接观察ICG磁性PLGA纳米粒在活体动物体内的运行情况,可以更直观的证实ICG磁性PLGA纳米粒的脑靶向作用,进一步减少以往组织分布实验对于动物取材时人员操作规范性和检测设备灵敏度的依赖。
综上所述,ICG磁性PLGA纳米粒具有一定的脑靶向作用,可用作脑部药物传递系统。
