玉米须衍生磁性多孔碳的制备及其对海水中孔雀石绿的萃取
2020-08-21陈柏森王希越连丽丽娄大伟
陈柏森,王希越,祝 波,连丽丽,娄大伟
(吉林化工学院 分析化学系,吉林 吉林 132022)
孔雀石绿(MG)作为一种三苯基甲烷染料,在渔业和水产养殖业中被广泛用作抗寄生虫剂和杀菌剂[1]。因其潜在的致畸、致癌性,许多国家禁止在水产养殖业中使用MG。然而,MG廉价易得,且对鱼卵、鱼体的水霉病及其他一些细菌性疾病有特效,在水产养殖业和渔业中仍被屡禁不止。因此,准确测定养殖海水中MG的状况具有重要意义。
实际样品中MG的浓度通常为痕量级,且存在多种干扰物质,因此在进行仪器分析前,有必要对MG进行富集、分离。从不同基质中提取MG的方法有多种,包括液-液萃取(LLE)[2]、固相萃取(SPE)[3]和固相微萃取(SPME)[2]等。近年来,磁性固相萃取技术(MSPE)[4]作为一种新型固相萃取技术受到了越来越多的关注。在MSPE过程中,磁性材料可以均匀地分散在溶液中,通过施加外部磁场可以很容易实现吸附剂的固液分离。因此,相比传统样品前处理方法,MSPE更加高效、环保、方便。其中,MSPE的吸附剂在该方法的萃取过程中起到了至关重要的作用。
由于具有优异的物化性质,碳纳米管[5]、活性碳[6]、石墨烯[7]以及生物碳等碳材料在分析化学领域得到了广泛应用。其中,生物碳是通过在惰性气体中高温加热生物质(如动植物废料)而产生的多孔碳材料,具有化学性质稳定、比表面积大、孔隙率高等特性[8]。将生物碳与Fe3O4、Fe2O3等磁性纳米粒子相结合,得到的复合材料兼具二者的优点,可用于吸附/提取不同基质中的目标组分。例如Huang等[9]以柚子皮为碳前驱体、以Fe2+和Fe3+为铁源,通过一步法制备了磁性吸附剂,并将该材料用于苯甲酸酯类和氟喹诺酮类化合物的萃取、分离。Chu等[10]利用豆渣作为碳前驱体,通过活化和热处理法制备了氮掺杂磁性生物碳,该复合材料对溶液中的Cr(Ⅵ)具有优异的吸附性能。此外,以油棕纤维[11]、椰壳[12]和木质素[13]为低成本碳源制备的磁性生物碳,被成功用于水中有机氯农药、苯酚、磷酸盐的吸附和分离。
玉米是我国北方的特色农作物,而不可食用的玉米须(CSs)通常被当作农业废弃物丢弃、焚烧或掩埋在土壤中。本研究以低廉环保的CSs作为碳前驱体,三氯化铁为铁源,采用溶剂热碳化法制备了表面负载铁氧化物(Fe3O4及Fe2O3)纳米粒子的磁性水热碳材料(MHC),并以氢氧化钾(KOH)作为化学活化剂,通过高温热解法制得活化的生物碳材料(AMC)。将AMC用于水中痕量MG的萃取,并对影响其萃取性能的主要因素(如pH值、萃取时间、吸附剂用量、洗脱液种类及洗脱时间等)进行了优化。结合超高效液相色谱仪(UPLC),建立了水中痕量MG分析的MSPE/UPLC-TUV分析方法。
1 实验部分
1.1 仪器与试剂
配有TUV紫外检测器的超高效液相色谱仪(美国Waters仪器公司);KSY-60-16高温燃烧管式炉(北京市永光明医疗仪器有限公司);KQ-250VDE型超声波清洗器(昆山超声仪器有限公司);XW-80A微型涡旋混合仪(上海沪西分析仪器厂有限公司);EM3200扫描电镜(SEM,日本JEOL);Vertex 80V型傅立叶红外光谱仪、D8 Advanced X-射线衍射仪(德国Bruker);Escalab 250Xi 型X射线光电子能谱(美国Thermo Fisher Scientific)。
孔雀石绿MG(色谱纯,上海阿拉丁试剂有限公司);甲醇、乙腈(色谱纯,美国TEDIA);三氯化铁(FeCl3·6H2O)、氢氧化钾KOH(分析纯,天津大茂化学品有限公司);乙酸铵(分析纯,上海阿拉丁试剂有限公司);Mill-Q超纯水(美国Millipore公司);其它试剂均为分析纯。养殖海水样品取自辽宁营口,于4 ℃冷藏保存,使用前经0.22 μm水系滤膜过滤。实验用水均为超纯水。
1.2 色谱条件
色谱柱:C18柱(4.6 mm×250 mm,5 μm,美国Waters仪器公司);检测波长:618 nm;流动相:乙腈(A)-5 mmol/L的乙酸铵(B)(70>∶30,体积比,下同);流速0.15 mL/min;柱温30 ℃;进样量10 μL。
1.3 磁性固相萃取吸附剂的制备
1.3.1 磁性水热碳(MHC)的制备[14]准确称取磨碎的CSs 1.00 g,FeCl3·6H2O 1.35 g,无水乙酸钠3.60 g和聚乙二醇1.00 g,溶于40 mL乙二醇中,搅拌30 min后将其移入50 mL不锈钢反应釜中密封,置于190 ℃烘箱中反应24 h。冷却后用水和无水乙醇洗涤至澄清,于60 ℃真空条件下干燥后得到MHC。
1.3.2 活化磁性生物碳(AMC)的制备将MHC与固体KOH粉末以1>∶2的质量比混合,置于高温燃烧管式炉中,于700 ℃氮气保护下热解2 h,反应结束后将得到的产物冷却,用大量水洗涤至中性,于60 ℃真空条件下干燥6 h,得到AMC。
1.4 等温吸附曲线
将5.0 mg AMC加入10 mL经甲醇配制的不同质量浓度(10~200 mg/L)的MG溶液中,在25 ℃恒温水浴条件下振荡8 h后,将磁性吸附剂与溶液进行磁性分离,用UPLC-TUV检测上清液中MG的残留浓度。
1.5 磁性固相萃取过程
将5.0 mg AMC分散在100 mL含有5 μg/L MG的溶液中,旋涡振荡20 min,进行磁性分离,弃去上清液。加入3.0 mL酸性甲醇(甲醇∶乙酸=9>∶1,体积比)作为洗脱液,旋涡振荡30 min洗脱目标分析物。将收集的洗脱液通过氮气吹干,用流动相(乙腈-5 mmol/L的乙酸铵,70>∶30)将残渣复溶至1.0 mL,离心10 min后,进行UPLC分析。
2 结果与讨论
2.1 吸附剂的制备与表征
AMC的合成流程如图1A所示:以CSs为碳前驱体,乙二醇为溶剂,采用溶剂热碳化法在190 ℃下合成表面分散铁氧化物的水热碳材料。经过一系列脱水、聚合和芳构化反应,CSs转化为致密的MHC,而生成的铁氧化物(Fe3O4及Fe2O3)纳米颗粒则均匀分布于MHC表面。然后,将制备的MHC浸入KOH粉末中,在氮气保护下700 ℃热解2 h,在此过程中,熔融的KOH与MHC的碳组分发生反应,生成CO、CO2和H2气体,从而在碳材料中产生大量的中孔,进而可用于溶液中痕量MG的高效富集和测定(图1B)。

图1 AMC的合成流程(A)及其对溶液中MG的萃取(B)Fig.1 Synthetic strategy of AMC(A) and its application in the extraction of MG(B)
使用扫描电镜对CSs和AMC的形态特征进行表征。如图2A所示,CSs的表面粗糙,有轻微的裂纹。经过碳化及KOH活化后,AMC形成了丰富的孔结构,氧化铁颗粒均匀地分散在碳基体表面(图2B)。多孔结构的产生为目标分析物提供了丰富的活性位点,而表面的磁性铁颗粒则有助于吸附剂及负载分析物从水溶液中快速分离。

图2D为AMC的XRD谱图,2θ=21.4°和44.5°处的衍射峰归属为石墨烯碳(002)和(101)晶面的特征衍射[16]。此外,在AMC的XRD谱图上可以清楚地观察到Fe3O4(JCPDS:75-0033)和Fe2O3(JCPDS:39-1364)的特征衍射峰,证明AMC中的铁元素以Fe3O4和Fe2O3的形式存在。


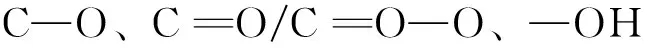
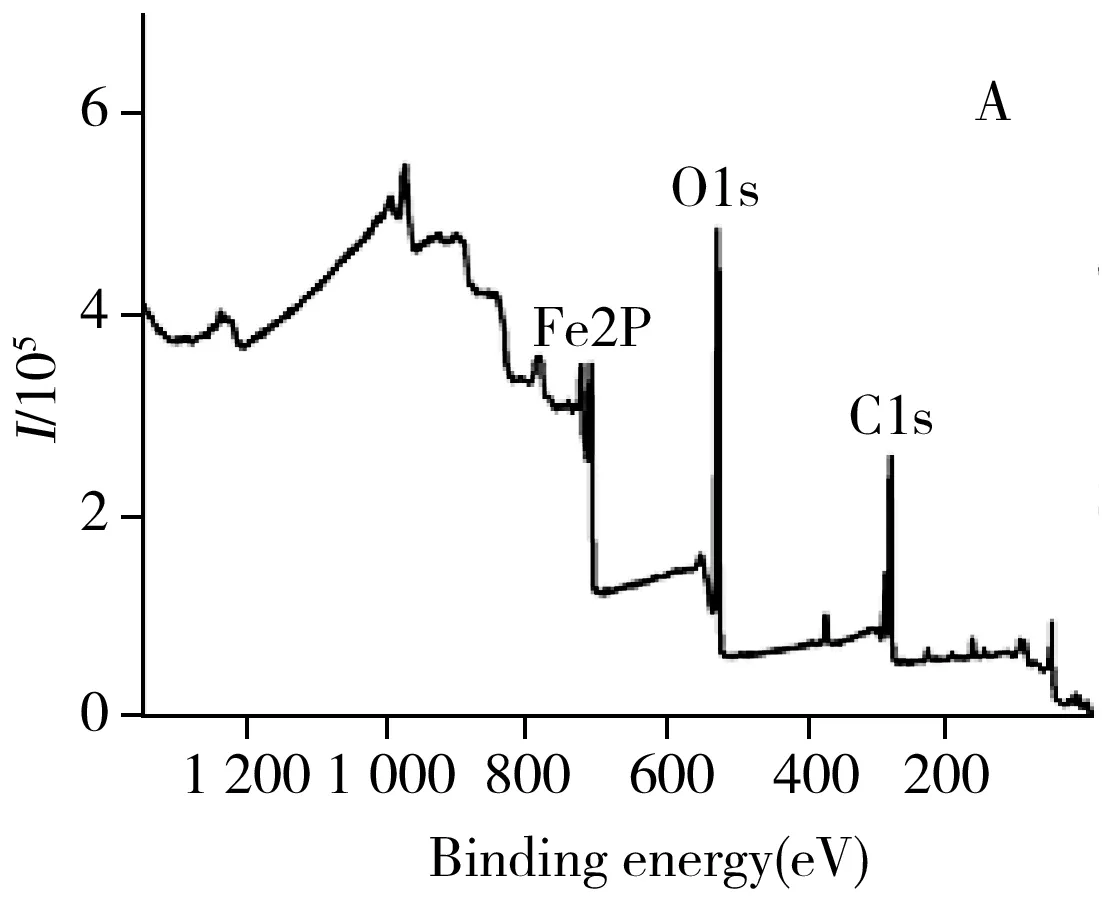
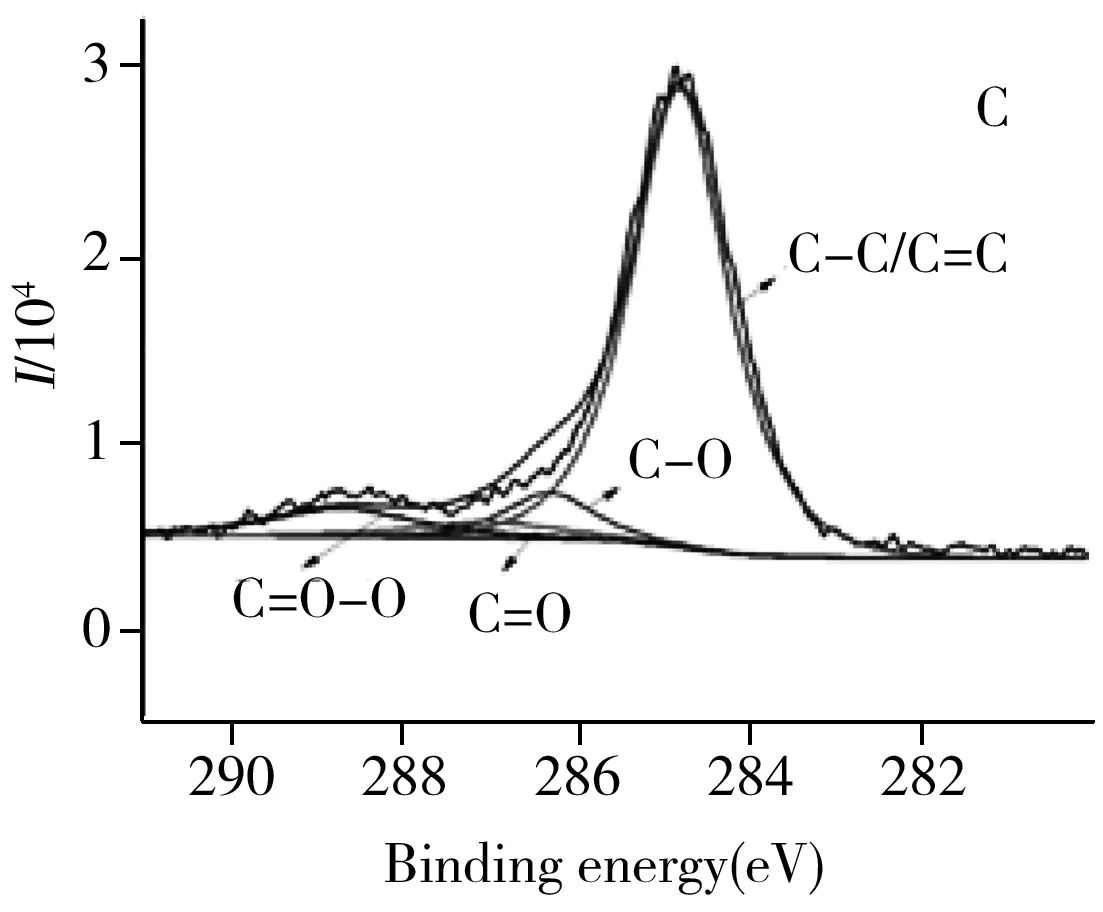
图4 不同MG初始浓度下,AMC和MHC对MG吸附量的变化Fig.4 Curves of adsorption capacity of AMC and MHC changed with different initial concentrations of MG
2.2 AMC和MHC的吸附性能
通过考察25 ℃、不同MG初始浓度下的等温吸附实验,评价AMC和MHC对MG的吸附能力。从图4可以看出,2种碳材料的吸附量(qe)均随着MG初始浓度(c0)的增加而逐渐增加,直至达到最大值。为了更深入了解吸附剂对MG的吸附行为,采用Langmuir等温方程和Freundlich等温方程对吸附数据进行拟合。通过比较两种等温吸附方程的R2值,发现Langmuir等温方程可以与吸附数据更好地拟合,说明MG在2种碳材料表面为均质单层吸附[22]。此外,AMC的最大吸附量为312.5 mg/g,远高于MHC对MG的最大吸附量(56.0 mg/g),说明以KOH为活化剂进行热解处理后,碳材料表面拥有更多的活性位点。此外,AMC对MG的吸附性能也显著高于其他生物质磁性碳材料,包括粉煤灰(89.3 mg/g)[23]、柚皮(209.6 mg/g)[24]、琼脂(142.9 mg/g)[25]、原棉秸秆(77.5 mg/g)[26]、花生壳(77.5 mg/g)[27]等吸附剂。
2.3 固相萃取条件的优化
2.3.1 萃取条件的优化在不同pH值(3.0~9.0)条件下,考察了AMC对MG的萃取性能。如图5A所示,当pH值从3.0增至7.0时,MG的峰面积逐渐增加,并于pH 7.0时获得最大萃取效率。MG是一种三苯甲烷类阳离子染料,分子中含有氨基、羟基及芳香基团,其pKa=6.9。在pH 7.0时,MG在溶液中多以中性分子的形式存在,可通过氢键、n-π和π-π作用被吸附在AMC上。在较低pH条件下,AMC表面的正电荷数量增加,与MG 之间产生静电排斥作用,导致萃取效率的下降;而当pH大于7.0时,溶液中的两性化合物MG发生自聚,导致分析物尺寸增大,进而降低了AMC对MG的萃取效率[28]。因此,选择溶液的最佳pH值为7.0。
吸附剂用量对MG的萃取效率起着重要作用。较大的吸附剂用量可以提供充足的结合位点,但过高的吸附剂用量会造成吸附材料的浪费。本实验将2.0~8.0 mg AMC用于萃取100 mL加标溶液中的MG,以考察吸附剂用量对萃取结果的影响。如图5B所示,目标分析物的峰面积随着吸附剂量的增加而增加,在6.0 mg时达到平衡,因此,实验选择6.0 mg 的AMC作为最佳吸附剂用量。同时,考察了不同吸附时间(10、20、30、40 min)对萃取结果的影响。结果显示,MG的峰面积随吸附时间的增加而增加,当增加至20 min时峰面积达到最大,继续延长吸附时间,峰面积无明显变化。因此,实验选择20 min为最佳萃取时间。
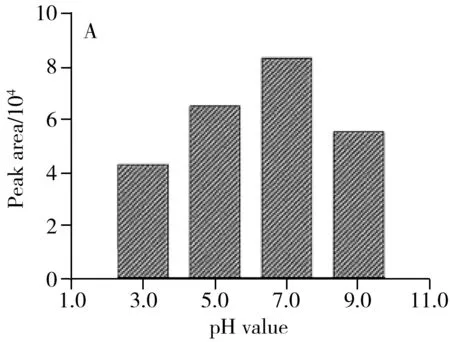
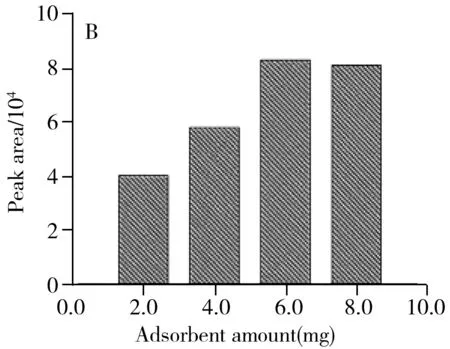

图5 MSPE条件的优化Fig.5 Optimization of MSPE parametersA.solution pH value;B.adsorbent amount;C.eluent type(1.methanol;2.methanol solution;3.alkaline methanol;4.acidic methanol)
2.3.2 洗脱条件的优化考察了甲醇、甲醇水溶液(甲醇>∶ 水=7>∶3)、碱性甲醇(甲醇>∶氨水=9>∶1)和酸性甲醇(甲醇>∶ 乙酸=9>∶1)4种洗脱液对目标分析物的洗脱效果。如图5C所示,采用3.0 mL酸性甲醇作为洗脱液时,可以有效地将MG从AMC表面洗脱。此时,MG以带正电荷的离子形式存在,其亲水性增强,且在酸性溶液中MG与AMC之间可产生较强的静电斥力。因此,实验选择酸性甲醇溶液作为洗脱剂。进一步考察了不同洗脱时间(10、20、30、40 min)对萃取结果的影响。结果显示,随着洗脱时间的增加,分析物的响应值逐渐增大,并于30 min时达到最大,因此实验选择30 min作为最佳洗脱时间。
2.4 方法的评价
在100 mL水中添加不同浓度的MG标准溶液,在优化的MSPE条件下经AMC萃取后进行UPLC分析,根据MG的峰面积和实际样品质量浓度进行线性回归。结果表明,在0.05~5 μg/L范围内,峰面积与MG质量浓度具有良好的线性关系(r=0.999 6),方法对MG的检出限(LOD,S/N=3)、定量下限(LOQ,S/N=10)分别为0.01 μg/L 和0.03 μg/L。在100 mL水中添加低、中、高3个质量浓度水平的MG标准溶液配制成0.25、1、5 μg/L 的样品溶液进行加标回收实验(n=3),测得加标回收率为94.5%~99.7%,相对标准偏差(RSD)不大于2.3%,说明该方法的准确度和精密度良好。
与其他测定MG的方法相比(见表1),该方法具有更低的LOD和更少的吸附剂消耗。同时,利用磁性吸附剂萃取样品中的目标分析物,不仅省去了繁琐的过滤和离心过程,缩短了样品前处理时间,而且减少了有机溶剂的消耗。此外,AMC还具有制备工艺简单、绿色、成本低等优点。
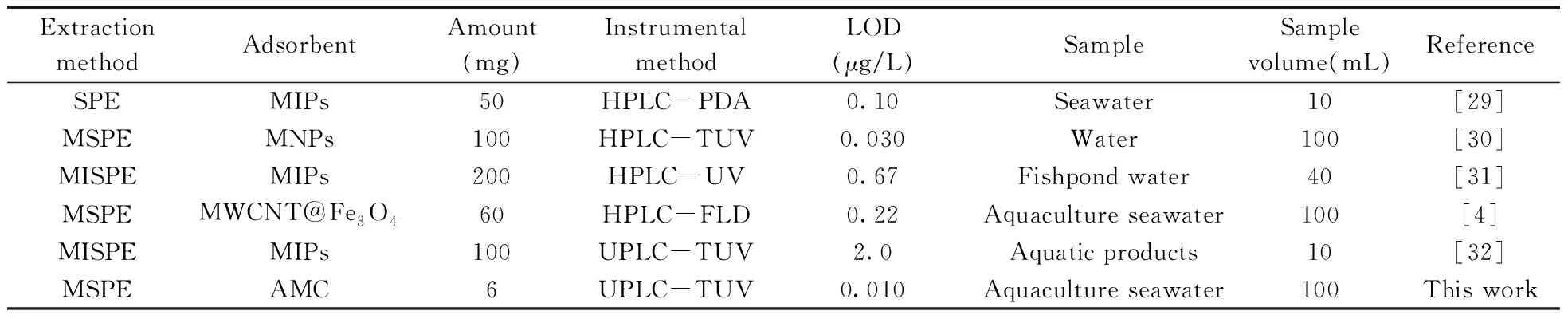
表1 与其他用于测定MG的方法比较Table 1 Comparison of the established method with other methods for the determination of MG
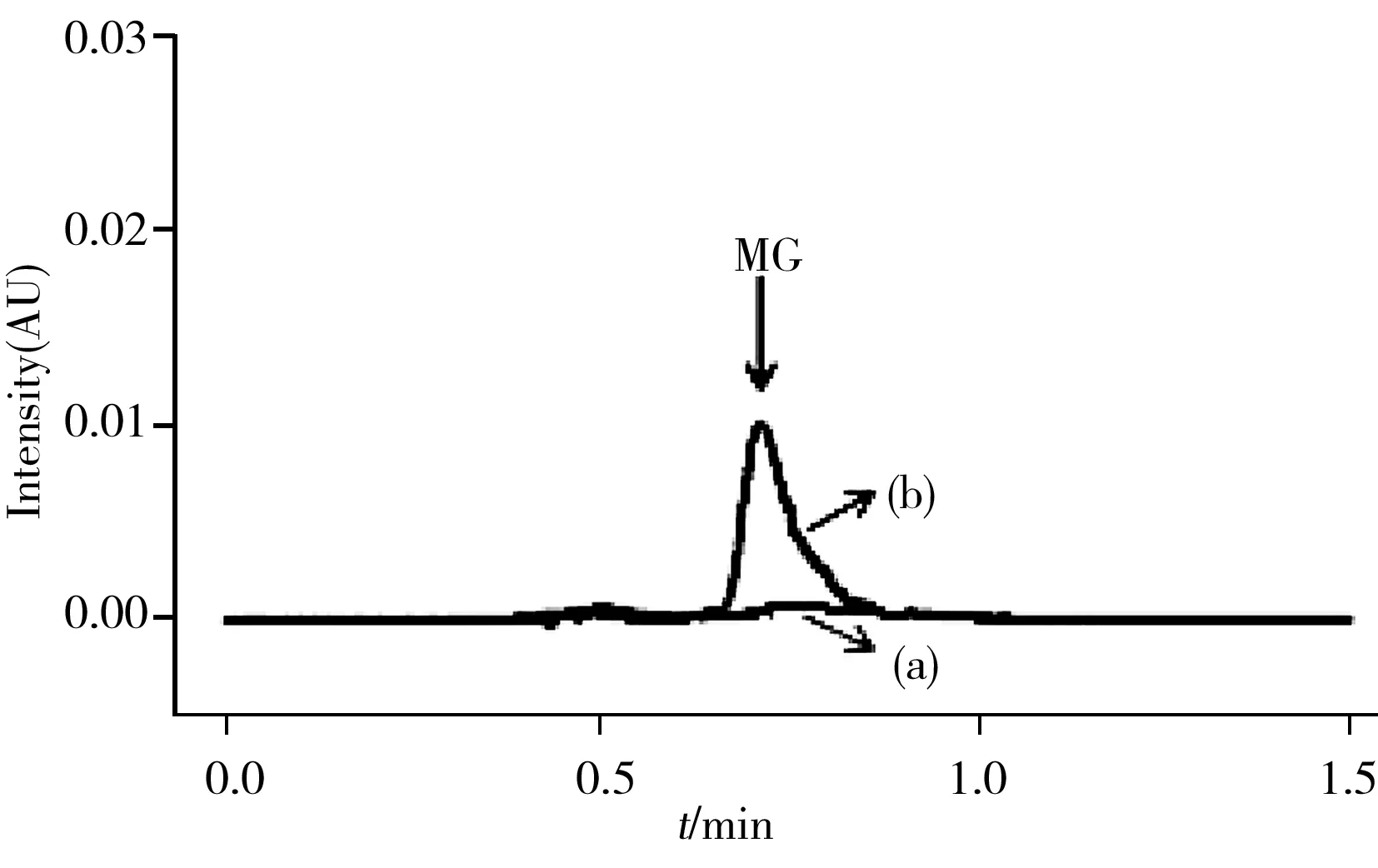
图6 加标养殖海水经本方法处理前(a)、后(b)的色谱图Fig.6 Chromatograms of the spiked aquaculture seawater before(a) and after(b) pretreated with the developed method
2.5 实际样品的测定
为了考察方法的实用性,从辽宁营口采集养殖海水样品,使用AMC作为MSPE吸附剂萃取样品中的MG,并通过UPLC-TUV对结果进行分析。结果显示,海水样本中未检出MG,对该样本在3个加标质量浓度下(0.25、1、5 μg/L)进行回收实验,得到加标回收率为104%~106%,RSD为1.7%~3.4%。图6为加标浓度为5 μg/L的养殖海水经本方法处理前后获得的色谱图,经过MSPE处理后,目标分析物的峰面积能满足定量分析要求,且无干扰峰存在。结果表明所建立的方法适用于养殖海水中微量MG的灵敏检测。
3 结 论
本文以可再生的生物质玉米须为碳源,KOH为活化剂,通过溶剂热碳化法和高温热解反应合成了一种生物质衍生磁性多孔碳材料AMC。铁氧化物(Fe3O4和Fe2O3)的成功负载,使得AMC具有优异的磁性,从而可通过磁性分离快速地从样品溶液中分离。AMC的多孔结构及丰富的活性位点使其对MG具有优异的吸附性能,其最大吸附量可达312.5 mg/g,远高于未经碳化活化的水热碳材料。本文还系统地研究了AMC对溶液中MG的MSPE条件,建立了基于AMC吸附、适用于大体积海水中痕量MG分析的MSPE/UPLC-TUV分析方法。该方法具有良好的线性关系,其LOQ和LOD分别为0.03 μg/L 和0.01 μg/L。该方法的不足在于AMC对分析物的选择性有限,碳材料可能对复杂基质(如食品、生物样品)中其他结构类似的干扰物也具有一定的吸附能力,因此,在实际应用中需注意分析样品的选择。
