创伤性脾出血介入治疗专家共识
2020-08-20中国医师协会介入医师分会急诊介入专业委员会
中国医师协会介入医师分会急诊介入专业委员会
中国研究型医院学会出血专业委员会
脾脏特殊的解剖位置和生理结构,使其成为腹腔脏器中最易损伤者之一。由于脾脏组织含有丰富的血窦,当脾损伤发生时容易因大量出血导致失血性休克,因此对脾损伤患者及时诊治,有助于提高生存率。外科手术是脾损伤传统治疗方式,但由于脾脏在人体免疫机制中起着重要作用,脾脏切除后可能发生凶险性感染严重并发症[1]。寻找既能有效止血,又能保存脾脏正常免疫功能的治疗方法,是脾损伤临床治疗研究的重点。自1981年美国学者Sclafani首次报道脾动脉栓塞术治疗创伤性脾出血以来,脾动脉栓塞术在脾损伤治疗中的应用越来越广泛,治疗有效性和安全性也得到临床认可[2-3]。近年文献报道脾动脉栓塞术后保脾成功率可高达97%[4]。相比于外科保脾手术,介入治疗具有微创、无需全身麻醉、手术时间短、恢复快等优势。随着介入医学发展,越来越多医院将脾动脉栓塞术应用于创伤性脾损伤治疗中,但对于创伤性脾出血的介入治疗,不同医院、不同医师在适应证和操作技术等诸方面存在较大差异,国内外尚缺乏相应的专家共识。为此,中国医师协会介入医师分会急诊介入专业委员会、中国研究型医院学会出血专业委员会组织国内相关领域专家,基于循证医学原则,通过深入研讨和论证,现制定关于创伤性脾出血介入治疗专家共识,旨在为创伤性脾出血介入治疗提供借鉴。
1 诊断
1.1 临床表现[5]
创伤性脾损伤临床表现,以腹腔内出血和血液对腹膜刺激为主要特征,并常与出血量和出血速度密切相关。出血量大而速度快的患者很快出现低血容量休克,伤情十分危急;出血量少而慢的患者症状轻微,除左上腹轻度疼痛外无其他明显症状,不易诊断,随着时间推移,出血量越来越多才出现休克前期表现,继而发生休克,也可出现迟发性大出血,即包膜下血肿突然破裂大出血。血液对腹膜的刺激而有腹痛,初起在左上腹最为明显,伴有压痛、反跳痛和腹肌紧张。临床上所见的脾损伤破裂,约85%为真性破裂,破裂部位较多见于脾上极及膈面,有时在裂口对应部位有肋骨骨折。破裂如发生在脏面,尤其邻近脾门者,有脾蒂撕裂可能,则出血量很大,可迅速发生休克,抢救不及时可致死亡。当伴发有其他腹腔实质脏器出血、空腔脏器破裂时,上述出血、腹膜刺激症状和休克表现会相应加重,或更早出现。
1.2 影像学检查
协助临床评估创伤性脾损伤的影像学检查,对于准确评估脾损伤程度和做出治疗决策具有十分重要的临床意义。选择影像学检查时应遵循“快速、全面、精准”的基本原则,并基于患者血流动力学状态,CT增强检查是评价金标准[6]。对于存在血流动力学不稳定患者,应尽量限制实施诊断性影像学检查。
1.2.1 CT检查 对于怀疑脾损伤或破裂患者,如果血流动力学稳定或对容量复苏有反应,应考虑立即行全腹部CT平扫和多期增强扫描[7]。增强扫描采用高压注射器经肘静脉注射碘对比剂(300~350 mg/mL)90~120 mL,速率3~5 mL/s,扫描延迟时间分别为动脉期 25~35 s,门静脉期 60~70 s,延迟期 3~5 min。采用后处理工作站行轴位(层厚3~5 mm)、冠状位(层厚3~5 mm)和矢状位(层厚3~5 mm)重建。对于怀疑活动性出血或血管损伤患者,建议分别行动脉期和门静脉期血管重建。CT评价内容应包括脾实质损伤和脾血管损伤[8]。除脾脏外,腹腔其他实质性和空腔脏器也应同时评价。
CT 分级:Marmery 等[7]于 2007 年 基 于 美 国 创伤外科协会(American Association for Surgery for Trauma,AAST)脾损伤分级量表(1994 年),提出创伤性脾损伤CT分级系统。这一CT分级系统后来得以广泛应用[9-11],被证明优于AAST脾损伤分级量表,部分以前分级较低的脾损伤已升级为Ⅳa或Ⅳb级,从而降低了选择非手术治疗的风险,更利于临床作出治疗决策。2018年AAST更新了腹部实质性脏器损伤分级量表,其中创伤性脾损伤CT分级[12]见表1。影像学评估结果必须与临床、实验室及血流动力学指标相结合,以确保临床选择最佳治疗方式。

表1 创伤性脾损伤CT分级
CT复查与随访:对于中度或以上损伤患者,依据病情变化可考虑重复CT扫描检查[6]。延迟并发症是指脾损伤后至少48 h发生的并发症,包括假性囊肿、脾脏脓肿、假性动脉瘤、迟发性破裂、再出血等。当患者出现相应症状时,通过CT随访能够作出准确诊断。
1.2.2 彩色超声检查 二维及彩色多普勒超声,能及时明确地诊断脾损伤并判断损伤程度,且可通过观察腹腔积液有无增加及增加快慢,间接诊断有无活动性出血及活动性出血快慢[13]。
检查技术:一般采用凸阵探头,频率3.5~5 MHz,置于左侧腋前线至腋后线间第7~11肋骨间隙,在左季肋区及左腹部多方位扇扫,观察脾脏包膜完整性,脾脏有无肿大,脾实质内回声是否均匀,脾包膜下及周围有无积液或弱回声、低回声、混合回声等改变;同时注意观察腹腔有无积液、积液深度及液体透声情况。彩色多普勒超声观察脾包膜下或实质内异常回声区域有无血流信号[14-15]。
脾损伤彩色超声表现及判定依据:①脾包膜下破裂:程度较轻者,脾脏无明显肿大,形态尚规则,包膜完整,脾实质内有欠清晰的斑片样低回声区,强弱不等,边界不清;程度较重者,脾脏体积肿大变形,外形失常,包膜尚完整,包膜下可见梭形或不规则形无回声或低回声肿块,肿块可造成脾脏受压而呈现出包膜表面凹凸不平;脾实质内还可见多个大小不等的无回声区,形状多为月牙环抱实质,内部可有散在分布的细小弱光点漂浮,无回声区不因呼吸运动及改变体位而变化。彩色多普勒显示脾周围及内部可见星点状血流信号。当血肿内有凝血块形成时,可见回声增强,伴机化时回声进一步增强[16-17]。②脾实质内血肿(中央型破裂):脾脏体积增大,包膜尚完整,脾实质内见散在无回声、低回声或混合性回声区,边界不清,内回声不均匀。不伴发其他脏器损伤情况下,腹腔通常无明显游离液暗区。彩色多普勒可见异常回声区内部少量星点状血流信号或无信号[18]。③脾实质破裂(真性脾破裂):脾脏外形失常,包膜不规则或连续性中断,脾实质内可见不规则的中等回声及低回声或无回声区,合并凝血块、机化时可伴片状不规则的混合回声或稍强回声;脾周围腹腔内可见液性暗区包绕脾脏,腹腔亦可见游离液暗区。彩色多普勒在脾损伤区未能显示彩色血流信号[19]。
脾损伤超声诊断新技术:对比增强超声(contrastenhanced ultrasound,CEUS)又称超声造影(ultrasonic contrast),可显著提高常规超声对脾损伤定位及范围的诊断准确率[20],并早期及时发现小范围损伤,从而较大程度上避免迟发性破裂[21]。脾损伤超声造影表现:①包膜下血肿、实质内血肿均表现为负性显影,无对比剂进入;②裂伤表现为造影过程中脾实质内可见不规则线性或条索状无回声区,无对比剂进入;③挫裂伤表现为造影过程中脾实质内可见回声强弱不等回声区及不规则无回声区;④活动性出血表现为对比剂微泡在裂口聚集或呈溢出脏器外[22]。超声造影还可直接、准确、快速地诊断有无活动性出血及活动性出血快慢:对比剂微泡不在损伤区域聚集或溢出脏器外,表示无活动性出血;对比剂微泡在损伤区快速大片聚集或呈喷泉状溢出脏器外,表示活动性出血且速度较快[23]。
1.3 实验室检查
创伤性脾出血患者在完成常规实验室检查后,需动态监测血常规,包括血红蛋白、血细胞压积等指标改变,以判断出血情况是否得到控制[24]。创伤性脾出血患者由于存在血液稀释和凝血因子消耗性下降,故应监测凝血功能,防止凝血障碍,必要时及时输注红细胞、血小板及凝血因子[25-26]。
2 治疗
2.1 急诊处理
创伤性脾损伤急诊处理原则是 “抢救生命第一,保脾第二”。尤其是对于腹部创伤合并休克患者,急诊处理首先应遵循高级创伤生命支持(advanced trauma life support,ATLS)策略和技术[27]。对于严重休克患者,应建立2个甚至3~4个输液通道进行快速输血补液。对于非控制性出血性休克患者(有活动性出血),在急诊室应迅速抽血做好术前准备,早期建议采取允许性低压复苏策略,复苏目标血压控制在收缩压80~90 mmHg(1 mmHg=0.133 kPa,平均动脉压在 50~60 mmHg)为宜,但低压复苏时间不宜超过120 min,若允许性低压复苏时间长,可短时间予低温(局部)辅助措施,以降低机体代谢,保护重要脏器功能[28-29];为维持更好的血流动力学参数,可小剂量应用缩血管药物如去甲肾上腺素[30],以延长黄金救治时间窗,为确定性治疗赢得时间[31-32];在出血已控制、心肺功能可耐受情况下,进行确定性复苏,以恢复机体有效循环血容量,稳定血流动力学。应快速检查、迅速判定是否还存在活动性出血和休克加重,必要时边抢救边送手术室或介入复合手术室治疗[31-32]。
为避免严重并发症发生和降低病死率,应基于致伤机制、伤后临床表现和辅助检查等进行动态评估。体检仍是腹部创伤评估的基础,对于主观性较强的腹膜刺激征,需要遵循“多次、多人检查”原则,以提高其客观性[27]。急诊常规处理包括生命体征、血氧饱和度和心电图监测,安置鼻胃管和导尿管后引流液观察,以及创伤超声重点评估(focused assessment with sonography for trauma,FAST)、诊断性腹腔穿刺术等。FAST是检查和监测腹腔脏器是否受损和腹腔出血最有效方法,操作简便快速,可由经超声专项培训的急诊等临床医师在床旁进行,建议对创伤患者有条件可选择地应用[33]。
2.2 保守治疗
脾损伤大多为实质的撕裂,且大多与脾轴呈垂直的段间破裂,脾门大血管损伤较少见,即大多不与段间血管相连,因此短时间内即可自行止血。上述特点为脾损伤行保守治疗可能性提供了理论依据,临床上大量非手术治疗脾损伤的成功,也证实了这一点。因此,如条件允许,应尽量保留脾或脾组织。
严格把握适应证是脾损伤保守治疗成功的关键。然而保守治疗适应证目前尚无统一标准。本共识认为应遵循个体化治疗原则[34],具体适应证如下:①患者血流动力学平稳,无失血性休克表现,或经较少容量复苏,血流动力学可维持平稳;②腹部CT扫描提示为脾损伤AAST分级Ⅰ、Ⅱ级和部分Ⅲ级;③排除其他腹腔内脏器损伤,尤其是空腔脏器破裂穿孔或合并其他腹腔内脏器损伤,但无需急诊手术;④与脾损伤相关的输血量小于2 U;⑤有连续监测并及时中转手术的医疗条件。对于年龄大于55岁和凝血功能障碍、严重感染和重要脏器衰竭患者,原则上不主张保守治疗。
对于符合上述适应证的创伤性脾损伤患者,均可采取保守治疗。但在保守治疗过程中,应密切监测患者血流动力学等各方面指标变化,监测力度甚至应大于手术患者。保守治疗方法及疗效评价具体如下:①绝对卧床休息1周以上;②严密监测生命体征;③早期禁食,必要时胃肠减压,广谱抗生素预防感染等对症支持治疗;④避免增加腹压动作;⑤保守治疗期间监测腹部情况,动态复查血常规、床旁超声及腹部CT;⑥病情平稳1周左右可进流质饮食,如经进一步治疗病情好转,2周后可根据损伤情况适当下床活动,3个月内避免剧烈活动。保守治疗后患者血流动力学、实验室和影像学检查稳定,则提示保守治疗成功可能性大。
在创伤性脾损伤保守治疗过程中,若及时发现以下情况之一,应送急诊介入或中转手术[35]:①腹痛及局部腹膜刺激征持续加重;②24 h内输血量>4 U而血流动力学仍不稳定;③血细胞比容持续下降而通过输血仍不能得到迅速纠正;④通过观察不能排除腹内其他脏器损伤。保守治疗失败多发生在96 h内,但出现在6~20 d亦非罕见,失败原因可为延迟出血、继发感染等。
2.3 介入治疗
创伤性脾出血介入治疗包括脾动脉栓塞术和影像导引下非血管介入治疗,主要方式为脾动脉栓塞术。创伤性脾出血介入治疗流程见图1。
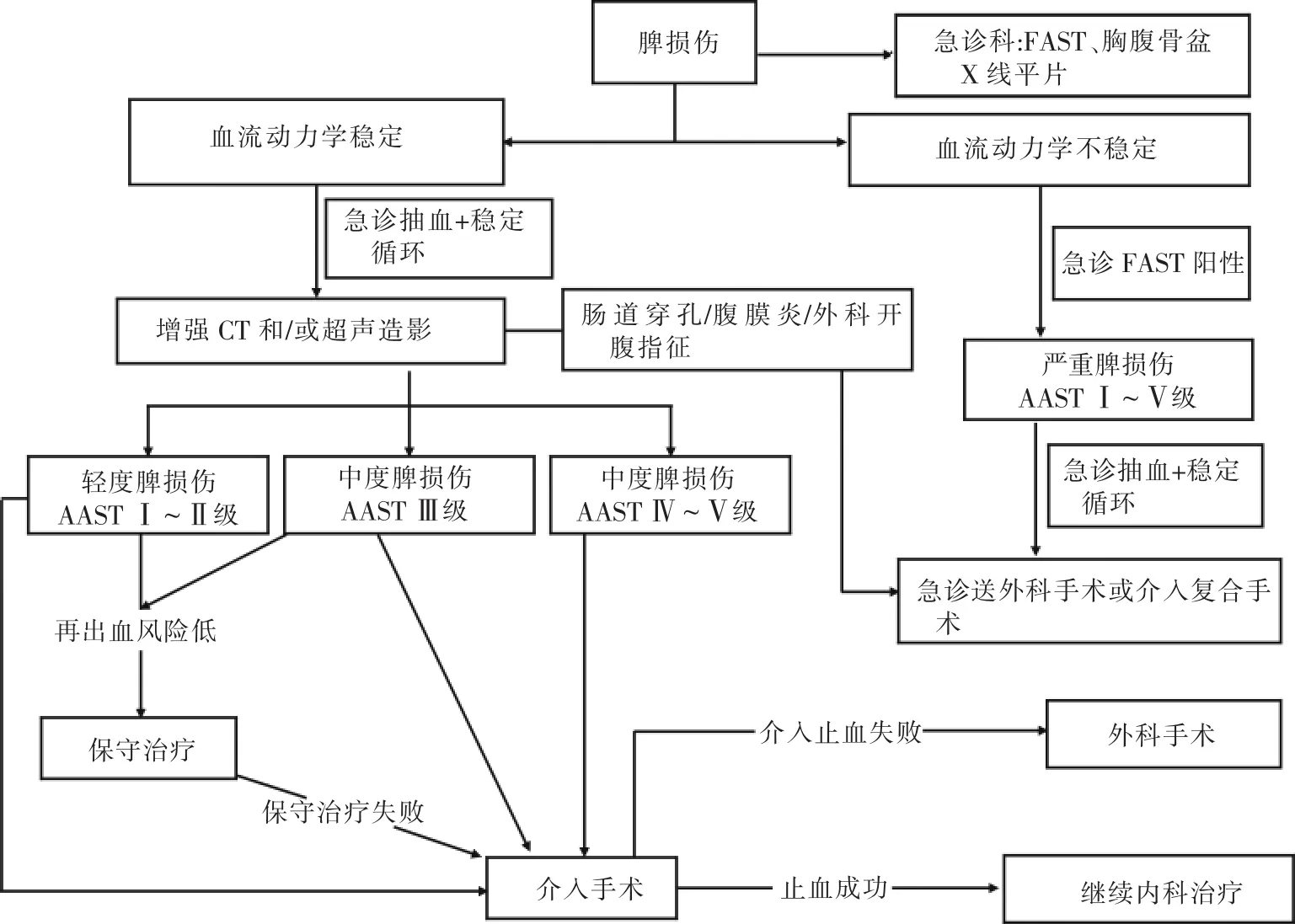
图1 创伤性脾出血介入治疗流程图
2.3.1 适应证 ①血流动力学稳定的低级别(AAST-Ⅰ、Ⅱ)脾损伤[15,36-41]伴有脾脏活动性出血或经保守治疗失败[6,41-42];②血流动力学稳定的高级别(AAST-Ⅲ、Ⅳ、Ⅴ)脾损伤[6,36,40-41,43-48];③血流动力学不稳定的Ⅳ级[47]和部分Ⅴ级脾损伤[48],或根据外科干预风险高低、介入技术应用熟练程度、设备是否便利及诊疗团队协作情况,对血流动力不稳定的脾损伤采用介入栓塞或外科手术[45];④脾损伤合并腹腔积血(真性脾破裂)[41,44,46];⑤影像学检查诊断有对比剂外溢、浓聚,假性动脉瘤,脾动静脉瘘[41,44,46];⑥对无外科治疗条件或无手术指征的脾损伤,即使血流动力学不稳定,也可在积极抗休克治疗同时实施介入栓塞治疗[45]。
2.3.2 禁忌证 无绝对禁忌证[49]。 相对禁忌证:①对比剂过敏[50];②严重感染或顽固性感染[49];③严重心肺功能不全和肝肾功能损害等血管内介入治疗常规禁忌证[50];④CT或其他影像学检查诊断为脾碎裂、脾门血管断裂(Ⅴ级脾损伤);⑤容量复苏无反应的脾损伤[41,50]或伤后短期即出现失血性休克、生命垂危[37,49];⑥存在原发疾病的脾损伤[45,50];⑦战地伤性脾损伤[45];⑧合并空腔脏器损伤、胃肠道穿孔[37]等,或开放性损伤[50];⑨合并其他部位严重创伤,如胸部创伤、颅脑损伤等[49-50];⑩合并其他实质性脏器损伤,如肝、肾破裂[47],预计动脉栓塞治疗可能一并处理者不应作为禁忌证。
2.3.3 术前检查和治疗准备 ①常规准备:严密监测并记录患者血压、心率、呼吸、体温、脉搏等基本生命体征,尽量维持血流动力学平稳。开通静脉通道,抗生素皮试、备血、备皮、更衣、放置胃管、留置导尿管、禁食、心电监测、吸氧。②实验室检查:完善实验室检查,如肝肾功能、血常规、凝血功能等,明确患者是否具有手术适应证,并及时纠正可能导致严重手术并发症的异常指标。③影像学检查:诊断创伤性脾损伤的金标准是增强CT检查[12],能明确创伤性脾损伤的程度、位置,有无活动性出血,是否存在其他脏器损伤等征象。根据CT检查计算AAST分级,对脾损伤是否进行栓塞治疗及选用何种栓塞方式(近端栓塞、远端栓塞、近端+远端栓塞)具有指导意义。超声检查可用于观察脾脏血管的血流信息情况。④肠道准备:对于非急诊手术,术前1~3 d予以泻药行肠道清洗,减少肠道菌群存在,可有效减少术后感染概率。⑤预防性抗生素应用:脾脏为人体最大的免疫脏器,栓塞后容易导致顽固性感染。由于主要感染细菌为荚膜细菌,如肺炎球菌、淋病奈瑟菌和流感嗜血杆菌,或者革兰阴性菌,如大肠埃希菌和假单胞菌[51],术前可预防性应用苯氧甲基青霉素、阿莫西林和红霉素。⑥知情同意:充分告知患者及家属手术必要性、手术方式、手术存在的风险、术后可能的并发症等情况,并要求患者本人或直系亲属或委托授权人签署知情同意书。⑦器材准备:DSA机、高压注射器、脾动脉造影导管、导丝、穿刺针、对比剂,聚乙烯醇(PVA)、明胶海绵或弹簧圈等栓塞材料;若需要近端栓塞时,还须准备球囊导管或血管塞等。
2.3.4 手术麻醉方式 创伤性脾损伤介入栓塞系微创手术,刺激小,成人可局部麻醉下进行。从舒适化角度出发可予镇痛镇静药物[52]。局部麻醉+镇静禁忌证[53]:①拒绝镇静/全身麻醉患者;②美国麻醉医师协会(ASA)健康状况分级为Ⅴ级患者;③血流动力学不稳定或伴随未控制症状的呼吸系统疾病患者;④有镇静药物过敏史及其他严重麻醉风险者。小儿及血流动力学不稳定/呼吸窘迫患者可予喉罩或气管插管全身麻醉。
2.3.5 术中穿刺与造影 经右侧或左侧股动脉穿刺,置入动脉鞘,将造影导管选择性插送至脾动脉中、远端,行DSA造影检查。在能看清出血病变的前提下,推荐应用低流率、低剂量和低压力注射对比剂,以免造成新鲜血痂脱落,诱发或加重术中出血[54-56]。若低流率、低剂量对比剂造影无法明确出血病变,可适当增加剂量,推荐注射速率3~5 mL/s,总量15~25 mL。创伤性脾损伤主要DSA征象包括[54,56]:①血管走向改变。 脾动脉分支受压移位或呈包绕征、末梢血管分离、脾实质内可见无血管区(充盈缺损)。②脾实质挫伤。呈局部不规则小片状或在实质期弥散的斑点影、团块状浓染阴影,有时仅见小血管呈边缘毛糙不清状,并持续至静脉期。③血肿。有中心型和包膜下型,动脉期显示血管移位,静脉期显示不同形态透亮区,周围有晕影,包膜下型末梢血管伸展不到脾脏外周。④血液喷射征。对比剂自损伤、破裂的血管喷涌而出,多见于出血量大、病情凶险患者。⑤创伤性假性动脉瘤。在脾动脉分支旁见圆形或类圆形囊凸影,边缘光滑,瘤内如有血栓形成则显示瘤体外形不完整。⑥动脉分支中断。脾动脉分支中断,血管远端可有或无对比剂外溢。⑦动-静脉瘘。脾静脉在动脉期提前显影,脾动脉分支因“盗血”作用而显影不充分或不显影。⑧脏器破裂。脾损伤常伴有其他脏器,如肝、肾、胰、胃、肠等损伤,诊断和处理时切勿遗漏。在进行脾栓塞术以后,应结合病情和术前影像学检查情况有针对性地对肝动脉、肾动脉和肠系膜上、下动脉行DSA检查。
2.3.6 血管栓塞方式 原则:根据AAST分级及患者血流动力学是否稳定,选择合适的治疗方式,包括保守治疗、脾动脉远端栓塞、脾动脉近端栓塞、脾动脉远端栓塞+近端栓塞以及外科手术。以上处理均基于单纯脾损伤,不涉及多脏器损伤。①对AAST分级Ⅰ级或Ⅱ级,无脾脏活动性出血、假性动脉瘤或外伤性动静脉瘘,血流动力学平稳患者,可行保守治疗;②对AAST分级Ⅰ级或Ⅱ级,同时伴发脾脏活动性出血、假性动脉瘤或外伤性动静脉瘘患者,行脾动脉远端栓塞;③对AAST分级Ⅲ级或Ⅲ级以上,不伴发脾脏活动性出血、假性动脉瘤或外伤性动静脉瘘患者,行脾动脉近端栓塞;④对AAST分级Ⅲ级或Ⅲ级以上,同时伴发脾脏活动性出血、假性动脉瘤或外伤性动静脉瘘患者,行脾动脉远端栓塞+近端栓塞;⑤对血流动力学不平稳或迟发性脾破裂患者,须急诊行介入手术或外科脾切除术/部分脾切除术。
脾动脉近端栓塞:精准位置应是胰背动脉至胰大动脉间,常规用弹簧圈(包括可控弹簧圈)栓塞。由于脾动脉血流量较快、流量较大,弹簧圈会顺血流移位,导致异位栓塞。近端脾动脉栓塞推荐2种方法,即血管塞近端脾动脉栓塞和球囊辅助弹簧圈脾动脉近端栓塞。脾动脉远端栓塞:将导管超选择插送至责任血管,必要时可使用微导管,根据出血部位选择微弹簧圈、明胶海绵、微球或PVA颗粒,栓塞颗粒需加入适量对比剂,在透视下缓慢注入。建议对脾段动脉以下破裂,用700~1 000μm粒径栓塞颗粒;对脾叶动脉破裂,用>1 000μm粒径 栓 塞 颗 粒 或/和 微 弹 簧 圈 栓 塞[46,54-55,57-58]。 当见到被栓塞动脉分支血流滞缓时,再次行脾动脉造影,以观察止血效果。对仍有出血者再次栓塞,直至出血征象消失。然后分别插管至肝总动脉、肾动脉和肠系膜上、下动脉行造影,观察有无合并其他脏器损伤;若有,做相应处理[54-55]。
2.3.7 腹腔引流和自体血液回输 栓塞术后在CT或彩色超声导引下选择腹腔积血最多处,局部麻醉后经穿刺针送入导丝至腹腔或盆腔,沿导丝送入多孔引流管引流腹腔积血[54]。对诊断明确的单纯创伤性脾损伤(未合并腹腔空腔脏器损伤),可通过穿刺引流管进行血液回收[59]。引流管接血液回收装置,将患者腹腔积血进行回收、抗凝、洗涤、滤过等处理,然后回输给患者[60]。血液回收必须采用合格设备,回收处理的血液必须达到一定的质量标准。应用时需以单独无菌吸引管道回收血液,并于回输时尽量使用白细胞滤器或微聚体滤器[61-62]。回输血液禁忌证[63]:①血液流出血管外超过 6 h;②怀疑血液含有癌细胞;③怀疑引流出的血液受到细菌、粪便等污染;④引流出的血液严重溶血。但与白细胞滤器联合使用时,紧急情况下可适当放宽使用适应证。
2.3.8 术后常规处理 脾动脉栓塞术后常规需要抗感染、禁食、补液治疗,对术后腹痛可在排除其他不明原因情况下进行对症止痛处理,可在无抗凝禁忌情况下应用低分子肝素抗凝,预防门静脉血栓治疗,重症患者需要严密心电监护和循环支持治疗,若有病情变化,及时予以再次介入或外科手术处理。
2.3.9 术后并发症处理 由于脾动脉解剖位置、血管条件及栓塞方式选择,脾动脉栓塞术后可能出现一系列并发症,需予以重视并及时处理。若处理不当,可产生严重后果,甚至导致死亡。①脾栓塞后综合征:术后最为常见,发生率较高,可表现为腹痛、腹胀、恶心、呕吐、间歇性发热等[64],考虑原因为脾栓塞后脾组织缺血坏死,脾脏肿胀、包膜紧张,前列腺素E2、白细胞介素等炎性介质和内生致热原释放,膈肌或膈神经引起膈肌阵发性痉挛[65]。腹痛多位于左上腹,栓塞面积大小与疼痛程度直接相关。栓塞面积<40%时疼痛较轻,>80%则疼痛较重。建议控制栓塞面积在<70%,最好<50%[66]。一般情况下,轻微腹痛予止痛对症处理即可。若剧烈腹痛,可予盐酸布桂嗪、吗啡止痛,也可予麻醉镇痛泵止痛。腹胀、恶心、呕吐可予禁食、补液,发热一般发生于栓塞后3 d左右,多为脾脏组织坏死和血肿吸收热,可采取物理降温治疗,脾损伤出血需警惕脾脓肿及腹腔内感染,可采用抗生素预防感染。②严重感染:脾栓塞术后严重感染为较严重并发症,包括腹膜炎和脾脓肿。严重并发症发生与脾脏栓塞面积过大、脾栓塞后免疫功能受损有关。术中无菌处理不良及肠道厌氧菌易位感染也可能为感染发生原因,有专家采取栓塞过程中向脾动脉推入抗生素方式预防术后脾脓肿[67],并且术后抗生素治疗是必要的。若出现严重感染,必要时可行穿刺引流或冲洗,甚至需要外科手术治疗[68-69]。③肺部并发症:脾栓塞后肺部并发症包括肺炎、肺不张和胸腔积液。通常出现在左侧,这与脾脏解剖位置相关。尤其是脾脏上极栓塞后,由于左上腹部疼痛加重,呼吸受限,胸膜炎性反应及淋巴引流不足导致渗出液增加,引起肺部感染、肺不张、胸腔积液。肺炎及轻中度胸腔积液可予有效抗生素和止痛治疗后吸收,大量胸腔积液需要行胸腔穿刺引流治疗。介入栓塞术中选择中下极脾脏栓塞,可减少这些并发症发生[68-69]。④异位栓塞:胰腺动脉意外栓塞和对比剂应用可能导致脾动脉手术后发生胰腺炎[68],甚至少见的肠道血运障碍,引起急性肠梗阻、急性腹膜炎等。这些情况通常可通过禁食、抗感染、补液等保守治疗缓解。但是对于腹痛突然加剧,伴有全腹压痛反跳痛症状,应注意有无异位栓塞引起的组织脏器坏死、化脓性胰腺炎、肠道穿孔等情况发生,及时外科处理。⑤门静脉血栓形成:脾动脉栓塞术后门静脉血流减少,血小板迅速增多,尤其是栓塞面积过大,可能导致门静脉血液处于高凝状态,进而门静脉血栓形成[68-69]。若明确无活动性出血且无抗凝禁忌,可予低分子肝素或口服抗凝药物抗凝治疗。⑥出血及脾破裂:脾动脉栓塞后仍有活动性出血,首先需要明确是否伴发有其他脏器损伤,其次脾损伤导致的脾静脉撕裂出血也是可能原因,另外脾动脉栓塞后出现脾脓肿或脾假性囊肿患者外伤或加重活动等原因,可导致脾脏再次破裂出血。若有这些情况,应考虑及时行外科手术治疗[68-69]。
2.3.10 疗效评价 创伤性脾损伤出血介入治疗结果与转归包括:①治愈——治疗后症状体征消失,出血停止,无并发症发生。②好转——治疗后一般情况好转,出血停止,有并发症发生,但经对症处理后治愈。③未愈——介入术后脾脏再发出血、血肿继发感染、膈下脓肿等,需二期手术处理。有研究表明,部分脾动脉栓塞术(PSE)治疗创伤性脾损伤的成功率为 90%以上[48]。
2.4 非血管介入治疗
非血管介入治疗包括超声引导下介入治疗和CT引导下介入治疗,主要以超声引导为主。超声引导下脾损伤微波消融止血[70]、脾损伤射频消融止血[71]技术已应用于脾损伤出血的止血治疗,另外超声联合微泡空化治疗技术等,未来有望成为新的无创治疗创伤性脾出血的方法[72]。
2.5 外科治疗
外科手术是救治创伤性脾损伤的方法之一。关键在于快速全面地诊断伤情,把握手术指征,正确安排救治先后次序,采取合适的手术方式,实施个体化治疗。全脾切除术是各种脾损伤治疗方式的基本保证,但术后并发症较多,人体免疫功能受损[73];各类保脾手术和全脾切除+自体脾片组织移植术,能够保留全部或部分脾脏,从而保留脾功能[74];腹腔镜手术是一种微创诊断与治疗脾损伤方法,符合损伤控制性手术原则,具有重要的临床意义[75]。应遵循“抢救生命第一、保留脾脏第二”及“损伤控制”原则[15],必要时果断切除脾脏,以免因过度延长手术时间,增加术中出血而导致严重后果。若患者无其他严重合并伤,且脾损伤程度较轻,可根据条件及术中经验选择合适的脾保留性手术或介入栓塞术。
[专家共识指导委员会成员:祝益民(湖南省卫生健康委员会)、向 华(湖南省人民医院)、吴金术(湖南省人民医院)、滕皋军(东南大学附属中大医院)、吕传柱(海南医学院)、陈玉国(山东大学齐鲁医院)、徐 克(中国医科大学附属第一医院)、于学忠(北京协和医院)、张国强(中日友好医院)、张 茂(浙江大学附属第二医院)、朱华栋(北京协和医院)、张小明(北京大学人民医院)、单 鸿(中山大学附属第五医院)、程英升(上海市第六人民医院东院)、邹英华(北京大学第一医院)。专家共识委员会成员(按姓氏拼音排序):曹友德(湖南省人民医院)、成 伟(湖南省人民医院)、顾建平(南京市第一医院)、顾玉明(徐州医科大学附属医院)、郭金和(东南大学附属中大医院)、韩国宏(西京医院)、韩小彤(湖南省人民医院)、韩新巍(郑州大学第一附属医院)、何晓峰(南方医科大学南方医院)、纪建松(浙江省丽水中心医院)、蒋 波(湖南省人民医院)、黎海亮(河南省肿瘤医院)、李茂全(上海市第十人民医院)、李天晓(河南省人民医院)、李 肖(中国医学科学院肿瘤医院)、陆骊工(珠海市人民医院)、刘际童(湖南省人民医院)、刘 鹏(湖南省人民医院)、罗荣光(南昌大学第一附属医院)、吕维富(安徽省立医院)、倪才方(苏州大学附属第一医院)、施海彬(江苏省人民医院)、宋景春(南昌大学附属长城医院)、宋 维(海南省人民医院)、宋振举(复旦大学附属中山医院)、王 峰(大连医科大学附属第一医院)、王 岗(西安交通大学第二附属医院)、王茂强(解放军总医院)、王 毅(陆军军医大学第三附属医院)、危 安(湖南省人民医院)、王忠敏(上海交通大学医学院附属瑞金医院)、徐 浩(徐州医科大学附属医院)、许硕贵(海军军医大学附属长海医院)、颜志平(复旦大学附属中山医院)、杨维竹(福建医科大学附属协和医院)、杨业发(海军军医大学东方肝胆外科医院)、翟水亭(河南省人民医院)、张剑锋(广西医科大学第二附属医院)、张 琳(清华大学附属北京清华长庚医院)、张 轶(湖南省人民医院)、赵增仁(河北医科大学第一医院)、郑传胜(华中科技大学同济医学院附属协和医院)、钟红珊(中国医科大学附属第一医院)、周 石(贵阳医学院附属医院)、朱 晖(中南大学湘雅二医院)。执笔:蔡煌兴(湖南省人民医院)、向 华(湖南省人民医院)]
