壳聚糖/聚乙烯醇/壳寡糖抑菌纳米纤维膜的制备和性能研究
2020-08-16刘永旭张大伟
刘永旭, 张大伟
(东北林业大学 材料科学与工程学院, 黑龙江 哈尔滨 150040)
纳米纤维膜具有孔隙率高、透气性好、比表面积高等特性,被广泛应用于储能材料、组织支架、伤口敷料、食品包装等领域[1-4]。在纳米纤维的制备技术中,静电纺丝因设备简单可靠、操作方便、制备纤维直径均一等优点,在实验室和工厂被大量应用[5-8]。天然高分子及其衍生物的静电纺丝纳米纤维因具有良好的生物相容性和细胞黏附性,以及来源广泛、价格便宜等优点,而日益受到研究者的关注。壳聚糖(CS)作为天然高分子材料甲壳素的脱乙酰基产物,具备较好的抑菌性、生物相容性、低抗原性、无毒无害等特性,这些特性使壳聚糖纳米纤维膜在组织工程、伤口敷料、酶固定化、药物传递、废水过滤和抗菌药物等很多领域中有巨大的发展前景[9-11]。壳聚糖分子间强烈的氢键作用,以及在酸性条件下的阳离子聚电解质的特性[12],使得在静电纺丝过程中,CS分子链间的正电荷群会形成较大的斥力,不利于CS的静电纺丝,为此常将其与聚乙烯醇(PVA)、聚乳酸(PLA)、聚环氧乙烷(PEO)等聚合物[13-15]混合纺丝。其中,PVA因具备较好的水溶性、生物相容性和降解性能,而常用于静电纺丝制备CS/PVA纳米纤维膜。壳聚糖相对分子质量大、分子间作用力强制约了纳米纤维膜的抑菌性,因此加强CS/PVA纳米纤维膜的抑菌性和吸收性,将更有利于CS基纳米纤维膜应用于生物医用领域。壳寡糖(CHOS)作为壳聚糖降解得到的小分子衍生物,相对分子质量只有几十到几百,低相对分子质量的特性使其易溶于水、抑菌性强、吸收性好、生物活性高[16-17],用CHOS改善壳聚糖纳米纤维膜的抑菌性和吸收性是一个可行的研究方向。本研究以CS、PVA、CHOS为原料,采用静电纺丝制备了搭载不同含量CHOS的CS/PVA纳米纤维膜,并通过电镜观测、抑菌测试、水接触角测试、溶解性能测试探究其各项性能,以便于CS/PVA/CHOS纳米纤维膜材料在生物医用领域有更广泛地应用。
1 实 验
1.1 原料与试剂
壳聚糖(CS),脱乙酰度为91%,黏度100 mPa·s,浙江金壳药物有限公司;聚乙烯醇(PVA),醇解度为88%,聚合度为1 700,阿拉丁生化科技股份有限公司;壳寡糖(CHOS),脱乙酰度为90%,黏度为10 mPa·s,浙江金壳药物有限公司;金黄色葡萄球菌(Staphylococcusaureus)CMCC 26003,广东省微生物保藏中心;PBS磷酸缓冲盐溶液,pH值为7.4,实验室自制;冰醋酸,天津致远试剂有限公司;蒸馏水,哈尔滨市文景蒸馏水厂。
1.2 纺丝液的配制
取PVA粉末放入80 ℃水中配制成质量分数为5%的PVA水溶液;称取一定量的CS粉末配制成悬浮液,并滴入等质量的冰醋酸,搅拌至CS完全溶解;然后再将CS悬浮液与5%的PVA溶液按比例混合,配制成CS与PVA的质量比分别为10 ∶90、 20 ∶80、 30 ∶70的溶液。再配制3组CS与PVA的质量比为20 ∶80的溶液,分别加入一定量的壳寡糖(CHOS),搅拌使之溶解,配制成CS、PVA和CHOS质量比分别为20 ∶80 ∶2、 20 ∶80 ∶5和20 ∶80 ∶10的溶液。再将所配制的溶液倒入50 mL的离心管中,放入超声波振荡器中,功率为120 W,超声波振荡20 min,使溶液分散均匀,得到静电纺丝液。
1.3 纳米纤维膜的纺制
将配制好的静电纺丝液注入10 mL的注射器中,注射器与水平线夹角为18°。使用高压电源提供高压电场,使用铝箔作为纳米纤维的负极收集板,正极为导线连接到注射器金属针头。在重力和电场的共同作用下,纺丝液从注射器针尖喷射出来形成纳米纤维,并在负极板上逐渐被收集。经36 h的连续纺制,制备得到一定厚度的纳米纤维膜。取制备的纳米纤维膜放入80 ℃烘箱中12 h,烘干水分以备测试。以CS与PVA的质量比10 ∶90、 20 ∶80、 30 ∶70的纺丝液制备的CS/PVA纳米纤维膜分别标记为CS/PVA-1、CS/PVA-2和CS/PVA-3;以CS、 PVA与CHOS质量比20 ∶80 ∶2、 20 ∶80 ∶5、 20 ∶80 ∶10的纺丝液制备的CS/PVA/CHOS纳米纤维膜分别标记为CS/PVA/CHOS-1、 CS/PVA/CHOS-2和CS/PVA/CHOS-3。
1.4 纳米纤维膜的表征
1.4.1扫描电镜(SEM)观测 将不同成分的纳米纤维膜裁剪成0.5 cm×0.5 cm,通过JSM-7500F型扫描电子显微镜(日本电子株式会社)分析膜的微观形态,并通过使用Digimizer软件任选膜中80根纤维进行测量并计算纤维平均直径及其标准差。
1.4.2红外(FT-IR)测试 选择纳米纤维膜的原料和成纤效果较好、组分比例合适的纳米纤维膜作为测试对象。使用TensorⅡ型红外光谱仪(德国BRUKER光谱仪器公司)表征纳米纤维膜的化学结构,光谱扫描范围为4000~400 cm-1,分辨率为4 cm-1。
1.4.3X射线衍射(XRD)测试 通过D/max-2200VPC型X射线衍射仪(日本理学电机株式会社)测定并分析纳米纤维膜的结晶度,扫描速度为5(°)/min,扫描范围(2θ)为5~55°。
1.4.4抑菌测试 将不同成分的纳米纤维膜裁剪成1 cm×1 cm大小的试样,放置于涂有金黄色葡萄球菌的琼脂培养基表面,在37 ℃恒温培养箱中培养24 h后,观察并使用Digimizer软件测量培养皿中纳米纤维膜周围的抑菌圈大小,比较各纳米纤维膜的抑菌性能。
1.4.5水接触角测试 借助OCA 20接触角测定仪(德国Dataphysics仪器股份有限公司)测量纳米纤维膜的水接触角,测量时水滴为5 μL,温度为25 ℃,使用数码相机记录液滴的形状,每个样品试验重复测量5次,取平均值。
1.4.6溶解性能测试 将不同成分的纳米纤维膜裁剪成2 cm×2 cm大小的试样,放入100 ℃烘箱中烘干,称量并记录质量(m1,g),放于pH值为7.4、温度为37 ℃的PBS溶液中(每组多个样品),在放置的第1、 4、 7天取出,取出试样后在100 ℃环境下烘干2 h,并记录残余质量(mn,g)。每个样品试验重复测量5次,取平均值。质量残留率(k,%)由下式计算:
k=mn/m1×100%
2 结果与分析
2.1 微观形貌分析
不同成分和比例的CS/PVA、CS/PVA/CHOS纳米纤维膜的扫描电镜图如图1所示,平均直径统计如表1所示。图1(a)~(c)是不同质量比的CS/PVA纳米纤维膜的电镜图,图1(d)~(f)是搭载不同含量的CHOS的CS/PVA/CHOS纳米纤维膜的电镜图。

m(CS) ∶m(PVA): a.10 ∶90; b.20 ∶80; c.30 ∶70
观察发现,几种不同的纳米纤维膜中,均无明显的串珠和缺陷存在,且纤维呈现无规则取向排列,纤维具有较好的连续性,这说明纳米纤维膜具备较好的微观形貌。由图1(a)~图1(c)并结合表1统计数据来看,当CS/PVA膜中的CS含量上升时,纤维的平均直径也随之上升,同时纤维直径的不均匀程度,即标准差也呈现出逐渐增大的变化趋势,这是由于在含有冰醋酸的酸性纺丝液中,CS分子链上的氨基会从溶液中结合氢离子,从而使壳聚糖成为带阳离子的聚电解质,因此静电纺丝过程中,纺丝液中CS分子链之间形成的正电荷群之间会产生较大的斥力,会增大纳米纤维的成纤阻力,因此CS含量越高,纤维的直径和不均匀度就越大[12]。
从图1(d)~(f)中可以发现,CS/PVA/CHOS纳米纤维膜也表现出均匀的微观形貌。表1中的统计数据显示,CS/PVA/CHOS纳米纤维的平均直径随着CHOS含量的增加而有所降低,此外,纤维直径的不均匀度(即标准差)也随着CHOS的含量增加而减小,这与CS/PVA纳米纤维直径随CS含量的变化规律正好相反。这主要是由于CHOS作为CS的小分子降解产物,在纺丝溶液中更易溶解和分散,因此在成纤过程中可纺性更好,所以当CHOS的含量增加时,溶液的可纺性也会增加,纤维在电场中能得到充分拉伸,纤维直径也随之变小且直径分布更加均匀,可以有效改善纳米纤维的成纤效果。
2.2 FT-IR分析
CS、 CHOS、 PVA、 CS/PVA-2以及CS/PVA/CHOS-3纳米纤维膜的红外光谱如图2所示。纯CS的红外特征光谱曲线a中3357 cm-1处的峰属于—NH2和—OH的特征峰[7]。1645和1538 cm-1处的特征峰分别属于酰胺I和酰胺II基团的混合振动。C—O—C振动导致1152、 1067和1031 cm-1处出现特征峰,2920和1491 cm-1处出现的特征峰属于—CH2和CH—OH伸缩振动[18]。

壳寡糖作为壳聚糖的降解产物,具有很多与壳聚糖相同的官能团。在图2曲线b中可以看到3480 cm-1左右为羟基与胺基的缔合峰,1640 cm-1为壳寡糖分子上酰胺基团振动吸收峰[20]。CS/PVA/CHOS纳米纤维膜的红外图谱与CHOS、CS和PVA红外图谱相比没有出现新的特征峰,因此推测壳寡糖在纳米纤维膜中是以共混的形式存在,这有助于CHOS更容易释放到环境中。
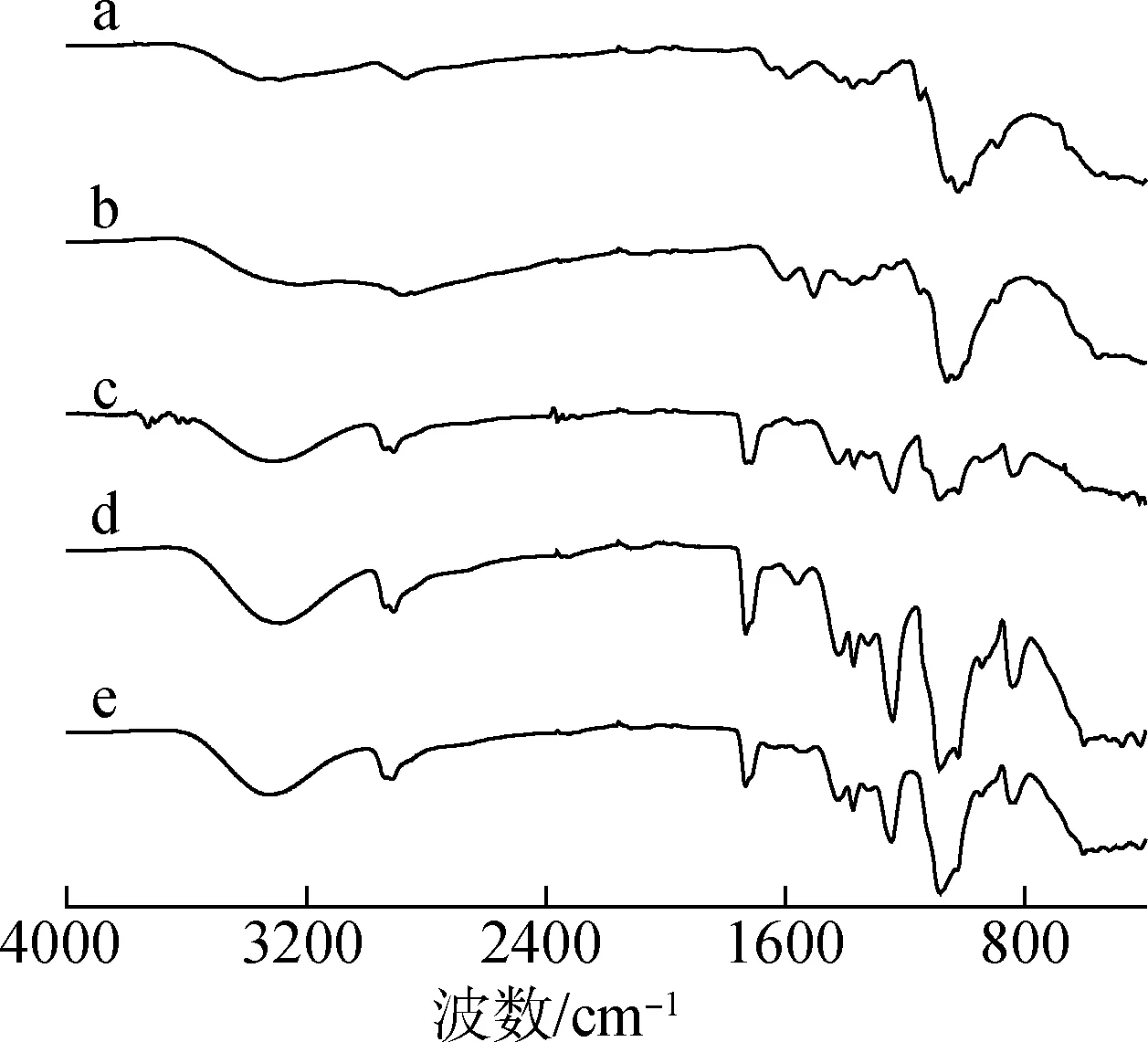
图2 样品的红外光谱图
2.3 XRD分析
CS粉末、纯PVA、CS/PVA-2纳米纤维膜以及CS/PVA/CHOS-3纳米纤维膜的XRD图谱如图3所示。
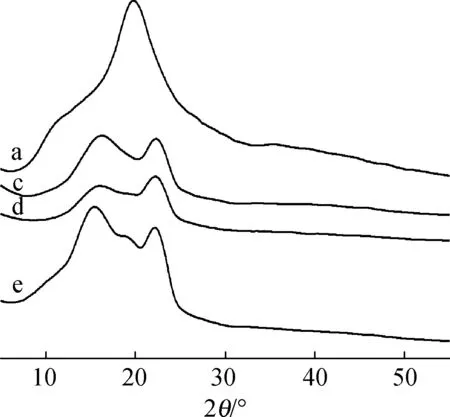
a.CS; b.CHOS; c.PVA; d.CS/PVA-2; e.CS/PVA/CHOS-3
由图3可知,纯CS在2θ为19.8°处出现特征衍射峰[21];而纯PVA在2θ为16.0°和22.4°处出现2个 尖锐的衍射峰[22]。当CS与PVA共混纺丝后,由于CS与PVA以分子级形式混合,且膜中PVA含量远高于CS,因而仅出现了PVA的衍射峰[23]。比较图3中的4条曲线可以发现,随着CHOS的添加,CS/PVA/CHOS纳米纤维膜的峰宽变宽,峰形变尖,表明CHOS的加入使得CS/PVA纳米纤维膜的结晶度发生变化。结晶度的变化推测有2个原因:一方面,在静电纺丝过程中,被拉伸的纤维分子链以较高的拉伸速率迅速凝固,阻碍了晶体的形成[23-24];另一方面,CS、PVA、CHOS分子间形成了较强的氢键作用力,增强了三者之间的相容性,也破坏了由相分离的PVA或CS产生的晶体结构[25]。晶体结构的破坏可能会在一定程度上降低纳米纤维的强度,但对于提升纳米纤维膜的吸水性及亲水性有帮助,从而使壳寡糖更快地释放到周围环境中,使其抑菌性能得到提升,这一推论在后面的抑菌实验、水接触角实验中能够获得支持。
2.4 抑菌性能测试
不同CS以及CHOS含量的CS/PVA和CS/PVA/CHOS纳米纤维膜对金黄色葡萄球菌抑制能力如图4 所示。从图4中可以发现,在培养皿中6个试样周围均具有较明显的抑菌圈,说明各纳米纤维膜对金黄色葡萄球菌均有一定的抑制能力,其中CS/PVA/CHOS-3的抑菌圈直径最大,说明其抑菌能力最为突出。

a.CS/PVA-1; b.CS/PVA-2; c.CS/PVA-3; d.CS/PVA/CHOS-1; e.CS/PVA/CHOS-2; f.CS/PVA/CHOS-3
从图4中还可以发现,随着壳聚糖的量从10%增加到30%,CS/PVA纳米纤维膜的抑菌圈直径从11.34 mm增大到14.58 mm,抑菌性能明显增强。由于壳聚糖的抗菌机理主要在于其线型分子链上的氨基侧基能结合H+而带正电荷,从而能与细菌蛋白质中带负电的部分结合,阻碍细菌吸收营养物质,使细菌失去活性[26]。因此制备的CS/PVA纳米纤维膜试样的抑菌性能与壳聚糖含量成正比。不同CHOS含量的CS/PVA/CHOS纳米纤维膜的抑菌实验表明,随着CHOS含量的增加,纳米纤维膜的抑菌圈直径呈逐步变大的趋势,相比未添加CHOS的CS/PVA-2膜,m(CS) ∶m(PVA) ∶m(CHOS)为20 ∶80 ∶10的CS/PVA/CHOS-3膜的抑菌圈直径从12.32 mm增大到了17.11 mm,抑菌圈直径扩大了38.9%。这是因为壳寡糖作为壳聚糖的小分子产物,结构和化学特性与CS基本一致,除了具备与CS相似的杀菌机理外,还能够利用小分子特性渗透到细胞内部,破坏细胞内物质,导致细菌死亡[27],这使得CHOS表现出更强的抑菌效果,所以制备的CS/PVA/CHOS纳米纤维膜的抑菌性能会随着CHOS含量的增加而增加。
2.5 水接触角测试
不同CS以及CHOS含量的CS/PVA-1、CS/PVA-2、CS/PVA-3、CS/PVA/CHOS-1、CS/PVA/CHOS-2和CS/PVA/CHOS-3纳米纤维膜的接触角分别为75.1°、 59.8°、 41.7°、 55.1°、 47.2°和37.5°。CS/PVA纳米纤维膜的水接触角随着CS含量的增加而减小,这是由于壳聚糖分子上带有大量的—OH、—NH2等强极性官能团,是一种高度亲水的高分子材料,因此随着CS含量的增加,纳米纤维膜的亲水性增加,水接触角减小。
CS/PVA/CHOS纳米纤维膜的水接触角随着CHOS含量的增加而减小,CS/PVA/CHOS-3纳米纤维膜的水接触角相比于CS/PVA-2纳米纤维膜,在搭载了10%的CHOS后,水接触角由59.8°降到了37.5°,降低了37.3%,这是由于壳寡糖作为壳聚糖的小分子产物,在水溶液中有更好的溶解性和分散性,因而具有更好的亲水性。因此随着纳米纤维膜中CHOS含量的增加,纳米纤维膜具备更好的亲水性能,水接触角也因此变小。
亲水性能是衡量生物医用材料,特别是创伤敷料的一个重要指标,有研究表明,湿润的伤口环境更有利于创伤的愈合[28],因此亲水性能好的纳米纤维膜在创伤敷料领域能有更好地应用。
2.6 溶解性能测试
不同CHOS含量的CS/PVA/CHOS纳米纤维膜在37 ℃的PBS缓冲液(pH值为7.4)中的溶解性能如图5所示。从图5可以发现,不同CHOS含量的纳米纤维膜具有相似的溶解特性,即在初始的24 h内快速溶胀溶解,但在后续的时间里溶解速度较平缓。这是因为CS/PVA/CHOS纳米纤维膜中的PVA在水溶液中会迅速遇水溶胀并溶解,导致纳米纤维膜迅速大量失重。

图5 纳米纤维膜在pH值7.4缓冲液中的溶解性能Fig.5 Solubility of nanofibrous membrane in buffer solution with pH value 7.4
由图5可以发现,不同CHOS含量的纳米纤维膜的溶解性能有所不同,CHOS含量越高,纳米纤维膜在相同时间内的溶解速度越快,质量残留率也更低。不含CHOS的纳米纤维膜第1天的质量残留率为75.7%,第7天的质量残留率为66.8%。但是当m(CS) ∶m(PVA) ∶m(CHOS)=20 ∶80 ∶10 时,纳米纤维膜第1天的质量残留率为58.6%,第7天的质量残留率为41.0%,质量残留率相比不添加CHOS时降低了38.6%,即溶解率提高了38.6%。即CHOS的加入加速了纳米纤维膜的溶解。出现这种情况的原因是,CHOS具有极好的亲水性和水溶性,因此含有CHOS的纳米纤维膜在溶液中溶胀溶解速度加快。高溶解率的纳米纤维膜质量残留率更低,在作为创伤敷料使用时,可以减少在去除敷料时对皮肤造成的二次伤害[29],因此可以更好地应用在伤口敷料等领域。
3 结 论
以CS、PVA和CHOS为原料,采用静电纺丝的方式制备了不同CS和CHOS含量的CS/PVA和CS/PVA/CHOS纳米纤维膜,并对纳米纤维膜的微观形貌、化学结构、抑菌性能、亲水性能、溶解性能进行了测试和分析。研究发现:CS/PVA/CHOS纳米纤维膜纤维直径均匀,无串珠等缺陷;FT-IR测试表明,CHOS被混合在CS/PVA/CHOS纳米纤维膜中;XRD测试表明,CHOS的加入促进了纳米纤维膜中各组分之间的相容性;CHOS的加入提升了纳米纤维膜针对金黄色葡萄球菌的抑菌性能,抑菌性能随着CHOS含量增加而提高,m(CS) ∶m(PVA) ∶m(CHOS)=20 ∶80 ∶10的CS/PVA/CHOS纳米纤维膜比m(CS) ∶m(PVA)=20 ∶80的CS/PVA纳米纤维膜的抑菌圈直径提升了38.9%。水接触角测试表明,m(CS) ∶m(PVA) ∶m(CHOS)=20 ∶80 ∶10的CS/PVA/CHOS纳米纤维膜相比m(CS) ∶m(PVA)=20 ∶80的CS/PVA纳米纤维膜水接触角下降了37.3%,CHOS的加入赋予了纳米纤维膜更好的亲水性。溶解性能测试表明CHOS的加入促进了CS/PVA纳米纤维膜在溶液中的溶解,溶解率最大提升了38.6%。综合来看,搭载有CHOS的CS/PVA纳米纤维膜,相比于传统的CS/PVA纳米纤维膜拥有更好的抑菌性、亲水性和溶解性,这将更有利于纳米纤维膜在伤口敷料、组织工程等生物医用方向的应用。
