含氮化合物废气选择性催化氧化技术研究进展
2020-08-14李伯东程彦虎王学明彭召静焦桂萍
王 涛,李伯东,程彦虎,王学明,彭召静,焦桂萍
(中国船舶重工集团公司第七一八研究所,河北 邯郸 056027)
随着我国经济结构的转型升级,以及世界范围内对环境污染问题的日益关注,各个国家对含有挥发性有机物废气的治理要求越来越严格。通过催化燃烧技术将醇类、酮类、醚类、酯类及芳香烃等常规性挥发性有机物氧化为水和二氧化碳已有较多报道[1-2]。含氯有机物中的氯代芳烃、氯代烷烃等在精细化工、医药、农药领域应用广泛,对其治理也有较多研究[3-5]。此外,含有杂原子的有机化合物也是废气中常见的污染物,但此类废气的相关治理报道及研究相对较少。含氮化合物种类较多,主要有氨气等含氮无机化合物及胺类、酰胺类、腈类等含氮有机化合物。含氮化合物多具有恶臭等刺激性气味,与常规挥发性有机物相比,对人体具有较大的伤害,是废气达标排放的重要监管参数之一。
针对不同的含氮化合物废气,治理手段主要有吸附法、吸收法及催化燃烧法。其中,吸附法常采用活性炭、分子筛等作为吸附剂,吸附剂具有丰富的微孔结构及大的比表面积,适用于低浓度含氮化合物废气的治理。由于吸附剂均具有一定的吸附容量,因此在使用过程中需循环再生或更换新的吸附剂。吸收法主要处理对象为含氨废气,由于氨气的亨利系数大于二氧化碳、甲烷、硫化氢等,因此常采用水或者稀酸溶液(HCl、HNO3、H2SO4)吸收氨气[6]。Melse R W等[7]采用稀酸溶液为吸收剂进行喷淋塔实验,结果发现,入口氨气体积分数0.000 8%~0.002 9%时,其净化效率可达到 90%~99%;入口氨气浓度为体积分数0.01%~0.04%时,其净化效率下降至75%~85%。催化燃烧法净化含氮化合物废气具有使用工况广泛,废气净化效率高,使用寿命相对较长等优点。其难点在于保持高净化效率的同时,将含氮化合物选择性氧化成氮气、水及二氧化碳,避免过度氧化生成氮氧化物(NOx)。这也在一定程度上限制了催化燃烧法净化含氮化合物废气在工业上的应用。该技术的突破点在于高活性、高稳定性,同时高N2选择性催化剂的研制。针对不同含氮化合物废气,研究者已开展了相关选择性催化氧化催化剂的研发,积累了一定的使用经验。
本文主要综述近几年氨气、腈类、胺类及其他含氮化合物废气选择性催化氧化研究进展。
1 含氮化合物废气选择氧化及反应机理
1.1 氨 气
氨气(NH3)是一种无色、具有刺激性气味的气体,主要来自农业源释放(氮肥)、工业源排放(石油化工及精细化工领域)或者移动源采用尿素等催化还原氮氧化物导致的氨逃逸[8]。有研究报道[9-11],氨气废气是我国雾霾产生的因素之一。
氨气的结构式简单,其选择性催化氧化生成氮气和水,涉及的反应主要有:
主反应:4NH3+ 3O2→ 2N2+ 6H2O
副反应:2NH3+ 5O2→ 4NO + 6H2O
2NH3+ 2O2→ N2O + 3H2O
氨气氧化为放热反应,其吉布斯自由能和反应平衡常数与温度的关系如图1所示[12]。由图1中吉布斯自由能可以看出,在热力学上,氨氧化生成N2比生成NO或者N2O更为有利。但在很宽的范围内,三个反应的平衡常数均很高,因此,N2及副产物NO和N2O均很容易生成。

图1 温度对氨氧化吉布斯自由能ΔG和反应平衡常数Keq的影响Figure 1 Effects of temperature on Gibbs free energy ΔG and reaction equilibrium constant Keq of ammoxidation
因此,氨氧化催化剂需要具有适中的氧化性,若氧化性不足,反应活性不高,氨气净化效率不达标;若氧化性过强,则工艺条件不好控制,氨气很容易被氧化成氮氧化物,造成氮氧化物超标排放。同时,催化剂需具有较强的稳定性,因为在反应过程中,反应物氨气与产物水作用产生弱碱性环境,对催化剂活性组分保持高分散提出了挑战。
在氨气选择性催化氧化催化剂研究中,活性组分包括贵金属(Ag、Pt、Au、Ir等),以及过渡金属氧化物(Fe3O4、Co3O4、NiO、CuO等)。目前,尚未研发出普遍认可的高效催化剂。
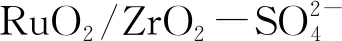
综上,贵金属催化剂虽然具有较低的转化温度,但产物N2的选择性不高。为优化催化剂性能,Jablonska M等[18]制备了不同过渡金属含量的Ag-Cu/Al2O3双功能催化剂。结果表明,质量分数1.5%Ag-10%Cu/Al2O3的催化剂性能较好,在反应温度375 ℃时,氨气可完全转化,N2选择性92%,NO和N2O选择性分别为2%和6%。添加过渡金属后,催化剂效率降低,反应物转化温度升高,但产物中N2选择性明显上升。为进一步提高N2选择性,除采用Al2O3、TiO2、SiO2、ZrO2等载体外,研究人员也尝试使用分子筛作为催化剂载体。由于分子筛具有酸性位点,易于吸附NH3,同时分子筛具有丰富的孔道结构和比表面积,有利于活性组分的高分散,从而提高催化剂活性[19]。Long R Q等[20]通过离子交换制备ZSM-5分子筛负载过渡金属Cr、Mn、Fe、Co、Ni、Cu等催化剂。在空速为230 000 h-1时,综合考虑NH3转化效率和N2选择性,催化剂活性大小顺序为Co-ZSM-5≈Ni-ZSM-5 腈类含氮化合物,如氰化氢(HCN)、乙腈(C2H3N)、丙烯腈(C3H3N)等低碳链化合物应用范围广泛。HCN废气来源有机动车尾气、石油化工及煤气化等;C2H3N、C3H3N等作为重要的有机合成中间体,在石油化工、精细化工、树脂、化纤及橡胶制品等行业应用广泛。腈类含氮化合物具有较强的毒性,其废气治理具有重要意义。 Zhao Haibo等[21]报道了质量分数0.5%Pt/Al2O3催化剂分解HCN性能。结果表明,在反应温度250 ℃,原料气为体积分数0.003%HCN、6%O2及0.355 %水汽条件下,HCN转化效率90%,但产物中N2选择性明显低于N2O。含氰化氢废气的选择性氧化催化剂研究多集中在过渡金属氧化物[22-23]。Krocher O等[24]报道了一系列用于催化分解HCN的催化剂。结果表明,Cu-ZSM-5和MnOx-Nb2O5-CeO2催化剂具有较高的活性及N2选择性。研究同时发现,在水及氧气同时存在的条件下,HCN在催化剂作用下同时发生氧化和水解反应,生成中间产物NH3,NH3进一步氧化分解为N2和H2O。Liu Ning等[25]通过浸渍法制备了不同分子筛负载的过渡金属催化剂,包括Cu-(Beta,FER,MCM-22,MCM-49,MOR),及M(M=Cu,Co,Fe,Mn,Ni)-ZSM-5催化剂。经过筛选,发现Cu-ZSM-5催化剂性能最佳,在反应温度350 ℃时,HCN转化率为90%,N2选择性达到95%。Ma Yixing等[26]通过溶胶凝胶法制备了TiO2负载的过渡金属(Ni、Fe、Co、Nb、Nb/La)催化剂,并用于催化HCN的水解,其中Nb/La-TiO2在反应温度300 ℃时,HCN基本完全转化。 对乙腈废气的选择性催化氧化的研究较少[27]。Rasko J等[28]利用傅里叶红外及质谱等分析方法,研究了乙腈在Al2O3负载贵金属(Pt、Rh、Au)催化剂上的吸附及表面反应特征。在氧气存在的反应过程中,Pt/Al2O3及Rh/Al2O3催化剂表面生成中间物种异腈酸盐(NCO),但在Au/Al2O3催化剂上没有发现该中间物种的生成。曹宇等[29]将过渡金属(Cu、Co、Cr、Mn)负载到SBA-15分子筛上,并用于乙腈催化燃烧反应。结果表明,Cu/SBA-15催化剂具有较高的乙腈废气催化燃烧活性和N2选择性,当反应温度高于350 ℃时,乙腈转化率接近100%,N2产率80%。 用于丙烯腈废气选择性氧化的催化剂研究包括贵金属催化剂及过渡金属催化剂。Nanba T等[30]考察了不同载体(ZSM-5、Al2O3、TiO2、SiO2、MgO、ZrO2)负载的Ag催化剂在丙烯腈氧化反应过程中的催化活性。其中,Ag/TiO2和Ag/SiO2催化剂具有较好的丙烯腈转化率和N2选择性,在两种催化剂上均发现了金属态和氧化态Ag物种,其中氧化态Ag物种有利于丙烯腈转化为中间物种NH3,金属态Ag物种则将NH3氧化为N2。为进一步提高产物N2的选择性,Liu Ning等[31]通过浸渍法制备了不同分子筛负载的Cu质量分数5%催化剂,催化剂活性顺序为Cu-ZSM-5(Si/Al=26)>Cu-MCM-49>Cu-MCM-22>Cu-Beta>Cu-Y。多种表征手段表明,Cu离子是反应的活性位点,低Si/Al比分子筛载体可以为铜离子提供更多交换位点,Cu-ZSM-5拥有最多的活性位点。研究者通过原位漫反射傅里叶变换红外和密度泛函计算提出了如下两种丙烯腈氧化机理: 1)无水参与 C2H3CN(g)+Cu-Za+O2(g)→C2H3CN-Cu-Z-O C2H3-Cu-Z-O→C2H3-(ad)+NCO(ad) NCO(ad)+O(ad)→N2(g)+CO2(g) C2H3-(ad)+O(ad)→CxHyOz(ad)(C2H3OH,CH3COOH)(ad) CxHyOz(ad)+O(ad)→CO2(g)+H2O(g) 2)有水参与 C2H3CN(g)+Cu-Za→C2H3CN(ad) C2H3CN(ad)→C2H3-(ad)+CN-(ad) CN-(ad)+H2O(g)→NH3(ad) NH3(ad)+O(ad)→N2(g)+H2O(g) C2H3-(ad)+O(ad)→CxHyOz(ad)(C2H3OH,CH3COOH)(ad) CxHyOz(ad)+O(ad)→CO2(g)+H2O(g) 无水参与时,丙烯腈吸附在催化剂上,与氧气反应生成中间产物NCO及C2H3-,NCO随后氧化为N2及CO2,C2H3-则经过多步反应,最终氧化为CO2和H2O。有水参与时,吸附态的丙烯腈水解为中间产物NH3及C2H3-,NH3氧化为N2及H2O,C2H3-氧化为CO2和H2O。文献[32-33]也提出了Cu-ZSM-5催化剂上丙烯腈选择性催化氧化反应机理,认为在反应过程中有中间产物NCO的生成,同时水的存在促进生成中间产物NH3,有利于提高丙烯腈的转化效率。 胺类,如三甲胺、三乙胺、正丁胺等在较低浓度下即有强烈的刺激性气味,关于含胺废气来源的相关报道较少,研究人员多以选择性氧化正丁胺为探针反应进行催化剂研发。Ma Mudi等[34]通过原位合成、浸渍法及锚接法制备了Pd/SiO2催化剂。结果表明,采用锚接法制备的Pd/SiO2催化剂具有最小的Pd粒径(1.72 nm),在反应温度234 ℃时,正丁胺转化率90%,但其NOx生成率比原位合成及浸渍法制备的催化剂均高。采用浸渍法制备的Pd/SiO2催化剂在反应温度240 ℃时,正丁胺转化率90%,NOx生成率0.99%。研究者还对比了SiO2载体比表面积对催化剂活性的影响。原位漫反射傅里叶变换红外光谱发现,较大的载体比表面积有利于反应过程中中间产物NHx的扩散,避免NOx的生成。Ma Mudi等[35]制备了不同比表面积的微介孔SBA-15分子筛载体,负载活性组分Pd后用于催化选择性氧化正丁胺。其中,Pd/S-5催化剂具有最大的比表面积及孔体积,有利于提高活性组分分散度,在反应温度230 ℃时,正丁胺转化率为90%,同时由于丰富微孔的存在,有利于降低NOx的生成,其收率为0.8%。为进一步降低产物中NOx的收率,Xing Xin等[36]通过浸渍法制备了不同分子筛载体(ZSM-5、MOR、MCM-22、Hβ及SAPO-34)负载的Cu质量分数5%催化剂,在正丁胺催化氧化反应中评价催化剂活性,筛选出Cu-ZSM-5催化剂活性最佳,在反应温度279 ℃时,正丁胺转化率90%,反应温度300 ℃时,正丁胺完全转化。研究者还考察了NOx副产物,包括N2O、NO和NO2的生成规律。在分子筛负载的铜基催化剂中,反应温度高于350 ℃时,N2O选择性下降明显,反应温度450 ℃时,Cu-ZSM-5催化剂上已没有N2O生成。反应温度(100~400) ℃时,NO生成量先升后降,但总体只有微量NO生成。在Cu-ZSM-5及Cu-SAPO-34催化剂上,反应温度>400 ℃时,NO生成量上升,同时伴随NO2产生,NO2的选择性不高于2%。 除上述氨气、腈类及胺类废气的选择性催化氧化研究外,其他含氮化合物废气的催化分解技术也有报道。含氮杂环化合物是一类使用广泛的溶剂及合成中间体。Matsuyama T等[37]报道了在惰性气氛下催化分解含氮环状化合物吡咯及吡啶。将FeCl3沉淀在粉状纤维素上,惰性气氛焙烧得到炭负载的纳米级Fe催化剂,Fe粒径(25~30) nm。有文献报道吡咯的热分解温度为(750~800) ℃[38],采用炭担载Fe基催化剂后,其完全分解温度降至600 ℃。在该催化剂作用下,吡啶完全分解温度为650 ℃。该催化剂稳定性有待提升,使用H2还原使用后的催化剂,活性有一定恢复。 含氮化合物种类繁多,使用场景复杂。与吸附、吸收等技术相比,选择性催化氧化处理含氮化合物废气具有适用浓度范围广,应用场景广泛,使用有效期长等优点。作为选择性催化氧化处理技术的核心,兼顾反应物转化率和产物中N2选择性的催化剂还在深入探索中。目前的研究报道中,催化剂活性组分主要为贵金属及过渡金属氧化物。贵金属具有较高的氧化性,可在较低温度下实现反应物的高效转化,稳定性较高,但其产物中N2选择性较低,导致在工程应用中出口NOx排放不达标。过渡金属氧化物可以较好的控制产物中N2选择性,但其活性温度有一定的提高。综合来看,今后含氮化合物废气选择性催化氧化技术的研究方向需着重考虑以下问题: (1) 高活性、高N2选择性催化剂的研发。为保证废气排放中NOx达标,综合目前选择性氧化催化剂的研究趋势,应以过渡金属为主要活性组分,通过添加微量贵金属或其他氧化性较强的物质作为助剂,或选择具有一定酸性位点的分子筛等作为载体,在保证高N2选择性的同时,进一步降低目前催化剂的反应温度。 (2) 含氮化合物复杂废气的综合治理。根据实际使用场景的废气排放状况来看,含氮化合物废气中通常也含有其他挥发性有机物,如烷烃、芳烃、醇、醚等。因此,催化剂研发需考虑在其他复杂气氛下的高稳定性。若研发出一款可同时高效净化含氮化合物和烃类、醇醚类化合物的催化剂,将具有可观的市场收益。1.2 腈类含氮化合物
1.3 胺类含氮化合物
2 其他含氮化合物废气的选择氧化
3 结语与展望
