奥美拉唑肠溶胶囊HPLC含量测定方法建立研究
2020-08-13袁鹰张悦朱梦凡陈雨嫣徐薇
袁鹰,张悦,朱梦凡,陈雨嫣,徐薇
(泰州职业技术学院,江苏泰州225300)
奥美拉唑,别名洛赛克,是由一个吡啶环通过亚矾基与苯并咪唑相连而构成的苯并咪类化合物,是一种新型、高效、低毒的抗消化道溃疡药,易于在酸性环境中积聚,其能选择性地抑制胃壁细胞的H+-K+-ATP酶,从而有效地抑制胃酸的分泌。奥美拉唑的含量测定有多种方法,紫外分光光度法操作简单,但易受辅料干扰;液相色谱-质谱联用多用于多种成分同时定量;高效液相色谱法操作简单,准确性好,灵敏度高,应用最为广泛。因此,笔者建立适合奥美拉唑的高效液相色谱法(HPLC)含量测定方法。
1 仪器和材料
1.1 实验仪器
高效液相色谱仪,LC-20A,日本岛津制作所;紫外-可见分光光度计,日本岛津公司;台式pH计,上海梅特勒-托利多仪器有限公司;电子天平,Mettler AE240。
1.2 试剂与试药
奥美拉唑对照品,中国食品药品检定研究院,批号:100367-201706,含量100%;奥美拉唑肠溶胶囊,阿斯利康制药有限公司,批号J20130093,规格20 mg;乙腈、磷酸氢二钠、磷酸,色谱纯;其他试剂为分析纯。
2 方法与结果
2.1 溶液的制备
2.1.1 供试品溶液的配制
取奥美拉唑肠溶胶囊,以氯化钠的盐酸溶液(取氯化钠1 g,加盐酸3.5 mL,加水至500 mL)500 mL为溶出介质,转速100 rpm,依法操作,经120 min时,在操作容器中加入预热至37℃的0.235 mol/L磷酸氢二钠溶液400 mL,转速不变,继续依法操作,定时吸取溶出液20 mL,滤过。精密量取续滤液5 mL,精密加入0.25 mol/L氢氧化钠溶液1 mL,摇匀,作为供试品溶液。
2.1.2 对照品溶液的配制
精密称取奥美拉唑对照品约20 mg,置于100 mL量瓶中,加入乙醇10 mL溶解后,用混合溶出介质[氯化钠的盐酸溶液-溶出介质(5:4)]稀释至刻度,摇匀,精密量取5 mL,置于50 mL量瓶中,用混合溶出介质稀释至刻度,摇匀;精密量取5 mL,精密加入0.25 mol/L氢氧化钠溶液1 mL,摇匀,作为对照品溶液。
2.1.3 空白样品溶液
按处方比例制备不含奥美拉唑的空白对照样品,按2.1.2项下样品溶液的制备方法制成空白样品溶液。
2.2 色谱条件
精密量取奥美拉唑对照品溶液和空白样品溶液适量,在190~400 nm的波长范围内进行紫外光吸收图谱扫描。根据扫描结果,奥美拉唑对照品在302 nm、275 nm处有最大吸收,在253 nm、281 nm处有最小吸收,辅料不干扰测定,参考2015版《中国药典(二部)》奥美拉唑肠溶胶囊含量测定项下的检测波长,选择302 nm为测定波长。
高效液相色谱分析采用岛津LC-20A高效液相色谱系统,色谱柱采用Syncronis-C18反相色谱柱(150×4.6 nm,5 μm),流动相为0.01 mol/mL磷酸氢二钠(磷酸调节 pH 至 7.6)-乙腈(70∶30),流速 1.0 mL/min,柱温30℃,进样量20 μL,理论塔板数按奧美拉唑峰面积计算,不得低于2 000。
2.3 方法学验证
2.3.1 专属性实验
精密量取供试品、对照品以及空白样品溶液各20 μL注入色谱仪,记录色谱图,结果显示:供试品与对照品溶液的保留时间一致,空白样品溶液对奥美拉唑的测定无干扰,如图1、图2和图3所示。
2.3.2 线性关系考查
精密量取对照品溶液5 μL、10 μL、15 μL、20 μL、25 μL、30 μL注入高效液相色谱仪,记录色谱图,以奥美拉唑质量为横坐标(X),峰面积为纵坐标(Y)进行线性回归,结果表明:奥美拉唑对照品在一定范围内峰面积与质量之间线性关系良好(Y=41 262X-2 632.1,r2=1.000 0),见表1、图4。
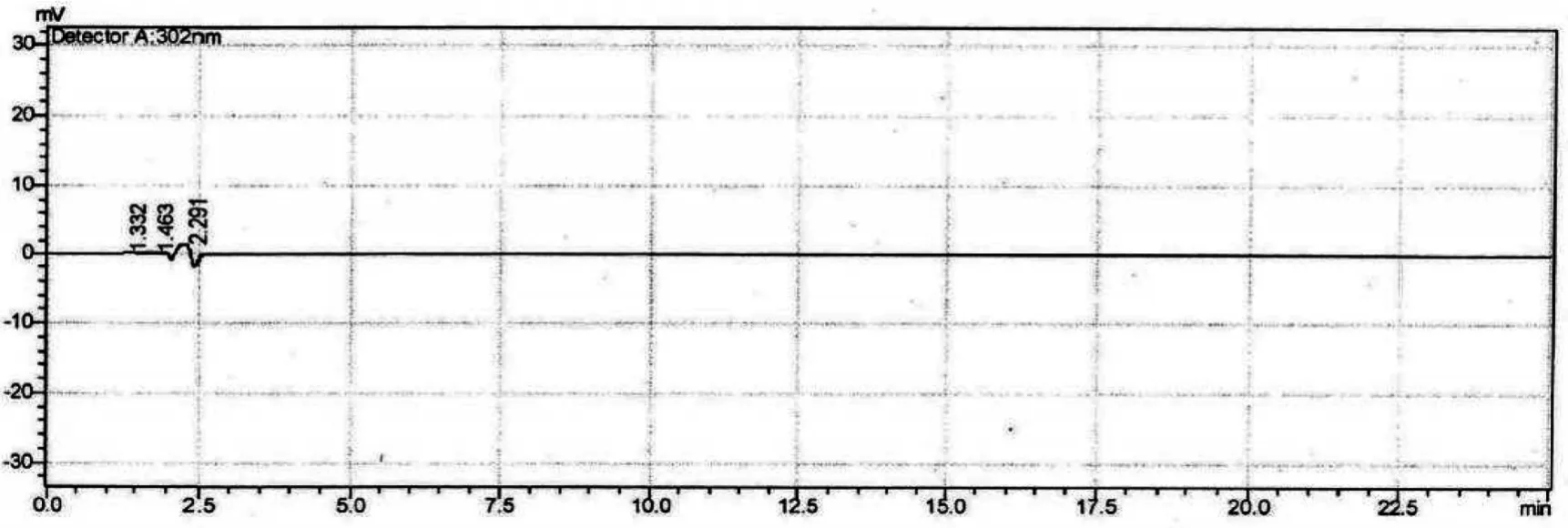
图1 空白样品溶液的HPLC色谱图
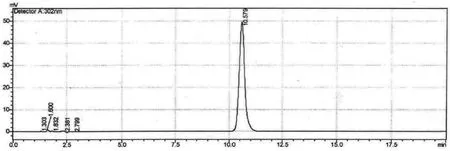
图2 供试品溶液的HPLC色谱图
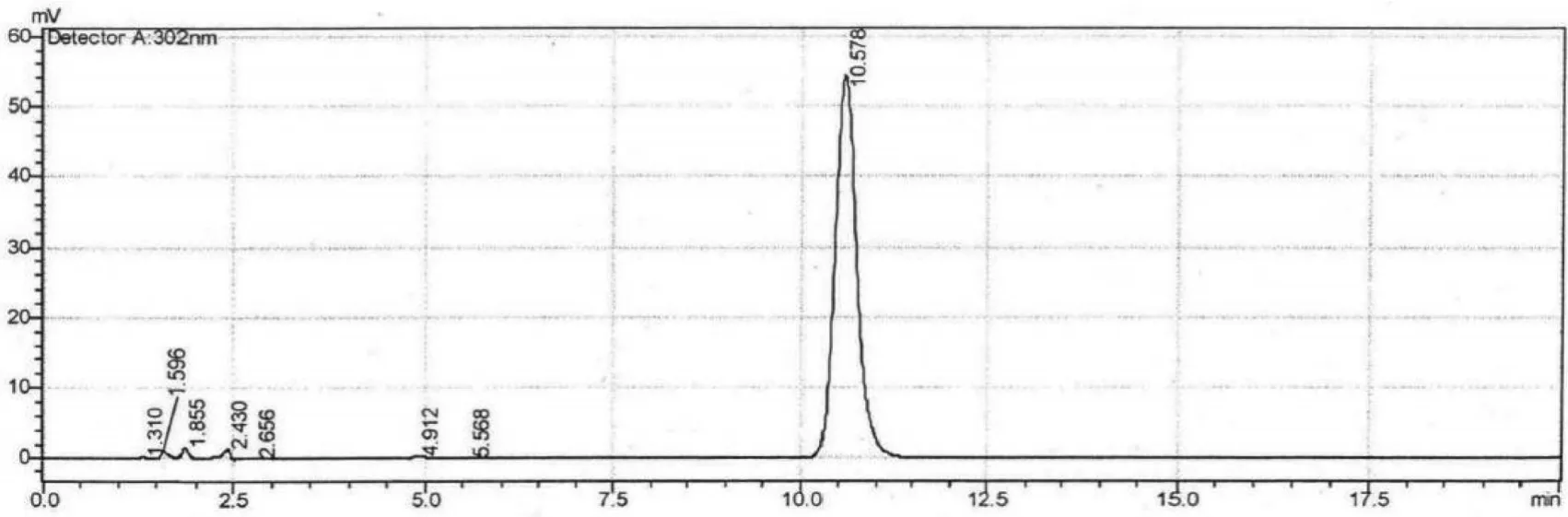
图3 对照品溶液的HPLC色谱图

表1 标准曲线及线性范围考查实验结果
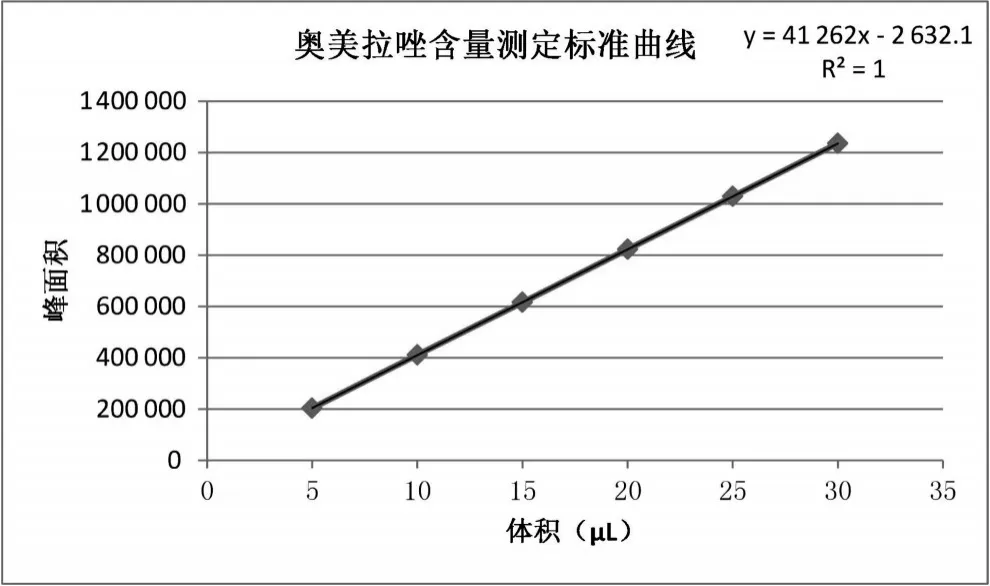
图4 奥美拉唑肠溶胶囊含量测定标准曲线
2.3.3 精密度实验
精密量取20 μL对照品溶液6个样品,记录色谱图,结果显示:6份对照品测定精密度良好,RSD为0.17%,如表2所示。
2.3.4 重复性实验
精密量取20 μL对照品溶液注入高效液相色谱仪,测定6个样品,记录色谱图,实验结果表明,此方法重复性良好,如表3所示。
2.3.5 回收率实验
精密称取奥美拉唑20 mg置于100 mL容量瓶中,加入乙醇20 mL、磷酸盐缓冲液(pH=11.0)约60 mL,超声处理使奥美拉唑溶解,用pH=11.0的磷酸盐缓冲液稀释至刻度,摇匀,过滤。精密量取续滤液1 mL,置于10 mL量瓶中,用pH=11.0的磷酸盐缓冲液稀释至刻度,摇匀,作为100%比例的供试品溶液。同法,分别称取奥美拉唑16.00 mg、24.00 mg,配制成80%、120%2个浓度的溶液,每个浓度各3份样,另精密称取奥美拉唑对照品20 mg,同法配制对照品溶液。量取20 μL配制好的样品注入高效液相色谱仪,记录色谱图,按外标法以峰面积计算含量,将实测值和理论值比较,计算回收率分别为99.7%、99.5%和99.6%,RSD分别为0.9、0.6和0.8,表明该测定方法的准确度良好,能够准确反映制剂中奥美拉唑的真实含量,如表4所示。

表2 精密度测定结果(n=6)

表3 重复性实验结果(n=6)
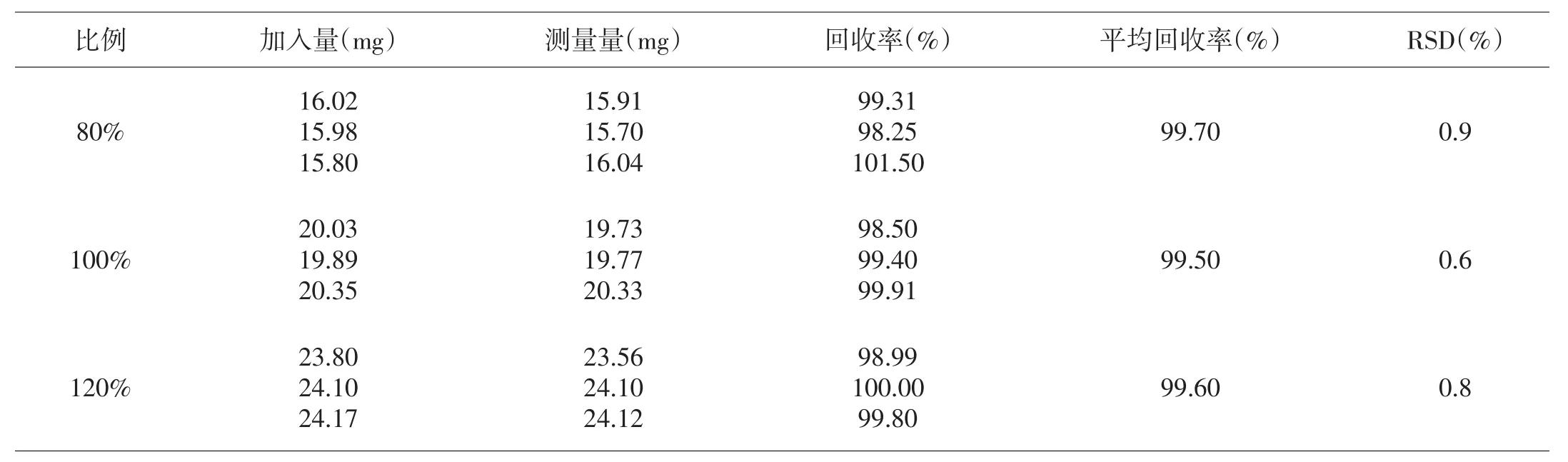
表4 回收率实验测定结果(n=3)

表5 溶液稳定性实验测定结果
2.3.6 耐用性实验
将对照品溶液放置于室温环境中,分别在放置0 h、2 h、4 h、6 h、8 h时取样20 μ L注入色谱仪中,结果表明,奥美拉唑溶液在8 h内测定色谱峰面积无明显变化,待测组分化学性质稳定,如表5所示。
2.4 样品的测定
取奥美拉唑肠溶胶囊样品,按2.1项下样品溶液及对照品溶液的制备方法操作,精密量取样品溶液和对照品溶液各20 μL,按照上述色谱条件进行测定,记录峰面积,按外标法计算样品含量,结果显示,样品的含量为99.88%,RSD(n=6)为0.20%。
3 结论
奥美拉唑原辅料相容性研究、含药丸芯上药率、肠溶微丸的含量测定等研究内容均需对主成分奥美拉唑进行定量分析,高效液相色谱法由于操作简单,准确性好,灵敏度高,应用最为广泛。笔者通过本文建立的高效液相色谱法,经过方法学验证,所建立的含量测定方法灵敏度高,专属性好,准确度和精密度均符合要求,可以用于奥美拉唑的含量测定。
