纳洛酮对蛛网膜下腔出血大鼠海马区神经细胞自噬的影响
2020-08-07李小亮李君李林孙林林陈扬付爱军
李小亮,李君,李林,孙林林,陈扬,付爱军
作者单位:1华北理工大学附属医院神经外科,河北 唐山063000;2开滦总医院林西医院神经外科,河北 唐山063000;3郑州市第七人民医院神经外科,河南 郑州450000
自发性蛛网膜下腔出血(SAH)是严重威胁人类健康的一种疾病,由于其发病突然、变化迅猛,给救治带来很大的挑战,绝大多数SAH为动脉瘤破裂所致[1],据不完全统计SAH发病率约为每年10.5∕10万人口[2],并且呈逐年上升趋势。随着显微脑血管外科、高分辨率影像后处理技术、麻醉理论及血管内介入水平的不断发展及提高,其病死率较前有所下降,但致残率一直处于较高水平[3],治疗后大概33%的SAH病人遗留严重的神经功能缺失并需长期护理[4],给病人和家庭带来沉重的经济负担以及身心上的双重创伤[5]。既往的学者认为,导致SAH病人神经功能缺失的主要因素为脑血管痉挛(CVS)[6],但是应用药物拮抗CVS的发生后,并未显著改善SAH病人的神经功能缺失。近年来文献报道,应用药物或其它措施对SAH早期脑损伤的尽早干预,可以减轻神经功能缺失[7]。目前对SAH早期脑损伤的机制研究中,自噬被广泛关注,适当活化的自噬可以减轻大鼠SAH模型早期脑损伤的损害性发展,从而保护神经功能[8]。纳洛酮注射液是阿片类受体阻滞剂,在临床上普遍使用,并取得了不错的疗效。有研究报道纳洛酮注射液在治疗SAH所致的脑损伤方面具有积极的意义[9],但相关机制尚不明确。
本研究于2016年10月至2018年10月采取刺破颈内动脉的方法制作SAH大鼠模型,观察纳洛酮注射液对大鼠行为学功能及自噬相关蛋白Beclin-1及微管相关蛋白1轻链3(LC3-Ⅱ)的影响,探讨纳洛酮注射液对SAH的可能作用机制,为临床治疗提供丰富的基础医学支持。
1 材料与方法
1.1材料
1.1.1 实验动物 108只健康雄性清洁级SD大鼠,周龄范围为9~12周,体质量(350±30)g,购于北京华阜康生物科技股份有限公司,生产许可证号SCXK(京)2014-0004。饲养于华北理工大学动物实验中心动物饲养室,正常通风光照,维持室温于(23±2)℃,湿度控制于(50±15)%,自由活动并正常饮水进食,避免不良刺激。在实验开始前1周进行环境适应。采用随机数字表法将108只大鼠分为三组,依次为假手术组、SAH组、纳洛酮组,每组36只,并相应做好标记,每组再依次分为6 h、24 h、72 h三个亚组,每个亚组12只。本研究符合一般动物实验伦理学原则。
1.1.2 药物和试剂 纳洛酮注射液(1 mL∶0.4 mg);Beclin-1(ABclonal生物技术有限公司)和LC3-Ⅱ抗体(GeneTex生物技术有限公司);内参微管蛋白(tubulin)(美国Abcam公司);二抗及显色用品(美国KPL公司)。
1.1.3 主要仪器 820-Ⅱ型切片机(德国Leica公司);OLYMPUS摄像显微镜(日本奥林巴斯公司);凝胶成像分析系统;图像采集及分析系统。
1.2方法
1.2.1 模型建立 根据文献采用颈动脉刺破法制作SAH大鼠模型[10]:腹腔内注射10%水合氯醛(300 mg∕kg)麻醉大鼠,刺激无反应后将其仰卧并固定,颈部术前无菌处理,纵行剪开,沿组织间隙进行分离,暴露并解剖颈总动脉及颈内外动脉,远心端扎闭并剪断颈外动脉,牵拉使其与颈内动脉进入颅内的方向一致,将锐化并标记好的纤芯自远心端穿入颈外动脉并沿颈内动脉直至颅内,刺破血管,造成SAH模型。然后将伤口消毒后缝合,正常饲养。以取脑时环池、基底池有血凝块为模型制备成功的标准。假手术组只将纤芯沿血管穿入颅内,避免刺穿血管,其它操作步骤与SAH组相同。
1.2.2 给药方法 纳洛酮组刺破颅内血管后立即给予腹腔内注射纳洛酮注射液(1 mg∕kg),每12小时1次,用药至处死的各时相点。假手术组和SAH组采用同样方法给予同等体积的0.9%氯化钠溶液。
1.2.3 穿梭箱实验 各组实验大鼠于造模前2 d开始进行训练,每天练习2次,以培养条件反射。术后于预设时间,首先在穿梭箱内让实验大鼠进行环境适应5 min,达到去除条件反射的目的,然后给予5 s声光刺激,再给予20 s电刺激(电击强度30 V,50 Hz)。观察大鼠的逃避情况,每间隔20 s训练1次,共计30次。视频分析实验大鼠的逃避情况。统计逃避次数及逃避反应时间(大鼠受到刺激至逃到安全区的平均次数与时间)。
1.2.4 苏木精-伊红(HE)染色于造模成功后的各个时间点,采取腹腔内注射10%水合氯醛(300 mg∕kg)将大鼠深度麻醉,待其无反应后进行左心室穿刺灌注,先灌注0.9%氯化钠溶液500 mL、再灌注4%多聚甲醛250 mL,在冰上解剖取出脑组织,并置于4%多聚甲醛中固定3 d。对固定好的脑组织进行常规石蜡包埋,层厚5μm做连续冠状位切片(包含海马组织),每只大鼠脑标本蜡块取3张进行HE染色。光学显微镜(×400)观察海马CA1区神经细胞形态及结构,按随机数字表法保存6个不同视野的照片,并用Motic-6.0分析系统统计结构无异常的神经细胞数量。
1.2.5 免疫组织化学染色 每只大鼠脑标本蜡块取6张切片,进行常规脱蜡、水化、高压修复、室温孵育。按随机数字表法等分成2组,一组滴加Beclin-1抗体(1∶100),另一组滴加LC3-Ⅱ抗体(1∶100),将滴加抗体的切片放入4℃冰箱过夜(超过12 h),滴加组化二抗,孵育、脱水、透明、显色、封固。光学显微镜(×400)观察海马CA1区神经细胞,按随机数字表法保存6个不同视野的照片,并用Motic-6.0分析系统统计阳性细胞数量。
1.3统计学方法使用Excel 2007收集计量资料,所得数据以xˉ±s表示,使用SPSS17.0软件进行单因素方差分析,采用LSD-t检验进行多组间的两两比较。显著性水平α=0.05。
2 结果
2.1穿梭箱实验与假手术组对比,SAH组6 h、24 h、72 h大鼠躲到安全区的次数均减少,躲到安全区的时间均延长(P<0.05);与SAH组对比,纳洛酮组6 h、24 h、72 h躲到安全区的次数均增多,躲到安全区的时间均缩短(P<0.05)。见表1,2。
表1各组大鼠各时间点逃避反应次数比较∕(次±s)

表1各组大鼠各时间点逃避反应次数比较∕(次±s)
注:与假手术组比较,a P<0.05;与SAH组比较,b P<0.05,SAH为蛛网膜下腔出血
组别假手术组SAH组纳洛酮组F值P值鼠数36 36 36 6 h 24.83±3.24 14.41±1.98a 16.50±1.93b 60.282 0.000 24 h 25.33±2.64 16.25±2.18a 19.25±2.30b 45.317 0.000 72 h 25.16±2.82 18.33±2.57a 22.50±2.20b 22.017 0.000
表2各组大鼠各时间点逃避反应时间比较
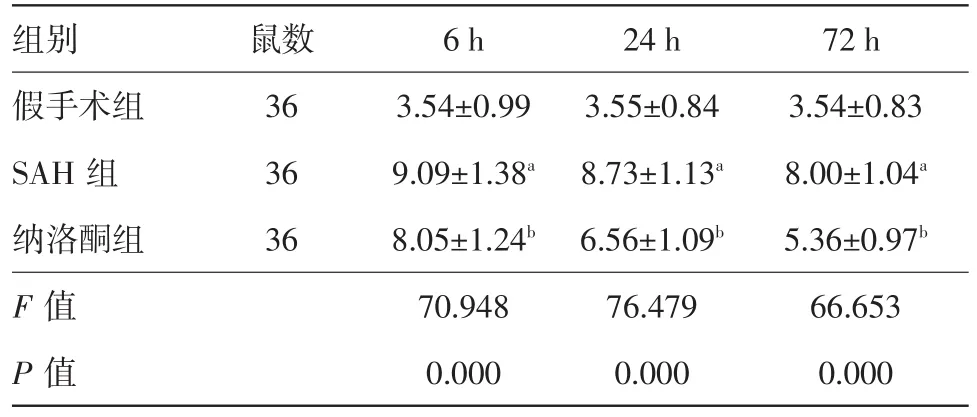
表2各组大鼠各时间点逃避反应时间比较
注:与假手术组比较,a P<0.05;与SAH组比较,b P<0.05,SAH为蛛网膜下腔出血
组别假手术组SAH组纳洛酮组F值P值鼠数36 36 36 6 h 3.54±0.99 9.09±1.38a 8.05±1.24b 70.948 0.000 24 h 3.55±0.84 8.73±1.13a 6.56±1.09b 76.479 0.000 72 h 3.54±0.83 8.00±1.04a 5.36±0.97b 66.653 0.000
2.2 HE染色假手术组6 h、24 h、72 h海马CA1区神经细胞绝大部分形态正常,细胞质均一,细胞核结构完整,染色适中。SAH组海马CA1区神经细胞情况:6 h亚组镜下显示少量细胞的细胞核染色加深、梭形固缩;24 h亚组细胞核深染、梭形固缩情况明显增多,并出现核破碎;72 h亚组细胞核深染、梭形固缩、核破碎情况进一步加剧。纳洛酮组对比SAH组,6 h、24 h、72 h细胞核深染、梭形固缩、核破碎等情况均相对减少。见表3。
2.3免疫组织化学染色选取自噬的特异性标志物Beclin-1和LC3-Ⅱ,经染色及显色后,胞质中出现棕黄、黄褐色颗粒样物质既表明该细胞发生了自噬。假手术组各个时间点可见少数细胞阳性表达。SAH组:6 h亚组胞质中出现棕黄、黄褐色颗粒样物质的细胞数较假手术组增多;24 h亚组细胞质中出现棕黄、黄褐色颗粒样物质的细胞数明显增多;72 h亚组细胞质中出现棕黄、黄褐色颗粒样物质的细胞数仍很多。纳洛酮组各个时间点细胞质中出现棕黄、黄褐色颗粒样物质的细胞数均比SAH组各个时间点增多。见表4,5。
表3 各组各时间点大鼠海马区结构无异常的神经细胞数量∕个,(±s)
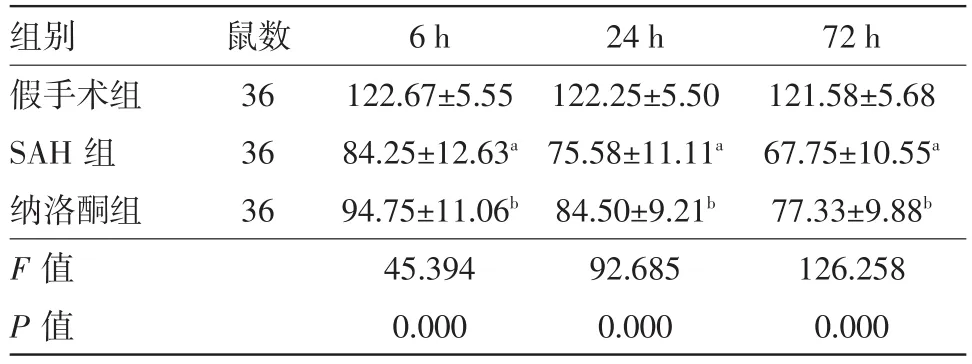
表3 各组各时间点大鼠海马区结构无异常的神经细胞数量∕个,(±s)
注:与假手术组比较,a P<0.05;与SAH组比较,b P<0.05,SAH为蛛网膜下腔出血
组别假手术组SAH组纳洛酮组F值P值鼠数36 36 36 6 h 122.67±5.55 84.25±12.63a 94.75±11.06b 45.394 0.000 24 h 122.25±5.50 75.58±11.11a 84.50±9.21b 92.685 0.000 72 h 121.58±5.68 67.75±10.55a 77.33±9.88b 126.258 0.000
表4 各组各时间点大鼠海马区Beclin-1蛋白阳性细胞数量∕(个,ˉ±s)
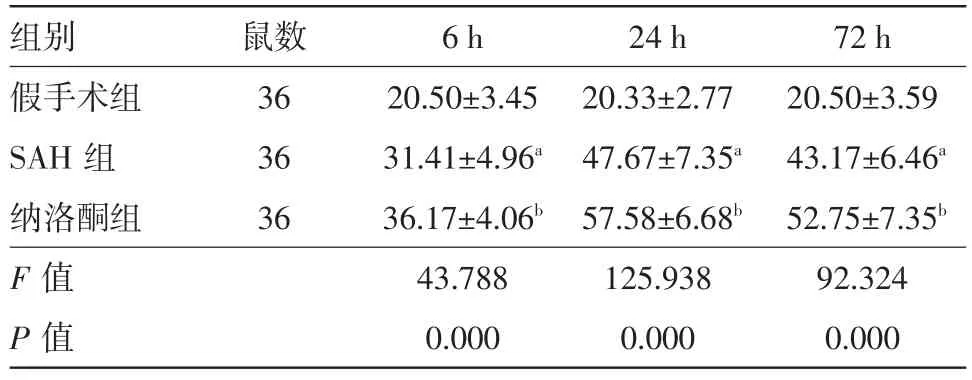
表4 各组各时间点大鼠海马区Beclin-1蛋白阳性细胞数量∕(个,ˉ±s)
注:与假手术组比较,a P<0.05;与SAH组比较,b P<0.05,SAH为蛛网膜下腔出血
组别假手术组SAH组纳洛酮组F值P值鼠数36 36 36 6 h 20.50±3.45 31.41±4.96a 36.17±4.06b 43.788 0.000 24 h 20.33±2.77 47.67±7.35a 57.58±6.68b 125.938 0.000 72 h 20.50±3.59 43.17±6.46a 52.75±7.35b 92.324 0.000
表5 各组各时间点大鼠海马区LC3-II蛋白阳性细胞数量∕(个ˉ±s)
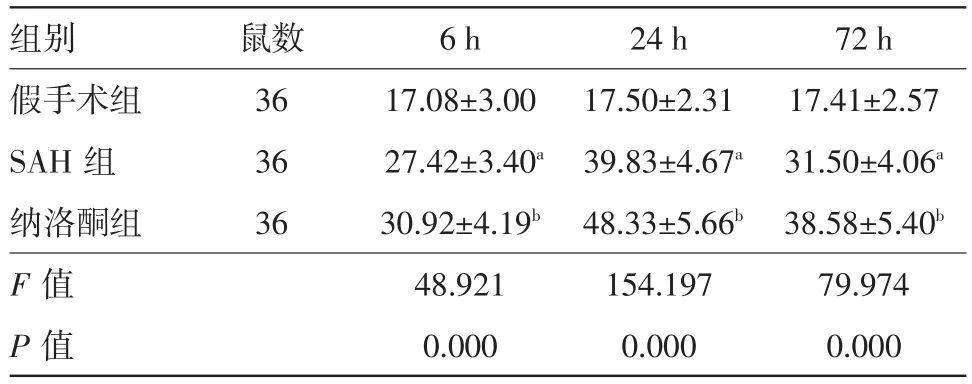
表5 各组各时间点大鼠海马区LC3-II蛋白阳性细胞数量∕(个ˉ±s)
注:与假手术组比较,a P<0.05;与SAH组比较,b P<0.05,SAH为蛛网膜下腔出血
组别假手术组SAH组纳洛酮组F值P值鼠数36 36 36 6 h 17.08±3.00 27.42±3.40a 30.92±4.19b 48.921 0.000 24 h 17.50±2.31 39.83±4.67a 48.33±5.66b 154.197 0.000 72 h 17.41±2.57 31.50±4.06a 38.58±5.40b 79.974 0.000
3 讨论
纳洛酮注射液作为经典的阿片类受体阻滞剂,具有很高的脂溶性,能够很好地透过血脑屏障进而作用于中枢神经系统。纳洛酮注射液最早在临床上应用是能够对抗阿片类药物复合麻醉恢复期或阿片类药物过量所致的呼吸功能减弱[11]。随着对病理生理学认识的不断深入,学者们检测到急性颅脑损伤病人和脑损伤模型动物的脑组织内内源性阿片肽(β-内啡肽和强啡肽等)的数值均显著上升,内源性阿片肽的毒性作用会导致神经细胞损害的进一步加重[12]。纳洛酮注射液可阻断内源性阿片肽的毒性作用进而可以减轻脑水肿、降低颅内压、改善脑代谢,并可以逆转呼吸抑制[13]。临床试验亦表明纳洛酮注射液对SHA病人[8]、高血压脑出血病人[14]、重度颅脑损伤病人[15]、急性脑梗死病人[16]均具有脑保护作用。研究显示,SAH模型大鼠的行为能力及其海马CA1区神经细胞会受到损害,其可能的原因被认为是SAH后脑组织及蛛网膜下腔内源性阿片肽含量增多,导致神经细胞损伤[13]。
自噬是真核细胞的程序性死亡方式之一,也是细胞面对损伤性刺激的自我保护机制[17]。通过溶酶体蛋白降解途径能够有效地清除受损的细胞器和细胞内的毒性物质,并能够为蛋白质的合成和细胞器的更新提供相应的原料,通过上述反应的发生可以很好地保持细胞的功能及结构,进而达到对抗损伤性刺激的目的[18]。在一定程度内发生的自噬可以有效地稳定细胞功能并能够降低致死率;自噬程度不足则会损伤细胞功能与结构,进而导致损伤性结果的发生[19]。既往学者实验结果显示,给予SAH动物模型药物处理能够在一定程度上增强实验动物海马区神经细胞自噬,经检测胞内出现自噬相关蛋白Beclin-1及LC3-Ⅱ的细胞数量升高,神经细胞死亡明显减少[20];应用药物降低自噬程度后,在一定程度上增加了细胞致死率[21]。
现阶段对于纳洛酮注射液对SAH神经保护作用的文献报道主要在临床,基础实验很少,在自噬方面的实验结果鲜有报道。该实验经过精心设计,参考文献采取颅内动脉刺破法制作SAH大鼠模型,并给予SAH大鼠药物干预,结果显示SAH后大鼠行为学功能减退,胞内出现自噬相关蛋白Beclin-1及LC3-Ⅱ的细胞数量升高,给予纳洛酮注射液处理后行为学功能得到改善,胞内出现自噬相关蛋白Beclin-1及LC3-Ⅱ的细胞数量进一步升高,这与以往相关文献[22]报道一致。
通过以上实验,我们得到结论,纳洛酮注射液能够恢复SAH大鼠的行为学功能,其机制可能是在一定程度上增强了SAH大鼠海马区神经细胞自噬,稳定了细胞的结构与功能。纳洛酮注射液对SAH的神经保护功效,涉及相当复杂的分子机制,尚需学者不断努力、深入探讨。
