帕金森病不同运动障碍亚型的临床特征比较
2020-08-06庞坚信黄沛钰王冬女黄善强刘素芝
庞坚信 黄沛钰 王冬女 黄善强 刘素芝
[摘要] 目的 比較不同运动障碍亚型帕金森病患者的临床特征,提高对帕金森病运动障碍的认识。 方法 收集帕金森病患者76例,据统一帕金森病评估量表(UPDRS)评分分为震颤为主型PD(TD-PD)组19例、姿势异常步态障碍为主型PD(PIGD-PD)组47例和不确定型PD组10例,记录所有PD患者年龄、性别、受教育程度、病程、起病年龄、起病部位、UPDRS评分、改良Hoehn-Yahr分期评分、简易精神状态监测量表(MMSE)评分、蒙特利尔认知量表(MoCA)评分、老年抑郁量表(GDS-15)评分、汉密尔顿焦虑量表(HAMA)评分、汉密尔顿抑郁量表(HAMD)评分、生活质量量表(PDQ-8)评分、Berg平衡量表(BBS)评分、冻结步态量表(NFOG-Q)评分、便秘临床评分量表(CCS)评分和便秘生活质量量表(PAC-QOL)评分,统计分析TD-PD组和PIGD-PD组临床特征的差异。 结果 性别构成在两组之间存在显著性差异(P<0.05),TD-PD组男性较多,而PIGD-PD组女性较多。两组患者UPDRS-Ⅰ、UPDRS-Ⅱ、改良Hoehn-Yahr分期、GDS-15、HAMA、HAMD、BBS、NFOG-Q、PAC-QOL评分均存在显著性差异(P<0.05)。 结论 帕金森病不同运动障碍亚型之间存在明显的异质性,提高对运动障碍亚型的认识利于分组诊治。
[关键词] 帕金森病;震颤;姿势异常步态障碍;运动障碍亚型;临床特征
[中图分类号] R742.5 [文献标识码] A [文章编号] 1673-9701(2020)16-0017-04
Comparison of clinical characteristics of Parkinson's disease with different dyskinesia subtypes
PANG Jianxin1 HUANG Peiyu2 WANG Dongnv1 HUANG Shanqiang1 LIU Suzhi1
1.Taizhou Hospital of Zhejiang Province, Linhai 317000, China; 2.The Second Affiliated Hospital of Zhejiang University School of Medicine, Hangzhou 310009, China
[Abstract] Objective To compare the clinical characteristics of patients with different dyskinesia subtypes of Parkinson's disease and improve their understanding of Parkinson's disease with dyskinesia. Methods A total of 76 patients with Parkinson's disease were collected and divided into tremor dominant PD (TD-PD) group (n=19), posture instability and gait disorder(PIGD-PD)group (n=47) and uncertain PD group (n=10), according to the unified Parkinson's disease rate scale (UPDRS) score. All PD patients' age, gender, education level, course of disease, age of onset, location of onset, UPDRS score, modified Hoehn-Yahr stage score, mini-mental state examination(MMSE)score, Montreal cognitive assessment (MoCA) score, Geriatric depression scale (GDS-15) score, Hamilton anxiety scale (HAMA) score, Hamilton depression scale(HAMD) score, Parkinson's disease quality of life scale(PDQ-8) score, Berg balance scale(BBS) score, frozen gait scale(NFOG-Q) score, constipation clinical score scale(CCS) score, and constipation quality of life scale(PAC-QOL) score were recorded. The differences in clinical characteristics between the TD-PD group and the PIGD-PD group were statistically analyzed. Results There was a significant difference in gender composition between the two groups(P<0.05). There were more males in the TD-PD group and more females in the PIGD-PD group. There were significant differences in UPDRS-Ⅰ,UPDRS-Ⅱ, modified Hoehn-Yahr staging, GDS-15, HAMA, HAMD, BBS,NFOG-Q, and PAC-QOL scores between the two groups(P<0.05). Conclusion There are obvious heterogeneity among different dyskinesia subtypes in Parkinson's disease. Improving the understanding of dyskinesia subtypes is helpful for group diagnosis and treatment.
[Key words] Parkinson's disease; Tremor; Posture instability and gait disorder; Dyskinesia subtype; Clinical characteristics
帕金森病(Parkinsons disease,PD)是一种常见于中老年人的慢性进展性中枢神经系统退行性疾病,在我国65岁以上人群的患病率为1700/10万,且随着年龄的增加而增加[1,2]。我国逐步进入到老年化社会,PD患者会越来越多,给家庭和社会带来沉重的负担。PD主要运动症状为运动迟缓(bradykinesia)、肌强直(rigdity)、静止性震颤(static tremor)和姿势步态障碍(postural instability gait difficulty),并伴随不同的非运动症状(non-motor symptoms,NMS),如嗅觉减退、抑郁、便秘、白天过度嗜睡等[1,3]。研究发现,不同患者其运动症状存在明显的不同,即有的患者以震颤为主要表现,而有的患者以姿势异常步态障碍为主要表现,以两种不同运动障碍为主要表现的患者在起病年龄、疾病进展速度、对多巴胺替代药物治疗的反应性及伴随的非运动症状等方面存在明显的异质性[4,5]。但目前关于PD不同运动障碍亚型的临床特征方面报道较少,且部分结果之间存在差异[6]。本研究选择浙江省台州医院2017年9月~2018年6月收治的76例PD患者,比较不同运动障碍亚型PD患者临床特征的差异,以提高对PD运动障碍亚型的认识,现报道如下。
1 资料与方法
1.1 一般资料
收集我院神经内科收治的PD患者76例,男41例,女35例,平均年龄(64.83±10.04)岁。入选标准如下:(1)PD诊断符合中华医学会神经病学分会帕金森病及运动障碍学组在《中华神经科杂志》刊发的“中国帕金森病的诊断标准(2016版)”[3]。(2)未进行过脑深部电刺激术(DBS)者[7]。(3)排除继发性帕金森综合征和帕金森叠加综合征者[8]。
在患者停药12 h后进行UPDRS评分、改良Hoehn-Yahr分期评分、简易精神状态监测量表(MMSE)评分、蒙特利尔认知量表(MoCA)评分、老年抑郁量表(GDS-15)评分、汉密尔顿焦虑量表(HAMA)评分、汉密尔顿抑郁量表(HAMD)评分、生活质量量表(PDQ-8)评分、Berg平衡量表(BBS)评分、冻结步态量表(NFOG-Q)评分、便秘临床评分量表(CCS)评分和便秘生活质量量表(PAC-QOL)评分,并记录患者的年龄、性别、受教育年限、病程、起病年龄、起病部位等病史信息。本研究通过医院伦理委员会审查,每位患者均签署知情同意书。
1.2 方法
根据UPDRS评分中震颤评分和姿势异常步态障碍评分将患者分为震颤为主型PD(TD-PD)组、姿势异常步态障碍为主型PD(PIGD-PD)组和不确定型PD组。具体标准如下[5,9,10]:记录UPDRS第二部分16项、第三部分20项及21项里共8条震颤评分,计算平均震颤评分;记录UPDRS第二部分13、14、15项和第三部分29、30项里共5条姿势异常步态障碍评分,计算平均姿势异常步态障碍评分。计算平均震颤评分和平均姿势异常步态障碍评分比值,当比值>1.5则定为TD-PD,当比值<1.0则定为PIGD-PD,介于1~1.5之间则定为不确定型PD。若震颤评分不为0,而姿势异常步态障碍评分为0,则定为TD-PD;若震颤评分为0,而姿势异常步态障碍评分不为0,则定为PIGD-PD;若两者评分均为0,则定为不确定型PD[9]。
1.3 统计学方法
利用统计学软件SPSS 22.0对数据进行处理和分析。数据符合正态分布者以均数±标准差(x±s)表示;偏态分布者以中位数(四分之一位数,四分之三位数)表示,即M(P25,P75)。数据组间平均数比较则根据数据分布类型选择成组t检验或Mann-Whitney U检验。计数资料以相对数(构成比或率,%)表示,采用χ2检验或Fisher确切概率法。P<0.05为差异有统计学意义。
2 结果
2.1 TD-PD组和PIGD-PD组病史资料比较
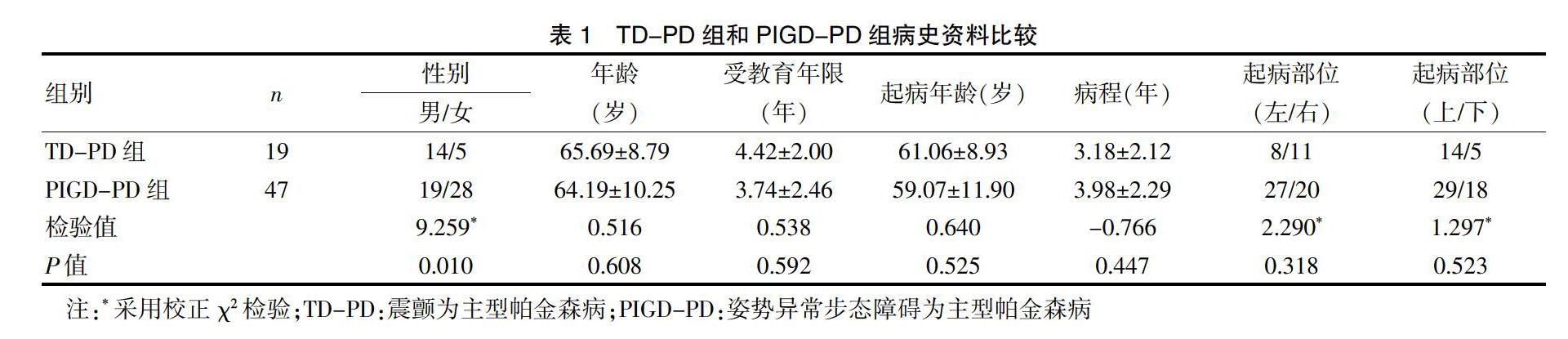
76例患者中TD-PD组19例,PIGD-PD组47例,不确定型PD组10例。TD-PD组和PIGD-PD组一般资料比较见表1。比较发现,性别构成在两组之间存在显著性差异(P<0.05),TD-PD组男性较多,而PIGD-PD组女性较多。两组患者的年龄、受教育年限、起病年龄、病程和起病部位均无显著性差异(P>0.05)。
2.2 TD-PD组和PIGD-PD组临床量表评分比较
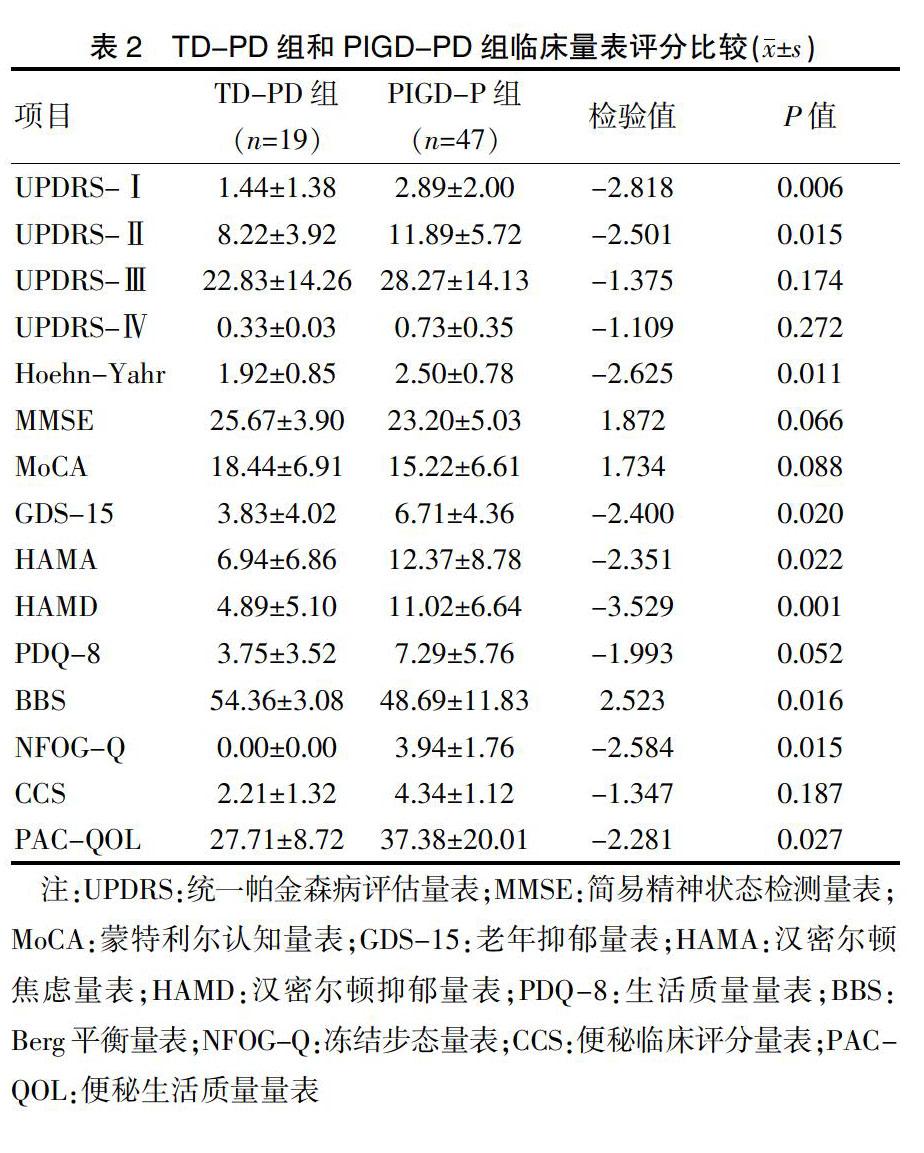
两组患者UPDRS-Ⅰ、UPDRS-Ⅱ、改良Hoehn-Yahr分期、GDS-15、HAMA、HAMD、BBS、NFOG-Q、PAC-QOL评分均有显著性差异(P<0.05),具体表现为与TD-PD组比较,PIGD-PD组的UPDRS-Ⅰ、UPDRS-Ⅱ、改良Hoehn-Yahr分期、GDS-15、HAMA、HAMD、NFOG-Q、PAC-QOL评分升高,BBS评分降低。两组患者的UPDRS-Ⅲ、UPDRS-Ⅳ、MMSE、MoCA、PDQ-8、CCS評分无显著性差异(P>0.05)。见表2。
3 讨论
PD是一种复杂的中枢神经系统退行性疾病,临床症状包括一系列运动症状和非运动症状。PD诊断的前提是确立存在帕金森综合征,即基于3个核心运动症状:必备运动迟缓和至少存在静止性震颤或肌强直2项症状中的1项,且上述症状必须是显而易见的[3]。运动症状在不同患者中表现不同,即有的患者以震颤为主,而有的患者以肌强直为主。除运动症状外,多数患者伴随的非运动症状也存在明显差别,而不同的非运动症状又是加重患者运动功能损伤、降低患者生活质量和缩短预期寿命的重要因素[6]。因此,多样化的运动症状和非运动症状表明PD具有明显的异质性,对PD进行分组研究具有重要意义。目前,根据PD不同临床表现进行分组的研究越来越多,分组有助于理解不同症状的发病机制,预测不同亚型的病程和预后,为PD的精准诊疗提供依据[11,12]。
既往研究者对PD的分组主要有:以起病年龄划分为早发型和晚发型[13];以主要运动障碍表现分为震颤为主型、姿势异常步态障碍为主型和不确定型;以伴随的非运动症状分组,如便秘组和非便秘组、伴认知障碍组和不伴认知障碍组[14]等。本研究根据统一帕金森病评估量表(Unified parkinsons disease rating scale,UPDRS)对患者进行较为准确的病情评估,以平均震颤评分和平均姿势异常步态障碍评分的比值来界定患者属于哪种亚型,该方法对于区分两种运动障碍亚型具有很高的敏感性和特异性[5]。本研究纳入的76例患者,按平均震颤评分和平均姿势异常步态障碍评分的比值划分为TD-PD组19例、PIGD-PD组47例和不确定型PD组10例,重点讨论TD-PD组和PIGD-PD组临床特征的差异,以加深对两种运动障碍亚型的认识。
就一般病史资料而言,本研究发现性别构成在两组之间存在显著性差异,TD-PD组男性较多,而PIGD-PD组女性较多。患者年龄、受教育年限、起病年龄、病程和起病部位均无显著性差异。PD的总体发病率男性较女性稍高,但在不同运动障碍亚型之间男女发病率之间的差异既往文献报道较少,本研究发现男性PD患者的运动障碍多以震颤为主,而女性PD患者则多以姿势异常步态障碍为主,这对于揭示性别因素在运动障碍亚型中的影响具有重要意义。Wickremaratchi MM等[15]以起病年龄分组研究PD运动障碍亚型,该研究发现晚发型PD多以姿势异常步态障碍为主要表现,这与本研究结果不一致,本研究以运动障碍亚型分组尚未发现起病年龄在两组之间有差异。该研究中晚发型患者起病年龄定为超过64岁,早发型患者起病年龄定为低于45岁,两组之间年龄跨度较大,而本研究76例患者平均起病年龄为60岁左右,起病年龄均较大,可能由于样本含量较低,起病年龄较低的患者样本含量不足而达不到统计效果,因此未来应继续增大样本含量。受教育程度、病程以及起病部位等因素往往与PD非运动症状有关,本研究以运动障碍进行分组,尚未发现其在两种运动障碍亚型之间存在差异。
临床上有一系列检查量表可用于PD病程分期、运动症状和非运动症状的评估以及PD患者的生活质量评估等,通过这些量表可以较为准确地进行量化研究。统一帕金森病评估量表(UPDRS)是国际上公认的且最为常用的检查量表[9],它有五个部分:第一部分(UPDRS-Ⅰ)是对精神、行为和情绪进行评估;第二部分(UPDRS-Ⅱ)是对日常生活活动进行评估;第三部分(UPDRS-Ⅲ)是对运动检查进行评估;第四部分(UPDRS-Ⅳ)是对治疗的并发症进行评估;第五部分(UPDRS-Ⅴ)也就是改良Hoehn-Yahr分期,通过这五个部分可以对PD患者日常生活能力、疾病发展速度、治疗后副作用和并发症情况进行准确而全面的评估,具有较高的可信度和效度[16]。本研究发现TD-PD组和PIGD-PD组在UPDRS-Ⅰ和UPDRS-Ⅱ及改良Hoehn-Yahr分期(UPDRS-Ⅴ)评分存在显著性差异,与TD-PD组比较,PIGD-PD组三个量表评分均升高,说明以姿势异常步态障碍为主要运动障碍的PD患者精神、行为、情绪和日常生活能力受影响较重,疾病严重程度更高,这一结果与仲玲玲等[17]的研究结果一致。
PD患者的非运动症状非常常见,约98.6%的患者存在非运动症状[11],且非运动症状严重影响着PD患者预后和生活质量[8]。非运动症状检查量表被广泛地应用于PD患者非运动症状的筛查和评估中,临床上常用的有简易精神状态监测量表(MMSE)、蒙特利尔认知量表(MoCA)、老年抑郁量表(GDS-15)、汉密尔顿焦虑量表(HAMA)、汉密尔顿抑郁量表(HAMD)、便秘临床评分量表(CCS)、便秘生活质量量表(PAC-QOL)评分等,可以对PD患者精神状态、认知功能、抑郁或焦虑及便秘情况等非运动症状进行评估[18]。本研究发现,PIGD-PD组GDS-15、HAMA、HAMD、PAC-QOL评分均较TD-PD组高,说明以姿势异常步态障碍为主要运动障碍表现的PD患者出现抑郁、焦虑和便秘更多,且对生活质量的影响更大。这与仲玲玲等[17]和Ba F等[19]的研究结果一致。
近年来,神经影像在PD不同运动障碍亚型的研究越来越受到关注[4,20]。脑铁沉积在PD发病机制中的作用得到病理和神经影像的双重认证,特别是黑质致密部(substantianigracompacta,SNc)铁沉积被认为是PD发病的基础,过量铁沉积造成氧自由基生成过多,从而引起多巴胺能神经元进行性凋亡、消失,黑质-纹状体通路多巴胺递质浓度下降,最后表现为运动迟缓、肌强直等PD临床表现。王波等[20]通过ESWAN成像研究脑内神经核团R2*值在不同运动障碍亚型之间的差异,发现TD-PD组和PIGD-PD组红核、黑质致密部R2*值存在显著性差异,提示两组之间存在脑内核团铁沉积的差异。沈柏等[4]通过静息态功能磁共振成像(rest-fMRI)研究不同运动障碍亚型帕金森病患者之间基于丘脑底核的功能连接差异脑区,发现在不同类型的帕金森病患者中,基于丘脑底核的功能連接差异的脑区与认知和情绪调控有关。这些研究结果均提示不同运动障碍亚型的PD存在不同的病理改变。有研究提示[21],以姿势异常步态障碍为主要表现的PD主要影响黑质-丘脑-皮层环路,而以震颤为主要表现的PD主要影响小脑-丘脑-皮层环路。我们可以通过一系列检查量表比较不同运动障碍亚型之间症状或体征的差异,再结合影像、病理或生化等研究手段,对于进一步揭示不同运动障碍表现的机制具有重大价值,为PD分组诊断和治疗提供参考。
本研究尚存以下不足:首先,样本含量相对较少,可能存在统计学误差,今后会进一步增大样本含量。其次,由于PD检查量表的评估耗时较长,本研究未设立正常对照组,无法得知两组运动障碍亚型PD患者与正常人之间的差异,今后尚需纳入一定样本量的正常对照组进行研究。再者,本研究对PD患者随访时间较短,对PD患者多巴胺替代药物治疗的反应性统计不全,可能存在误诊的情况,今后会加大对PD患者的随访,降低误诊的可能性。
综上所述,PD患者的运动障碍表现存在明显的差异,不同运动障碍亚型之间在性别构成、非运动症状表现、生活质量影响程度等方面存在明显的异质性,提高对PD不同运动障碍亚型的认识是PD精准诊断和治療的前提,应得到临床医生的关注。
[参考文献]
[1] 中华医学会神经病学分会帕金森病及运动障碍学组.中国帕金森病治疗指南(第三版)[J].中华神经科杂志,2014,47(6):428-433.
[2] Zhang ZX,Roman GC,Hong Z,et al.Parkinson's disease in China:Prevalence in Beijing,Xian,and Shanghai[J].Lancet,2005,365(9459):595-597.
[3] 中华医学会神经病学分会帕金森病及运动障碍学组,中国医师协会神经内科医师分会帕金森病及运动障碍专业委员会.中国帕金森病的诊断标准(2016版)[J].中华神经科杂志,2016,49(4):268-271.
[4] 沈柏,朱骏,潘杨,等.帕金森病不同亚型的功能连接分析[J].中华神经科杂志,2017,50(1):17-23.
[5] Thenganatt MA,Jankovic J.Parkinson disease subtypes[J].Jama Neurol,2014,71(4):499-504.
[6] 徐翠萍,庄平,李勇杰.帕金森病临床分型的研究进展[J].中华神经外科杂志,2016,32(11):1175-1178.
[7] van der Heeden JF,Marinus J,Martinez-martin P,et al. Postural instability and gait are associated with severity and prognosis of Parkinson disease[J]. Neurology,2016, 86(24):2243-2250.
[8] 李淑华,陈海波.帕金森病非运动症状研究进展及临床意义[J].中华神经科杂志,2017,50(1):71-74.
[9] Stebbins GT,Goetz CG,Burn DJ,et al.How to identify tremor dominant and postural instability/gait difficulty groups with the movement disorder society unified Parkinson's disease rating scale:Comparison with the unified Parkinson's disease rating scale[J].Movement Disord,2013,28(5):668-670.
[10] Jankovic J.Parkinson's disease:Clinical features and diagnosis[J]. Journal of Neurology,Neurosurgery & Psychiatry,2008,79(4):368-376.
[11] Garcia-ruiz PJ,Chaudhuri KR,Martnez-martin P.Non-motor symptoms of Parkinson's disease:A review from the past[J]. J Neurol Sci,2014,338(1-2):30-33.
[12] 彭珊,杨飞,张树山,等.帕金森病非运动症状研究进展[J].中国临床神经科学,2017,25(5):567-572,594.
[13] 陈慧敏,李芳菲,冯涛.早发型帕金森病及其基因研究进展[J].中华神经科杂志,2015,(8):729-731.
[14] 于群涛,孔敏,巴茂文,等.帕金森病患者认知功能障碍与同型半胱氨酸的相关性研究[J].中华老年心脑血管病杂志,2018,20(6):631-634.
[15] Wickremaratchi MM,Knipe MD,Sastry BS,et al. The motor phenotype of Parkinson's disease in relation to age at onset[J]. Movement Disord,2011,26(3):457-463.
[16] Wu Y,Guo XY,Wei QQ,et al.Non-motor symptoms and quality of life in tremor dominant vs postural instability gait disorder Parkinson′s disease patients[J]. Acta Neurol Scand,2016,133(5):330-337.
[17] 仲玲玲,宋亚頎,曹化,等.不同运动分型帕金森病患者的非运动症状分析[J].中华全科医师杂志,2018,17(1):56-59.
[18] 杨改清,李晓昶,张晓艺,等.不同亚型帕金森病患者认知功能障碍的临床观察[J].中国实用神经疾病杂志,2018,21(1):51-54.
[19] Ba F,Obaid M,Wieler M,et al.Parkinson disease:The relationship between non-motor symptoms and motor phenotype[J].Canadian Journal of Neurological Sciences/Journal Canadien des Sciences Neurologiques,2016,43(2):261-267.
[20] 王波,芮茂萍,陈渝晖,等.R2*值在不同运动障碍亚型原发性帕金森病异质性的研究价值[J].中风与神经疾病杂志,2017,34(11):997-1002.
[21] Helmich RC,Hallett M,Deuschi G,et al.Cerebral causes and consequences of parkinsonian resting tremor:A tale of two circuits?[J]. Brain,2012,135(Pt 11):3206-3226.
(收稿日期:2020-01-30)
